Steroidogenní faktor 1 - Steroidogenic factor 1
The steroidogenní faktor 1 (SF-1) protein je transkripční faktor zahrnutý do něčeho, zůčastnit se čeho určení pohlaví kontrolou činnosti genů souvisejících s reprodukčními žlázami nebo pohlavní žlázy a nadledviny.[5] Tento protein je kódován NR5A1 gen, člen podrodiny jaderných receptorů, umístěný na dlouhém rameni chromozomu 9 v poloze 33.3. Původně byl identifikován jako regulátor kódování genů cytochrom P450 steroidní hydroxylázy Od té doby však byly objeveny další role v endokrinní funkci.[6]
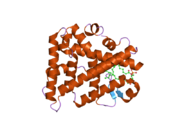
Struktura
The NR5A1 Gen kóduje 461-aminokyselinový protein, který sdílí několik konzervovaný domény shodné s členy podrodiny jaderných receptorů.[6] N-koncová doména zahrnuje dva zinkové prsty a je odpovědná za vazbu DNA prostřednictvím specifického rozpoznávání cílových sekvencí. Variace AGGTCA DNA motivů umožňuje SF-1 interagovat s hlavní drážkou šroubovice DNA a monomerně se vázat.[7] Po navázání závisí trans-aktivace cílových genů na náboru koaktivátorů, jako je SRC-1, GRIP1, PNRC nebo GCN5. Mezi další důležité domény SF-1 patří pantová oblast bohatá na prolin, doména vázající ligand a doména aktivace C-terminálu pro transkripční interakce. 30minokyselinové prodloužení domény vázající DNA známé jako A-box stabilizuje monomerní vazbu působením jako DNA kotva. Pantová oblast může podstoupit post-transkripční a translační modifikace, jako je fosforylace pomocí kináza závislá na cAMP, které dále zvyšují stabilitu a transkripční aktivitu.[8]
SF-1 je považován za osiřelý receptor, protože vysoce afinitní přirozeně se vyskytující ligandy ještě nebyly identifikovány.
Homologie
Analýza myší SF-1 cDNA odhalila podobnost sekvence s Drosophila fushi tarazu faktor I (FTZ-F1), který reguluje fushi tarazu homeobox gen.[9] Několik dalších FTZ-F1 homology byly identifikovány, které implikují vysokou úroveň zachování sekvence mezi obratlovci a bezobratlými. Například cDNA SF-1 sdílí identickou sekvenci 1017 párů bází s cDNA embryonálního dlouhého terminálního proteinu opakující se vazbu (ELP) izolovaného z buňky embryonálního karcinomu, lišící se pouze svými koncovými konci.[9]
Výraz
Dospělá steroidogenní tkáň
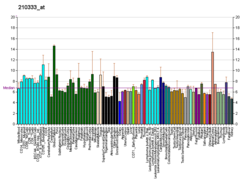
Exprese SF-1 je lokalizována do dospělých steroidogenních tkání korelujících se známými profily exprese steroidních hydroxyláz. Použitím in situ hybridizace pomocí SF-1 cRNA specifické sondy detekovaly genové transkripty v adrenokortikální buňky, Leydigovy buňky a ovariální theca a granulosa buňky.[9] Studie specifických protilátek proti SF-1 potvrdily profil exprese SF-1 u potkanů[10] a lidé[11] odpovídající místům detekce přepisu.
Embryonální steroidogenní tkáň
Genetické pohlaví u savců je určeno přítomností nebo nepřítomností Y chromozom při oplodnění. Sexuálně dimorfní vývoj embryonálních pohlavních žláz do varlat nebo vaječníků je aktivován SRY genový produkt.[12] Sexuální diferenciace je pak řízena hormony produkovanými embryonálními varlaty, přítomností vaječníků nebo úplnou absencí pohlavních žláz. Transkripty SF-1 se zpočátku lokalizují do urogenitálního hřebene, než se buňky exprimující SF-1 rozpadnou na odlišné adrenokortikální a gonadální prekurzory, které nakonec způsobí vznik kůry nadledvin a gonád.
Transkripty SF-1 předcházejí nástupu exprese SRY ve fetálních varlatech, což naznačuje vývojovou roli gonád. SRY ovlivňuje diferenciaci fetálních varlat do odlišných kompartmentů: testikulární šňůry a intersticiální oblast obsahující Leydigovy buňky.[12] Zvýšení proteinu SF-1 a detekce ve steroidogenních Leydigových buňkách a testikulárních šňůrách se shoduje s vývojem.
Ve vaječnících je však pohlavní diferenciace pohlavních žláz usnadněna snížením transkriptu a proteinu SF-1. Hladiny SF-1 jsou silně exprimovány na počátku vývoje folikulů v theca a granulózové buňky, které předcházejí expresi aromatáza enzym odpovědný za estrogen biosyntéza.
Jiné stránky
Bylo zjištěno, že transkripty embryonálních myší SF-1 se nacházejí v regionech vyvíjejícího se diencefalonu a následně v ventromediální hypotalamické jádro (VMH) navrhující role nad rámec steroidogenní údržby.[9]
RT-PCR přístupy detekovaly transkripty myšího genu FTZ-F1 v placentě a slezině; a transkripty SF-1 v lidské placentě.[13]
Posttranslační nařízení
Transkripční kapacitu SF-1 lze ovlivnit posttranslační modifikací. Konkrétně fosforylace serin 203 zprostředkovává cyklin-dependentní kináza 7. Mutace na CDK7 zabraňují interakci s bazálním transkripčním faktorem, TFIIH a tvorba komplexu kinázy aktivující CDK. Ukázalo se, že tato nečinnost potlačuje fosforylaci transkripce závislé na SF-1 a SF-1.[14]
Funkce
SF-1 je kritickým regulátorem reprodukce, který reguluje transkripci klíčových genů podílejících se na sexuálním vývoji a reprodukci, zejména Hvězda a P450SCC. Může tvořit transkripční komplex s TDF up-regulovat transkripci Sox9 gen. Mezi jeho cíle patří geny na všech úrovních osa hypotalamus-hypofýza-gonadální, stejně jako mnoho genů zapojených do gonadal a nadledvin steroidogeneze.[15]
SF-1 byl identifikován jako transkripční regulátor pro řadu různých genů souvisejících s určením pohlaví a diferenciací, reprodukce, a metabolismus prostřednictvím vazby na jejich promotéry. Například SF-1 řídí expresi Amh gen v Sertoliho buňky, přičemž přítomnost nebo nepřítomnost genového produktu ovlivňuje vývoj Müllerovy struktury. Zvýšené hladiny proteinu AMH vedou k regresi těchto struktur.[6] Leydigovy buňky exprimujte SF-1 k regulaci transkripce steroidogeneze a testosteron geny biosyntézy způsobující virilizaci u mužů.
Cílové geny
Steroidogenní buňky
Nejprve identifikované jako regulátor steroidních hydroxyláz v adrenokortikálních buňkách, studie zaměřené na definování lokalizace a exprese SF-1 od té doby odhalily aktivitu enzymu v jiných steroidogenních buňkách.[6]
| druh | Gen | Buňka / tkáň |
|---|---|---|
| krysa | P450scc | granulózní buňky |
| myš | P450scc | Y1 adrenokortikální buňky |
| hovězí | Oxytocin | vaječník |
| myš | Hvězda | Buňky MA-10 Leydig |
Sertoliho buňky
The Müllerova inhibiční látka (MIS nebo AMH) gen v buňkách Sertoli obsahuje konzervovaný motiv identický s optimální vazebnou sekvencí pro SF-1. Experimenty posunu gelové mobility a použití SF-1 specifické polyklonální protilátky zavedené vazebné komplexy SF-1 k MIS,[16] jiné studie však naznačují, že promotor MIS je potlačen a není aktivován vazbou SF-1.
Gonadotropy
Gonadotropní specifický prvek nebo GSE v promotoru genu kódujícího α-podjednotku glykoproteiny (α-GSU) připomíná vazebné otce SF-1. Studie implikovaly SF-1 jako předřazený regulátor sbírky genů potřebných pro funkci gonadotropů prostřednictvím GSE.[17]
VMH
Myši s knockoutem SF-1 vykazovaly hluboké defekty ve VMH, což naznačuje potenciální cílové geny v místě. Cílové geny dosud nebyly identifikovány kvůli obtížím při studiu genové exprese v neuronech.
Vyřazení genu SF-1
Bylo použito několik přístupů cílené narušení genu v myších embryonálních kmenových buňkách s cílem identifikovat potenciální cílové geny SF-1. Různé strategie cílení zahrnují narušení exonů kódujících motiv zingových prstů, narušení 3’-exonu a cílenou mutaci iniciátoru methioninu. Bylo zjištěno, že odpovídající pozorované fenotypové účinky na vývoj a funkci endokrinního systému jsou velmi podobné.[6]
Vykazované knoflíkové myši Sf-1 se zmenšily kortikosteron úrovně při zachování zvýšené ACTH úrovně. Pozorované morfologické změny a fragmentace DNA byly v souladu s apoptózou a strukturální regresí vedoucí k úmrtí všech myší do 8 dnů po narození.[18]
Bylo zjištěno, že funkce Sf-1 je nezbytná pro vývoj primární steroidogenní tkáně, o čemž svědčí úplný nedostatek nadledvinek a pohlavních žláz ve vyřazení. Rovněž bylo pozorováno obrácení pohlavních orgánů mezi muži a ženami.[19]
Klinický význam
Mutace v NR5A1 mohou produkovat intersexuální genitálie, absenci puberty a neplodnost. Jedná se o jednu příčinu zástavy funkce vaječníků u žen <40 let, která se vyskytuje u 1% všech žen.
Selhání nadledvin a pohlavních žláz
Dvě varianty SF-1 spojené s primárním selháním nadledvin a úplná gonadální dysgeneze byly nahlášeny jako způsobené NR5A1 mutace. Bylo zjištěno, že jeden nahlášený případ měl de novo heterozygotní p.G35E změna na doménu P-boxu.[20] Ovlivněná oblast umožňuje specifičnost vazby DNA prostřednictvím interakcí s regulačními prvky reakce cílových genů. Tato změna p.G35E může mít mírný kompetitivní nebo dominantní negativní účinek na transaktivaci vedoucí k závažným defektům gonád a dysfunkci nadledvin. Podobně, homozygotní Změna p.R92Q v A-boxu interferovala s monomerní vazebnou stabilitou a sníženou funkční aktivitou.[20] Tato změna vyžaduje mutace obou alel k zobrazení fenotypových účinků, protože heterozygotní nosiči vykazovali normální funkci nadledvin.
Missense, v rámu a mutace posunu snímků NR5A1 byly nalezeny v rodinách s 46, XY poruchami sexuálního vývoje, 46, XX gonadální dysgeneze a 46, XX primární ovariální nedostatečnost. 46, XY jedinci mohou mít dvojznačné nebo ženské genitálie. Jednotlivci obou karyotyp nemusí vstoupit do puberty, ačkoli výraz fenotyp, pronikavost, plodnost a způsoby dědičnosti se mohou lišit. Některé mutace jsou dominantní, někteří jsou recesivní.[21]
46, XY poruchy pohlavního vývoje
Heterozygotní NR5A1 změny se objevují jako častý přispěvatel do 46, XY úplná gonadální dysgeneze.[20] U postižených jedinců sexuální vývoj neodpovídá jejich chromozomálnímu složení. Muži, přestože měli 46, XY karyotyp, vyvinout vnější zevní genitálie žen, stejně jako dělohu a vejcovody spolu s defekty pohlavních žláz, které je činí nefunkčními.[22] NR5A1 mutace byly také spojeny s částečnou gonadální dysgenezí, přičemž postižené osoby mají nejednoznačné genitálie, urogenitální sinus, chybějící nebo rudimentární Müllerovy struktury a další abnormality.[20]
Typicky jsou tyto genetické změny shifthift, nesmysl nebo missense mutace, které mění vazbu DNA a transkripci genů. Zatímco mnozí jsou de novo, třetina případů byla zděděna mateřským způsobem podobným způsobem jako Dědičnost spojená s X.. Dále byla odhalena jedna zpráva o homozygotní mutaci missense p.D293N v doméně vázající ligand SF-1. autosomálně recesivní dědictví bylo také možné.[21]
Neplodnost
Analýza NR5A1 u mužů s neobstrukční neplodnost mužského faktoru zjistili, že pacienti se změnami genů měli závažnější formy neplodnosti a nižší hladinu testosteronu.[23] Tyto změny ovlivnily pantovou oblast SF-1. Je důležité si uvědomit, že k prokázání vztahu mezi změnami SF-1 a neplodností jsou nutné další studie.
Další interakce
Bylo také prokázáno, že SF-1 interaguje s:
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000136931 - Ensembl, Květen 2017
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000026751 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ Reference, Genetics Home. "Gen NR5A1". Genetická domácí reference. Citováno 2017-11-30.
- ^ A b C d E Parker KL, Schimmer BP (červen 1997). „Steroidogenní faktor 1: klíčový determinant endokrinního vývoje a funkce“. Endokrinní hodnocení. 18 (3): 361–77. doi:10.1210 / edrv.18.3.0301. PMID 9183568.
- ^ Mangelsdorf DJ, Thummel C, Beato M, Herrlich P, Schütz G, Umesono K, Blumberg B, Kastner P, Mark M, Chambon P, Evans RM (prosinec 1995). „Nadrodina jaderných receptorů: druhé desetiletí“. Buňka. 83 (6): 835–9. doi:10.1016 / 0092-8674 (95) 90199-x. PMC 6159888. PMID 8521507.
- ^ Honda S, Morohashi K, Nomura M, Takeya H, Kitajima M, Omura T (duben 1993). „Ad4BP regulující steroidogenní gen P-450 je členem nadrodiny receptorů steroidních hormonů“. The Journal of Biological Chemistry. 268 (10): 7494–502. PMID 8463279.
- ^ A b C d Ikeda Y, Lala DS, Luo X, Kim E, moisanský poslanec, Parker KL (červenec 1993). „Charakterizace myšího genu FTZ-F1, který kóduje klíčový regulátor exprese genu pro steroidní hydroxylázu“. Molekulární endokrinologie. 7 (7): 852–60. doi:10.1210 / oprava 7.7.8413309. PMID 8413309.
- ^ Morohashi K, Iida H, Nomura M, Hatano O, Honda S, Tsukiyama T, Niwa O, Hara T, Takakusu A, Shibata Y (květen 1994). „Funkční rozdíl mezi Ad4BP a ELP a jejich distribuce ve steroidogenních tkáních“. Molekulární endokrinologie. 8 (5): 643–53. doi:10.1210 / oprava.8.5.8058072. PMID 8058072.
- ^ Takayama K, Sasano H, Fukaya T, Morohashi K, Suzuki T, Tamura M, Costa MJ, Yajima A (září 1995). "Imunohistochemická lokalizace proteinu vázajícího se na Ad4 s korelací s expresí steroidogenních enzymů v cyklování lidských vaječníků a stromálních nádorů pohlavních kordů". The Journal of Clinical Endocrinology and Metabolism. 80 (9): 2815–21. doi:10.1210 / jcem.80.9.7673429. PMID 7673429.
- ^ A b ""Mužský vývoj chromosomálně ženských myší transgenních pro gen Sry "(1991), Peter Koopman a kol. | Encyklopedie projektu Embryo". embryo.asu.edu. Citováno 2017-11-30.
- ^ Ninomiya Y, Okada M, Kotomura N, Suzuki K, Tsukiyama T, Niwa O (1995). "Genomická organizace a izoformy myšího genu ELP". Journal of Biochemistry. 118 (2): 380–9. doi:10.1093 / oxfordjournals.jbchem.a124918. PMID 8543574.
- ^ Lewis AE, Rusten M, Hoivik EA, Vikse EL, Hansson ML, Wallberg AE, Bakke M (leden 2008). „Fosforylace steroidogenního faktoru 1 je zprostředkována cyklin-dependentní kinázou 7“. Molekulární endokrinologie. 22 (1): 91–104. doi:10.1210 / me.2006-0478. PMC 5419630. PMID 17901130.
- ^ Jameson JL (prosinec 2004). „O myších a lidech: příběh o steroidogenním faktoru-1“. The Journal of Clinical Endocrinology and Metabolism. 89 (12): 5927–9. doi:10.1210 / jc.2004-2047. PMID 15579738.
- ^ Shen WH, Moore CC, Ikeda Y, Parker KL, Ingraham HA (červen 1994). „Jaderný receptor steroidogenní faktor 1 reguluje gen mülleriánské inhibiční látky: odkaz na kaskádu určování pohlaví“. Buňka. 77 (5): 651–61. doi:10.1016/0092-8674(94)90050-7. PMID 8205615. S2CID 13364008.
- ^ Ingraham HA, Lala DS, Ikeda Y, Luo X, Shen WH, Nachtigal MW, Abbud R, Nilson JH, Parker KL (říjen 1994). „Jaderný receptor steroidogenní faktor 1 působí na více úrovních reprodukční osy“. Geny a vývoj. 8 (19): 2302–12. doi:10,1101 / gad.8.19.2302. PMID 7958897.
- ^ Luo X, Ikeda Y, Schlosser DA, Parker KL (září 1995). „Steroidogenní faktor 1 je základním přepisem myšího genu Ftz-F1“. Molekulární endokrinologie. 9 (9): 1233–9. doi:10.1210 / opravit 9.9.7491115. PMID 7491115.
- ^ Luo X, Ikeda Y, Parker KL (květen 1994). „Buněčný specifický jaderný receptor je nezbytný pro vývoj nadledvin a pohlavních žláz a sexuální diferenciaci.“ Buňka. 77 (4): 481–90. doi:10.1016/0092-8674(94)90211-9. PMID 8187173. S2CID 28194376.
- ^ A b C d Ferraz-de-Souza B, Lin L, Achermann JC (duben 2011). „Steroidogenní faktor-1 (SF-1, NR5A1) a lidská nemoc“. Molekulární a buněčná endokrinologie. 336 (1–2): 198–205. doi:10.1016 / j.mce.2010.11.006. PMC 3057017. PMID 21078366.
- ^ A b Lourenço D, Brauner R, Lin L, De Perdigo A, Weryha G, Muresan M, Boudjenah R, Guerra-Junior G, Maciel-Guerra AT, Achermann JC, McElreavey K, Bashamboo A (březen 2009). "Mutace v NR5A1 spojené s ovariální nedostatečností". The New England Journal of Medicine. 360 (12): 1200–10. doi:10.1056 / NEJMoa0806228. PMC 2778147. PMID 19246354.
- ^ Reference, Genetics Home. "Swyerův syndrom". Genetická domácí reference. Citováno 2017-11-30.
- ^ Bashamboo A, Ferraz-de-Souza B, Lourenço D, Lin L, Sebire NJ, Montjean D, Bignon-Topalovic J, Mandelbaum J, Siffroi JP, Christin-Maitre S, Radhakrishna U, Rouba H, Ravel C, Seeler J, Achermann JC, McElreavey K (říjen 2010). "Mužská neplodnost spojená s mutacemi v NR5A1 kódujícím steroidogenní faktor 1". American Journal of Human Genetics. 87 (4): 505–12. doi:10.1016 / j.ajhg.2010.09.009. PMC 2948805. PMID 20887963.
- ^ Kennell JA, O'Leary EE, Gummow BM, Hammer GD, MacDougald OA (srpen 2003). „T-buněčný faktor 4N (TCF-4N), nová izoforma myšího TCF-4, synergizuje s beta-kateninem za účelem koaktivace transkripčních faktorů C / EBPalfa a steroidogenního faktoru 1“. Molekulární a buněčná biologie. 23 (15): 5366–75. doi:10.1128 / MCB.23.15.5366-5375.2003. PMC 165725. PMID 12861022.
- ^ Mizusaki H, Kawabe K, Mukai T, Ariyoshi E, Kasahara M, Yoshioka H, Swain A, Morohashi K (duben 2003). „Transkripce genu Dax-1 (pohlavně reverzní adrenální hypoplázie kongenita kongenita na chromozomu X, gen 1) je regulována pomocí wnt4 v ženské vyvíjející se pohlavní žláze“. Molekulární endokrinologie. 17 (4): 507–19. doi:10.1210 / me.2002-0362. PMID 12554773.
- ^ Lopez D, Shea-Eaton W, Sanchez MD, McLean MP (prosinec 2001). „DAX-1 potlačuje lipoproteinový receptor s vysokou hustotou prostřednictvím interakce s pozitivními regulátory protein-1a vázající regulační prvek na sterol a steroidogenní faktor-1“. Endokrinologie. 142 (12): 5097–106. doi:10.1210 / endo.142.12.8523. PMID 11713202.
- ^ Sugawara T, Saito M, Fujimoto S (srpen 2000). „Sp1 a SF-1 interagují a spolupracují při regulaci exprese lidského steroidogenního akutního regulačního proteinu genu“. Endokrinologie. 141 (8): 2895–903. doi:10.1210 / en.141.8.2895. PMID 10919277.
- ^ Mellgren G, Børud B, Hoang T, Yri OE, Fladeby C, Lien EA, Lund J (květen 2003). "Charakterizace receptoru interagujícího proteinu RIP140 při regulaci cílových genů reagujících na SF-1". Molekulární a buněčná endokrinologie. 203 (1–2): 91–103. doi:10.1016 / S0303-7207 (03) 00097-2. PMID 12782406. S2CID 733221.
- ^ Sugawara T, Abe S, Sakuragi N, Fujimoto Y, Nomura E, Fujieda K, Saito M, Fujimoto S (srpen 2001). „RIP 140 moduluje transkripci genu pro steroidogenní akutní regulační protein prostřednictvím interakcí s SF-1 i DAX-1“. Endokrinologie. 142 (8): 3570–7. doi:10.1210 / cs.142.8.3570. PMID 11459805.
- ^ De Santa Barbara P, Bonneaud N, Boizet B, Desclozeaux M, Moniot B, Sudbeck P, Scherer G, Poulat F, Berta P (listopad 1998). „Přímá interakce proteinu SOX9 souvisejícího se SRY a steroidogenního faktoru 1 reguluje transkripci lidského genu pro anti-Müllerian hormon“. Molekulární a buněčná biologie. 18 (11): 6653–65. doi:10,1128 / mcb.18.11.6653. PMC 109250. PMID 9774680.
- ^ Gizard F, Lavallee B, DeWitte F, Teissier E, Staels B, Hum DW (říjen 2002). „Protein regulující transkripci 132 kDa (TReP-132) zvyšuje transkripci genu P450scc prostřednictvím interakce se steroidogenním faktorem-1 v lidských buňkách nadledvin.“. The Journal of Biological Chemistry. 277 (42): 39144–55. doi:10,1074 / jbc.M205786200. PMID 12101186.
Další čtení
- Morohashi KI, Omura T (prosinec 1996). „Ad4BP / SF-1, transkripční faktor nezbytný pro transkripci genů pro steroidogenní cytochrom P450 a pro stanovení reprodukční funkce“. FASEB Journal. 10 (14): 1569–77. doi:10.1096 / fasebj.10.14.9002548. PMID 9002548. S2CID 13891159.
- Achermann JC, Meeks JJ, Jameson JL (prosinec 2001). "Fenotypové spektrum mutací v DAX-1 a SF-1". Molekulární a buněčná endokrinologie. 185 (1–2): 17–25. doi:10.1016 / S0303-7207 (01) 00619-0. PMID 11738790. S2CID 20651430.
- Ozisik G, Achermann JC, Jameson JL (červen 2002). „Role SF1 v nadledvinách a reprodukční funkci: pohled z přirozeně se vyskytujících mutací u lidí“. Molekulární genetika a metabolismus. 76 (2): 85–91. doi:10.1016 / S1096-7192 (02) 00032-X. PMID 12083805.
- de-Souza BF, Lin L, Achermann JC (červen 2006). „Steroidogenní faktor-1 (SF-1) a jeho význam pro pediatrickou endokrinologii“. Recenze pediatrické endokrinologie. 3 (4): 359–64. doi:10.1159/000094108. PMID 16816804.
- Sadovsky Y, Crawford PA, Woodson KG, polský JA, Clements MA, Tourtellotte LM, Simburger K, Milbrandt J (listopad 1995). „Myši s nedostatkem steroidogenního faktoru 1 pro vzácná onemocnění nemají nadledviny a pohlavní žlázy, ale exprimují enzym štěpící postranní řetězec P450 v placentě a mají normální hladinu kortikosteroidů v séru.“. Sborník Národní akademie věd Spojených států amerických. 92 (24): 10939–43. doi:10.1073 / pnas.92.24.10939. PMC 40546. PMID 7479914.
- Sasano H, Shizawa S, Suzuki T, Takayama K, Fukaya T, Morohashi K, Nagura H (srpen 1995). "Ad4BP v lidské kůře nadledvin a její poruchy". The Journal of Clinical Endocrinology and Metabolism. 80 (8): 2378–80. doi:10.1210 / jc.80.8.2378. PMID 7629233.
- Oba K, Yanase T, Nomura M, Morohashi K, Takayanagi R, Nawata H (září 1996). "Strukturální charakterizace lidského genu Ad4bp (SF-1)". Sdělení o biochemickém a biofyzikálním výzkumu. 226 (1): 261–7. doi:10.1006 / bbrc.1996.1343. PMID 8806624.
- Asa SL, Bamberger AM, Cao B, Wong M, Parker KL, Ezzat S (červen 1996). „Aktivátor transkripce steroidogenní faktor-1 je přednostně exprimován v lidské hypofýze gonadotropní“. The Journal of Clinical Endocrinology and Metabolism. 81 (6): 2165–70. doi:10.1210 / jc.81.6.2165. PMID 8964846.
- Bamberger AM, Ezzat S, Cao B, Wong M, Parker KL, Schulte HM, Asa SL (červen 1996). „Exprese mRNA a proteinu steroidogenního faktoru-1 (SF-1) v lidské placentě“. Molekulární lidská reprodukce. 2 (6): 457–61. doi:10.1093 / mol / 2.6.457. PMID 9238716.
- Crawford PA, polský JA, Ganpule G, Sadovsky Y (říjen 1997). „Aktivační funkce-2 hexamer steroidogenního faktoru-1 je nutná, ale není dostatečná pro potenciaci SRC-1“. Molekulární endokrinologie. 11 (11): 1626–35. doi:10.1210 / me.11.11.1626. PMID 9328345.
- Nachtigal MW, Hirokawa Y, Enyeart-VanHouten DL, Flanagan JN, Hammer GD, Ingraham HA (květen 1998). „Wilmsův nádor 1 a Dax-1 modulují osiřelý jaderný receptor SF-1 v genově specifické expresi genu“. Buňka. 93 (3): 445–54. doi:10.1016 / S0092-8674 (00) 81172-1. PMID 9590178. S2CID 19015882.
- Hammer GD, Krylova I, Zhang Y, Darimont BD, Simpson K, Weigel NL, Ingraham HA (duben 1999). „Fosforylace jaderného receptoru SF-1 moduluje nábor kofaktorů: integrace hormonální signalizace do reprodukce a stresu“. Molekulární buňka. 3 (4): 521–6. doi:10.1016 / S1097-2765 (00) 80480-3. PMID 10230405.
- Achermann JC, Ito M, Ito M, Hindmarsh PC, Jameson JL (červen 1999). „Mutace v genu kódujícím steroidogenní faktor-1 způsobuje reverzi pohlaví XY a selhání nadledvin u lidí“. Genetika přírody. 22 (2): 125–6. doi:10.1038/9629. PMID 10369247. S2CID 27674149.