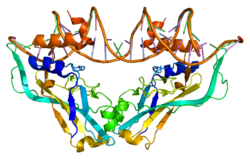
TBX2 - TBX2
Transkripční faktor T-boxu 2 Tbx2 je transkripční faktor který je kódován Tbx2 gen na chromozomu 17q21-22 u lidí.[5][6][7] Tento gen je členem fylogeneticky konzervované rodiny genů, které sdílejí společnou doménu vázající DNA, T-box. Tbx2 a Tbx3 jsou jedinými transkripčními faktory T-boxu, které fungují spíše jako transkripční represory než transkripční aktivátory, a jsou úzce spjaty z hlediska vývoje a tumorigeneze.[8] Tento gen hraje významnou roli v embryonálním a fetálním vývoji prostřednictvím kontroly genové exprese a má také důsledky pro různé druhy rakoviny. Tbx2 je spojen s mnoha signálními cestami, BMP, TGFβ, Wnt, a FGF, které umožňují modelování a proliferaci během organogeneze ve vývoji plodu.[8]
Role ve vývoji
Během vývoje plodu naznačuje vztah Tbx2 k signálním drahám FGF, BMP a Wnt jeho rozsáhlou kontrolu nad vývojem různých orgánových systémů. Funguje převážně ve vzorcích vývoje orgánů spíše než v proliferaci tkání. Tbx2 má důsledky ve vývoji končetin, atrioventrikulárním vývoji srdce a vývoji předních mozkových tkání.[9][10][11]
Během vývoje pupenů končetiny stimuluje Shh a FGF signalizace růstu končetiny. V určitém bodě jsou koncentrace Tbx2 takové, že je ukončena signalizace Shh a FGF, což zastavuje další postup a růst vývoje končetiny. K tomu dochází přímo skrze Tbx2 potlačující expresi Grem1, vytvářející negativní zónu Grem1, čímž narušuje signalizaci růstu Shh a FGF.[9]
Srdeční vývoj je silně regulován a vyžaduje vývoj čtyř srdečních komor, přepážky a různých součástí chlopně pro odtok a přítok. Při vývoji srdce je Tbx2 up-regulován BMP2 stimulovat atrioventrikulární vývoj.[10] Vývoj modelu myši s knockoutem Tbx2 umožnil stanovení specifických rolí Tbx2 ve vývoji srdce a vědci určili, že Tbx2 a Tbx3 jsou nadbytečné ve většině vývoje srdce.[10] Dále použití těchto knockoutových modelů určilo význam Tbx2 v signální dráze BMP pro vývoj atrioventrikulárního kanálu, atrioventrikulárního uzlového fenotypu a atrioventrikulárního polštáře.[10]
Signální kaskáda atrioventrikulárního kanálu zahrnuje gen síňového natriuretického faktoru (ANF). Tento gen je jedním z prvních znaků tvorby komory ve vyvíjejícím se myokardu. Malý fragment v tomto genu může potlačit promotor srdečního troponinu I (cTnI) selektivně v atrioventrikulárním kanálu. Faktor T-box a prvek vázající faktor NK2-homeobox se podílejí na represi atrioventrikulárního kanálu bez ovlivnění jeho aktivity v komoře. Tbx2 tvoří komplex s Nkx2,5 na genu ANF k potlačení jeho promotorové aktivity, takže exprese genu je inhibována v atrioventrikulárním kanálu během diferenciace komory.[12] Atrioventrikulární kanál je také původem atrioventrikulární uzlové osy a pomáhá nakonec koordinovat tlukot srdce. Úlohou Tbx2 při tvorbě polštářů ve vyvíjejícím se srdci je spolupráce s Tbx3 na spuštění smyčky dopředného předávání s BMP2 pro koordinovaný vývoj těchto polštářů.[10] Bylo také zjištěno, že Tbx2 dočasně potlačuje proliferaci a diferenciaci podmnožiny primárních buněk myokardu.[13]
Nakonec během vývoje předního mozku stimuluje BMP expresi Tbx2, která potlačuje signalizaci FGF. Toto potlačení FGF signalizace dále potlačuje expresi Flrt3, který je nezbytný pro přední vývoj mozku.
Související vrozené vady
Je známo, že Tbx2 funguje způsobem závislým na dávce; duplikace nebo delece oblasti zahrnující Tbx2 proto může způsobit různé vrozené vady, včetně: mikrocefalie, různé defekty komorového septa a abnormality skeletu.[14][15][16] Některé specifické abnormality jsou popsány níže. Mutace v TBX2 způsobují predispozici k kýly.[17]
Abnormality číslic
Během vývoje končetinových pupenů down-regulace Tbx2 neinhibuje signalizaci Shh / FGF4; proto, což má za následek zvýšenou velikost končetinových pupenů a duplikaci 4. číslice, polydaktylie.[9] Naproti tomu, když je Tbx2 nadměrně vyjádřen nebo duplikován, pupeny končetin jsou menší a mohou mít snížený počet číslic kvůli předčasnému ukončení Psst a FGF4 signalizace.[9]
Poruchy komorového septa
Jedná se o širokou kategorii zahrnující mnoho konkrétnějších vrozených srdečních vad. Z těch, které souvisejí s Tbx2, jsou některé způsobeny duplikací nebo nadměrnou expresí Tbx2 a jiné jsou způsobeny delecí oblasti genu Tbx2. Například u pacientů s duplikací oblasti genu Tbx2 se projevily atrioventrikulární abnormality zahrnující: defekt mezikomorového septa, patent foramen ovale, koarktace aorty, nedostatečnost trikuspidální chlopně a stenóza mitrální chlopně.[16] Naopak pacienti s delecí genu Tbx2 vykazovali plicní hypertenzi a další srdeční vady, ale je méně hlášen.[18][15]
Role v tumorigenezi
Tbx2 se podílí na rakovině spojené s plicemi, prsy, kostmi, slinivkou břišní a melanomem. Je známo, že je v této skupině rakoviny nadměrně exprimován a mění signální dráhy buněk vedoucí k tumorigenezi. Bylo navrženo a studováno několik drah pomocí myších knockoutových modelů genů v signálních drahách. V současné době je výzkum využívající knockoutový model Tbx2 pro studium tumorigeneze omezený.
p14ARF / MDM2 / p35 / p21CIP1 Cesta. Když je zvýšena regulace, Tbx2 inhibuje p21CIP1. p21CIP1 je nezbytný pro stárnutí tkáně, a pokud je ohrožen, zanechává tkáň citlivou na signály podporující nádor.[19]
Cesta Wnt / beta-katenin. Role Tbx2 ve Wnt signalizaci musí být ještě potvrzena; up-regulace Tbx2 v beta-katenin signální dráha vede ke ztrátě adhezní molekuly E-kadherin.[20] To vrací buňky do mezenchymálního stavu a usnadňuje invazi nádorových buněk.
Signální cesta EGR1. Nakonec up-regulace Tbx2 zvyšuje jeho interakci s EGR1. EGR1 potlačuje NDGR1 ke zvýšení proliferace buněk, což vede k metastázám nebo rozvoji nádoru.[21]
Společně může upregulace Tbx2 na těchto signálních drahách vést k rozvoji maligních nádorů.
Cíl léčby rakoviny
Pochopení signálních drah a role Tbx2 v tumorigenezi může pomoci při vývoji léčby rakoviny zaměřené na geny. Protože Tbx2 je nadměrně regulován u různých typů rakovinných buněk v mnoha orgánových systémech, potenciál pro genovou terapii je optimistický. Vědci se zajímají o cílení na malou doménu Tbx2 a Tbx3 ke snížení její exprese a využití malých peptidů, o nichž je známo, že potlačují nádorové geny, k inhibici proliferace. Studie in vitro používající buněčnou linii lidské rakoviny prostaty blokovala endogenní Tbx2 s použitím Tbx2 dominantně negativních retrovirových vektorů zjistila sníženou proliferaci nádorových buněk.[22] Stejná studie dále navrhuje cílení WNT3A kvůli jeho roli v buněčné signalizaci s Tbx2, využitím antagonisty WNT, jako je SFRP-2. Protože somatické buňky mají nízkou expresi Tbx2, cílené ošetření genem Tbx2 by ponechalo zdravé somatické buňky nepoškozené, což by poskytlo léčbu s nízkou toxicitou a negativními vedlejšími účinky.[8] K určení účinnosti těchto specifických genových cílů pro protinádorovou léčbu je stále zapotřebí mnoho výzkumu.
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000121068 - Ensembl, Květen 2017
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000000093 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ Campbell C, Goodrich K, Casey G, Beatty B (červenec 1995). „Klonování a mapování lidského genu (TBX2) sdílejícího vysoce konzervovaný proteinový motiv s genem Drosophila omb“. Genomika. 28 (2): 255–60. doi:10.1006 / geno.1995.1139. PMID 8530034.
- ^ „Entrez Gene: TBX2 T-box 2“.
- ^ Law DJ, Gebuhr T, Garvey N, Agulnik SI, Silver LM (listopad 1995). "Identifikace, charakterizace a lokalizace chromozomu 17q21-22 lidského homologu TBX2, člena konzervované vývojové genové rodiny". Savčí genom. 6 (11): 793–7. doi:10.1007 / bf00539006. hdl:2027.42/47017. PMID 8597636. S2CID 15779406.
- ^ A b C Lu J, Li XP, Dong Q, Kung HF, He ML (prosinec 2010). „TBX2 a TBX3: speciální hodnota pro protinádorové léky“. Biochimica et Biophysica Acta (BBA) - Recenze na rakovinu. 1806 (2): 268–74. doi:10.1016 / j.bbcan.2010.07.001. PMC 7127380. PMID 20624445.
- ^ A b C d Farin HF, Lüdtke TH, Schmidt MK, Placzko S, Schuster-Gossler K, Petry M, Christoffels VM, Kispert A (2013-04-25). „Tbx2 ukončuje signalizaci shh / fgf ve vyvíjejícím se končetině myší končetiny přímým potlačením gremlin1“. Genetika PLOS. 9 (4): e1003467. doi:10.1371 / journal.pgen.1003467. PMC 3636256. PMID 23633963.
- ^ A b C d E Singh R, Hoogaars WM, Barnett P, Grieskamp T, Rana MS, Buermans H, Farin HF, Petry M, Heallen T, Martin JF, Moorman AF, 't Hoen PA, Kispert A, Christoffels VM (duben 2012). „Tbx2 a Tbx3 indukují vývoj atrioventrikulárního myokardu a tvorbu polštáře endokardu“. Buněčné a molekulární biologické vědy. 69 (8): 1377–89. doi:10.1007 / s00018-011-0884-2. PMC 3314179. PMID 22130515.
- ^ Cho GS, Park DS, Choi SC, Han JK (leden 2017). „Tbx2 reguluje přední neurální specifikaci potlačením signální dráhy FGF“. Vývojová biologie. 421 (2): 183–193. doi:10.1016 / j.ydbio.2016.11.020. PMID 27913219.
- ^ Habets PE, Moorman AF, Clout DE, van Roon MA, Lingbeek M, van Lohuizen M, Campione M, Christoffels VM (květen 2002). „Kooperativní působení Tbx2 a Nkx2,5 inhibuje expresi ANF v atrioventrikulárním kanálu: důsledky pro tvorbu srdeční komory“. Geny a vývoj. 16 (10): 1234–46. doi:10,1101 / gad.222902. PMC 186286. PMID 12023302.
- ^ Aanhaanen WT, Brons JF, Domínguez JN, Rana MS, Norden J, Airik R, Wakker V, de Gier-de Vries C, Brown NA, Kispert A, Moorman AF, Christoffels VM (červen 2009). „Primární myokard Tbx2 + atrioventrikulárního kanálu tvoří atrioventrikulární uzel a základnu levé komory“. Výzkum oběhu. 104 (11): 1267–74. doi:10.1161 / CIRCRESAHA.108.192450. PMID 19423846.
- ^ Pang S, Liu Y, Zhao Z, Huang W, Chen D, Yan B (září 2013). "Nové a funkční varianty sekvencí v promotoru genu TBX2 u defektů komorového septa". Biochimie. 95 (9): 1807–9. doi:10.1016 / j.biochi.2013.05.007. PMID 23727221.
- ^ A b Nimmakayalu M, major H, Sheffield V, Solomon DH, Smith RJ, Patil SR, Shchelochkov OA (únor 2011). „Mikrodelece 17q22q23.2 zahrnující TBX2 a TBX4 u pacienta s vrozenou mikrocefalií, cystou štítné žlázy, senzorineurální ztrátou sluchu a plicní hypertenzí“. American Journal of Medical Genetics. Část A. 155A (2): 418–23. doi:10,1002 / ajmg.a.33827. PMID 21271665. S2CID 24377700.
- ^ A b Radio FC, Bernardini L, Loddo S, Bottillo I, Novelli A, Mingarelli R, Dallapiccola B (srpen 2010). "Duplikace genu TBX2 spojená se složitou srdeční vadou a malformacemi skeletu". American Journal of Medical Genetics. Část A. 152A (8): 2061–6. doi:10,1002 / ajmg.a.33506. PMID 20635360. S2CID 13614834.
- ^ Zhang, Y .; Han, Q .; Fan, H .; Li, W .; Xing, Q .; Yan, B. (2014). „Genetická analýza promotoru genu TBX2 u nepřímé tříselné kýly - PubMed“. Hernia: The Journal of Hernias and Abdominal Wall Surgery. 18 (4): 513–7. doi:10.1007 / s10029-013-1199-z. PMID 24309999. S2CID 10028037.
- ^ Puusepp H, Zilina O, Teek R, Männik K, Parkel S, Kruustük K, Kuuse K, Kurg A, Ounap K (01.01.2009). „5,9 Mb mikrodelece v chromozomovém pásmu 17q22-q23.2 spojená s tracheo-jícnovou píštělí a vodivou ztrátou sluchu“. European Journal of Medical Genetics. 52 (1): 71–4. doi:10.1016 / j.ejmg.2008.09.006. PMID 18983945.
- ^ Prince S, Carreira S, Vance KW, Abrahams A, Goding CR (březen 2004). „Tbx2 přímo potlačuje expresi inhibitoru kinázy závislé na cyklinu p21 (WAF1)“. Výzkum rakoviny. 64 (5): 1669–74. doi:10.1158 / 0008-5472.can-03-3286. PMID 14996726.
- ^ Rodriguez M, Aladowicz E, Lanfrancone L, Goding CR (říjen 2008). „Tbx3 potlačuje expresi E-kadherinu a zvyšuje invazivitu melanomu“. Výzkum rakoviny. 68 (19): 7872–81. doi:10.1158 / 0008-5472.can-08-0301. PMID 18829543.
- ^ Redmond KL, Crawford NT, Farmer H, D'Costa ZC, O'Brien GJ, Buckley NE, Kennedy RD, Johnston PG, Harkin DP, Mullan PB (červen 2010). „T-box 2 potlačuje NDRG1 prostřednictvím mechanismu závislého na EGR1 k podpoře množení buněk rakoviny prsu“. Onkogen. 29 (22): 3252–62. doi:10.1038 / dne 2010.84. PMID 20348948.
- ^ Nandana S, Tripathi M, Duan P, Chu CY, Mishra R, Liu C, Jin R, Yamashita H, Zayzafoon M, Bhowmick NA, Zhau HE, Matusik RJ, Chung LW (březen 2017). „Metastázu kostí rakoviny prostaty lze terapeuticky zaměřit na signální osu TBX2-WNT“. Výzkum rakoviny. 77 (6): 1331–1344. doi:10.1158 / 0008-5472.can-16-0497. PMC 5783646. PMID 28108510.
Další čtení
- Bonaldo MF, Lennon G, Soares MB (září 1996). „Normalizace a odčítání: dva přístupy k usnadnění objevování genů“. Výzkum genomu. 6 (9): 791–806. doi:10,1101 / gr. 6.9.791. PMID 8889548.
- Campbell CE, Casey G, Goodrich K (leden 1998). „Genomická struktura TBX2 naznačuje ochranu pomocí vzdálených příbuzných genů T-boxu“. Savčí genom. 9 (1): 70–3. doi:10,1007 / s003359900682. PMID 9434949. S2CID 22349.
- Carreira S, Dexter TJ, Yavuzer U, Easty DJ, Goding CR (září 1998). „Transkripční faktor Tbx2 související s Brachyury a potlačení promotoru TRP-1 specifického pro melanocyty“. Molekulární a buněčná biologie. 18 (9): 5099–108. doi:10,1128 / mcb.18.9.5099. PMC 109095. PMID 9710594.
- He MI, Wen L, Campbell CE, Wu JY, Rao Y (srpen 1999). „Transkripční represe pomocí Xenopus ET a jeho lidského ortologu TBX3, genu podílejícího se na ulnárně-prsním syndromu“. Sborník Národní akademie věd Spojených států amerických. 96 (18): 10212–7. Bibcode:1999PNAS ... 9610212H. doi:10.1073 / pnas.96.18.10212. PMC 17868. PMID 10468588.
- Sinha S, Abraham S, Gronostajski RM, Campbell CE (listopad 2000). „Diferenciální vazba DNA a modulace transkripce třemi T-box proteiny, T, TBX1 a TBX2“. Gen. 258 (1–2): 15–29. doi:10.1016 / S0378-1119 (00) 00417-0. PMID 11111039.
- Brummelkamp TR, Kortlever RM, Lingbeek M, Trettel F, MacDonald ME, van Lohuizen M, Bernards R (únor 2002). „TBX-3, gen mutovaný v Ulnar-Mammarově syndromu, je negativním regulátorem p19ARF a inhibuje stárnutí“. The Journal of Biological Chemistry. 277 (8): 6567–72. doi:10,1074 / jbc.M110492200. PMID 11748239.
- Lingbeek ME, Jacobs JJ, van Lohuizen M (červenec 2002). „T-box represory TBX2 a TBX3 specificky regulují tumor supresorový gen p14ARF prostřednictvím variantního T-místa v iniciátoru“. The Journal of Biological Chemistry. 277 (29): 26120–7. doi:10,1074 / jbc.M200403200. PMID 12000749.
- Habets PE, Moorman AF, Clout DE, van Roon MA, Lingbeek M, van Lohuizen M, Campione M, Christoffels VM (květen 2002). „Kooperativní působení Tbx2 a Nkx2,5 inhibuje expresi ANF v atrioventrikulárním kanálu: důsledky pro tvorbu srdeční komory“. Geny a vývoj. 16 (10): 1234–46. doi:10,1101 / gad.222902. PMC 186286. PMID 12023302.
- Andelfinger G, Etter L, Dyment M, Hitte C, Galibert F, Kirkness E, Benson DW (srpen 2003). "Radiační hybridní mapování a genomická organizace psích TBX2 a TBX4". Genetika zvířat. 34 (4): 307–9. doi:10.1046 / j.1365-2052.2003.01018.x. PMID 12873224.
- Borke JL, Yu JC, Isales CM, Wagle N, Do NN, Chen JR, Bollag RJ (listopad 2003). „Snížení exprese konexinu 43 v kraniálních stezích vyvolané napětím souvisí s transkripční regulací prostřednictvím TBX2“. Annals of Plastic Surgery. 51 (5): 499–504. doi:10.1097 / 01.SAP.0000067964.14122.3E. PMID 14595187. S2CID 21955969.
- Vance KW, Carreira S, Brosch G, Goding CR (březen 2005). „Tbx2 je nadměrně exprimován a hraje důležitou roli při udržování proliferace a potlačení stárnutí u melanomů“. Výzkum rakoviny. 65 (6): 2260–8. doi:10.1158 / 0008-5472.CAN-04-3045. PMID 15781639.
- Bilican B, Goding CR (červenec 2006). "Regulace buněčného cyklu transkripčního faktoru T-box tbx2". Experimentální výzkum buněk. 312 (12): 2358–66. doi:10.1016 / j.yexcr.2006.03.033. PMID 16730707.
externí odkazy
- TBX2 + protein, + člověk v americké národní lékařské knihovně Lékařské předměty (Pletivo)