Etynodiol diacetát - Etynodiol diacetate
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Continuin, Demulen, Femulen, Luteonorm, Luto-Metrodiol, Metrodiol, Ovulen, další |
| Ostatní jména | Ethynodiol diacetát; Norethindrol diacetát; 3p-hydroxynorethisteron 3p, 17p-diacetát;[1] 17a-Ethynylestr-4-en-3p, 17p-diyl diacetát; CB-8080; SC-11800 |
| Trasy z správa | Pusou |
| Třída drog | Progestogen; Progestin; Ester progestogenu |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Identifikátory | |
| |
| Číslo CAS |
|
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.005.496 |
| Chemické a fyzikální údaje | |
| Vzorec | C24H32Ó4 |
| Molární hmotnost | 384.516 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
Etynodiol diacetátnebo ethynodiol diacetát, prodávané pod obchodními názvy Demulen a Femulen mimo jiné je a progestin léky, které se používají v antikoncepční pilulky.[2][3][4] Lék je k dispozici pouze v kombinaci s estrogen.[5] Je to přijato pusou.[6]
Etynodiol diacetát je progestin nebo syntetický progestogen, a proto je agonista z receptor progesteronu, biologický cíl progestogenů jako progesteron.[7][8] Má slabé androgenní a estrogenní činnost a žádné další důležité hormonální aktivita.[9][10][11] Léčba je a proléčivo z norethisteron v těle, s etynodiol vyskytující se jako středně pokročilí.[7][8][12]
Etynodiol, příbuzná sloučenina, byl objeven v roce 1954 a etynodiol diacetát byl zaveden pro lékařské použití v roce 1965.[13][14] Léky jsou dnes dostupné pouze v EU Spojené státy, Kanada a několik dalších zemí.[4][5]
Lékařské použití
Etynodiol diacetát se používá v kombinaci s estrogen jako ethinylestradiol nebo mestranol v kombinované orální antikoncepce pro ženy.[6]
Vedlejší efekty
Farmakologie

Etynodiol diacetát je z hlediska prakticky neaktivní afinita pro progesteron a androgenní receptory a působí jako rychle se měnící proléčivo z norethisteron, s etynodiol vyskytující se jako středně pokročilí.[7][8][12] Na ústní podání a během metabolismus prvního průchodu v játra, etynodiol diacetát se rychle převádí na esterázy do etynodiolu,[12] po kterém následuje okysličování C3 hydroxylová skupina produkovat norethisteron.[8] Kromě své progestogenní aktivity má etynodiol diacetát slabý androgenní aktivita,[9][10] a na rozdíl od většiny progestinů, ale podobně jako norethisteron a noretynodrel,[15] také nějaké má estrogenní aktivita.[10][11]
The farmakokinetika etynodiol diacetátu byly přezkoumány.[16]
| Sloučenina | TypA | PR | AR | ER | GR | PAN | SHBG | CBG |
|---|---|---|---|---|---|---|---|---|
| Norethisteron | – | 67–75 | 15 | 0 | 0–1 | 0–3 | 16 | 0 |
| 5α-dihydronorethisteron | Metabolit | 25 | 27 | 0 | 0 | ? | ? | ? |
| 3α, 5α-tetrahydronorethisteron | Metabolit | 1 | 0 | 0–1 | 0 | ? | ? | ? |
| 3α, 5β-Tetrahydronorethisteron | Metabolit | ? | 0 | 0 | ? | ? | ? | ? |
| 3β, 5a-tetrahydronorethisteron | Metabolit | 1 | 0 | 0–8 | 0 | ? | ? | ? |
| Ethinylestradiol | Metabolit | 15–25 | 1–3 | 112 | 1–3 | 0 | 0.18 | 0 |
| Norethisteron-acetát | Proléčivo | 20 | 5 | 1 | 0 | 0 | ? | ? |
| Norethisteron enanthate | Proléčivo | ? | ? | ? | ? | ? | ? | ? |
| Noretynodrel | Proléčivo | 6 | 0 | 2 | 0 | 0 | 0 | 0 |
| Etynodiol | Proléčivo | 1 | 0 | 11–18 | 0 | ? | ? | ? |
| Etynodiol diacetát | Proléčivo | 1 | 0 | 0 | 0 | 0 | ? | ? |
| Lynestrenol | Proléčivo | 1 | 1 | 3 | 0 | 0 | ? | ? |
| Poznámky: Hodnoty jsou procenta (%). Odkaz ligandy (100%) byly promegeston pro PR, metribolon pro AR, estradiol pro ER, dexamethason pro GR, aldosteron pro PAN, dihydrotestosteron pro SHBG, a kortizol pro CBG. Poznámky pod čarou: A = Aktivní nebo neaktivní metabolit, proléčivo nebo ani norethisteron. Zdroje: Viz šablona. | ||||||||
Chemie
Etynodiol diacetát, také známý jako 3β-hydroxy-17α-ethynyl-19-nortestosteron 3β, 17β-diaceaát, 3β-hydroxynorethisteron 3β, 17β-diacetát nebo 17α-ethynylestr-4-en-3β, 17β-diol 3β, 17β- diacetát, je a syntetický estrane steroid a a derivát z testosteron.[1][3][4] Jedná se konkrétně o derivát 19-nortestosteron a 17α-ethynyltestosteron nebo norethisteron (17α-ethynyl-19-nortestosteron), ve kterém je C3 keton skupina byl dehydrogenovaný do C3β hydroxyl skupina a acetát estery byly připojeny v polohách C3β a C17p.[3][4] Etynodiol diacetát je 3β, 17β-diacetát ester z etynodiol (17a-ethynylestr-4-en-3p, 17p-diol).[3][4]
Syntéza
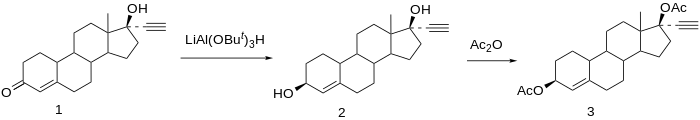
Chemické syntézy etynodiol diacetátu.[16]
Snížení norethisteron (1) poskytuje 3,17-diol. 3β-hydroxy sloučenina je požadovaný produkt; protože reakce na C3 neukazují téměř stereoselektivita jako u C17 na základě relativního nedostatku stereofonních přímých substituentů je tvorba požadovaného isomeru vyvolána použitím objemného redukčního činidla, lithium tri-terc-butoxyaluminium hydridu. Acetylace 3β, 17β-diolu poskytuje ethynodiol diacetát (3).[17]
Dějiny
Etynodiol byl první syntetizován v roce 1954, přes snížení z norethisteron a etynodiol diacetát byl zaveden pro lékařské použití v roce 1965.[13][14]
Společnost a kultura
Obecné názvy
Etynodiol diacetát je druhové jméno drogy ( HOSPODA jeho volné formy alkoholu je etynodiol), zatímco ethynodiol diacetát je jeho USAN, ZÁKAZ, a JAN.[3][4][5] Je také známý svými dřívějšími vývojovými kódovými jmény CB-8080 a SC-11800.[3][4][5]
Názvy značek
Etynodiol diacetát je nebo byl uveden na trh pod obchodními značkami jako Conova, Continuin, Demulen, Femulen, Kelnor, Luteonorm, Luto-Metrodiol, Metrodiol, Ovulen, Soluna, Zovia a další.[3][4][5]
Dostupnost
Etynodiol diacetát zůstává na trhu pouze v několika zemích, včetně EU Spojené státy, Kanada, Argentina, a Omán.[5]
Reference
- ^ A b Schindler, Adolf E; Campagnoli, Carlo; Druckmann, René; Huber, Johannes; Pasqualini, Jorge R; Schweppe, Karl W; Thijssen, Jos H.H (2003). "Klasifikace a farmakologie progestinů". Maturitas. 46: 7–16. doi:10.1016 / j.maturitas.2003.09.014. ISSN 0378-5122. PMID 14670641.
- ^ Donna Shoupe; Florence P. Haseltine (6. prosince 2012). Antikoncepce. Springer Science & Business Media. str. 21–. ISBN 978-1-4612-2730-4.
- ^ A b C d E F G J. Elks (14. listopadu 2014). Slovník léčiv: Chemická data: Chemická data, struktury a bibliografie. Springer. str. 522–. ISBN 978-1-4757-2085-3.
- ^ A b C d E F G h Index Nominum 2000: International Drug Directory. Taylor & Francis USA. 2000. str. 422. ISBN 978-3-88763-075-1. Citováno 30. května 2012.
- ^ A b C d E F https://www.drugs.com/international/etynodiol.html
- ^ A b Robert W. Blum (22. října 2013). Péče o zdraví adolescentů: Klinické problémy. Elsevierova věda. 216–. ISBN 978-1-4832-7738-7.
- ^ A b C Hammerstein J (1990). „Proléčiva: výhoda nebo nevýhoda?“. Dopoledne. J. Obstet. Gynecol. 163 (6 Pt 2): 2198–203. doi:10.1016 / 0002-9378 (90) 90561-K. PMID 2256526.
- ^ A b C d Pracovní skupina IARC pro hodnocení karcinogenních rizik pro člověka; Světová zdravotnická organizace; Mezinárodní agentura pro výzkum rakoviny (2007). Kombinovaná antikoncepce s estrogenem a progestogenem a kombinovaná menopauzální léčba estrogenem a gestagenem. Světová zdravotnická organizace. str. 146–. ISBN 978-92-832-1291-1.
- ^ A b Armen H. Tashjian; Ehrin J. Armstrong (21. července 2011). Principy farmakologie: Patofyziologické základy farmakoterapie. Lippincott Williams & Wilkins. str. 523–. ISBN 978-1-4511-1805-6.
- ^ A b C Kenneth L. Becker (24. dubna 2001). Principy a praxe endokrinologie a metabolismu. Lippincott Williams & Wilkins. str. 1004. ISBN 978-0-7817-1750-2. Citováno 30. května 2012.
- ^ A b Allan H. Goroll; Albert G. Mulley (27. ledna 2009). Medicína primární péče: Kancelářské hodnocení a řízení dospělého pacienta. Lippincott Williams & Wilkins. str. 876. ISBN 978-0-7817-7513-7. Citováno 30. května 2012.
- ^ A b C Stanczyk FZ (2002). „Farmakokinetika a účinnost progestinů používaných pro hormonální substituční terapii a antikoncepci“. Rev Endocr Metab Disord. 3 (3): 211–24. doi:10.1023 / A: 1020072325818. PMID 12215716. S2CID 27018468.
- ^ A b Pokrok v medicinální chemii. Butterworth-Heinemann. 21. září 2011. s. 180–. ISBN 978-0-08-086256-9.
- ^ A b Nakladatelství William Andrew (22. října 2013). Farmaceutická výrobní encyklopedie, 3. vydání. Elsevier. str. 1516–. ISBN 978-0-8155-1856-3.
- ^ Benno Clemens Runnebaum; Thomas Rabe; Ludwig Kiesel (6. prosince 2012). Ženská antikoncepce: aktualizace a trendy. Springer Science & Business Media. str. 36–. ISBN 978-3-642-73790-9.
- ^ A b Die Gestagene. Springer-Verlag. 27. listopadu 2013. s. 14–15, 286. ISBN 978-3-642-99941-3.
- ^ A b Klimstra, P .; Colton, F. (1967). "Syntéza 3β-hydroxyestr-4-en-17-onu a 3β-hydroxiandrost-4-en-17-onu". Steroidy. 10 (4): 411–424. doi:10.1016 / 0039-128X (67) 90119-5. PMID 6064262.
- ^ Sondheimer, F .; Klibanský, Y. (1959). „Syntéza 3β-hydroxy analogů steroidních hormonů, biologicky aktivní třída sloučenin“. Čtyřstěn. 5: 15–26. doi:10.1016/0040-4020(59)80066-1.
