Androsteron - Androsterone
 | |
 | |
| Klinické údaje | |
|---|---|
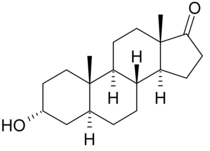
| Ostatní jména | 3α-hydroxy-5α-androstan-17-on, 5α-androstan-3α-ol-17-on |
| ATC kód |
|
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| ChEBI | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.000.159 |
| Chemické a fyzikální údaje | |
| Vzorec | C19H30Ó2 |
| Molární hmotnost | 290.447 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| (ověřit) | |
Androsteronnebo 3α-hydroxy-5α-androstan-17-on, je endogenní steroidní hormon, neurosteroid a domnělý feromon.[1] Je to slabé androgen s potence to je přibližně 1/7 oproti testosteron.[2] Androsteron je metabolit testosteronu a dihydrotestosteron (DHT). Kromě toho jej lze převést zpět na DHT pomocí 3α-hydroxysteroid dehydrogenáza a 17β-hydroxysteroid dehydrogenáza, obcházející konvenční meziprodukty, jako je androstendion a testosteron a jako takový lze považovat za a metabolický meziprodukt v jeho právu.[3][4]
Androsteron je také známý jako inhibiční androstan neurosteroid,[5][6] jednající jako pozitivní alosterický modulátor z GABAA receptor,[7] a vlastní antikonvulzivum účinky.[8] Nepřirozený enantiomer androsteronu je účinnější jako pozitivní alosterický modulátor GABAA receptory a jako antikonvulzivum než přírodní forma.[9] Androsteronův 3β-izomer je epiandrosteron a jeho 5β-epimer je etiocholanolon. 3β, 5p-isomer je epietiocholanolon.
Biologická funkce
Androsteron byl obecně považován za neaktivní metabolit testosteronu, který při konjugaci s glukuronidací a sulfatací umožňuje odstranění testosteronu z těla, ale je to slabý neurosteroid které mohou přejít do mozku a mohou mít vliv na funkci mozku.[8]
Pohled na androsteron jako obecně málo významný se však zdá být třeba přezkoumat ve světle výzkumu 21. století, který naznačuje, že androsteron významně ovlivňuje maskulinizace u plodů savců. Maskulinizace vnějších genitálií u lidí podléhá dihydrotestosteronu (DHT) odvozenému uznávanou androgenní cestou a také prostřednictvím zadní vrátka.[10] Androstandiol může být proto použit jako marker zadní cesty syntézy DHT.[11] Spektrometrické studie identifikují androsteron jako hlavní androgen zadní vrátka u lidského plodu muže. Hladiny v oběhu jsou závislé na pohlaví, přičemž DHT v zásadě chybí u žen, přičemž titry meziproduktů na zadní straně jsou také velmi nízké.[10]
U mužů se meziprodukty zadní vrátka vyskytují hlavně v játrech a nadledvinách plodu a v placentě - ve varlatech téměř vůbec. Místo toho je progesteron v placentě hlavním substrátem pro syntézu androgenu. To je rovněž v souladu s pozorováním, že placentární nedostatečnost byla spojena s narušením vývoje genitálií plodu.[10]
Feromon
Androsteron se nachází v člověku axilla a kůže stejně jako v moč.[12] Může být také vylučován člověkem mazové žlázy.[12] Je popsáno, že má pižmový zápach podobný vůni androstenol.[12] Bylo zjištěno, že androsteron ovlivňuje lidské chování, když je cítit.[12]
Biochemie
Biosyntéza
Androsteron a jeho 5β-izomer, etiocholanolon, se v těle produkují jako metabolity testosteron. Testosteron se převádí na 5α-dihydrotestosteron a 5β-dihydrotestosteron podle 5α-reduktáza a 5β-reduktáza, resp. Enzym 3α-hydroxysteroid dehydrogenáza převede redukované formuláře na 3α-androstandiol a 3β-androstandiol, které následně převádí 17β-hydroxysteroid dehydrogenáza na androsteron a etiocholanolon. Androsteron a etiocholanolon mohou být také vytvořeny z androstendion působením tvorby 5α-reduktázy a 5β-reduktázy 5α-androstandion a 5β-androstandion které se poté převádějí na androsteron a etiocholanolon 3α-hydroxysteroid dehydrogenáza a 3β-hydroxysteroid dehydrogenáza, resp.[8]
Metabolismus
Androsteron je sulfatovaný do androsteron sulfát a glukuronidovaný do androsteron glukuronid a tyto konjugáty jsou vylučován v moč.
Chemie
Zdroje
Ukázalo se, že androsteron se přirozeně vyskytuje v borovice pyl a v mnoha je dobře známý zvíře druh.[13]
Dějiny
Androsteron byl poprvé izolován v roce 1931 autorem Adolf Friedrich Johann Butenandt a Kurt Tscherning. Destilovali více než 17 000 litrů mužské moči (3 700 imp gal; 4 500 US gal), z nichž dostali 50 miligramů (0,77 g) krystalického androsteronu, což stačilo k zjištění, že chemický vzorec byl velmi podobný estron.
Viz také
- Androgenní zadní cesta
- Seznam androgenů / anabolických steroidů
- Seznam neurosteroidů § Androstanes
- Seznam neurosteroidů § Feromony a feriny
Reference
- ^ Motofei, Ion G. (2011). „Dvojí fyziologický charakter pro mozkové mechanismy sexuality a poznávání: běžné somatické periferní aferenty“. BJU International. 108 (10): 1634–1639. doi:10.1111 / j.1464-410X.2011.10116.x. ISSN 1464-4096. PMID 21489118. S2CID 25941894.
- ^ Scott T (1996). Stručná encyklopedie biologie. Walter de Gruyter. p. 49. ISBN 978-3-11-010661-9. Citováno 25. května 2012.
- ^ Henderson BE; Ponder BAJ; Ross RK (13. března 2003). Hormony, geny a rakovina. Oxford University Press. p. 23. ISBN 978-0-19-513576-3. Citováno 25. května 2012.
- ^ Kamrath C, Hochberg Z, Hartmann MF, Remer T, Wudy SA (březen 2012). „Zvýšená aktivace alternativní dráhy„ zadní vrátka “u pacientů s nedostatkem 21-hydroxylázy: důkazy z analýzy steroidních hormonů v moči“. The Journal of Clinical Endocrinology and Metabolism. 97 (3): E367–75. doi:10.1210 / jc.2011-1997. PMID 22170725.
- ^ Reddy DS, Rogawski MA (2012). „Neurosteroidy - endogenní regulátory citlivosti na záchvaty a role v léčbě epilepsie“. In Noebels JL, Avoli M, Rogawski MA a kol. (eds.). Jasperovy základní mechanismy epilepsií [internet]. 4. vydání. Bethesda (MD): Národní centrum pro biotechnologické informace (USA). Národní centrum pro biotechnologické informace (USA).
- ^ Reddy DS (2010). Neurosteroidy: endogenní role v lidském mozku a terapeutické potenciály. Prog. Brain Res. Pokrok ve výzkumu mozku. 186. 113–37. doi:10.1016 / B978-0-444-53630-3.00008-7. ISBN 9780444536303. PMC 3139029. PMID 21094889.
- ^ Li P, Bracamontes J, Katona BW, Covey DF, Steinbach JH, Akk G (červen 2007). „Přírodní a enantiomerní etiocholanolon interaguje s odlišnými místy na krysím alfa1beta2gamma2L receptoru GABAA“. Mol. Pharmacol. 71 (6): 1582–90. doi:10,1124 / mol 106,033407. PMID 17341652. S2CID 44286086.
- ^ A b C Kaminski RM, Marini H, Kim WJ, Rogawski MA (červen 2005). "Antikonvulzivní aktivita androsteronu a etiocholanolonu". Epilepsie. 46 (6): 819–27. doi:10.1111 / j.1528-1167.2005.00705.x. PMC 1181535. PMID 15946323.
- ^ Zolkowska D, Dhir A, Krishnan K, Covey DF, Rogawski MA (září 2014). „Antikonvulzivní účinky enantiomerů neurosteroidů androsteronu a etiocholanolonu převyšují účinky přírodních forem“. Psychofarmakologie. 231 (17): 3325–32. doi:10.1007 / s00213-014-3546-x. PMC 4134984. PMID 24705905.
- ^ A b C O'Shaughnessy PJ, Antignac JP, Le Bizec B, Morvan ML, Svechnikov K, Söder O, Savchuk I, Monteiro A, Soffientini U, Johnston ZC, Bellingham M, Hough D, Walker N, Filis P, Fowler PA (únor 2019 ). „Alternativní (zadní vrátka) produkce androgenu a maskulinizace u lidského plodu“. PLOS Biology. 17 (2): e3000002. doi:10.1371 / journal.pbio.3000002. PMC 6375548. PMID 30763313.
- ^ Rohayem J, Zitzmann M, Laurentino S, Kliesch S, Nieschlag E, Holterhus PM, Kulle A (září 2020). "Role gonadotropinů v testikulárních a adrenálních biosyntézách androgenů - Insights od mužů s vrozeným hypogonadotropním hypogonadismem na hCG / rFSH a na substituci testosteronu". Klinická endokrinologie. doi:10.1111 / cen.14324. PMID 32871622.
- ^ A b C d Maiworm, R.E .; Langthaler, W. U. (1992). Chemické signály u obratlovců 6. str. 575–579. doi:10.1007/978-1-4757-9655-1_88. ISBN 978-1-4757-9657-5.
- ^ Janeczko A, Skoczowski A (2005). "Savčí pohlavní hormony v rostlinách". Folia Histochemica et Cytobiologica. 43 (2): 71–79. PMID 16044944.
