Anabolický steroid - Anabolic steroid
| Anabolické androgenní steroidy | |
|---|---|
| Třída drog | |
 Chemická struktura přírodního AAS testosteron (androst-4-en-17p-ol-3-on). | |
| Identifikátory třídy | |
| Synonyma | Anabolické steroidy; Androgeny |
| Použití | Rozličný |
| ATC kód | A14A |
| Biologický cíl | Androgenní receptor |
| Chemická třída | Steroidy; Androstany; Estranes |
| Klinické údaje | |
| Drugs.com | Třídy drog |
| externí odkazy | |
| Pletivo | D045165 |
| Na Wikidata | |
Anabolické steroidy, také známý více správně jako anabolické androgenní steroidy (AAS),[1] jsou steroidní androgeny které zahrnují přírodní androgeny jako testosteron stejně jako syntetické androgeny, které jsou strukturně příbuzné a mají podobné účinky jako testosteron. Oni jsou anabolický a zvýšit protein v rámci buňky, speciálně v kosterní svalstvo, a také mají různé stupně androgenní a virilizující účinky, včetně vyvolání vývoje a údržby mužský sekundární sexuální charakteristiky jako je růst obličeje a chlupy. Slovo anabolický, s odkazem na anabolismus, pochází z řečtiny ἀναβολή anabole„to, co je vyvrženo, mohyla“. Androgeny nebo AAS jsou jedním ze tří typů agonisté pohlavních hormonů, ostatní jsou estrogeny jako estradiol a progestogeny jako progesteron.
AAS byly syntetizovány ve třicátých letech minulého století a nyní se terapeuticky používají v medicíně ke stimulaci růstu svalů a chuť, přimět muže puberta a léčit chronické plýtvání podmínky, jako např rakovina a AIDS. The Americká vysoká škola sportovní medicíny uznává, že AAS za přítomnosti přiměřené stravy může přispět ke zvýšení tělesná hmotnost, často s nárůstem štíhlé hmoty a nárůstem v svalová síla dosažené pomocí vysoce intenzivního cvičení a správné stravy lze u některých jedinců dodatečně zvýšit použitím AAS.[2]
Zdravotní rizika mohou být vyvolána dlouhodobým užíváním nebo nadměrnými dávkami AAS.[3][4] Mezi tyto účinky patří škodlivé změny v cholesterol úrovně (zvýšené lipoprotein s nízkou hustotou a snížil se lipoprotein s vysokou hustotou ), akné, vysoký krevní tlak, poškození jater (hlavně u většiny orálních AAS) a nebezpečné změny ve struktuře levá komora z srdce.[5] Tato rizika se dále zvyšují, když sportovci, jak to často dělají, užívají steroidy spolu s jinými léky, což způsobuje podstatně větší poškození jejich těl.[6] Účinek anabolických steroidů na srdce může způsobit infarkt myokardu a tahy.[6] Podmínky týkající se hormonální nerovnováha jako gynekomastie a zmenšení velikosti varlat může být také způsoben AAS.[7] U žen a dětí může AAS způsobit nevratnost maskulinizace.[7]
Ergogenní použití pro AAS ve sportu, závodění, a kulturistika tak jako léky zvyšující výkon jsou kontroverzní kvůli jejich nepříznivým účinkům a potenciálu získat nespravedlivou výhodu ve fyzických soutěžích. Jejich použití se označuje jako doping a zakázáno většinou hlavních sportovních subjektů. Sportovci hledali drogy, aby zvýšili své atletické schopnosti, od zahájení olympijských her ve starověkém Řecku.[6] Po mnoho let byly AAS zdaleka nejvíce zjištěnými dopingovými látkami MOV -akreditované laboratoře.[8][9] V zemích, kde jsou AAS regulované látky, často existuje Černý trh ve kterých se pašovalo, tajně vyrábělo nebo dokonce padělané drogy jsou prodávány uživatelům.
Použití
Lékařský
Od objevu a syntézy testosteronu ve třicátých letech minulého století používají lékaři AAS k mnoha účelům s různou mírou úspěchu. Ty lze obecně rozdělit na anabolické, androgenní a další použití.
Anabolické
- Kostní dřeň stimulace: Po celá desetiletí byly AAS základem léčby hypoplastický anémie kvůli leukémie, selhání ledvin nebo aplastická anémie.[10]
- Růst stimulace: AAS může být použit dětských endokrinologů zacházet s dětmi selhání růstu.[11] Nicméně, dostupnost syntetických růstový hormon, který má méně nežádoucích účinků, z něj dělá sekundární léčbu.
- Stimulace chuť a zachování a zvýšení sval mše: AAS byly dány lidem s chronické plýtvání jako rakovina a AIDS.[12][13]
- Stimulace svalové hmoty a prevence úbytek kostní hmoty u starších mužů, jak naznačují některé studie.[14][15][16] Avšak placebem kontrolovaná studie z roku 2006 s doplňováním nízkých dávek testosteronu u starších mužů s nízkou hladinou testosteronu však nezjistila žádný přínos pro složení těla, fyzický výkon, citlivost na inzulín nebo kvalita života.[17]
- Prevence nebo léčba osteoporóza v postmenopauzální ženy.[18][19] Nandrolon dekanoát je pro toto použití schválen.[20] Ačkoliv byly pro tuto indikaci indikovány, AAS viděl velmi malé použití pro tento účel kvůli jejich virilizujícím vedlejším účinkům.[18][21]
- Pomoc přibývání na váze Následující chirurgická operace nebo fyzické trauma, v době chronická infekce, nebo v kontextu nevysvětlených ztráta váhy.[22][23]
- Působí proti katabolický dlouhodobý účinek kortikosteroidy terapie.[22][23]
- Oxandrolon zlepšuje krátkodobé i dlouhodobé výsledky u lidí zotavujících se z těžkých popálenin a je dobře zaveden jako bezpečná léčba této indikace.[24][25]
- Léčba idiopatický nízký vzrůst, dědičný angioedém, alkoholická hepatitida, a hypogonadismus.[26][27]
- Methyltestosteron se používá k léčbě opožděná puberta, hypogonadismus, kryptorchismus, a erektilní dysfunkce u mužů a v nízkých dávkách k léčbě menopauzální příznaky (konkrétně pro osteoporóza, návaly horka a zvýšit libido a energie ), po porodu bolest prsou a překrvení, a rakovina prsu u žen.[28][29][30]
Androgenní
- Androgenní substituční terapie pro muže s nízké hladiny testosteronu; také účinné při zlepšování libida u starších mužů.[31][32][33][34]
- Vyvolání muže puberta: Androgeny se dávají mnoha extrémně zoufalým chlapcům zpoždění puberty. Testosteron je nyní téměř jediným androgenem používaným pro tento účel a bylo prokázáno, že zvyšuje výšku, váhu a beztukovou hmotu u chlapců se zpožděnou pubertou.[35]
- Maskulinizační hormonální terapie pro transgender muži, jiný transmaskulin lidé a intersex lidí tím, že produkuje mužské sekundární sexuální vlastnosti, jako je a prohlubování hlasu, zvýšená kostní a svalová hmota, distribuce mužského tuku, vlasy na obličeji a na těle a zvětšení klitorisu, stejně jako duševní změny, jako je zmírnění genderová dysforie a zvýšený sexuální apetit.[36][37][38][39][40]
jiný
- Léčba rakovina prsu u žen, i když jsou nyní pro tento účel velmi zřídka používány kvůli jejich výrazným virilizujícím vedlejším účinkům.[41][18][42]
- V nízkých dávkách jako součást hormonální terapie pro postmenopauzální a transgender ženy, například zvýšit energie, pohoda, libido, a kvalita života, stejně jako ke snížení návaly horka.[43][44][45][46] Pro tento účel se obvykle používá testosteron methyltestosteron je také používán.[46][47]
- Mužská hormonální antikoncepce; v současné době experimentální, ale potenciál pro použití jako efektivní, bezpečná, spolehlivá a reverzibilní mužská antikoncepce.[48]
Zvýšení výkonu

Většina uživatelů steroidů nejsou sportovci.[49] Ve Spojených státech se předpokládá, že AAS používaly 1 milion až 3 miliony lidí (1% populace).[50] Studie ve Spojených státech ukázaly, že uživatelé AAS bývají většinou střední třídy heterosexuální muži s medián ve věku kolem 25 let, kteří jsou nekompetitivní kulturisté a ne-sportovci a užívají tyto drogy pro kosmetické účely.[51] „U chlapců ve věku 12 až 17 let užívání steroidů a podobných drog vyskočilo v letech 1999 až 2000 o 25 procent, přičemž 20 procent uvedlo, že je užívají spíše pro vzhled než pro sport, zjistila studie pojišťovny Blue Cross Blue Shield.“ (Eisenhauer) Další studie zjistila, že nelékařské použití AAS mezi studenty vysokých škol bylo na nebo méně než 1%.[52] Podle nedávného průzkumu bylo 78,4% uživatelů steroidů nekonkurenceschopných kulturistů a ne-sportovců, zatímco přibližně 13% uvedlo nebezpečné injekční postupy, jako je opakované použití jehel, sdílení jehel a sdílení vícedávkových lahviček,[53] ačkoli studie z roku 2007 zjistila, že sdílení jehel bylo mezi osobami používajícími AAS pro jiné než lékařské účely extrémně neobvyklé, méně než 1%.[54] Další studie z roku 2007 zjistila, že 74% nelékařských uživatelů AAS mělo postsekundární vzdělání a více absolvovalo vysokou školu a méně z nich nedokončilo střední školu, než se od běžné populace očekává.[54] Stejná studie zjistila, že jednotlivci využívající AAS k jiným než lékařským účelům měli vyšší míru zaměstnanosti a vyšší příjem domácnosti než běžná populace.[54] Uživatelé AAS mají tendenci zkoumat léky, které užívají, více než ostatní uživatelé kontrolovaných látek; Mezi hlavní zdroje konzultované uživateli steroidů však patří přátelé, nelékařské příručky, internetová fóra, blogy a fitness časopisy, které mohou poskytovat pochybné nebo nepřesné informace.[55]
Uživatelé AAS bývají nespokojeni s tím, jak jsou AAS v médiích a v politice smrtící.[56] Podle jedné studie uživatelé AAS také nedůvěřují svým lékařům a ve vzorku 56% neprozradilo jejich použití AAS svým lékařům.[57] Další studie z roku 2007 měla podobná zjištění, která ukazují, že zatímco 66% osob užívajících AAS k jiným než lékařským účelům bylo ochotných vyhledat lékařský dohled nad užíváním steroidů, 58% nemělo důvěru ve své lékaře, 92% mělo pocit, že znalost lékařské komunity o nelékařské užívání AAS chybělo a 99% se domnívalo, že veřejnost má přehnaný názor na vedlejší účinky užívání AAS.[54] Nedávná studie také ukázala, že u dlouhodobých uživatelů AAS se častěji vyskytly příznaky svalová dysmorfie a také ukázal silnější podporu konvenčnějších mužských rolí.[58] Nedávná studie v časopise Journal of Health Psychology ukázala, že mnoho uživatelů věřilo, že steroidy užívané s mírou jsou bezpečné.[59]
AAS byly používány muži a ženami v mnoha různých druzích profesionálních sportů k dosažení konkurenční výhody nebo jako pomoc při zotavení ze zranění. Mezi tyto sporty patří kulturistika, vzpírání, vrh koulí a další atletický, cyklistika, baseball, zápas, kombinovaná bojová umění, box, Fotbal, a kriket. Takové použití je zakázáno pravidly řídících orgánů většiny sportů. Užívání AAS se vyskytuje u dospívajících, zejména u těch, kteří se účastní závodních sportů. Bylo navrženo, že prevalence užívání mezi studenty středních škol v USA může dosahovat až 2,7%.[60] Studenti mužského pohlaví užívali AAS častěji než studentky a ti, kteří se účastnili sportu, užívali v průměru častěji steroidy než ti, kteří ne.
Dávky
| Léky | Trasa | Rozsah dávkování[A] | ||
|---|---|---|---|---|
| Danazol | Ústní | 100–800 mg / den | ||
| Drostanolon propionát | Injekce | 100 mg 3x týdně | ||
| Ethylestrenol | Ústní | 2–8 mg / den | ||
| Fluoxymesteron | Ústní | 2–40 mg / den | ||
| Mesterolon | Ústní | 25–150 mg / den | ||
| Metandienon | Ústní | 2,5–15 mg / den | ||
| Metenolon-acetát | Ústní | 10–150 mg / den | ||
| Metenolon enanthate | Injekce | 25–100 mg / týden | ||
| Methyltestosteron | Ústní | 1,5–200 mg / den | ||
| Nandrolon dekanoát | Injekce | 12,5–200 mg / týden[b] | ||
| Nandrolon fenylpropionát | Injekce | 6,25–200 mg / týden[b] | ||
| Norethandrolon | Ústní | 20–30 mg / den | ||
| Oxandrolon | Ústní | 2,5–20 mg / den | ||
| Oxymetholon | Ústní | 1–5 mg / kg / den nebo 50–150 mg / den | ||
| Stanozolol | Ústní | 2–6 mg / den | ||
| Injekce | 50 mg až každé dva týdny | |||
| Testosteron | Ústní[C] | 400–800 mg / den[b] | ||
| Injekce | 25–100 mg až třikrát týdně | |||
| Testosteron cypionát | Injekce | 50–400 mg až každé čtyři týdny | ||
| Testosteron enanthát | Injekce | 50–400 mg až každé čtyři týdny | ||
| Testosteron propionát | Injekce | 25–50 mg až třikrát týdně | ||
| Testosteron undekanoát | Ústní | 80-240 mg / den[b] | ||
| Injekce | 750–1000 mg až každých 10 týdnů | |||
| Trenbolon HBC | Injekce | 75 mg každých 10 dní | ||
| Zdroje: [61][62][63][64][18][65][66][67][68][69] | ||||
Dostupné formuláře
AAS, které se v medicíně používají nejčastěji, jsou testosteron a jeho mnoho estery (ale nejčastěji testosteron undekanoát, testosteron enanthate, testosteron cypionate, a testosteron propionát ),[70] nandrolon estery (typicky nandrolon dekanoát a nandrolon fenylpropionát ), stanozolol, a metandienon (methandrostenolon).[1] Mezi další, které jsou také běžně dostupné a používané, ale v menší míře, patří methyltestosteron, oxandrolon, mesterolon, a oxymetholon, stejně jako drostanolon propionát (dromostanolon propionát), metenolon estery (methylandrostenolonu) (konkrétně metenolon-acetát a metenolon enanthate ), a fluoxymesteron.[1] Dihydrotestosteron (DHT), známý jako androstanolon nebo stanolon při lékařském použití, a jeho estery jsou také pozoruhodné, i když se v medicíně příliš nepoužívají.[66] Boldenon undecylenate a trenbolon-acetát jsou používány v veterinární medicína.[1]
Značkové steroidy jsou AAS, které nebyly schváleny a uvedeny na trh pro lékařské použití, ale byly distribuovány prostřednictvím černého trhu.[71] Mezi příklady pozoruhodných značkových steroidů patří 1-testosteron (dihydroboldenon), methasteron, trenbolon enanthate, desoxymethyltestosteron, tetrahydrogestrinon, a methylstenbolon.[71]
Cesty podávání

Existují čtyři běžné formy podávání AAS: perorální pilulky; injekční steroidy; krémy / gely pro lokální aplikaci; a kožní náplasti. Nejvýhodnější je orální podání. Testosteron podávaný ústy se rychle vstřebává, ale do značné míry se přeměňuje na neaktivní metabolity a v aktivní formě je k dispozici pouze asi šestina. Aby byly dostatečně aktivní, pokud jsou podávány ústy, jsou deriváty testosteronu alkylovány v poloze 17a, např. methyltestosteron a fluoxymesteron. Tato modifikace snižuje schopnost jater rozkládat tyto sloučeniny dříve, než dosáhnou systémového oběhu.
Testosteron lze podávat parenterálně, ale má nepravidelnější prodlouženou dobu vstřebávání a větší aktivitu ve svalu enanthate, undecanoate nebo cypionát ester formulář. Tyto deriváty jsou hydrolyzovány, aby uvolňovaly volný testosteron v místě injekce; míra absorpce (a tedy i schéma vstřikování) se u různých esterů liší, ale lékařské injekce se obvykle provádějí kdekoli mezi polotýdnem a jednou za 12 týdnů. Může být žádoucí častější plán, aby se v systému udržovala konstantní hladina hormonu.[72] Injekční steroidy se obvykle podávají do svalu, nikoli do žíly, aby se zabránilo náhlým změnám v množství léčiva v krvi. Navíc, protože esterifikovaný testosteron je rozpuštěn v oleji, může intravenózní injekce způsobit nebezpečnost embolie (sraženina) v krevním řečišti.
Transdermální náplasti (adhezivní náplasti umístěné na kůži) lze také použít k podání stálé dávky kůží a do krevního řečiště. K dispozici jsou také krémy a gely obsahující testosteron, které se denně aplikují na pokožku, ale absorpce je neúčinná (zhruba 10%, u jednotlivých jedinců) a tato ošetření bývají nákladnější. Osoby, které jsou obzvláště fyzicky aktivní a / nebo se koupou, často nemusí být dobrými kandidáty, protože léky mohou být vypláchnuty a může trvat až šest hodin, než se úplně vstřebají. Existuje také riziko, že intimní partner nebo dítě může přijít do styku s místem aplikace a nechtěně si dávkovat; děti a ženy jsou vysoce citlivé na testosteron a mohou trpět nezamýšlenou maskulinizací a účinky na zdraví, a to i při malých dávkách. Injekce je nejběžnější metoda používaná osobami, které podávají AAS pro jiné než lékařské účely.[54]
Tradiční způsoby podávání nemají rozdílné účinky na účinnost léku. Studie ukazují, že anabolické vlastnosti AAS jsou relativně podobné navzdory rozdílům ve farmakokinetických principech, jako je metabolismus prvního průchodu. Orálně dostupné formy AAS však mohou způsobit poškození jater ve vysokých dávkách.[9][73]
Nepříznivé účinky
Známo možné vedlejší efekty AAS zahrnují:[7][74][75][76][77]
- Dermatologické /integumentální: mastná pleť, akné vulgaris, akné conglobata, seborrhea, strie (kvůli rychlému zvětšení svalů ), hypertrichóza (nadměrný růst ochlupení na těle), androgenní alopecie (vypadávání vlasů; plešatost pokožky hlavy), zadržování tekutin /otok.
- Reprodukční /endokrinní: libido změny, reverzibilní neplodnost, hypogonadotropní hypogonadismus.
- Specifické pro muže: spontánní erekce, noční emise, priapismus, erektilní dysfunkce, gynekomastie (většinou pouze s aromatizovatelný a tudíž estrogenní AAS), oligospermie /azoospermie, atrofie varlat, intratestikulární leiomyosarkom, hypertrofie prostaty, rakovina prostaty.
- Specifické pro ženy: maskulinizace, nevratné prohlubování hlasu, hirsutismus (nadměrný růst vlasů na obličeji / těle), menstruační poruchy (např., anovulace, oligomenorea, amenorea, dysmenorea ), zvětšení klitorisu, atrofie prsu, atrofie dělohy, teratogenita (u žen plody ).
- Specifické pro dítě: předčasné uzávěr epifýzy a související nízký vzrůst, předčasná puberta u chlapců, opožděná puberta a contrasexual precocity u dívek.
- Psychiatrické /neurologický: změny nálady, podrážděnost, agrese, násilné chování, impulzivita /bezohlednost, hypomanie /mánie, euforie, Deprese, úzkost, dysforie, sebevražednost, bludy, psychóza, vybrání, závislost, neurotoxicita, kognitivní porucha.[78][79]
- Muskuloskeletální: svalová hypertrofie, svalové napětí, prasknutí šlachy, rhabdomyolýza.
- Kardiovaskulární: dyslipidemie (např. zvýšené LDL úrovně, snížené HDL úrovně, snížené apo-A1 úrovně), ateroskleróza, hypertenze, hypertrofie levé komory, kardiomyopatie, hypertrofie myokardu, polycytémie /erytrocytóza, arytmie, trombóza (např., embolie, mrtvice ), infarkt myokardu, nenadálá smrt.[80][81]
- Jaterní: zvýšené jaterní funkční testy (AST, ALT, bilirubin, LDH, HORSKÁ PASTVINA ), hepatotoxicita, žloutenka, jaterní steatóza, hepatocelulární adenom, hepatocelulární karcinom, cholestáza, peliosis hepatis; všechny většinou nebo výhradně s 17α-alkylovaným AAS.[82]
- Renální: hypertrofie ledvin, nefropatie, akutní selhání ledvin (sekundární k rhabdomyolýze), fokální segmentová glomeruloskleróza, karcinom ledvin.
- Ostatní: intolerance glukózy, rezistence na inzulín, imunitní dysfunkce.[83]
Fyziologický
V závislosti na délce užívání drog existuje možnost poškození imunitního systému. Většina z těchto nežádoucích účinků závisí na dávce, nejčastější jsou zvýšené krevní tlak, zejména u pacientů s již existujícími hypertenze.[84] Kromě morfologických změn srdce, které mohou mít trvalý nepříznivý vliv na kardiovaskulární účinnost.
Ukázalo se, že AAS mění testy tolerance cukru a glukózy nalačno.[85] AAS, jako je testosteron, také zvyšují riziko kardiovaskulární onemocnění[3] nebo ischemická choroba srdeční.[86][87] Akné je docela běžný mezi uživateli AAS, většinou kvůli stimulaci mazové žlázy zvýšenou hladinou testosteronu.[8][88] Konverze testosteronu na DHT může urychlit rychlost předčasného plešatost u mužů s genetickou predispozicí, ale samotný testosteron může u žen způsobit plešatost.[89]
Pokud dospívající používá AAS, může se objevit řada závažných nežádoucích účinků. Například AAS může předčasně zastavit prodloužení kostí (předčasné fúze epifýzy prostřednictvím zvýšené úrovně estrogen metabolity ), což má za následek nedostatečným růstem. Mezi další efekty patří mimo jiné zrychlení zrání kostí, zvýšená frekvence a doba trvání erekce a předčasný sexuální vývoj. Použití AAS v dospívání je také korelovaný s horšími postoji souvisejícími se zdravím.[90]
Rakovina
Organizace WHO Mezinárodní agentura pro výzkum rakoviny (IARC) seznam AAS pod Skupina 2A: Pravděpodobně karcinogenní pro člověka.[91]
Kardiovaskulární
Další vedlejší účinky mohou zahrnovat změny ve struktuře srdce, jako zvětšení a zesílení levé komory, což zhoršuje jeho kontrakci a relaxace, a tedy snížení objemu vysunuté krve.[5] Možné účinky těchto změn v srdci jsou hypertenze, srdeční arytmie, městnavé srdeční selhání, infarkty, a náhlá srdeční smrt.[92] Tyto změny lze pozorovat také u pacientů, kteří neužívají drogy sportovci, ale užívání steroidů může tento proces urychlit.[93][94] Byla však zpochybněna souvislost mezi změnami ve struktuře levé komory a sníženou srdeční funkcí, jakož i souvislost s užíváním steroidů.[95][96]
Použití AAS může způsobit škodlivé změny v systému Windows cholesterol úrovně: Některé steroidy způsobují zvýšení LDL „špatný“ cholesterol a pokles v HDL „dobrý“ cholesterol.[97]
Poruchy růstu
Užívání AAS u dospívajících zrychluje zrání kostí a ve vysokých dávkách může snížit výšku dospělých.[Citace je zapotřebí ] Nízké dávky AAS jako např oxandrolon se používají při léčbě idiopatický nízký vzrůst, ale to může pouze urychlit zrání, spíše než zvyšovat výšku dospělých.[98]
Feminizace

Existují také vedlejší účinky AAS specifické pro pohlaví. Vývoj prsní tkáně u mužů, stav zvaný gynekomastie (což je obvykle způsobeno vysokou úrovní oběhu estradiol ), mohou nastat kvůli zvýšené přeměně testosteronu na estradiol enzymem aromatáza.[99] Snížené sexuální funkce a dočasné neplodnost může se vyskytnout také u mužů.[100][101][102] Dalším vedlejším účinkem specifickým pro muže, který se může objevit, je atrofie varlat způsobené potlačením přirozené hladiny testosteronu, které inhibuje produkce spermií (většina z varlat vyvíjí spermie). Tento vedlejší účinek je dočasný; velikost varlat se obvykle vrátí k normálu během několika týdnů po ukončení užívání AAS, protože se obnoví normální produkce spermií.[103]
Maskulinizace
Mezi nežádoucí účinky specifické pro ženy patří zvýšení ochlupení na těle, trvalé prohlubování hlasu, zvětšený klitoris a dočasný pokles v% menstruační cykly. Změna plodnost a ovariální cysty se mohou vyskytnout také u žen.[104] Pokud je užíván během těhotenství, AAS může ovlivnit vývoj plodu vyvoláním vývoje mužských rysů u ženského plodu a ženských rysů u mužského plodu.[105]
Problémy s ledvinami
Testy na ledviny odhalily, že devět z deseti uživatelů steroidů vyvinulo stav zvaný fokální segmentová glomeruloskleróza, druh jizvy v ledvinách. Poškození ledvin u kulturistů má podobnost s poškozením u morbidně obézních pacientů, ale zdá se být ještě závažnější.[106]
Problémy s játry
Mohou způsobit vysoké dávky orálních sloučenin AAS poškození jater.[4] Peliosis hepatis byl s využitím AAS stále více uznáván.
Neuropsychiatrické

Recenze z roku 2005 v Léky na CNS rozhodl, že „významné psychiatrické příznaky včetně agrese a násilí, mánie a méně často psychóza a sebevražda byly spojeny se steroidy zneužívání. U dlouhodobě zneužívajících steroidů se mohou objevit příznaky závislost a vybrání o ukončení AAS ".[79] Produkují vysoké koncentrace AAS, srovnatelné s těmi, které pravděpodobně utrpí mnoho rekreačních uživatelů AAS apoptotický účinky na neurony,[Citace je zapotřebí ] zvyšování spektra možné nevratné neurotoxicity. Rekreační užívání AAS se zdá být spojeno s řadou potenciálně prodloužených psychiatrických účinků, včetně syndromů závislosti, poruchy nálady a postup k dalším formám zneužívání návykových látek, ale prevalence a závažnost těchto různých účinků zůstává špatně pochopena.[108] Neexistují žádné důkazy, ze kterých se vyvíjí závislost na steroidech terapeutický užívání AAS k léčbě zdravotních poruch, ale u vzpěračů a kulturistů, kteří chronicky podávali suprafyziologické dávky, byly hlášeny případy závislosti na AAS.[109] Poruchy nálady (např. Deprese, [hypo-] mánie, psychotické rysy) budou pravděpodobně závislé na dávce a drogách, ale zdá se, že závislost na AAS nebo abstinenční účinky se vyskytují pouze u malého počtu uživatelů AAS.[8]
Dlouhodobé rozsáhlé studie psychiatrických účinků na uživatele AAS nejsou v současné době k dispozici.[108] V roce 2003 zjistila první naturalistická dlouhodobá studie na deseti uživatelích, z nichž sedm dokončilo studii, vysoký výskyt poruch nálady a zneužívání návykových látek, ale během studie bylo zaznamenáno jen málo klinicky významných změn ve fyziologických parametrech nebo laboratorních opatřeních, a tyto změny jednoznačně nesouvisely s obdobími uváděného použití AAS.[110] 13měsíční studie, která byla zveřejněna v roce 2006 a která zahrnovala 320 kulturistů a sportovců, naznačuje, že široká škála psychiatrických vedlejších účinků vyvolaných užíváním AAS souvisí se závažností zneužívání.[111]
Diagnostické statistické manuální tvrzení
DSM-IV seznamy Obecná diagnostická kritéria pro pokyn týkající se poruchy osobnosti, že „Tento vzorec nelze lépe považovat za projev jiné duševní poruchy nebo za přímé fyziologické účinky látky (např. drogy nebo léky) nebo celkového zdravotního stavu (např. úraz hlavy).“ . Výsledkem je, že uživatelé AAS mohou být špatně diagnostikováni psychiatrem, který jim neřekl o svém zvyku.[112]
Profily osobnosti
Cooper, Noakes, Dunne, Lambert a Rochford zjistili, že u jedinců užívajících AAS je vyšší pravděpodobnost hranice (4,7krát), asociální (3,8krát), paranoidní (3,4krát), schizotypní (3,1krát), teatrální (2,9krát), pasivně agresivní (2,4krát) a narcistický (1,6krát) profily osobnosti než nepoužívající uživatelé.[113] Další studie naznačují, že antisociální porucha osobnosti je o něco pravděpodobnější u uživatelů AAS než u neužívajících (Pope & Katz, 1994).[112] Bipolární dysfunkce,[114] závislost na látce, a porucha chování byly také spojeny s používáním AAS.[115]
Nálada a úzkost
Afektivní poruchy jsou již dlouho považovány za komplikaci užívání AAS. Případové zprávy popisují hypománii i mánii, spolu s podrážděností, euforií, nedbalostí, závodními myšlenkami a pocity síly a neporazitelnosti, které nesplňovaly kritéria pro mánii / hypománii.[116] Z 53 kulturistů, kteří užívali AAS, 27 (51%) uvedlo nespecifikovanou poruchu nálady.[117]
Agrese a hypomanie
Od poloviny 80. let média sdělovala „roid rage“ jako vedlejší účinek AAS.[118]:23
Recenze z roku 2005 zjistila, že některé, ale ne všechny, randomizované kontrolované studie zjistily, že použití AAS koreluje s hypomanie a zvýšená agresivita, ale poukázal na to, že pokusy určit, zda užívání AAS spouští násilné chování, selhaly, zejména kvůli vysoké míře neúčasti.[119] Studie z roku 2008 na celostátně reprezentativním vzorku mladých dospělých mužů ve Spojených státech zjistila souvislost mezi celoživotním užíváním AAS za poslední rok a účastí na násilných činech. Ve srovnání s jedinci, kteří neužívali steroidy, uváděli mladí dospělí muži, kteří užívali AAS, větší zapojení do násilného chování i po kontrole účinků klíčových demografických proměnných, předchozího násilného chování a užívání více drog.[120] Přezkum z roku 1996 zkoumající slepé studie v té době k dispozici také zjistili, že prokázali souvislost mezi agresí a užíváním steroidů, ale poukázali na to, že s odhady více než jednoho milionu minulých nebo současných uživatelů steroidů v USA v té době se extrémně malé procento uživatelů užívajících steroidy objevuje trpět natolik závažnými duševními poruchami, které by vyústily v klinickou léčbu nebo lékařské případové zprávy.[121]
1996 randomizovaná kontrolovaná studie, který zahrnoval 43 mužů, nezjistil nárůst výskytu rozzlobeného chování během 10 týdnů podávání testosteron enanthate v dávce 600 mg / týden, ale tato studie provedla screening subjektů, které dříve zneužívaly steroidy nebo měly nějaké psychiatrické předchůdce.[122][123] Pokus provedený v roce 2000 za použití testosteron cypionate při 600 mg / týden zjistili, že léčba významně vzrostla manický skóre na YMRS a agresivní reakce na několika stupnicích. Léková odpověď byla velmi variabilní. Nicméně: 84% subjektů vykazovalo minimální psychiatrické účinky, 12% se stalo mírně hypomanickými a 4% (2 subjekty) se staly výrazně hypomanickými. Mechanismus těchto proměnných reakcí nelze vysvětlit demografickými, psychologickými, laboratorními nebo fyziologickými opatřeními.[124]
Studie z roku 2006 o dvou párech identických dvojčat, ve kterých jedno dvojče používalo AAS a druhé ne, zjistilo, že v obou případech dvojčata užívající steroidy vykazovala vysokou úroveň agresivity, nepřátelství, úzkosti a paranoidních myšlenek, které nebyly nalezeny v „ kontrolní "dvojče.[125] Zjistila to malá studie 10 uživatelů AAS shluk B poruchy osobnosti byly matoucími faktory pro agresi.[126]
Vztah mezi užíváním AAS a depresí je neprůkazný. U dospívajících uživatelů steroidů byly zaznamenány neoficiální zprávy o depresích a sebevraždách,[127] ale málo systematických důkazů. Přehled z roku 1992 zjistil, že AAS může jak zmírnit, tak způsobit depresi, a že ukončení nebo snížené užívání AAS může také vést k depresi, ale požadoval další studie kvůli různorodým údajům.[128] V případě sebevraždy uvedlo 3,9% vzorku 77 osob klasifikovaných jako uživatelé AAS pokus o sebevraždu během odnětí (Malone, Dimeff, Lombardo, & Sample, 1995).[129]
Reprodukční
Androgeny jako testosteron, androstendion a dihydrotestosteron jsou potřebné pro vývoj orgánů v mužský reprodukční systém, včetně semenné váčky, nadvarlete, vas deferens, penis a prostata.[130] AAS jsou deriváty testosteronu určené k maximalizaci anabolický účinky testosteronu.[131] AAS jsou spotřebovány elitní sportovci soutěžit v sportovní jako vzpírání, kulturistika, a atletický.[132] Mužští rekreační sportovci užívají AAS k dosažení „vylepšeného“ fyzický vzhled.[133]
Spotřeba AAS narušuje osa hypotalamus – hypofýza – gonadální (Osa HPG) u mužů.[130] V ose HPG hormon uvolňující gonadotropin (GnRH) je vylučován z obloukovité jádro z hypotalamus a stimuluje přední hypofýza vylučovat ty dva gonadotropiny, hormon stimulující folikuly (FSH) a luteinizační hormon (LH).[134] U dospělých mužů LH stimuluje Leydigovy buňky v testy k produkci testosteronu, který je nezbytný pro tvorbu nového spermie přes spermatogeneze.[130] Spotřeba AAS vede k dávkově závislé potlačení uvolňování gonadotropinu prostřednictvím potlačení GnRH z hypotalamu (mechanismus dlouhé smyčky) nebo z přímého negativní zpětná vazba na přední hypofýze k inhibici uvolňování gonadotropinu (mechanismus krátké smyčky), což vede k AAS hypogonadismus.[130]
Farmakologie
Mechanismus účinku
The farmakodynamika AAS jsou podobné peptid hormony. Ve vodě rozpustné peptidové hormony nemohou proniknout do tuků buněčná membrána a pouze nepřímo ovlivnit jádro cíle buňky prostřednictvím jejich interakce s povrchem buňky receptory. Avšak jako hormony rozpustné v tucích jsou AAS propustné pro membránu a ovlivňují jádro buněk přímým působením. Farmakodynamický účinek AAS začíná, když exogenní hormon pronikne membránou cílové buňky a váže se na androgenní receptor (AR) umístěný v cytoplazma té buňky. Odtud sloučenina hormon-receptor difunduje do jádra, kde buď mění výraz z geny[136] nebo aktivuje procesy, které vysílat signály do jiných částí buňky.[137] Různé typy AAS se vážou k AAR s různými spřízněnosti, v závislosti na jejich chemické struktuře.[8]
Účinek AAS na svalovou hmotu je způsoben nejméně dvěma způsoby:[138] nejprve zvyšují produkce bílkovin; zadruhé, zkracují dobu zotavení blokováním účinků stresového hormonu kortizol na svalové tkáni, takže katabolismus svalové hmoty je výrazně snížena. Bylo to předpokládal že toto snížení rozpadu svalů může nastat prostřednictvím AAS, který inhibuje působení jiných nazývaných steroidních hormonů glukokortikoidy které podporují rozpad svalů.[139] AAS také ovlivňuje počet buněk, které se vyvinou v buňky akumulující tuky tím, že zvýhodňují buněčná diferenciace místo toho do svalových buněk.[140]
Anabolické a androgenní účinky
| Léky | PoměrA |
|---|---|
| Testosteron | ~1:1 |
| Androstanolon (DHT) | ~1:1 |
| Methyltestosteron | ~1:1 |
| Methandriol | ~1:1 |
| Fluoxymesteron | 1:1–1:15 |
| Metandienon | 1:1–1:8 |
| Drostanolon | 1:3–1:4 |
| Metenolon | 1:2–1:30 |
| Oxymetholon | 1:2–1:9 |
| Oxandrolon | 1:3–1:13 |
| Stanozolol | 1:1–1:30 |
| Nandrolon | 1:3–1:16 |
| Ethylestrenol | 1:2–1:19 |
| Norethandrolon | 1:1–1:20 |
| Poznámky: U hlodavců. Poznámky pod čarou: A = Poměr androgenní k anabolické aktivitě. Zdroje: Viz šablona. | |
Jak naznačuje jejich název, AAS mají dva různé, ale překrývající se typy efektů: anabolický, což znamená, že podporují anabolismus (růst buněk) a androgenní (nebo virilizující), což znamená, že ovlivňují vývoj a udržování mužských vlastností.
Některé příklady anabolických účinků těchto hormonů se zvyšují proteosyntéza z aminokyseliny, zvýšená chuť k jídlu, zvýšená přestavba a růst kostí a stimulace kostní dřeň, což zvyšuje produkci červené krvinky. Prostřednictvím řady mechanismy AAS stimulují tvorbu svalových buněk, a tím způsobují zvětšení velikosti kosterní svalstvo, což vede ke zvýšení pevnosti.[141][142][143]
Androgenní účinky AAS jsou četné. V závislosti na délce užívání mohou být vedlejší účinky steroidu nevratné. Mezi ovlivněné procesy patří pubertální růst, mazová žláza produkce ropy a sexualita (zejména ve vývoji plodu). Některé příklady virilizujících účinků jsou růst klitorisu u žen a penis u mužských dětí (velikost penisu pro dospělé se nemění kvůli steroidům[nutná lékařská citace ] ), zvýšil hlasivky velikost, zvětšená libido potlačení přírodní pohlavní hormony a postižené produkce spermií.[144] Účinky na ženy zahrnují prohloubení hlasu, růst ochlupení na obličeji a případně zmenšení velikosti prsou. U mužů se může vyvinout zvětšení prsní tkáně, známé jako gynekomastie, atrofie varlat a snížený počet spermií.[Citace je zapotřebí ]Androgenní: anabolický poměr AAS je důležitým faktorem při určování klinické aplikace těchto sloučenin. Sloučeniny s vysokým poměrem androgenních a anabolických účinků jsou lékem volby v androgenní substituční terapii (např. hypogonadismus u mužů), zatímco sloučeniny se sníženým poměrem androgenní: anabolické jsou výhodné pro anémii a osteoporózu a pro zvrácení ztráty bílkovin po úrazu, chirurgickém zákroku nebo prodloužené imobilizaci. Stanovení androgenního: anabolického poměru se obvykle provádí ve studiích na zvířatech, což vedlo k prodeji některých sloučenin, o nichž se tvrdí, že mají anabolickou aktivitu se slabými androgenními účinky. Tato disociace je méně výrazná u lidí, kde všechny AAS mají významné androgenní účinky.[72]
Běžně používaný protokol pro stanovení androgenního: anabolického poměru, který sahá až do 50. let 20. století, používá relativní váhy ventrální prostata (VP) a levator ani sval (LA) muže krysy. Hmotnost VP je indikátorem androgenního účinku, zatímco hmotnost LA je indikátorem anabolického účinku. Dvě nebo více šarží potkanů jsou kastrovaný a nedostal žádnou léčbu, respektive některé AAS, které nás zajímají. The Poměr LA / VP pro AAS se vypočítá jako poměr přírůstků hmotnosti LA / VP produkovaných ošetřením touto sloučeninou s použitím kastrovaných, ale neléčených krys jako základní linie: (LAc, t-LOS ANGELESC) / (VPc, t–VPC). Poměr přírůstku hmotnosti LA / VP z experimentů na potkanech není u testosteronu jednotný (obvykle 0,3–0,4), ale je normalizován pro účely prezentace a používá se jako základ pro srovnání u jiných AAS, u nichž jsou jejich androgenní: anabolické poměry odpovídajícím způsobem upraveny ( jak je uvedeno v tabulce výše).[145][146] Na počátku dvacátých let byl tento postup standardizován a zobecněn OECD v čem je nyní známý jako Hershbergerův test.
Vylepšení složení těla a síly
Tělesná hmotnost u mužů se může zvýšit o 2 až 5 kg v důsledku krátkodobého (<10 týdnů) užívání AAS, které lze připsat hlavně nárůstu štíhlé hmoty. Studie na zvířatech také zjistily, že tuková hmota byla snížena, ale většina studií u lidí nedokázala objasnit významné snížení tukové hmoty. Ukázalo se, že účinky na štíhlou tělesnou hmotnost jsou závislé na dávce. Oba svalová hypertrofie a vznik nových svalová vlákna byly pozorovány. Hydratace libové hmoty zůstává ovlivněna použitím AAS, i když nelze vyloučit malé zvýšení objemu krve.[8]
Horní část těla (hrudník, krk, ramena a horní část paže) se zdá být náchylnější k AAS než jiné oblasti těla kvůli převaze AR v horní části těla.[Citace je zapotřebí ] Největší rozdíl ve velikosti svalových vláken mezi uživateli AAS a neuživateli byl pozorován u svalových vláken typu I v vastus lateralis a trapézový sval v důsledku dlouhodobé samosprávy AAS. Po vysazení léku účinky pomalu ustupují, ale mohou přetrvávat déle než 6–12 týdnů po ukončení užívání AAS.[8]
Zlepšení síly v rozmezí 5 až 20% výchozí síly, do značné míry v závislosti na použitých lécích a dávce a období podávání. Celkově lze říci, že cvičení, kde byla pozorována nejvýznamnější zlepšení, je bench press.[8] Po téměř dvě desetiletí se předpokládalo, že AAS vykazuje významné účinky pouze u zkušených silových sportovců.[147][148] A randomized controlled trial demonstrated, however, that even in novice athletes a 10-week strength training program accompanied by testosteron enanthate at 600 mg/week may improve strength more than training alone does.[8][122] This dose is sufficient to significantly improve lean muscle mass relative to placebo even in subjects that did not exercise at all.[122] The anabolic effects of testosterone enanthate were highly dose dependent.[8][149]
Dissociation of effects
Endogenous/natural AAS like testosterone and DHT and synthetic AAS mediate their effects by binding to and activating the AR.[1] On the basis of animal biologické testy, the effects of these agents have been divided into two partially dissociable types: anabolic (myotrophic) and androgenic.[1] Dissociation between the ratios of these two types of effects relative to the ratio observed with testosterone is observed in rat bioassays with various AAS.[1] Theories for the dissociation include differences between AAS in terms of their intracelulární metabolismus, funkční selektivita (differential recruitment of coactivators ), a non-genomic mechanisms (i.e., signaling through non-AR membrane androgen receptors, or mARs).[1] Support for the latter two theories is limited and more hypothetical, but there is a good deal of support for the intracellular metabolism theory.[1]
The measurement of the dissociation between anabolic and androgenic effects among AAS is based largely on a simple but outdated and unsophisticated model using rat tissue bioassays.[1] Byl označován jako „myotrophic–androgenic index ".[1] In this model, myotrophic or anabolic activity is measured by change in the weight of the rat bulbocavernosus /levator ani muscle, and androgenic activity is measured by change in the weight of the rat ventral prostate (or, alternatively, the rat semenné váčky ), in response to exposure to the AAS.[1] The measurements are then compared to form a ratio.[1]
Intracellular metabolism
Testosterone is metabolizován in various tissues by 5α-reduktáza into DHT, which is 3- to 10-fold more potent as an AR agonist, and by aromatáza do estradiol, což je estrogen and lacks significant AR affinity.[1] In addition, DHT is metabolized by 3α-hydroxysteroid dehydrogenáza (3α-HSD) and 3β-hydroxysteroid dehydrogenáza (3β-HSD) into 3α-androstandiol a 3β-androstandiol, respectively, which are metabolity with little or no AR affinity.[1] 5α-reductase is widely distributed throughout the body, and is concentrated to various extents in skin (particularly the scalp, face, and genital areas), prostate, seminal vesicles, liver, and the brain.[1] In contrast, expression of 5α-reductase in kosterní sval is undetectable.[1] Aromatase is highly expressed in tuková tkáň and the brain, and is also expressed significantly in skeletal muscle.[1] 3α-HSD is highly expressed in skeletal muscle as well.[66]
Natural AAS like testosterone and DHT and synthetic AAS are analogues and are very similar structurally.[1] For this reason, they have the capacity to bind to and be metabolized by the same steroid-metabolizing enzymy.[1] According to the intracellular metabolism explanation, the androgenic-to-anabolic ratio of a given AR agonist is related to its capacity to be transformed by the aforementioned enzymes in conjunction with the AR activity of any resulting products.[1] For instance, whereas the AR activity of testosterone is greatly potentiated by local conversion via 5α-reductase into DHT in tissues where 5α-reductase is expressed, an AAS that is not metabolized by 5α-reductase or is already 5α-reduced, such as DHT itself or a derivative (like mesterolone nebo drostanolon ), would not undergo such potentiation in said tissues.[1] Moreover, nandrolone is metabolized by 5α-reductase, but unlike the case of testosterone and DHT, the 5α-reduced metabolite of nandrolone has much lower affinity for the AR than does nandrolone itself, and this results in reduced AR activation in 5α-reductase-expressing tissues.[1] As so-called "androgenic" tissues such as skin/hair follicles and male reproductive tissues are very high in 5α-reductase expression, while skeletal muscle is virtually devoid of 5α-reductase, this may primarily explain the high myotrophic–androgenic ratio and dissociation seen with nandrolone, as well as with various other AAS.[1]
Aside from 5α-reductase, aromatase may inactivate testosterone signaling in skeletal muscle and adipose tissue, so AAS that lack aromatase affinity, in addition to being free of the potential side effect of gynekomastie, might be expected to have a higher myotrophic–androgenic ratio in comparison.[1] In addition, DHT is inactivated by high activity of 3α-HSD in skeletal muscle (and cardiac tissue), and AAS that lack affinity for 3α-HSD could similarly be expected to have a higher myotrophic–androgenic ratio (although perhaps also increased long-term cardiovascular risks).[1] In accordance, DHT, mestanolon (17α-methyl-DHT), and mesterolone (1α-methyl-DHT) are all described as very poorly anabolic due to inactivation by 3α-HSD in skeletal muscle, whereas other DHT derivatives with other structural features like metenolon, oxandrolon, oxymetholone, drostanolon, a stanozolol are all poor substrates for 3α-HSD and are described as potent anabolics.[66]
The intracellular metabolism theory explains how and why remarkable dissociation between anabolic and androgenic effects might occur despite the fact that these effects are mediated through the same signaling receptor, and why this dissociation is invariably incomplete.[1] In support of the model is the rare condition congenital 5α-reductase type 2 deficiency, ve kterém 5α-reductase type 2 enzyme is defective, production of DHT is impaired, and DHT levels are low while testosterone levels are normal.[150][151] Males with this condition are born with ambiguous genitalia and a severely underdeveloped or even absent prostate gland.[150][151] In addition, at the time of puberty, such males develop normal musculature, voice deepening, and libido, but have reduced facial hair, a female pattern of body hair (i.e., largely restricted to the pubic triangle and underarms), no incidence of male pattern hair loss, and no prostate enlargement or incidence of rakovina prostaty.[151][152][153][154][155] They also notably do not develop gynecomastia as a consequence of their condition.[153]
| Sloučenina | rAR (%) | hAR (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| Testosteron | 38 | 38 | ||||||
| 5α-Dihydrotestosterone | 77 | 100 | ||||||
| Nandrolon | 75 | 92 | ||||||
| 5α-dihydronandrolon | 35 | 50 | ||||||
| Ethylestrenol | ND | 2 | ||||||
| Norethandrolon | ND | 22 | ||||||
| 5α-dihydronorethandrolon | ND | 14 | ||||||
| Metribolon | 100 | 110 | ||||||
| Zdroje: Viz šablona. | ||||||||
Funkční selektivita
An animal study found that two different kinds of androgen response elements could differentially respond to testosterone and DHT upon activation of the AR.[156][157] Whether this is involved in the differences in the ratios of anabolic-to-myotrophic effect of different AAS is unknown however.[156][157][1]
Non-genomic mechanisms
Testosterone signals not only through the nuclear AR, but also through mARs, including ZIP9 a GPRC6A.[158][159] It has been proposed that differential signaling through mARs may be involved in the dissociation of the anabolic and androgenic effects of AAS.[1] Indeed, DHT has less than 1% of the affinity of testosterone for ZIP9, and the synthetic AAS metribolon a mibolerone are ineffective competitors for the receptor similarly.[159] This indicates that AAS do show differential interactions with the AR and mARs.[159] However, women with complete androgen insensitivity syndrome (CAIS), who have a 46,XY ("male") genotyp a testy but a defect in the AR such that it is non-functional, are a challenge to this notion.[160] They are completely insensitive to the AR-mediated effects of androgens like testosterone, and show a perfectly female fenotyp despite having testosterone levels in the high end of the normal male range.[160] These women have little or no kožní maz production, incidence of akné, or body hair growth (including in the pubic and axillary areas).[160] Moreover, CAIS women have hubená tělesná hmotnost that is normal for females but is of course greatly reduced relative to males.[161] These observations suggest that the AR is mainly or exclusively responsible for masculinization and myotrophy caused by androgens.[160][161][162] The mARs have however been found to be involved in some of the health-related effects of testosterone, like modulation of prostate cancer risk and progression.[159][163]
Antigonadotropic effects
Changes in endogenous testosterone levels may also contribute to differences in myotrophic–androgenic ratio between testosterone and synthetic AAS.[66] AR agonists are antigonadotropní – that is, they dose-dependently suppress gonadal testosterone production and hence reduce systemic testosterone concentrations.[66] By suppressing endogenous testosterone levels and effectively replacing AR signaling in the body with that of the exogenous AAS, the myotrophic–androgenic ratio of a given AAS may be further, dose-dependently increased, and this hence may be an additional factor contributing to the differences in myotrophic–androgenic ratio among different AAS.[66] In addition, some AAS, such as 19-nortestosterone derivatives like nandrolone, are also potent progestogeny, and activation of the receptor progesteronu (PR) is antigonadotropic similarly to activation of the AR.[66] The combination of sufficient AR and PR activation can suppress circulating testosterone levels into the castrate range in men (i.e., complete suppression of gonadal testosterone production and circulating testosterone levels decreased by about 95%).[48][164] As such, combined progestogenic activity may serve to further increase the myotrophic–androgenic ratio for a given AAS.[66]
GABAA receptor modulation
Some AAS, such as testosterone, DHT, stanozolol, and methyltestosterone, have been found to modulate the GABAA receptor similarly to endogenous neurosteroids jako alopregnanolon, 3α-androstandiol, dehydroepiandrosterone sulfate, a pregnenolon sulfát.[1] It has been suggested that this may contribute as an alternative or additional mechanism to the neurological and behavioral effects of AAS.[1][165][166][167][168][169][170]
Comparison of AAS
AAS differ in a variety of ways including in their capacities to be metabolizován podle steroidogenic enzymy jako 5α-reduktáza, 3-hydroxysteroid dehydrogenases, a aromatáza, in whether their potency as AR agonists is potentiated or diminished by 5α-reduction, in their ratios of anabolický /myotrophic na androgenní effect, in their estrogenní, progestogenní, a neurosteroid activities, in their ústní activity, and in their capacity to produce hepatotoxicita.[66][1][171]
| Sloučenina | Třída | 5α-R | AROM | 3-HSD | AAR | Estr | Prog | Ústní | Hepat |
|---|---|---|---|---|---|---|---|---|---|
| Androstanolone | DHT | – | – | + | * | – | – | – | – |
| Boldenone | T | – | ± | – | ** | ± | – | – | – |
| Drostanolon | DHT | – | – | – | *** | – | – | – | – |
| Ethylestrenol | 19-NT; 17α-A | + (↓) | ± | – | *** | + | + | + | + |
| Fluoxymesteron | T; 17α-A | + (↑) | – | – | * | – | – | + | + |
| Mestanolone | DHT; 17α-A | – | – | + | * | – | – | + | + |
| Mesterolon | DHT | – | – | + | * | – | – | ± | – |
| Metandienon | T; 17α-A | – | ± | – | ** | + | – | + | + |
| Metenolon | DHT | – | – | – | ** | – | – | ± | – |
| Methyltestosteron | T; 17α-A | + (↑) | + | – | * | + | – | + | + |
| Nandrolon | 19-NT | + (↓) | ± | – | *** | ± | + | – | – |
| Norethandrolon | 19-NT; 17α-A | + (↓) | ± | – | *** | + | + | + | + |
| Oxandrolon | DHT; 17α-A | – | – | – | *** | – | – | + | ± |
| Oxymetholon | DHT; 17α-A | – | – | – | *** | + | – | + | + |
| Stanozolol | DHT; 17α-A | – | – | – | *** | – | – | + | + |
| Testosteron | T | + (↑) | + | – | * | + | – | ±A | – |
| Trenbolon | 19-NT | – | – | – | *** | – | + | – | – |
| Klíč: + = Yes. ± = Low. – = No. ↑ = Potentiated. ↓ = Inactivated. *** = High. ** = Moderate. * = Low. Zkratky: 5α-R = Metabolized by 5α-reduktáza. AROM = Metabolized by aromatáza. 3-HSD = Metabolized by 3α- a / nebo 3β-HSD. AAR = Anabolic-to-androgenic ratio (amount of anabolický (myotrophic ) effect relative to androgenní effect). Estr = Estrogenní. Prog = Progestogenic. Oral = Ústní aktivita. Hepat = Hepatotoxicita. Poznámky pod čarou: A = As testosteron undekanoát. Zdroje: Viz šablona. | |||||||||
| Steroid | Chemický název | Relativní vazebné afinity (%) | ||||||
|---|---|---|---|---|---|---|---|---|
| PR | AR | ER | GR | PAN | SHBG | CBG | ||
| Androstanolone | DHT | 1.4–1.5 | 60–120 | <0.1 | <0.1–0.3 | 0.15 | 100 | 0.8 |
| Boldenone | Δ1-T | <1 | 50–75 | ? | <1 | ? | ? | ? |
| Danazol | 2,3-Isoxazol-17α-Ety-T | 9 | 8 | ? | <0.1A | ? | 8 | 10 |
| Dienolon | ∆9-19-NT | 17 | 134 | <0.1 | 1.6 | 0.3 | ? | ? |
| Dimethyldienolone | ∆9-7α,17α-DiMe-19-NT | 198 | 122 | 0.1 | 6.1 | 1.7 | ? | ? |
| Dimethyltrienolon | ∆9,11-7α,17α-DiMe-19-NT | 306 | 180 | 0.1 | 22 | 52 | ? | ? |
| Drostanolon | 2α-Me-DHT | ? | ? | ? | ? | ? | 39 | ? |
| Ethisteron | 17α-Ety-T | 35 | 0.1 | <1.0 | <1.0 | <1.0 | 25–92 | 0.3 |
| Ethylestrenol | 3-DeO-17α-Et-19-NT | ? | ? | ? | ? | ? | <1 | ? |
| Fluoxymesteron | 9α-F-11β-OH-17α-Me-T | ? | ? | ? | ? | ? | ≤3 | ? |
| Gestrinon | ∆9,11-17α-Ety-18-Me-19-NT | 75–76 | 83–85 | <0.1–10 | 77 | 3.2 | ? | ? |
| Levonorgestrel | 17α-Ety-18-Me-19-NT | 170 | 84–87 | <0.1 | 14 | 0.6–0.9 | 14–50 | <0.1 |
| Mestanolone | 17α-Me-DHT | 5–10 | 100–125 | ? | <1 | ? | 84 | ? |
| Mesterolon | 1α-Me-DHT | ? | ? | ? | ? | ? | 82–440 | ? |
| Metandienon | ∆1-17α-Me-T | ? | ? | ? | ? | ? | 2 | ? |
| Metenolon | ∆1-1-Me-DHT | ? | ? | ? | ? | ? | 3 | ? |
| Methandriol | 17α-Me-A5 | ? | ? | ? | ? | ? | 40 | ? |
| Methasteron | 2α,17α-DiMe-DHT | ? | ? | ? | ? | ? | 58 | ? |
| Methyldienolon | ∆9-17α-Me-19-NT | 71 | 64 | <0.1 | 6 | 0.4 | ? | ? |
| Methyltestosteron | 17α-Me-T | 3 | 45–125 | <0.1 | 1–5 | ? | 5–64 | <0.1 |
| Methyl-1-testosteron | ∆1-17α-Me-DHT | ? | ? | ? | ? | ? | 69 | ? |
| Metribolon | ∆9,11-17α-Me-19-NT | 208–210 | 199–210 | <0.1 | 10–26 | 18 | 0.2–0.8 | ≤0.4 |
| Miboleron | 7α,17α-DiMe-19-NT | 214 | 108 | <0.1 | 1.4 | 2.1 | 6 | ? |
| Nandrolon | 19-NT | 20 | 154–155 | <0.1 | 0.5 | 1.6 | 1–16 | 0.1 |
| Norethandrolon | 17α-Et-19-NT | ? | ? | ? | ? | ? | 3 | ? |
| Norethisteron | 17α-Ety-19-NT | 155–156 | 43–45 | <0.1 | 2.7–2.8 | 0.2 | 5–21 | 0.3 |
| Norgestrienon | ∆9,11-17α-Ety-19-NT | 63–65 | 70 | <0.1 | 11 | 1.8 | ? | ? |
| Normethandrone | 17α-Me-19-NT | 100 | 146 | <0.1 | 1.5 | 0.6 | 7 | ? |
| Oxandrolon | 2-Oxa-17α-Me-DHT | ? | ? | ? | ? | ? | <1 | ? |
| Oxymetholon | 2-OHMeEne-17α-Me-DHT | ? | ? | ? | ? | ? | ≤3 | ? |
| RU-2309 (17α-Me-THG) | ∆9,11-17α,18-DiMe-19-NT | 230 | 143 | <0.1 | 155 | 36 | ? | ? |
| Stanozolol | 2,3-Pyrazol-17α-Me-DHT | ? | ? | ? | ? | ? | 1–36 | ? |
| Testosteron | T | 1.0–1.2 | 100 | <0.1 | 0.17 | 0.9 | 19–82 | 3–8 |
| 1-testosteron | ∆1-DHT | ? | ? | ? | ? | ? | 98 | ? |
| Tibolon | 7α-Me-17α-Ety-19-N-5(10)-T | 12 | 12 | 1 | ? | ? | ? | ? |
| Δ4-Tibolon | 7α-Me-17α-Ety-19-NT | 180 | 70 | 1 | <1 | 2 | 1–8 | <1 |
| Trenbolon | ∆9,11-19-NT | 74–75 | 190–197 | <0.1 | 2.9 | 1.33 | ? | ? |
| Trestolon | 7α-Me-19-NT | 50–75 | 100–125 | ? | <1 | ? | 12 | ? |
| Poznámky: Hodnoty jsou procenta (%). Odkaz ligandy (100%) byly progesteron pro PR, testosteron pro AR, estradiol pro ER, dexamethason pro GR, aldosteron pro PAN, dihydrotestosteron pro SHBG, a kortizol pro CBG. Poznámky pod čarou: A = 1-hour incubation time (4 hours is standard for this assay; may affect affinity value). Zdroje: Viz šablona. | ||||||||
| Léky | Formulář | Hlavní značky | Doba trvání |
|---|---|---|---|
| Testosteron | Vodná suspenze | Andronaq, Sterotate, Virosterone | 2–3 days |
| Testosteron propionát | Olejový roztok | Androteston, Perandren, Testoviron | 3–4 days |
| Testosterone phenylpropionate | Olejový roztok | Testolent | 8 dní |
| Testosteron isobutyrát | Vodná suspenze | Agovirin Depot, Perandren M | 14 dní |
| Smíšené estery testosteronuA | Olejový roztok | Triolandren | 10–20 days |
| Smíšené estery testosteronub | Olejový roztok | Testosid Depot | 14–20 days |
| Testosteron enanthát | Olejový roztok | Delatestryl | 14–28 days |
| Testosteron cypionát | Olejový roztok | Depovirin | 14–28 days |
| Smíšené estery testosteronuC | Olejový roztok | Sustanon 250 | 28 dní |
| Testosteron undekanoát | Olejový roztok | Aveed, Nebido | 100 days |
| Testosteron bukiclátd | Vodná suspenze | 20 Aet-1, CDB-1781E | 90–120 days |
| Nandrolon fenylpropionát | Olejový roztok | Durabolin | 10 dní |
| Nandrolon dekanoát | Olejový roztok | Deca Durabolin | 21–28 days |
| Methandriol | Vodná suspenze | Notandron, Protandren | 8 dní |
| Methandriol bisenanthoyl-acetát | Olejový roztok | Notandron Depot | 16 dní |
| Metenolon-acetát | Olejový roztok | Primobolan | 3 dny |
| Metenolon enanthate | Olejový roztok | Primobolan Depot | 14 dní |
| Poznámka: All are via i.m. injekce. Poznámky pod čarou: A = TP, televize, a TUe. b = TP a TKL. C = TP, TPP, TiCa, a TD. d = Studied but never marketed. E = Developmental code names. Zdroje: Viz šablona. | |||
| Testosterone ester | Formulář | Trasa | Tmax | t1/2 | MR T |
|---|---|---|---|---|---|
| Testosteron undekanoát | Oil-filled capsules | Ústní | ? | 1,6 hodiny | 3.7 hours |
| Testosteron propionát | Olejový roztok | Intramuskulární injekce | ? | 0.8 days | 1.5 days |
| Testosteron enanthát | Castor oil solution | Intramuskulární injekce | 10 dní | 4.5 days | 8.5 days |
| Testosteron undekanoát | Tea seed oil solution | Intramuskulární injekce | 13.0 days | 20.9 days | 34.9 days |
| Testosteron undekanoát | Castor oil solution | Intramuskulární injekce | 11.4 days | 33.9 days | 36.0 days |
| Testosteron bukiclátA | Vodná suspenze | Intramuskulární injekce | 25.8 days | 29.5 days | 60.0 days |
| Poznámky: Testosteron cypionát has similar pharmacokinetics to TE. Poznámky pod čarou: A = Nikdy na trhu. Zdroje: Viz šablona. | |||||
5α-Reductase and androgenicity
Testosterone can be robustly converted by 5α-reduktáza into DHT in so-called androgenic tissues such as kůže, skalp, prostata, a semenné váčky, ale ne v sval nebo kost, where 5α-reductase either is not expressed or is only minimally expressed.[1] As DHT is 3- to 10-fold more potent as an agonist of the AR than is testosterone, the AR agonist activity of testosterone is thus markedly and selectively potentiated in such tissues.[1] In contrast to testosterone, DHT and other 4,5α-dihydrogenated AAS are already 5α-reduced, and for this reason, cannot be potentiated in androgenic tissues.[1] 19-Nortestosterone derivatives like nandrolon může být metabolizován by 5α-reductase similarly to testosterone, but 5α-reduced metabolites of 19-nortestosterone derivatives (e.g., 5α-dihydronandrolone ) tend to have reduced activity as AR agonists, resulting in reduced androgenic activity in tissues that express 5α-reductase.[1] In addition, some 19-nortestosterone derivatives, including trestolone (7α-methyl-19-nortestosterone (MENT)), 11β-methyl-19-nortestosterone (11β-MNT), and dimethandrolone (7α,11β-dimethyl-19-nortestosterone), cannot be 5α-reduced.[172] Conversely, certain 17α-alkylated AAS like methyltestosterone are 5α-reduced and potentiated in androgenic tissues similarly to testosterone.[1][66] 17α-Alkylated DHT derivatives cannot be potentiated via 5α-reductase however, as they are already 4,5α-reduced.[1][66]
The capacity to be metabolized by 5α-reductase and the AR activity of the resultant metabolites appears to be one of the major, if not the most important determinant of the androgenic–myotrophic ratio for a given AAS.[1] AAS that are not potentiated by 5α-reductase or that are weakened by 5α-reductase in androgenic tissues have a reduced risk of androgenic side effects such as akné, androgenní alopecie (male-pattern baldness), hirsutismus (excessive male-pattern hair growth), benigní hyperplazie prostaty (prostate enlargement), and rakovina prostaty, while incidence and magnitude of other effects such as muscle hypertrophy, bone changes,[173] voice deepening, and changes in sexuální apetit show no difference.[1][174]
Aromatase and estrogenicity
Testosterone can be metabolizován podle aromatáza do estradiol, and many other AAS can be metabolized into their corresponding estrogenní metabolites as well.[1] As an example, the 17α-alkylated AAS methyltestosteron a metandienon are converted by aromatase into methylestradiol.[175] 4,5α-Dihydrogenated derivatives of testosterone such as DHT cannot be aromatized, whereas 19-nortestosterone derivatives like nandrolone can be but to a greatly reduced extent.[1][176] Some 19-nortestosterone derivatives, such as dimethandrolone and 11β-MNT, cannot be aromatized due to sterická překážka provided by their 11β-methyl group, whereas the closely related AAS trestolone (7α-methyl-19-nortestosterone), in relation to its lack of an 11β-methyl group, can be aromatized.[176] AAS that are 17α-alkylated (and not also 4,5α-reduced or 19-demethylated) are also aromatized but to a lesser extent than is testosterone.[1][177] However, it is notable that estrogens that are 17α-substituted (e.g., ethinylestradiol and methylestradiol) are of markedly increased estrogenic potency due to improved metabolic stability,[175] and for this reason, 17α-alkylated AAS can actually have high estrogenicity and comparatively greater estrogenic effects than testosterone.[175][66]
The major effect of estrogenicity is gynekomastie (woman-like breasts).[1] AAS that have a high potential for aromatization like testosterone and particularly methyltestosterone show a high risk of gynecomastia at sufficiently high dosages, while AAS that have a reduced potential for aromatization like nandrolone show a much lower risk (though still potentially significant at high dosages).[1] In contrast, AAS that are 4,5α-reduced, and some other AAS (e.g., 11β-methylated 19-nortestosterone derivatives), have no risk of gynecomastia.[1] In addition to gynecomastia, AAS with high estrogenicity have increased antigonadotropic activity, which results in increased potency in suppression of the osa hypotalamus-hypofýza-gonadální a gonadal testosterone production.[178]
Progestogenní aktivita
Many 19-nortestosterone derivatives, including nandrolone, trenbolon, ethylestrenol (ethylnandrol), metribolon (R-1881), trestolone, 11β-MNT, dimethandrolone, and others, are potent agonists of the receptor progesteronu (AR) and hence are progestogeny in addition to AAS.[1][179] Similarly to the case of estrogenic activity, the progestogenic activity of these drugs serves to augment their antigonadotropic activity.[179] This results in increased potency and effectiveness of these AAS as antispermatogenic agents a male contraceptives (or, put in another way, increased potency and effectiveness in producing azoospermie and reversible mužská neplodnost ).[179]
Oral activity and hepatotoxicity
Non-17α-alkylated testosterone derivatives such as testosterone itself, DHT, and nandrolone all have poor oral bioavailability due to extensive first-pass hepatic metabolism and hence are not orally active.[1] A notable exception to this are AAS that are androgen prekurzory nebo prohormony, počítaje v to dehydroepiandrosterone (DHEA), androstenediol, androstendion, boldione (androstadienedione), bolandiol (norandrostenediol), bolandione (norandrostenedione), dienedione, mentabolan (MENT dione, trestione), and methoxydienone (methoxygonadiene) (although these are relatively weak AAS).[180][181] AAS that are not orally active are used almost exclusively in the form of estery spravuje intramuskulární injekce, which act as depa and function as long-acting proléčiva.[1] Examples include testosterone, as testosteron cypionate, testosteron enanthate, a testosteron propionát, and nandrolone, as nandrolon fenylpropionát a nandrolon dekanoát, among many others (see tady for a full list of testosterone and nandrolone esters).[1] An exception is the very long-chain ester testosteron undekanoát, which is orally active, albeit with only very low oral bioavailability (approximately 3%).[182] In contrast to most other AAS, 17α-alkylated testosterone derivatives show resistance to metabolism due to steric hindrance and are orally active, though they may be esterified and administered via intramuscular injection as well.[1]
In addition to oral activity, 17α-alkylation also confers a high potential for hepatotoxicita, and all 17α-alkylated AAS have been associated, albeit uncommonly and only after prolonged use (different estimates between 1 and 17%),[183][184] with hepatotoxicity.[1][185][186] V porovnání, estery testosteronu have only extremely rarely or never been associated with hepatotoxicity,[184] and other non-17α-alkylated AAS only rarely,[Citace je zapotřebí ] although long-term use may reportedly still increase the risk of hepatic changes (but at a much lower rate than 17α-alkylated AAS and reportedly not at replacement dosages).[183][187][70][jsou zapotřebí další citace ] In accordance, D-ring glucuronides of testosterone and DHT have been found to be cholestatic.[188]
Aside from prohormones and testosterone undecanoate, almost all orally active AAS are 17α-alkylated.[189] A few AAS that are not 17α-alkylated are orally active.[1] Some examples include the testosterone 17-ethers cloxotestosterone, quinbolone, a silandrone,[Citace je zapotřebí ] which are prodrugs (to testosterone, boldenon (Δ1-testosterone), and testosterone, respectively), the DHT 17-ethers mepitiostane, mesabolone, a prostanozol (which are also prodrugs), the 1-methylated DHT derivatives mesterolone a metenolon (although these are relatively weak AAS),[1][70] and the 19-nortestosterone derivatives dimethandrolone and 11β-MNT, which have improved resistance to first-pass hepatic metabolism due to their 11β-methyl groups (in contrast to them, the related AAS trestolone (7α-methyl-19-nortestosterone) is not orally active).[1][179] As these AAS are not 17α-alkylated, they show minimal potential for hepatotoxicity.[1]
Neurosteroid activity
DHT, via its metabolite 3α-androstandiol (produkovaný 3α-hydroxysteroid dehydrogenáza (3α-HSD)), is a neurosteroid that acts via positive allosteric modulation z GABAA receptor.[1] Testosterone, via conversion into DHT, also produces 3α-androstanediol as a metabolite and hence has similar activity.[1] Some AAS that are or can be 5α-reduced, including testosterone, DHT, stanozolol, and methyltestosterone, among many others, can or may modulate the GABAA receptor, and this may contribute as an alternative or additional mechanism to their centrální nervový systém effects in terms of mood, anxiety, aggression, and sex drive.[1][165][166][167][168][169][170]
Chemie
AAS are androstan nebo estrane steroidy. They include testosterone (androst-4-en-17β-ol-3-one) and deriváty s různými structural modifications jako:[1][190][66]
- 17α-Alkylation: methyltestosteron, metandienon, fluoxymesteron, oxandrolon, oxymetholone, stanozolol, norethandrolon, ethylestrenol
- 19-Demethylation: nandrolon, trenbolon, norethandrolon, ethylestrenol, trestolone, dimethandrolone
- 5α-Reduction: androstanolone, drostanolon, mestanolon, mesterolone, metenolon, oxandrolon, oxymetholon, stanozolol
- 3β- a / nebo 17p-esterifikace: testosteron enanthate, nandrolon dekanoát, drostanolon propionát, boldenon undecylenate, trenbolon-acetát
Stejně jako ostatní jako 1-dehydrogenace (např., metandienon, boldenon ), 1-střídání (např., mesterolon, metenolon ), 2-střídání (např., drostanolon, oxymetholon, stanozolol ), 4-střídání (např., clostebol, oxabolon ) a různé další úpravy.[1][190][66]
| Třídy | Androgen | Struktura | Chemický název | Funkce |
|---|---|---|---|---|
| Testosteron | 4-HydroxytestosteronA | 4-Hydroxytestosteron | – | |
| AndrostendiolA | 5-Androstendiol (androst-5-en-3β, 17β-diol) | Prohormon | ||
| AndrostendionA | 4-Androstendion (androst-4-en-3,17-dion) | Prohormon | ||
| Boldenone | 1-dehydrotestosteron | – | ||
| BoldioneA | 1-dehydro-4-androstendion | Prohormon | ||
| Clostebol | 4-chlortestosteron | – | ||
| Kloxotestosteron | Testosteron 17-chloral hemiacetal ether | Éter | ||
| Prasterone | 5-dehydroepiandrosteron (androst-5-en-3β-ol-17-on) | Prohormon | ||
| Chinbolon | 1-Dehydrotestosteron 17β-cyklopentenyl enol ether | Éter | ||
| SilandroneA | Testosteron 17β-trimethylsilyl ether | Éter | ||
| Testosteron | Androst-4-en-17β-ol-3-on | – | ||
| 17α-alkylovaný testosteron | Bolasteron | 7α, 17α-dimethyltestosteron | – | |
| Calusterone | 7p, 17a-dimethyltestosteron | – | ||
| ChlorodehydromethylandrostendiolA | L-Dehydro-4-chlor-17a-methyl-4-androstendiol | Prohormon | ||
| Chlorodehydromethyltestosteron | 1-dehydro-4-chlor-17a-methyltestosteron | – | ||
| ChlormethylandrostendiolA | 4-Chlor-17a-methyl-4-androstendiol | – | ||
| EnestebolA | 1-dehydro-4-hydroxy-17a-methyltestosteron | – | ||
| EthyltestosteronA | 17α-ethyltestosteron | – | ||
| Fluoxymesteron | 9α-fluor-llp-hydroxy-17a-methyltestosteron | – | ||
| Formebolon | L-Dehydro-2-formyl-lla-hydroxy-17a-methyltestosteron | – | ||
| HydroxystenozolA | 17α-methyl-2'H-androsta-2,4-dieno [3,2-c] pyrazol-17p-ol | Kroužkově tavený | ||
| Metandienon | 1-dehydro-17α-methyltestosteron | – | ||
| Methandriol | 17α-methyl-5-androstendiol | Prohormon | ||
| MethylclostebolA | 4-chlor-17α-methyltestosteron | – | ||
| Methyltestosteron | 17α-methyltestosteron | – | ||
| Methyltestosteron hexyl ether | 17a-Methyltestosteron 3-hexyl enol ether | Éter | ||
| Oxymesteron | 4-Hydroxy-17α-methyltestosteron | – | ||
| Penmesterol | 17a-Methyltestosteron 3-cyklopentyl enol ether | Éter | ||
| Tiomesteron | La, 7a-diacetylthio-17a-methyltestosteron | – | ||
| Další 17α-substituovaný testosteron | Danazol | 2,3-Isoxazol-17a-ethynyltestosteron | Kroužkově tavený | |
| Dihydrotestosteron | 1-testosteronA | 1-dehydro-4,5α-dihydrotestosteron | – | |
| Androstanolone | 4,5α-dihydrotestosteron | – | ||
| Bolazine | C3 azinový dimer drostanolonu | Dimer | ||
| Drostanolon | 2α-methyl-4,5α-dihydrotestosteron | – | ||
| Epitiostanol | 2α, 3α-epithio-3-deketo-4,5α-dihydrotestosteron | Kroužkově tavený | ||
| Mepitiostan | 2α, 3α-Epithio-3-deketo-4,5α-dihydrotestosteron 17β- (1-methoxycyklopentan) ether | Kroužkově tavený; Éter | ||
| MesolabolonA | 1-dehydro-4,5α-dihydrotestosteron 17β- (1-methoxycyklohexan) ether | Éter | ||
| Mesterolon | 1α-methyl-4,5α-dihydrotestosteron | – | ||
| Metenolon | 1-Dehydro-1-methyl-4,5α-dihydrotestosteron | – | ||
| ProstanozolA | 2'H-5α-Androst-2-eno [3,2-C] pyrazol-17p-ol 17p-tetrahydropyranether | Éter | ||
| Stenbolon | 1-dehydro-2-methyl-4,5α-dihydrotestosteron | – | ||
| 17α-alkylovaný dihydrotestosteron | Androisoxazol | 17α-methyl-5α-androstano [3,2-C] isoxazol-17p-ol | Kroužkově tavený | |
| DesoxymethyltestosteronA | 2-dehydro-3-deketo-4,5a-dihydro-17a-methyltestosteron | – | ||
| Furazabol | 17α-methyl-5α-androstano [2,3-C] [1,2,5] oxadiazol-17p-ol | Kroužkově tavený | ||
| Mebolazin | C3 azinový dimer methasteronu | Dimer | ||
| Mestanolone | 4,5α-dihydro-17α-methyltestosteron | – | ||
| MethasteronA | 2α, 17α-dimethyl-4,5α-dihydrotestosteron | – | ||
| Methyl-1-testosteronA | 1-dehydro-4,5α-dihydro-17α-methyltestosteron | – | ||
| MethyldiazinolA | 3-Deketo-3-azi-4,5a-dihydro-17a-methyltestosteron | – | ||
| MethylepitiostanolA | 2α, 3α-epithio-3-deketo-4,5α-dihydro-17α-methyltestosteron | – | ||
| MethylstenbolonA | 1-dehydro-2,17a-dimethyl-4,5α-dihydrotestosteron | – | ||
| Oxandrolon | 2-Oxa-4,5α-dihydro-17α-methyltestosteron | – | ||
| Oxymetholon | 2-Hydroxymethylen-4,5α-dihydro-17α-methyltestosteron | – | ||
| Stanozolol | 17α-Methyl-2 'H-5α-androst-2-eno [3,2-C] pyrazol-17p-ol | Kroužkově tavený | ||
| 19-Nortestosteron | Llp-methyl-19-nortestosteronA | Llp-methyl-19-nortestosteron | – | |
| 19-Nor-5-androstendiolA | 19-Nor-5-androstendiol | Prohormon | ||
| 19-nordehydroepiandrosteronA | 19-Nor-5-dehydroepiandrosteron | Prohormon | ||
| BolandiolA | 19-Nor-4-androstendiol | Prohormon | ||
| BolandioneA | 19-Nor-4-androstendion | Prohormon | ||
| BolmantalátA | 19-Nortestosteron 17β-adamantoát | Ester | ||
| DienedioneA | 9-dehydro-19-nor-4-androstendion | Prohormon | ||
| DienolonA | 9-dehydro-19-nortestosteron | – | ||
| DimethandrolonA | 7α, llp-dimethyl-19-nortestosteron | – | ||
| MethoxydienonA | 2,5 (10) -didehydro-18-methyl-19-norepiandrosteron 3-methylether | Prohormon; Éter | ||
| Nandrolon | 19-Nortestosteron | – | ||
| Norclostebol | 4-chlor-19-nortestosteron | – | ||
| Oxabolon | 4-Hydroxy-19-nortestosteron | – | ||
| TrestolonA | 7α-methyl-19-nortestosteron | – | ||
| Trenbolon | 9,11-didehydro-19-nortestosteron | – | ||
| TrendioneA | 9,11-didehydro-19-nor-4-androstendion | Prohormon | ||
| TrestioneA | 7α-Methyl-19-nor-4-androstendion | Prohormon | ||
| 17α-alkylovaný 19-nortestosteron | DimethyltrienolonA | 7α, 17α-dimethyl-9,11-didehydro-19-nortestosteron | – | |
| DimethyldienoloneA | 7a, 17a-dimethyl-9-dehydro-19-nortestosteron | – | ||
| EthyldienoloneA | 9-dehydro-17a-ethyl-19-nortestosteron | – | ||
| Ethylestrenol | 17α-Ethyl-3-deketo-19-nortestosteron | – | ||
| MethyldienolonA | 9-dehydro-17a-methyl-19-nortestosteron | – | ||
| MethylhydroxynandrolonA | 4-Hydroxy-17a-methyl-19-nortestosteron | – | ||
| MetribolonA | 9,11-didehydro-17a-methyl-19-nortestosteron | – | ||
| Miboleron | 7α, 17α-dimethyl-19-nortestosteron | – | ||
| NorboletonA | 17α-ethyl-18-methyl-19-nortestosteron | – | ||
| Norethandrolon | 17α-ethyl-19-nortestosteron | – | ||
| Normethandrone | 17α-methyl-19-nortestosteron | – | ||
| Propetandrol | 17α-Ethyl-19-nortestosteron 3-propionát | Ester | ||
| RU-2309A | 9,11-didehydro-17a, 18-dimethyl-19-nortestosteron | – | ||
| TetrahydrogestrinonA | 9,11-didehydro-17a-ethyl-18-methyl-19-nortestosteron | – | ||
| Další 17α-substituovaný 19-nortestosteron | Gestrinon | 9,11-didehydro-17a-ethynyl-18-methyl-19-nortestosteron | – | |
| Tibolon | 5 (10) -dehydro-7α-methyl-17α-ethynyl-19-nortestosteron | – | ||
| VinyltestosteronA | 17α-Ethenyltestosteron | – | ||
| Poznámky: Estery androgenů a anabolických steroidů nejsou v této tabulce většinou zahrnuty; vidět tady namísto. Slabě androgenní progestiny nejsou v této tabulce většinou zahrnuty; vidět tady namísto. Poznámky pod čarou: A = Nikdy na trhu. | ||||
| Androgen | Struktura | Ester | Relativní mol. hmotnost | Relativní T obsahb | Doba trváníC | ||||
|---|---|---|---|---|---|---|---|---|---|
| Pozice | Skupina | Typ | DélkaA | Hodnost | Skupina | ||||
| Testosteron | – | – | – | – | 1.00 | 1.00 | 11 | Krátký | |
| Testosteron propionát | C17β | Kyselina propanová | Mastná kyselina s přímým řetězcem | 3 | 1.19 | 0.84 | 10 | Krátký | |
| Testosteron isobutyrát | C17β | Kyselina isomáselná | Aromatická mastná kyselina | – (~3) | 1.24 | 0.80 | 9 | Mírný | |
| Testosteron cypionát | C17β | Kyselina cyklopentylpropanová | Aromatická mastná kyselina | – (~6) | 1.43 | 0.70 | 8 | Mírný | |
| Testosteron fenylpropionát | C17β | Kyselina fenylpropanová | Aromatická mastná kyselina | – (~6) | 1.46 | 0.69 | 7 | Mírný | |
| Testosteron isocaproate | C17β | Kyselina isohexanová | Mastná kyselina s rozvětveným řetězcem | – (~5) | 1.34 | 0.75 | 6 | Mírný | |
| Testosteron kaproát | C17β | Kyselina hexanová | Mastná kyselina s přímým řetězcem | 6 | 1.35 | 0.75 | 5 | Mírný | |
| Testosteron enanthát | C17β | Kyselina heptanová | Mastná kyselina s přímým řetězcem | 7 | 1.39 | 0.72 | 4 | Mírný | |
| Testosteron dekanoát | C17β | Kyselina dekanová | Mastná kyselina s přímým řetězcem | 10 | 1.53 | 0.65 | 3 | Dlouho | |
| Testosteron undekanoát | C17β | Kyselina undekanová | Mastná kyselina s přímým řetězcem | 11 | 1.58 | 0.63 | 2 | Dlouho | |
| Testosteron bukiclátd | C17β | Kyselina bucyklickáE | Aromatická karboxylová kyselina | – (~9) | 1.58 | 0.63 | 1 | Dlouho | |
| Poznámky pod čarou: A = Délka ester v uhlík atomy pro mastné kyseliny s přímým řetězcem nebo přibližná délka esteru v atomech uhlíku pro aromatické mastné kyseliny. b = Relativní obsah testosteronu podle hmotnosti (tj. Relativní androgenní /anabolický potence ). C = Doba trvání podle intramuskulární nebo subkutánní injekce v olejový roztok (až na TiB a TB, které jsou v vodná suspenze ). d = Nikdy na trhu. E = Kyselina bucyklická = transKyselina -4-butylcyklohexan-l-karboxylová. Zdroje: Podívejte se na jednotlivé články. | |||||||||
| Anabolický steroid | Struktura | Ester | Relativní mol. hmotnost | Relativní AAS obsahb | Doba trváníC | ||||
|---|---|---|---|---|---|---|---|---|---|
| Pozice | Skupina | Typ | DélkaA | ||||||
| Boldenon undecylenate | C17β | Kyselina undecylenová | Mastná kyselina s přímým řetězcem | 11 | 1.58 | 0.63 | Dlouho | ||
| Drostanolon propionát | C17β | Kyselina propanová | Mastná kyselina s přímým řetězcem | 3 | 1.18 | 0.84 | Krátký | ||
| Metenolon-acetát | C17β | Kyselina etanová | Mastná kyselina s přímým řetězcem | 2 | 1.14 | 0.88 | Krátký | ||
| Metenolon enanthate | C17β | Kyselina heptanová | Mastná kyselina s přímým řetězcem | 7 | 1.37 | 0.73 | Dlouho | ||
| Nandrolon dekanoát | C17β | Kyselina dekanová | Mastná kyselina s přímým řetězcem | 10 | 1.56 | 0.64 | Dlouho | ||
| Nandrolon fenylpropionát | C17β | Kyselina fenylpropanová | Aromatická mastná kyselina | – (~6–7) | 1.48 | 0.67 | Dlouho | ||
| Trenbolonacetát | C17β | Kyselina etanová | Mastná kyselina s přímým řetězcem | 2 | 1.16 | 0.87 | Krátký | ||
| Trenbolon enanthated | C17β | Kyselina heptanová | Mastná kyselina s přímým řetězcem | 7 | 1.41 | 0.71 | Dlouho | ||
| Poznámky pod čarou: A = Délka ester v uhlík atomy pro mastné kyseliny s přímým řetězcem nebo přibližná délka esteru v atomech uhlíku pro aromatické mastné kyseliny. b = Relativní obsah androgenů / anabolických steroidů podle hmotnosti (tj. Relativní androgenní /anabolický potence ). C = Doba trvání podle intramuskulární nebo subkutánní injekce v olejový roztok. d = Nikdy na trhu. Zdroje: Podívejte se na jednotlivé články. | |||||||||
Detekce v tělních tekutinách
Nejčastěji používaným lidským fyziologickým vzorkem pro detekci použití AAS je moč, ačkoli pro tento účel byla vyšetřována jak krev, tak vlasy. AAS, ať už endogenního nebo exogenního původu, podléhají rozsáhlé jaterní biotransformaci různými enzymatickými cestami. Primární metabolity v moči mohou být detekovatelné až 30 dní po posledním použití, v závislosti na konkrétním činidle, dávce a způsobu podání. Řada léčiv má společné metabolické dráhy a jejich profily vylučování se mohou překrývat s profily endogenních steroidů, což činí interpretaci výsledků testování velmi významnou výzvou pro analytika. Metody detekce látek nebo produktů jejich vylučování ve vzorcích moči obvykle zahrnují plynová chromatografie – hmotnostní spektrometrie nebo kapalinová chromatografie - hmotnostní spektrometrie.[191][192][193][194]
Dějiny
| Obecné jméno | Třída[A] | Jméno značky | Trasa[b] | Intr. | ||
|---|---|---|---|---|---|---|
| Androstanolone[C][d] | DHT | Andractim | PO[E], IM, TD | 1953 | ||
| Boldenon undecylenate[F] | Ester | Rovnováha[G] | IM | 1960 | ||
| Danazol | Alkyl | Danocrine | PO | 1971 | ||
| Drostanolon propionát[E] | DHT Ester | Masteron | IM | 1961 | ||
| Ethylestrenol[d] | 19-NT alkyl | Maxibolin[G] | PO | 1961 | ||
| Fluoxymesteron[d] | Alkyl | Halotestin[G] | PO | 1957 | ||
| Mestanolone[E] | DHT alkyl | Androstalone[G] | PO | 1950 | ||
| Mesterolon | DHT | Proviron | PO | 1967 | ||
| Metandienon[d] | Alkyl | Dianabol | PO, IM | 1958 | ||
| Metenolon-acetát[d] | DHT Ester | Primobolan | PO | 1961 | ||
| Metenolon enanthate[d] | DHT Ester | Primobolan Depot | IM | 1962 | ||
| Methyltestosteron[d] | Alkyl | Metandren | PO | 1936 | ||
| Nandrolon dekanoát | 19-NT Ester | Deca-Durabolin | IM | 1962 | ||
| Nandrolon fenylpropionát[d] | 19-NT Ester | Durabolin | IM | 1959 | ||
| Norethandrolon[d] | 19-NT alkyl | Nilevar[G] | PO | 1956 | ||
| Oxandrolon[d] | DHT alkyl | Oxandrin[G] | PO | 1964 | ||
| Oxymetholon[d] | DHT alkyl | Anadrol[G] | PO | 1961 | ||
| Prasterone[h] | Prohormon | Intrarosa[G] | PO, IM, vaginální | Sedmdesátá léta | ||
| Stanozolol[E] | DHT alkyl | Winstrol[G] | PO, IM | 1962 | ||
| Testosteron cypionát | Ester | Depo-testosteron | IM | 1951 | ||
| Testosteron enanthát | Ester | Delatestryl | IM | 1954 | ||
| Testosteron propionát | Ester | Testoviron | IM | 1937 | ||
| Testosteron undekanoát | Ester | Andriol[G] | PO, IM | Sedmdesátá léta | ||
| Trenbolonacetát[F] | 19-NT Ester | Finajet[G] | IM | Sedmdesátá léta | ||
| ||||||
Objev androgenů
Použití gonadal steroidy antedatuje jejich identifikaci a izolaci. Extrakce hormonů z močí začala v Číně c. 100 př. N. L.[Citace je zapotřebí ] Lékařské použití varle extrakt začal na konci 19. století, zatímco jeho účinky na sílu byly ještě studovány.[144] Izolaci gonadálních steroidů lze vysledovat až do roku 1931, kdy Adolf Butenandt, chemik v Marburg, vyčistilo 15 miligramů mužského hormonu androstenon z desítek tisíc litrů moči. Tento steroid byl následně syntetizován v roce 1934 Leopold Ružička, chemik v Curych.[195]
Ve třicátých letech se již vědělo, že testy obsahují silnější androgen než androstenon a tři skupiny vědců, financované soutěžícími farmaceutické společnosti v Nizozemsku, Německu a Švýcarsku se ho snažili izolovat.[195][196] Tento hormon poprvé identifikovali Karoly Gyula David, E. Dingemanse, J. Freud a Ernst Laqueur v příspěvku z května 1935 „O krystalickém mužském hormonu z varlat (testosteron)“.[197] Pojmenovali hormon testosteron, od stonky z varle a sterol a přípona keton. The chemická syntéza testosteronu bylo dosaženo v srpnu téhož roku, kdy Butenandt a G. Hanisch publikovali dokument popisující „Metodu pro přípravu testosteronu z cholesterolu“.[198] Pouze o týden později třetí skupina, Ruzicka a A. Wettstein, ohlásili patentovou přihlášku v článku „O umělé přípravě testosteronového hormonu Testosteron (Androsten-3-one-17-ol)“.[199] Ruzicka a Butenandtovi byl nabídnut rok 1939 Nobelova cena za chemii za jejich práci, ale nacistický Vláda přinutila Butenandta odmítnout čest, ačkoli cenu přijal po skončení druhé světové války.[195][196]
Klinické studie na lidech zahrnující buď PO dávky methyltestosteron nebo injekce testosteron propionát, začalo již v roce 1937.[195] Testosteron propionát je zmíněn v dopise redaktorovi Síla a zdraví časopis v roce 1938; toto je nejdříve známý odkaz na AAS v USA vzpírání nebo kulturistika časopis.[195] Často se objevují zvěsti, že němečtí vojáci byli během druhé světové války spravováni AAS, přičemž cílem bylo zvýšit jejich agresi a vytrvalost, ale zatím nejsou prokázány.[118]:6 Adolf Hitler sám, podle jeho lékaře, byl injekčně podáván s deriváty testosteronu k léčbě různých onemocnění.[200] AAS byly použity při experimentech prováděných nacisty na vězních v koncentračních táborech,[200] a později spojenci pokoušející se léčit podvyživené oběti, které přežily nacistické tábory.[118]:6 Prezident John F. Kennedy byl podáván steroidy před i během jeho prezidentování.[201]
Vývoj syntetických AAS
Rozvoj vlastností testosteronu při budování svalů byl sledován ve 40. letech 20. století v Sovětském svazu a v Východní blok země jako východní Německo, kde byly ke zvýšení výkonu použity steroidní programy olympijský a další amatér vzpěrači. V reakci na úspěch ruských vzpěračů lékař amerického olympijského týmu John Ziegler spolupracoval se syntetickými chemiky na vývoji AAS se sníženými androgenními účinky.[202] Zieglerova práce vyústila ve výrobu methandrostenolone, kterou společnost Ciba Pharmaceuticals prodávala jako Dianabol. Nový steroid byl schválen pro použití v USA Úřad pro kontrolu potravin a léčiv (FDA) v roce 1958. Nejčastěji se podávalo popáleninám obětí a starším lidem. Drogy off-label uživatelé byli většinou kulturisté a vzpěrači. Ačkoli Ziegler předepisoval sportovcům jen malé dávky, brzy zjistil, že ti, kteří zneužívali Dianabol, trpěli zvětšenou prostatou a atrofovanými varlaty.[203] AAS byly zařazeny na seznam zakázaných látek EU Mezinárodní olympijský výbor (IOC) v roce 1976 a o deset let později zavedla komise dopingové testy „mimo soutěž“, protože mnoho sportovců používalo AAS ve svém tréninkovém období spíše než během závodu.[8]
Tři hlavní myšlenky se řídily modifikacemi testosteronu do mnoha AAS: Alkylace na pozici C17α s methyl nebo ethylová skupina vytvořil aktivní sloučeniny POly, protože zpomaluje degradaci léčiva játry; esterifikace testosteronu a nortestosteron v poloze C17p umožňuje podávání látky parenterálně a zvyšuje dobu účinnosti, protože látky rozpustné v olejových kapalinách mohou být v těle přítomny několik měsíců; a změny kruhové struktury byly aplikovány jak pro PO, tak pro parenterální látky k hledání různých poměrů anabolického účinku na androgenní účinek.[8]
Společnost a kultura
Etymologie
Androgeny byly objeveny ve třicátých letech minulého století a byly charakterizovány jako látky s účinky popsanými jako androgenní (tj. Virilizace) a anabolický (např. myotropní, renotrofní).[66][1] Termín anabolický steroid lze datovat přinejmenším do poloviny 40. let 20. století, kdy byla použita k popisu tehdejší hypotetické koncepce steroidu odvozeného od testosteronu s anabolickými účinky, ale s minimálními nebo žádnými androgenními účinky.[204] Tento koncept byl formulován na základě pozorování, že steroidy měly poměry renotrofické a androgenní síly, které se významně lišily, což naznačuje, že anabolické a androgenní účinky mohou být oddělitelné.[204]
V roce 1953, steroid odvozený od testosteronu známý jako norethandrolon (17a-ethyl-19-nortestosteron) byl syntetizován při G. D. Searle & Company a byl studován jako progestin, ale nebyl uveden na trh.[205] Následně, v roce 1955, byl znovu zkoumán na aktivitu podobnou testosteronu u zvířat a bylo zjištěno, že má podobnou anabolickou aktivitu jako testosteron, ale pouze šestnáctou jeho androgenní účinnosti.[205][206] Byl to první steroid s výrazným a příznivým oddělením anabolických a androgenních účinků, který byl objeven, a byl proto popsán jako „první anabolický steroid“.[207][208] Norethandrolon byl zaveden pro lékařské použití v roce 1956 a byl rychle následován například mnoha podobnými steroidy nandrolon fenylpropionát v roce 1959 a stanozolol v roce 1962.[207][208][209][210] S tímto vývojem anabolický steroid se stal preferovaným termínem pro označení těchto steroidů (nad „androgen“) a vstoupil do širokého použití.
Ačkoli anabolický steroid původně zamýšlel specificky popisovat steroidy odvozené od testosteronu s výraznou disociací anabolických a androgenních účinků, dnes se používá bez rozdílu na všechny steroidy s anabolickými účinky založenými na agonismu AR bez ohledu na jejich androgenní účinnost, včetně dokonce i nesyntetických steroidů, jako je testosteron.[66][1][205] Zatímco mnoho anabolických steroidů snížilo androgenní účinnost ve srovnání s anabolickou účinností, neexistuje žádný anabolický steroid, který by byl výhradně anabolický, a proto si všechny anabolické steroidy zachovávají alespoň určitý stupeň androgenicity.[66][1][205] (Stejně tak všechny „androgeny“ jsou ze své podstaty anabolické.)[66][1][205] Pravděpodobně není možné plně oddělit anabolické účinky od androgenních, protože oba typy účinků jsou zprostředkovány stejným signálním receptorem, AR.[1] Jako takový, rozdíl mezi pojmy anabolický steroid a androgen je sporné, a to je základ pro revidovaný a novější termín anabolický androgenní steroid (AAS).[66][1][205]
Právní status
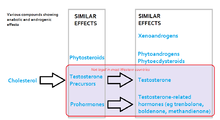
Právní status AAS se v jednotlivých zemích liší: některé mají přísnější kontrolu nad jejich použitím nebo předpisem než jiné, i když v mnoha zemích nejsou nezákonné. V USA jsou AAS v současné době uvedeny jako plán III regulované látky pod Zákon o regulovaných látkách, což z jednoduchého držení těchto látek bez lékařského předpisu činí federální trestný čin, za který lze za první trestný čin uložit až jeden rok vězení. Protiprávní distribuce nebo držení s úmyslem distribuovat AAS jako první trestný čin se trestá až deseti lety vězení.[211] V Kanadě jsou AAS a jejich deriváty součástí Zákon o kontrolovaných drogách a látkách a jsou Rozvrh IV látky, což znamená, že je nezákonné je získávat nebo prodávat bez lékařského předpisu; držení však není trestné, důsledek vyhrazený pro látky plánu I, II nebo III. Ti, kdo se provinili nákupem nebo prodejem AAS v Kanadě, mohou být uvězněni až na 18 měsíců.[212] Podobné sankce jsou spojeny také s dovozem a vývozem.
V Kanadě dospěli vědci k závěru, že užívání steroidů mezi studenty sportovců je extrémně rozšířené. Studie provedená v roce 1993 Kanadským centrem pro sport bez drog zjistila, že téměř 83 000 Kanaďanů ve věku od 11 do 18 let užívá steroidy.[213] AAS jsou také nezákonné bez lékařského předpisu v Austrálii,[214] Argentina,[Citace je zapotřebí ] Brazílie,[Citace je zapotřebí ] a Portugalsko,[Citace je zapotřebí ] a jsou uvedeny jako třída C. Kontrolované léky ve Velké Británii. AAS jsou snadno dostupné bez lékařského předpisu v některých zemích, jako je Mexiko a Thajsko.
Spojené státy

Historie amerických právních předpisů o AAS sahá do konce 80. let, kdy Americký kongres považováno za umístění AAS podle zákona o kontrolovaných látkách po skončení kontroverze Ben Johnson vítězství na Letní olympijské hry 1988 v Soul. AAS byly přidány do přílohy III zákona o kontrolovaných látkách v EU Zákon o kontrole anabolických steroidů z roku 1990.[215]
Stejný zákon také zavedl přísnější kontroly s vyššími trestními sankcemi za trestné činy zahrnující nelegální distribuci AAS a lidského růstového hormonu. Na začátku 90. let, poté, co byly v USA naplánovány AAS, několik farmaceutických společností zastavilo výrobu nebo prodej produktů v USA, včetně Ciba, Searle, Syntex, a další. V zákoně o kontrolovaných látkách jsou AAS definovány jako jakékoli léky nebo hormonální látky chemicky a farmakologicky související s testosteronem (jiné než estrogeny, progestiny, a kortikosteroidy ), které podporují růst svalů. Zákon byl změněn zákonem o kontrole anabolických steroidů z roku 2004, který přidal prohormony do seznamu regulované látky, s účinností od 20. ledna 2005.[216]
Spojené království
Ve Spojeném království jsou AAS klasifikovány jako drogy třídy C pro jejich potenciál nelegálního zneužívání, což je řadí do stejné třídy jako benzodiazepiny. AAS jsou v příloze 4, která je rozdělena na 2 části; Část 1 obsahuje většinu benzodiazepinů a část 2 obsahuje AAS.
Drogy 1. části podléhají úplné kontrole dovozu a vývozu, přičemž jejich držení je trestným činem bez příslušného předpisu. Neexistuje žádné omezení držení, pokud je součástí léčivého přípravku. Léky v části 2 vyžadují povolení ministerstva vnitra pro dovoz a vývoz, pokud není látka ve formě léčivého přípravku a není určena k vlastní aplikaci osobou.[217]
Postavení ve sportu
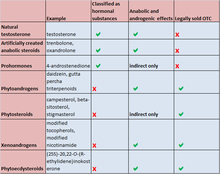
AAS jsou zakázány všemi významnými sportovními subjekty včetně Asociace tenisových profesionálů, Major League Baseball, Fédération Internationale de Football Association[218] the Olympiáda,[219] the Národní Basketbalová asociace,[220] the Národní hokejová liga,[221] World Wrestling Entertainment a Národní fotbalová liga.[222] The Světová antidopingová agentura (WADA) udržuje seznam látek zvyšujících výkonnost používaných mnoha významnými sportovními subjekty a zahrnuje všechny anabolické látky, které zahrnují všechny AAS a prekurzory i všechny hormony a příbuzné látky.[223][224] Španělsko přijalo antidopingový zákon o zřízení národní antidopingové agentury.[225] Itálie přijala zákon v roce 2000, kde se tresty pohybují až na tři roky vězení, pokud má sportovec pozitivní test na zakázané látky.[226] V roce 2006 ruský prezident Vladimír Putin podepsána ratifikace zákona Mezinárodní úmluva proti dopingu ve sportu což by podpořilo spolupráci s WADA. Mnoho dalších zemí má podobné právní předpisy zakazující AAS ve sportu, včetně Dánska,[227] Francie,[228] Nizozemí[229] a Švédsko.[230]
Používání
Vymáhání práva
Federální úředníci pro vymáhání práva USA vyjádřili znepokojení nad používáním AAS policisty. „Je to velký problém a podle počtu případů je to něco, co bychom neměli ignorovat. Nejde o to, že jsme se rozhodli cílit na policisty, ale když jsme uprostřed aktivního vyšetřování steroidy, bylo poměrně málo případů, které vedly zpět k policistům, “říká Lawrence Payne, tiskový mluvčí Spojených států. Správa pro vymáhání drog.[231] Bulletin FBI pro vymáhání práva uvedl, že „zneužívání anabolických steroidů ze strany policistů je vážný problém, který si zaslouží větší povědomí ze strany útvarů po celé zemi“.[232] Rovněž se věří, že policisté ve Spojeném království „užívají zločince k nákupu steroidů“, což je podle něj nejvyšší rizikový faktor pro policejní korupce.
Profesionální wrestling
V návaznosti na vražda-sebevražda Chrise Benoita v roce 2007, Výbor pro dohled a reformu vlády zkoumali užívání steroidů v zápasnickém průmyslu.[233] Výbor to vyšetřoval WWE a Total Nonstop Action Wrestling (nyní známý jako Impact Wrestling ), požadující dokumentaci drogové politiky jejich společností. CEO a předseda WWE, Linda a Vince McMahon oba svědčili. Dokumenty uváděly, že 75 zápasníků - zhruba 40 procent - mělo pozitivní test na užívání drog od roku 2006, nejčastěji na steroidy.[234][235]
Ekonomika

AAS se často vyrábějí ve farmaceutických laboratořích, ale v zemích, kde platí přísnější zákony, se vyrábějí také v malých domácích podzemních laboratořích, obvykle ze surovin dovážených ze zahraničí.[236] V těchto zemích se většina steroidů získává nelegálně prostřednictvím Černý trh obchod.[237][238] Tyto steroidy se obvykle vyrábějí v jiných zemích, a proto musí být pašovaný přes mezinárodní hranice. Stejně jako u nejvýznamnějších pašeráckých operací organizovaný zločin je zapojen.[239]
Na konci dvacátých let celosvětový obchod s nelegálními AAS významně vzrostl a úřady oznámily rekordní odchyt na třech kontinentech. V roce 2006 finské úřady oznámily rekordní zabavení 11,8 milionů tablet AAS. O rok později se DEA zabaveno 11,4 milionu jednotek AAS v dosud největším zabavení v USA. V prvních třech měsících roku 2008 ohlásily australské celní orgány rekordních 300 zadržení zásilek AAS.[240]
V USA, Kanadě a Evropě se nelegální steroidy někdy nakupují stejně jako jakékoli jiné nelegální drogy prostřednictvím prodejců, kteří jsou schopni drogy získat z mnoha zdrojů. Nelegální AAS se někdy prodávají v tělocvičnách a na soutěžích a poštou, ale lze je získat také prostřednictvím lékárníků, veterinářů a lékařů.[241] Kromě toho se značný počet padělaných výrobků prodává jako AAS, zejména prostřednictvím zásilkového prodeje z webů, které se vydávají za zámořské lékárny. V USA pokračuje dovoz na černý trh z Mexika, Thajska a dalších zemí, kde jsou steroidy snadněji dostupné, protože jsou legální.[242]
Výzkum
AAS, samostatně a v kombinaci s progestogeny, byly studovány jako potenciální mužská hormonální antikoncepce.[48] Duální AAS a progestiny jako trestolon a dimethandrolon undekanoát byly rovněž studovány jako mužská antikoncepce, přičemž druhá z nich je od roku 2018 aktivně vyšetřována.[243][179][244]
Topické androgeny byly použity a studovány při léčbě celulitida u žen.[245] Bylo zjištěno, že topický androstanolon na břiše významně snižuje podkožní břišní tuk u žen, a proto může být užitečný pro zlepšení siluety těla.[245] Nicméně, muži a hyperandrogenní ženy mají vyšší množství břišního tuku než zdravé ženy a bylo zjištěno, že androgeny zvyšují břišní tuk v postmenopauzální ženy a transgender muži také.[246]
Viz také
Reference
- ^ A b C d E F G h i j k l m n Ó p q r s t u proti w X y z aa ab ac inzerát ae af ag ah ai aj ak al dopoledne an ao ap vod ar tak jako na au av aw sekera ano az ba bb před naším letopočtem bd být bf bg bh bi bj bk bl bm bn bo Kicman, A T (2008). "Farmakologie anabolických steroidů". British Journal of Pharmacology. 154 (3): 502–521. doi:10.1038 / bjp.2008.165. PMC 2439524. PMID 18500378.
- ^ Powers M (2011). Houglum J, Harrelson GL (eds.). Drogy zvyšující výkon. Principy farmakologie pro atletické trenéry (2. vyd.). SLACK Incorporated. p. 345. ISBN 978-1-55642-901-9.
- ^ A b Barrett-Connor EL (1995). "Testosteron a rizikové faktory pro kardiovaskulární onemocnění u mužů". Diabete Metab. 21 (3): 156–61. PMID 7556805.
- ^ A b Yamamoto Y, Moore R, Hess HA, Guo GL, Gonzalez FJ, Korach KS, Maronpot RR, Negishi M (2006). „Estrogenový receptor alfa zprostředkovává 17alfa-ethynylestradiol způsobující hepatotoxicitu“. J Biol Chem. 281 (24): 16625–31. doi:10,1074 / jbc.M602723200. PMID 16606610. S2CID 83319949.
- ^ A b De Piccoli B, Giada F, Benettin A, Sartori F, Piccolo E (1991). „Užívání anabolických steroidů u kulturistů: echokardiografická studie morfologie a funkce levé komory“. Int J Sports Med. 12 (4): 408–12. doi:10.1055 / s-2007-1024703. PMID 1917226.
- ^ A b C Zelená GA (září 2009). „Užívání drog zvyšujících výkon“. Ortopedie. 32 (9): 647–649. doi:10.3928/01477447-20090728-39. PMID 19751025.
- ^ A b C Turillazzi E, Perilli G, Di Paolo M, Neri M, Riezzo I, Fineschi V (2011). "Vedlejší účinky zneužívání AAS: přehled". Mini Rev Med Chem. 11 (5): 374–89. doi:10.2174/138955711795445925. PMID 21443513.
- ^ A b C d E F G h i j k Hartgens F, Kuipers H (2004). "Účinky androgenních-anabolických steroidů u sportovců". Sports Med. 34 (8): 513–54. doi:10.2165/00007256-200434080-00003. PMID 15248788. S2CID 15234016.
- ^ A b Kicman AT, Gower DB (červenec 2003). „Anabolické steroidy ve sportu: biochemické, klinické a analytické perspektivy“. Ann. Clin. Biochem. 40 (Pt 4): 321–56. doi:10.1258/000456303766476977. PMID 12880534. S2CID 24339701.

- ^ Basaria S, Wahlstrom JT, Dobs AS (listopad 2001). „Clinical review 138: Anabolic-androgenic steroid therapy in the treatment of chronic addresses“. J. Clin. Endokrinol. Metab. 86 (11): 5108–17. doi:10.1210 / jcem.86.11.7983. PMID 11701661.
- ^ Ranke MB, Bierich JR (1986). "Léčba nedostatku růstového hormonu". Kliniky endokrinologie a metabolismu. 15 (3): 495–510. doi:10.1016 / S0300-595X (86) 80008-1. PMID 2429792.
- ^ Grunfeld C, Kotler DP, Dobs A, Glesby M, Bhasin S (2006). „Oxandrolon při léčbě úbytku hmotnosti u mužů související s HIV: randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie“. J. Acquir. Imunitní deficit. Syndr. 41 (3): 304–14. doi:10.1097 / 01.qai.0000197546.56131.40. PMID 16540931. S2CID 25911263.
- ^ Berger JR, Pall L, Hall CD, Simpson DM, Berry PS, Dudley R (1996). „Oxandrolon při myopatii plýtvající AIDS“. AIDS. 10 (14): 1657–62. doi:10.1097/00002030-199612000-00010. PMID 8970686. S2CID 9832782.
- ^ Kenny AM, Prestwood KM, Gruman CA, Marcello KM, Raisz LG (2001). "Účinky transdermálního testosteronu na kosti a svaly u starších mužů s nízkou biologicky dostupnou hladinou testosteronu". J. Gerontol. Biol. Sci. Med. Sci. 56 (5): M266–72. doi:10.1093 / gerona / 56.5.M266. PMID 11320105.
- ^ Baum NH, Crespi CA (2007). "Náhrada testosteronu u starších mužů". Geriatrie. 62 (9): 14–8. PMID 17824721.
- ^ Francis RM (2001). "Náhrada androgenu u stárnoucích mužů". Calcif. Tissue Int. 69 (4): 235–8. doi:10.1007 / s00223-001-1051-9. PMID 11730258. S2CID 24170276.
- ^ Nair KS, Rizza RA, O'Brien P, Dhatariya K, Short KR, Nehra A, Vittone JL, Klee GG, Basu A, Basu R, Cobelli C, Toffolo G, Dalla Man C, Tindall DJ, Melton LJ, Smith GE , Khosla S, Jensen MD (říjen 2006). „DHEA u starších žen a DHEA nebo testosteron u starších mužů“. N. Engl. J. Med. 355 (16): 1647–59. doi:10.1056 / NEJMoa054629. PMID 17050889. S2CID 42844580.
- ^ A b C d Mangus BC, Miller MG (11. ledna 2005). Farmakologická aplikace v atletickém tréninku. F.A. Davis. str. 151–. ISBN 978-0-8036-2027-8.
- ^ Royal College of Physicians of London (1999). Osteoporóza: Klinické pokyny pro prevenci a léčbu. Královská vysoká škola lékařů. str. 51–. ISBN 978-1-86016-079-0.
- ^ Davis SR (1999). "Terapeutické použití androgenů u žen". J. Steroid Biochem. Mol. Biol. 69 (1–6): 177–84. doi:10.1016 / s0960-0760 (99) 00054-0. PMID 10418991. S2CID 23520067.
- ^ William N. Taylor, M.D. (16. ledna 2002). Anabolické steroidy a sportovec, 2. vydání. McFarland. 193–. ISBN 978-0-7864-1128-3.
- ^ A b „Oxandrolone Tablets, USP - Rx only“ (PDF). Drogy @ FDA. US Food and Drug Administration. 1. prosince 2006. Citováno 21. června 2016.
- ^ A b „Oxandrin (tablety oxandrolonu, USP)“ (PDF). Drogy @ FDA. BTG Pharmaceuticals, US Food and Drug Administration. 21.dubna 2003. Citováno 21. června 2016.
- ^ Li H, Guo Y, Yang Z, Roy M, Guo Q (červen 2016). „Účinnost a bezpečnost léčby oxandrolonem u pacientů s těžkými popáleninami: systematický přehled a metaanalýza“. Popáleniny. 42 (4): 717–27. doi:10.1016 / j.burns.2015.08.023. PMID 26454425.
- ^ Rojas Y, Finnerty CC, Radhakrishnan RS, Herndon DN (prosinec 2012). „Popáleniny: aktuální informace o současné farmakoterapii“. Znalecký posudek na farmakoterapii. 13 (17): 2485–94. doi:10.1517/14656566.2012.738195. PMC 3576016. PMID 23121414.
- ^ Bork K (srpen 2012). "Současné možnosti léčby dědičného angioedému". Aktuální zprávy o alergii a astmatu. 12 (4): 273–80. doi:10.1007 / s11882-012-0273-4. PMID 22729959. S2CID 207323793.
- ^ Choi G, Runyon BA (květen 2012). „Alkoholická hepatitida: průvodce lékaře“. Kliniky jaterních chorob. 16 (2): 371–85. doi:10.1016 / j.cld.2012.03.015. PMID 22541704.
- ^ Manuchair Ebadi (31. října 2007). Desk Reference of Clinical Pharmacology, druhé vydání. CRC Press. 434–. ISBN 978-1-4200-4744-8.
- ^ Yagiela JA, Dowd FJ, Johnson B, Mariotti A, Neidle EA (19. března 2010). Farmakologie a terapeutika pro zubní lékařství - elektronická kniha. Elsevier Health Sciences. 569–. ISBN 978-0-323-07824-5.
- ^ https://www.accessdata.fda.gov/drugsatfda_docs/label/2014/083976s031lbl.pdf
- ^ Shah K, Montoya C, Persons RK (duben 2007). „Klinické dotazy. Zvyšují injekce testosteronu libido u starších pacientů s hypogonadami?“. J Fam Pract. 56 (4): 301–3. PMID 17403329.
- ^ Yassin AA, Saad F (březen 2007). "Zlepšení sexuální funkce u mužů s pozdním nástupem hypogonadismu léčených pouze testosteronem". J Sex Med. 4 (2): 497–501. doi:10.1111 / j.1743-6109.2007.00442.x. PMID 17367445.
- ^ Arver S, Dobs AS, Meikle AW, Caramelli KE, Rajaram L, Sanders SW, Mazer NA (prosinec 1997). „Dlouhodobá účinnost a bezpečnost transdermálního systému testosteronu se zvýšenou permeací u hypogonadálních mužů“. Clin. Endokrinol. 47 (6): 727–37. doi:10.1046 / j.1365-2265.1997.3071113.x. PMID 9497881. S2CID 31976796.
- ^ Nieschlag E, Büchter D, Von Eckardstein S, Abshagen K, Simoni M, Behre HM (prosinec 1999). „Opakované intramuskulární injekce undekanoátu testosteronu pro substituční terapii u hypogonadálních mužů“. Clin. Endokrinol. 51 (6): 757–63. doi:10.1046 / j.1365-2265.1999.00881.x. PMID 10619981. S2CID 19174381.
- ^ Arslanian S, Suprasongsin C (1997). „Léčba testosteronem u dospívajících se zpožděnou pubertou: změny ve složení těla, metabolismu bílkovin, tuků a glukózy“. J. Clin. Endokrinol. Metab. 82 (10): 3213–20. doi:10.1210 / jc.82.10.3213. PMID 9329341.
- ^ Moore E, Wisniewski A, Dobs A (srpen 2003). „Endokrinní léčba transsexuálních lidí: přehled léčebných režimů, výsledků a nežádoucích účinků“. J. Clin. Endokrinol. Metab. 88 (8): 3467–73. doi:10.1210 / jc.2002-021967. PMID 12915619.
- ^ Genderqueer, Pansexual, LGBTQ: Bude pohlaví existovat 100 let ode dneška? - Restartováno. 24. října 2013. Citováno 17. listopadu 2014.
- ^ Mladí lidé zkoumající jiné než genderové role - SF Gate. 12. února 2014. Citováno 17. listopadu 2014.
- ^ Warne GL, Grover S, Zajac JD (2005). "Hormonální terapie pro jedince s intersexuálními stavy: protokol pro použití". Léčba v endokrinologii. 4 (1): 19–29. doi:10.2165/00024677-200504010-00003. PMID 15649098. S2CID 71737774.
- ^ Co je Intersex - Intersex FAQ od Inter / Act - Inter / Act Youth Archivováno 07.12.2014 na Wayback Machine. 12. září 2014. Citováno 5. prosince 2014.
- ^ Perry MC, Doll DC, Freter CE (30. července 2012). Perry's The Chemotherapy Source Book. Lippincott Williams & Wilkins. 409–. ISBN 978-1-4698-0343-2.
- ^ Allegra JC, Bertino J, Bonomi P, Byrne P, Carpenter J, Catalano R, Creech R, Dana B, Durivage H, Einhorn L (prosinec 1985). „Metastatický karcinom prsu: předběžné výsledky při perorální hormonální terapii“. Semin. Oncol. 12 (4 Suppl 6): 61–4. PMID 3909420.
- ^ Bachmann GA (1999). „Androgenní terapie v menopauze: vyvíjející se výhody a výzvy“. Dopoledne. J. Obstet. Gynecol. 180 (3 Pt 2): S308–11. doi:10.1016 / S0002-9378 (99) 70724-6. PMID 10076169.
- ^ Kotz K, Alexander JL, Dennerstein L (2006). „Estrogenová a androgenní hormonální terapie a pohoda u chirurgicky postmenopauzálních žen“. J Zdraví žen (Larchmt). 15 (8): 898–908. doi:10.1089 / jwh.2006.15.898. PMID 17087613.
- ^ Garefalakis M, Hickey M (2008). „Role androgenů, progestinů a tibolonu v léčbě menopauzálních symptomů: přehled klinických důkazů“. Klinické stárnutí. 3 (1): 1–8. doi:10.2147 / CIA.S1043. PMC 2544356. PMID 18488873.
- ^ A b Somboonporn W (2006). "Androgen a menopauza". Curr. Opin. Obstet. Gynecol. 18 (4): 427–32. doi:10.1097 / 01.gco.0000233938.36554,37. PMID 16794424. S2CID 8030248.
- ^ Davis S (2001). "Nedostatek testosteronu u žen". J Reprod Med. 46 (3 doplňky): 291–6. PMID 11304877.
- ^ A b C Nieschlag E (2010). „Klinické studie u mužské hormonální antikoncepce“ (PDF). Antikoncepce. 82 (5): 457–70. doi:10.1016 / j. Antikoncepce.2010.03.020. PMID 20933120.
- ^ „Většina uživatelů steroidů nejsou sportovci: studie“. Reuters. Reuters. 21. 11. 2007. Citováno 2014-01-03.
- ^ Sjöqvist F, Garle M, Rane A (květen 2008). "Užívání dopingových látek, zejména anabolických steroidů, ve sportu a ve společnosti". Lanceta. 371 (9627): 1872–82. doi:10.1016 / S0140-6736 (08) 60801-6. PMID 18514731. S2CID 10762429.
- ^ Yesalis CE, Kennedy NJ, Kopstein AN, Bahrke MS (1993). „Užívání anabolicko-androgenních steroidů ve Spojených státech“. JAMA. 270 (10): 1217–21. doi:10.1001 / jama.270.10.1217. PMID 8355384.
- ^ McCabe SE, Brower KJ, West BT, Nelson TF, Wechsler H (2007). „Trendy v nelékařském užívání anabolických steroidů vysokoškoláky z USA: výsledky čtyř národních průzkumů“. Závislost na drogách a alkoholu. 90 (2–3): 243–51. doi:10.1016 / j.drugalcdep.2007.04.004. PMC 2383927. PMID 17512138.
- ^ Parkinson AB, Evans NA (duben 2006). „Anabolické androgenní steroidy: průzkum mezi 500 uživateli“. Med Sci Sports Exerc. 38 (4): 644–51. doi:10.1249 / 01.mss.0000210194.56834.5d. PMID 16679978.
- ^ A b C d E Cohen J, Collins R, Darkes J, Gwartney D (2007). „Liga jejich vlastních: demografie, motivace a vzorce užívání 1955 dospělých dospělých nelékařských anabolických steroidů ve Spojených státech“. J Int Soc Sports Nutr. 4: 12. doi:10.1186/1550-2783-4-12. PMC 2131752. PMID 17931410.
- ^ Copeland J, Peters R, Dillon P (březen 1998). „Studie 100 uživatelů anabolicko-androgenních steroidů“. Med. J. Aust. 168 (6): 311–2. doi:10.5694 / j.1326-5377.1998.tb140177.x. PMID 9549549. S2CID 8699231.
- ^ Eastley T (18. ledna 2006). „Steroidní studie odhaluje stereotypy uživatelů“. ABC. Citováno 2014-01-03.
- ^ Papež HG, Kanayama G, Ionescu-Pioggia M, Hudson JI (září 2004). "Postoj uživatelů anabolických steroidů k lékařům". Závislost. 99 (9): 1189–94. doi:10.1111 / j.1360-0443.2004.00781.x. PMID 15317640.
- ^ Kanayama G, Barry S, Hudson JI, papež HG (duben 2006). „Obraz těla a postoje k mužským rolím u uživatelů anabolicko-androgenních steroidů“. Jsem J. Psychiatrie. 163 (4): 697–703. doi:10.1176 / appi.ajp.163.4.697. PMID 16585446. S2CID 38738640.
- ^ Grogan S, Shepherd S, Evans R, Wright S, Hunter G (listopad 2006). "Zkušenosti s užíváním anabolických steroidů". Journal of Health Psychology. 11 (6): 845–856. doi:10.1177/1359105306069080. PMID 17035257. S2CID 5794238.
- ^ Hickson RC, Czerwinski SM, Falduto MT, Young AP (1990). „Glukokortikoidový antagonismus cvičením a androgenní-anabolické steroidy“. Medicína a věda ve sportu a cvičení. 22 (3): 331–40. doi:10.1249/00005768-199006000-00010. PMID 2199753.
- ^ „Drugs @ FDA: FDA Approved Drug Products“. United States Food and Drug Administration. Citováno 1. prosince 2019.
- ^ Richard Joseph Hamilton; Nancy Anastasi Duffy; Daniel Stone (2014). Lékopis Tarascon. Vydavatelé Jones & Bartlett. 174–. ISBN 978-1-284-05671-6.
- ^ Susan M. Fordová; Sally S. Roach (2010). Roachova úvodní klinická farmakologie. Lippincott Williams & Wilkins. 499–. ISBN 978-1-60547-633-9.
- ^ Thomas L. Lemke; David A. Williams (24. ledna 2012). Foyeho principy léčivé chemie. Lippincott Williams & Wilkins. str. 1358–. ISBN 978-1-60913-345-0.
- ^ John A. Thomas (6. prosince 2012). Drogy, sportovci a fyzická výkonnost. Springer Science & Business Media. str. 20–. ISBN 978-1-4684-5499-4.
- ^ A b C d E F G h i j k l m n Ó p q r s t William Llewellyn (2011). Anabolika. Molecular Nutrition LLC. ISBN 978-0-9828280-1-4.
- ^ Burkett, Lee N .; Falduto, Michael T. (1984). „Užívání steroidů sportovci v metropolitní oblasti“. Lékař a sportovní medicína. 12 (8): 69–74. doi:10.1080/00913847.1984.11701923. ISSN 0091-3847.
- ^ J. Bain; Wolf-Bernhard Schill; L. Schwarzstein (6. prosince 2012). Léčba mužské neplodnosti. Springer Science & Business Media. 176–177. ISBN 978-3-642-68223-0.
- ^ Snyder, PJ (1984). „Klinické použití androgenů“. Roční přehled medicíny. 35 (1): 207–217. doi:10.1146 / annurev.me.35.020184.001231. ISSN 0066-4219. PMID 6372655.
- ^ A b C Becker KL (2001). Principy a praxe endokrinologie a metabolismu. Lippincott Williams & Wilkins. str. 1185–1186. ISBN 978-0-7817-1750-2.
- ^ A b Rahnema CD, Crosnoe LE, Kim ED (březen 2015). „Designérské steroidy - volně prodejné doplňky a jejich androgenní složka: recenze narůstajícího problému“. Andrologie. 3 (2): 150–5. doi:10.1111 / andr.307. PMID 25684733. S2CID 6999218.
- ^ A b Chrousos GP (2012). "Gonadální hormony a inhibitory". V Katzung BG (ed.). Základní a klinická farmakologie. New York London: distributor McGraw-Hill Medical McGraw-Hill. ISBN 978-0071764018.
- ^ Mutzebaugh C (1998). „Znamená skutečně volba alfa-AAS rozdíl?“. Hotline pro HIV. 8 (5–6): 10–1. PMID 11366379.
- ^ Casavant MJ, Blake K, Griffith J, Yates A, Copley LM (2007). "Důsledky užívání anabolických androgenních steroidů". Pediatr. Clin. North Am. 54 (4): 677–90, x. doi:10.1016 / j.pcl.2007.04.001. PMID 17723870.
- ^ Pope HG, Wood RI, Rogol A, Nyberg F, Bowers L, Bhasin S (2014). „Nežádoucí účinky léků zvyšujících výkonnost na zdraví: vědecké prohlášení endokrinní společnosti“. Endocr. Rev. 35 (3): 341–75. doi:10.1210 / er.2013-1058. PMC 4026349. PMID 24423981.
- ^ Fragkaki AG, Angelis YS, Koupparis M, Tsantili-Kakoulidou A, Kokotos G, Georgakopoulos C (2009). "Strukturální charakteristiky anabolických androgenních steroidů přispívající k vazbě na androgenní receptor a k jejich anabolickým a androgenním aktivitám. Aplikované úpravy ve steroidní struktuře". Steroidy. 74 (2): 172–97. doi:10.1016 / j.steroids.2008.10.016. PMID 19028512. S2CID 41356223.
- ^ Nieschlag E, Vorona E (2015). „MECHANISMY V ENDOKRINOLOGII: Lékařské důsledky dopingu anabolickými androgenními steroidy: účinky na reprodukční funkce“. Eur. J. Endocrinol. 173 (2): R47–58. doi:10.1530 / EJE-15-0080. PMID 25805894.
- ^ Hall RC, Hall RC, Chapman MJ (2005). "Psychiatrické komplikace zneužívání anabolických steroidů". Psychosomatika. 46 (4): 285–90. doi:10.1176 / appi.psy.46.4.285. PMID 16000671.
- ^ A b Trenton AJ, Currier GW (2005). "Behaviorální projevy užívání anabolických steroidů". Léky na CNS. 19 (7): 571–95. doi:10.2165/00023210-200519070-00002. PMID 15984895. S2CID 32243658.
- ^ Vanberg P, Atar D (2010). "Zneužívání androgenních anabolických steroidů a kardiovaskulární systém". Příručka experimentální farmakologie. 195 (195): 411–57. doi:10.1007/978-3-540-79088-4_18. ISBN 978-3-540-79087-7. PMID 20020375.
- ^ Achar S, Rostamian A, Narayan SM (2010). „Srdeční a metabolické účinky zneužívání anabolicko-androgenních steroidů na lipidy, krevní tlak, rozměry levé komory a rytmus“. Dopoledne. J. Cardiol. 106 (6): 893–901. doi:10.1016 / j.amjcard.2010.05.013. PMC 4111565. PMID 20816133.
- ^ Solimini R, Rotolo MC, Mastrobattista L, Mortali C, Minutillo A, Pichini S, Pacifici R, Palmi I (2017). "Hepatotoxicity associated with illicit use of anabolic androgenic steroids in doping". Eur Rev Med Pharmacol Sci. 21 (1 Suppl): 7–16. PMID 28379599.
- ^ Brenu EW, McNaughton L, Marshall-Gradisnik SM (2011). "Is there a potential immune dysfunction with anabolic androgenic steroid use?: A review". Mini Rev Med Chem. 11 (5): 438–45. doi:10.2174/138955711795445907. PMID 21443507.
- ^ Grace F, Sculthorpe N, Baker J, Davies B (2003). "Blood pressure and rate pressure product response in males using high-dose anabolic-androgenic steroids (AAS)". J Sci Med Sport. 6 (3): 307–12. doi:10.1016/S1440-2440(03)80024-5. PMID 14609147.
- ^ "DailyMed: About DailyMed". Dailymed.nlm.nih.gov. Citováno 2008-11-03.
- ^ Bagatell CJ, Knopp RH, Vale WW, Rivier JE, Bremner WJ (1992). "Physiologic testosterone levels in normal men suppress high-density lipoprotein cholesterol levels". Annals of Internal Medicine. 116 (12 Pt 1): 967–73. doi:10.7326/0003-4819-116-12-967. PMID 1586105.
- ^ Mewis C, Spyridopoulos I, Kühlkamp V, Seipel L (1996). "Manifestation of severe coronary heart disease after anabolic drug abuse". Klinická kardiologie. 19 (2): 153–5. doi:10.1002/clc.4960190216. PMID 8821428. S2CID 37024092.
- ^ Melnik B, Jansen T, Grabbe S (2007). "Abuse of anabolic-androgenic steroids and bodybuilding acne: an underestimated health problem". Journal der Deutschen Dermatologischen Gesellschaft. 5 (2): 110–7. doi:10.1111/j.1610-0387.2007.06176.x. PMID 17274777. S2CID 13382470.
- ^ Vierhapper H, Maier H, Nowotny P, Waldhäusl W (July 2003). "Production rates of testosterone and of dihydrotestosterone in female pattern hair loss". Metab. Clin. Exp. 52 (7): 927–9. doi:10.1016/S0026-0495(03)00060-X. PMID 12870172.
- ^ Irving LM, Wall M, Neumark-Sztainer D, Story M (2002). "Steroid use among adolescents: findings from Project EAT". The Journal of Adolescent Health. 30 (4): 243–52. doi:10.1016/S1054-139X(01)00414-1. PMID 11927236.
- ^ "Known and Probable Human Carcinogens". Americká rakovinová společnost. 2011-06-29.
- ^ Sullivan ML, Martinez CM, Gallagher EJ (1999). "Atrial fibrillation and anabolic steroids". The Journal of Emergency Medicine. 17 (5): 851–7. doi:10.1016/S0736-4679(99)00095-5. PMID 10499702.
- ^ Dickerman RD, Schaller F, McConathy WJ (1998). "Left ventricular wall thickening does occur in elite power athletes with or without anabolic steroid Use". Kardiologie. 90 (2): 145–8. doi:10.1159/000006834. PMID 9778553. S2CID 22123696.
- ^ George KP, Wolfe LA, Burggraf GW (1991). "The 'athletic heart syndrome'. A critical review". Sportovní medicína. 11 (5): 300–30. doi:10.2165/00007256-199111050-00003. PMID 1829849. S2CID 45280834.
- ^ Dickerman RD, Schaller F, Zachariah NY, McConathy WJ (1997). "Left ventricular size and function in elite bodybuilders using anabolic steroids". Clin J Sport Med. 7 (2): 90–3. doi:10.1097/00042752-199704000-00003. PMID 9113423. S2CID 42891343.
- ^ Salke RC, Rowland TW, Burke EJ (1985). "Left ventricular size and function in body builders using anabolic steroids". Medicína a věda ve sportu a cvičení. 17 (6): 701–4. doi:10.1249/00005768-198512000-00014. PMID 4079743.
- ^ Tokar S (February 2006). "Liver Damage And Increased Heart Attack Risk Caused By Anabolic Steroid Use". University of California – San Francisco. Citováno 2007-04-24.
- ^ Wit JM, Oostdijk W (2015). "Novel approaches to short stature therapy". Best Practice & Research. Clinical Endocrinology & Metabolism. 29 (3): 353–66. doi:10.1016/j.beem.2015.01.003. PMID 26051296.
- ^ Marcus R, Korenman SG (1976). "Estrogens and the human male". Annu Rev Med. 27: 357–70. doi:10.1146/annurev.me.27.020176.002041. PMID 779604.
- ^ Matsumoto AM (1990). "Effects of chronic testosterone administration in normal men: safety and efficacy of high dosage testosterone and parallel dose-dependent suppression of luteinizing hormone, follicle-stimulating hormone, and sperm production". J. Clin. Endokrinol. Metab. 70 (1): 282–7. doi:10.1210/jcem-70-1-282. PMID 2104626.
- ^ Hoffman JR, Ratamess NA (June 1, 2006). "Medical Issues Associated with Anabolic Steroid Use: Are they Exaggerated?" (PDF). Journal of Sports Science and Medicine. Archivováno (PDF) from the original on 20 June 2007. Citováno 2007-05-08.
- ^ Meriggiola MC, Costantino A, Bremner WJ, Morselli-Labate AM (2002). "Higher testosterone dose impairs sperm suppression induced by a combined androgen-progestin regimen". J. Androl. 23 (5): 684–90. doi:10.1002/j.1939-4640.2002.tb02311.x (neaktivní 11. 11. 2020). PMID 12185103.CS1 maint: DOI neaktivní od listopadu 2020 (odkaz)
- ^ Alén M, Reinilä M, Vihko R (1985). "Response of serum hormones to androgen administration in power athletes". Medicína a věda ve sportu a cvičení. 17 (3): 354–9. doi:10.1249/00005768-198506000-00009. PMID 2991700.
- ^ Franke WW, Berendonk B (July 1997). "Hormonal doping and androgenization of athletes: a secret program of the German Democratic Republic government". Klinická chemie. 43 (7): 1262–79. doi:10.1093/clinchem/43.7.1262. PMID 9216474.
- ^ Manikkam M, Crespi EJ, Doop DD, Herkimer C, Lee JS, Yu S, Brown MB, Foster DL, Padmanabhan V (February 2004). "Fetal programming: prenatal testosterone excess leads to fetal growth retardation and postnatal catch-up growth in sheep". Endokrinologie. 145 (2): 790–8. doi:10.1210/en.2003-0478. PMID 14576190.
- ^ Herlitz LC, Markowitz GS, Farris AB, Schwimmer JA, Stokes MB, Kunis C, Colvin RB, D'Agati VD (October 29, 2009). Development of FSGS Following Anabolic Steroid Use in Bodybuilders (PDF). 42nd Annual Meeting and Scientific Exposition of the American Society of Nephrology. Bodybuilding With Steroids Damages Kidneys. Shrnutí ležel – ScienceDaily (October 30, 2009).
- ^ Nutt D, King LA, Saulsbury W, Blakemore C (March 2007). "Development of a rational scale to assess the harm of drugs of potential misuse". Lanceta. 369 (9566): 1047–53. doi:10.1016/S0140-6736(07)60464-4. PMID 17382831. S2CID 5903121.
- ^ A b Kanayama G, Hudson JI, Pope HG (November 2008). "Long-Term Psychiatric and Medical Consequences of Anabolic-Androgenic Steroid Abuse: A Looming Public Health Concern?". Drug Alcohol Depend. 98 (1–2): 1–12. doi:10.1016/j.drugalcdep.2008.05.004. PMC 2646607. PMID 18599224.
- ^ Brower KJ (October 2002). "Anabolic steroid abuse and dependence". Curr Psychiatry Rep. 4 (5): 377–87. doi:10.1007/s11920-002-0086-6. PMID 12230967. S2CID 25684227.
- ^ Fudala PJ, Weinrieb RM, Calarco JS, Kampman KM, Boardman C (2003). "An evaluation of anabolic-androgenic steroid abusers over a period of 1 year: seven case studies". Annals of Clinical Psychiatry. 15 (2): 121–30. doi:10.3109/10401230309085677. PMID 12938869.
- ^ Pagonis TA, Angelopoulos NV, Koukoulis GN, Hadjichristodoulou CS (2006). "Psychiatric side effects induced by supraphysiological doses of combinations of anabolic steroids correlate to the severity of abuse". Eur. Psychiatrie. 21 (8): 551–62. doi:10.1016/j.eurpsy.2005.09.001. PMID 16356691.
- ^ A b Rashid H, Ormerod S, Day E (2007). "Anabolic androgenic steroids: What the psychiatrist needs to know". Pokroky v psychiatrické léčbě. 13 (3): 203–211. doi:10.1192/apt.bp.105.000935.
- ^ Cooper CJ, Noakes TD, Dunne T, Lambert MI, Rochford K (September 1996). "A high prevalence of abnormal personality traits in chronic users of anabolic-androgenic steroids". Br J Sports Med. 30 (3): 246–50. doi:10.1136/bjsm.30.3.246. PMC 1332342. PMID 8889121.
- ^ "Dr. Ritchi Morris". Vitalquests.org. Archivovány od originál dne 03.12.2013. Citováno 2013-12-01.
- ^ Kanayama G, Brower KJ, Wood RI, Hudson JI, Pope HG (December 2009). "Anabolic-androgenic steroid dependence: an emerging disorder". Závislost. 104 (12): 1966–78. doi:10.1111/j.1360-0443.2009.02734.x. PMC 2780436. PMID 19922565.
- ^ Eisenberg ER, Galloway GP (1992). "Anabolic androgenic steroids". In Lowinson JH, Ruiz P, Millman RB (eds.). Substance Abuse: A Comprehensive Textbook. Lippincott Williams & Wilkins. JAKO V B0049VACMW.
- ^ Lindström M, Nilsson AL, Katzman PL, Janzon L, Dymling JF (1990). "Use of anabolic-androgenic steroids among body builders—frequency and attitudes". J. Intern. Med. 227 (6): 407–11. doi:10.1111/j.1365-2796.1990.tb00179.x. PMID 2351927. S2CID 22121959.
- ^ A b C Lenahan P (2003). Anabolic Steroids: And Other Performance-enhancing Drugs. Londýn: Taylor & Francis. ISBN 0-415-28030-3.
- ^ Thiblin I, Petersson A (February 2005). "Pharmacoepidemiology of anabolic androgenic steroids: a review". Fundam Clin Pharmacol. 19 (1): 27–44. doi:10.1111/j.1472-8206.2004.00298.x. PMID 15660958. S2CID 2009549.
- ^ Beaver KM, Vaughn MG, Delisi M, Wright JP (December 2008). "Anabolic-Androgenic Steroid Use and Involvement in Violent Behavior in a Nationally Representative Sample of Young Adult Males in the United States". Am J Public Health. 98 (12): 2185–7. doi:10.2105/AJPH.2008.137018. PMC 2636528. PMID 18923108.
- ^ Bahrke MS, Yesalis CE, Wright JE (1996). "Psychological and behavioural effects of endogenous testosterone and anabolic-androgenic steroids. An update". Sportovní medicína. 22 (6): 367–90. doi:10.2165/00007256-199622060-00005. PMID 8969015. S2CID 23846419.
- ^ A b C Bhasin S, Storer TW, Berman N, Callegari C, Clevenger B, Phillips J, Bunnell TJ, Tricker R, Shirazi A, Casaburi R (July 1996). "The effects of supraphysiologic doses of testosterone on muscle size and strength in normal men". N. Engl. J. Med. 335 (1): 1–7. doi:10.1056/NEJM199607043350101. PMID 8637535.
- ^ Tricker R, Casaburi R, Storer TW, Clevenger B, Berman N, Shirazi A, Bhasin S (October 1996). "The effects of supraphysiological doses of testosterone on angry behavior in healthy eugonadal men—a clinical research center study". J. Clin. Endokrinol. Metab. 81 (10): 3754–8. doi:10.1210/jcem.81.10.8855834. PMID 8855834.
- ^ Pope HG, Kouri EM, Hudson JI (February 2000). "Effects of supraphysiologic doses of testosterone on mood and aggression in normal men: a randomized controlled trial". Oblouk. Gen. psychiatrie. 57 (2): 133–40, discussion 155–6. doi:10.1001/archpsyc.57.2.133. PMID 10665615.

- ^ Pagonis TA, Angelopoulos NV, Koukoulis GN, Hadjichristodoulou CS, Toli PN (2006). "Psychiatric and hostility factors related to use of anabolic steroids in monozygotic twins". Eur. Psychiatrie. 21 (8): 563–9. doi:10.1016/j.eurpsy.2005.11.002. PMID 16529916.
- ^ Perry PJ, Kutscher EC, Lund BC, Yates WR, Holman TL, Demers L (May 2003). "Measures of aggression and mood changes in male weightlifters with and without androgenic anabolic steroid use". J. Forensic Sci. 48 (3): 646–51. doi:10.1520/JFS2002240. PMID 12762541.
- ^ "Teens & Steroids: A Dangerous Mix". CBS Broadcasting Inc. 2004-06-03. Archivováno z původního dne 10. července 2007. Citováno 2007-06-27.
- ^ Uzych L (February 1992). "Anabolic-androgenic steroids and psychiatric-related effects: a review". Může J psychiatrie. 37 (1): 23–8. doi:10.1177/070674379203700106. PMID 1551042. S2CID 22571743.
- ^ "Anabolic Steroids and Suicide – A Brief Review of the Evidence". Thinksteroids.com. 2005-07-12. Citováno 2013-12-01.
- ^ A b C d El Osta R, Almont T, Diligent C, Hubert N, Eschwège P, Hubert J (2016). "Anabolic steroids abuse and male infertility". Basic Clin Androl. 26 (2): 2. doi:10.1186/s12610-016-0029-4 (neaktivní 11. 11. 2020). PMC 4744441. PMID 26855782.CS1 maint: DOI neaktivní od listopadu 2020 (odkaz)
- ^ Kickman AT (2008). "Farmakologie anabolických steroidů". Br J Pharmacol. 154 (3): 502–521. doi:10.1038 / bjp.2008.165. PMC 2439524. PMID 18500378.
- ^ Stromme SB, Meen HD, Aakvaag A (1974). "Effects of an androgenic-anabolic steroid on strength development and plasma testosterone levels in normal males". Med Sci Sports. 6 (3): 203–208. PMID 4437350.
- ^ Sagoe D, Molde H, Andreassen CS, Torsheim T, Pallesen S (2014). "The global epidemiology of anabolic-androgenic steroid use: a meta-analysis and meta-regression analysis". Ann Epidemiol. 24 (5): 383–398. doi:10.1007/s40279-017-0709-z. PMID 24582699. S2CID 42489596.
- ^ Christou MA, Christou PA, Markozannes G, Tsatsoulis A, Mastorakos G, Tigas S (2017). "Effects of Anabolic Androgenic Steroids on the Reproductive System of Athletes and Recreational Users: A Systematic Review and Meta-Analysis". Sports Med. 47 (9): 1869–1883. doi:10.1007/s40279-017-0709-z. PMID 28258581. S2CID 42489596.
- ^ Pereira de Jésus-Tran K, Côté PL, Cantin L, Blanchet J, Labrie F, Breton R (2006). "Comparison of crystal structures of human androgen receptor ligand-binding domain complexed with various agonists reveals molecular determinants responsible for binding affinity". Protein Sci. 15 (5): 987–99. doi:10.1110/ps.051905906. PMC 2242507. PMID 16641486.
- ^ Lavery DN, McEwan IJ (2005). "Structure and function of steroid receptor AF1 transactivation domains: induction of active conformations". Biochem. J. 391 (Pt 3): 449–64. doi:10.1042/BJ20050872. PMC 1276946. PMID 16238547.
- ^ Cheskis BJ (2004). "Regulation of cell signalling cascades by steroid hormones". J. Cell. Biochem. 93 (1): 20–7. doi:10.1002/jcb.20180. PMID 15352158. S2CID 43430651.
- ^ Brodsky IG, Balagopal P, Nair KS (1996). "Effects of testosterone replacement on muscle mass and muscle protein synthesis in hypogonadal men—a clinical research center study". J. Clin. Endokrinol. Metab. 81 (10): 3469–75. doi:10.1210/jc.81.10.3469. PMID 8855787.
- ^ Hickson RC, Czerwinski SM, Falduto MT, Young AP (1990). "Glucocorticoid antagonism by exercise and androgenic-anabolic steroids". Med Sci Sports Exerc. 22 (3): 331–40. doi:10.1249/00005768-199006000-00010. PMID 2199753.
- ^ Singh R, Artaza JN, Taylor WE, Gonzalez-Cadavid NF, Bhasin S (2003). "Androgens stimulate myogenic differentiation and inhibit adipogenesis in C3H 10T1/2 pluripotent cells through an androgen receptor-mediated pathway". Endokrinologie. 144 (11): 5081–8. doi:10.1210/en.2003-0741. PMID 12960001.
- ^ Schroeder ET, Vallejo AF, Zheng L, Stewart Y, Flores C, Nakao S, Martinez C, Sattler FR (2005). "Six-week improvements in muscle mass and strength during androgen therapy in older men". J Gerontol A Biol Sci Med Sci. 60 (12): 1586–92. doi:10.1093/gerona/60.12.1586. PMID 16424293.
- ^ Grunfeld C, Kotler DP, Dobs A, Glesby M, Bhasin S (2006). "Oxandrolone in the treatment of HIV-associated weight loss in men: a randomized, double-blind, placebo-controlled study". J Acquir Immune Defic Syndr. 41 (3): 304–14. doi:10.1097/01.qai.0000197546.56131.40. PMID 16540931. S2CID 25911263.
- ^ Giorgi A, Weatherby RP, Murphy PW (1999). "Muscular strength, body composition and health responses to the use of testosterone enanthate: a double blind study". Journal of Science and Medicine in Sport / Sports Medicine Australia. 2 (4): 341–55. doi:10.1016/S1440-2440(99)80007-3. PMID 10710012.
- ^ A b Kuhn CM (2002). "Anabolic steroids". Nedávný program. Horm. Res. 57: 411–34. doi:10.1210/rp.57.1.411. PMID 12017555.
- ^ Roselli CE (1998). "The effect of anabolic-androgenic steroids on aromatase activity and androgen receptor binding in the rat preoptic area". Brain Res. 792 (2): 271–6. doi:10.1016/S0006-8993(98)00148-6. PMID 9593936. S2CID 29441013.
- ^ Hershberger LG, Shipley EG, Meyer RK (1953). "Myotrophic activity of 19-nortestosterone and other steroids determined by modified levator ani muscle method". Proceedings of the Society for Experimental Biology and Medicine (New York, N.Y.). 83 (1): 175–80. doi:10.3181/00379727-83-20301. PMID 13064212. S2CID 2628925.
- ^ Hervey GR, Hutchinson I, Knibbs AV, Burkinshaw L, Jones PR, Norgan NG, Levell MJ (October 1976). ""Anabolic" effects of methandienone in men undergoing athletic training". Lanceta. 2 (7988): 699–702. doi:10.1016/S0140-6736(76)90001-5. PMID 61389. S2CID 22417506.

- ^ Hervey GR, Knibbs AV, Burkinshaw L, Morgan DB, Jones PR, Chettle DR, Vartsky D (April 1981). "Effects of methandienone on the performance and body composition of men undergoing athletic training". Clin. Sci. 60 (4): 457–61. doi:10.1042/cs0600457. PMID 7018798. S2CID 30590287.
- ^ Bhasin S, Woodhouse L, Casaburi R, Singh AB, Bhasin D, Berman N, Chen X, Yarasheski KE, Magliano L, Dzekov C, Dzekov J, Bross R, Phillips J, Sinha-Hikim I, Shen R, Storer TW (December 2001). "Testosterone dose-response relationships in healthy young men". Dopoledne. J. Physiol. Endokrinol. Metab. 281 (6): E1172–81. doi:10.1152/ajpendo.2001.281.6.E1172. PMID 11701431. S2CID 2344757.
- ^ A b Imperato-McGinley J, Peterson RE, Gautier T, Sturla E (May 1979). "Androgens and the evolution of male-gender identity among male pseudohermaphrodites with 5alpha-reductase deficiency". The New England Journal of Medicine. 300 (22): 1233–7. doi:10.1056/NEJM197905313002201. PMID 431680.
- ^ A b C Marks LS (2004). "5α-reductase: history and clinical importance". Rev Urol. 6 Suppl 9: S11–21. PMC 1472916. PMID 16985920.
- ^ Sloane E (2002). Biology of Women. Cengage Learning. str. 160–. ISBN 0-7668-1142-5.
- ^ A b Hanno PM, Guzzi TJ, Malkowicz SB, J Wein A (26 January 2014). Penn Clinical Manual of Urology. Elsevier Health Sciences. pp. 782–. ISBN 978-0-323-24466-4.
- ^ Jain NK, Siddiqi M, Weisburger JH (2006). Protective Effects of Tea on Human Health. CABI. str. 95–. ISBN 978-1-84593-113-1.
- ^ Harper C (1 August 2007). Intersex. Berg. pp. 123–. ISBN 978-1-84788-339-1.
- ^ A b Basaria S, Wahlstrom JT, Dobs AS (2001). "Clinical review 138: Anabolic-androgenic steroid therapy in the treatment of chronic diseases". J. Clin. Endokrinol. Metab. 86 (11): 5108–17. doi:10.1210/jcem.86.11.7983. PMID 11701661.
[...] in a recent animal study, Hsiao et al. (10) found two different kinds of androgen response elements that could respond differentially to T and DHT. Therefore, it is possible that a selective androgen response element sequence may play a role in differential T vs. DHT AR trans-activation.
- ^ A b Basaria S, Dobs AS (2001). "Hypogonadism and androgen replacement therapy in elderly men". Dopoledne. J. Med. 110 (7): 563–72. doi:10.1016/s0002-9343(01)00663-5. PMID 11343670.
Although both testosterone and dihydrotestosterone activate the same androgen receptor, differences in the sequence of androgen response elements are responsible for differential regulation of these hormones (21).
- ^ Wang C, Liu Y, Cao JM (2014). "G protein-coupled receptors: extranuclear mediators for the non-genomic actions of steroids". Int J Mol Sci. 15 (9): 15412–25. doi:10.3390/ijms150915412. PMC 4200746. PMID 25257522.
- ^ A b C d Thomas P, Converse A, Berg HA (2018). "ZIP9, a novel membrane androgen receptor and zinc transporter protein". Gen. Comp. Endokrinol. 257: 130–136. doi:10.1016/j.ygcen.2017.04.016. PMID 28479083.
- ^ A b C d Mongan NP, Tadokoro-Cuccaro R, Bunch T, Hughes IA (2015). "Androgen insensitivity syndrome". Best Pract. Res. Clin. Endokrinol. Metab. 29 (4): 569–80. doi:10.1016/j.beem.2015.04.005. PMID 26303084.
- ^ A b Orwoll ES, Bilezikian JP, Vanderschueren D (30 November 2009). Osteoporosis in Men: The Effects of Gender on Skeletal Health. Akademický tisk. str. 114–. ISBN 978-0-08-092346-8.
- ^ Rahwan, R. G. (1988). The Pharmacology of Androgens and Anabolic Steroids. American Journal of Pharmaceutical Education, 52(2), 167–177.
- ^ Pi M, Quarles LD (2012). "GPRC6A regulates prostate cancer progression". Prostata. 72 (4): 399–409. doi:10.1002/pros.21442. PMC 3183291. PMID 21681779.
- ^ Wu FC, Balasubramanian R, Mulders TM, Coelingh-Bennink HJ (January 1999). "Oral progestogen combined with testosterone as a potential male contraceptive: additive effects between desogestrel and testosterone enanthate in suppression of spermatogenesis, pituitary-testicular axis, and lipid metabolism". J. Clin. Endokrinol. Metab. 84 (1): 112–22. doi:10.1210/jcem.84.1.5412. PMID 9920070.
- ^ A b Bitran D, Kellogg CK, Hilvers RJ (1993). "Treatment with an anabolic-androgenic steroid affects anxiety-related behavior and alters the sensitivity of cortical GABAA receptors in the rat". Horm Behav. 27 (4): 568–83. doi:10.1006/hbeh.1993.1041. PMID 8294123. S2CID 29134676.
- ^ A b Masonis AE, McCarthy MP (1995). "Direct effects of the anabolic/androgenic steroids, stanozolol and 17α-methyltestosterone, on benzodiazepine binding to the γ-aminobutyric acidA receptor". Neurosci. Lett. 189 (1): 35–8. doi:10.1016/0304-3940(95)11445-3. PMID 7603620. S2CID 54394931.
- ^ A b Masonis AE, McCarthy MP (1996). "Effects of the androgenic/anabolic steroid stanozolol on GABAA receptor function: GABA-stimulated 36Cl− influx and [35S] TBPS binding". J. Pharmacol. Exp. Ther. 279 (1): 186–93. PMID 8858992.
- ^ A b Rivera-Arce JC, Morales-Crespo L, Vargas-Pinto N, Velázquez KT, Jorge JC (2006). "Central effects of the anabolic steroid 17alpha methyltestosterone in female anxiety". Pharmacol. Biochem. Chovat se. 84 (2): 275–81. doi:10.1016/j.pbb.2006.05.009. PMID 16814373. S2CID 31725431.
- ^ A b Henderson LP (2007). "Steroid modulation of GABAA receptor-mediated transmission in the hypothalamus: effects on reproductive function". Neurofarmakologie. 52 (7): 1439–53. doi:10.1016/j.neuropharm.2007.01.022. PMC 1985867. PMID 17433821.
- ^ A b Schwartzer JJ, Ricci LA, Melloni RH (2009). "Interactions between the dopaminergic and GABAergic neural systems in the lateral anterior hypothalamus of aggressive AAS-treated hamsters". Chovat se. Brain Res. 203 (1): 15–22. doi:10.1016/j.bbr.2009.04.007. PMID 19376158. S2CID 26938839.
- ^ Schänzer W (1996). "Metabolism of anabolic androgenic steroids" (PDF). Clin. Chem. 42 (7): 1001–20. doi:10.1093/clinchem/42.7.1001. PMID 8674183.
- ^ Attardi BJ, Hild SA, Koduri S, Pham T, Pessaint L, Engbring J, Till B, Gropp D, Semon A, Reel JR (October 2010). "The potent synthetic androgens, dimethandrolone (7α,11β-dimethyl-19-nortestosterone) and 11β-methyl-19-nortestosterone, do not require 5α-reduction to exert their maximal androgenic effects". The Journal of Steroid Biochemistry and Molecular Biology. 122 (4): 212–8. doi:10.1016/j.jsbmb.2010.06.009. PMC 2949447. PMID 20599615.
- ^ Orwoll ES, Bilezikian JP, Vanderschueren D (30 November 2009). Osteoporosis in Men: The Effects of Gender on Skeletal Health. Akademický tisk. pp. 296–. ISBN 978-0-08-092346-8.
- ^ Fillit HM, Rockwood K, Woodhouse K (10 May 2010). Brocklehurst's Textbook of Geriatric Medicine and Gerontology. Elsevier Health Sciences. 166–167. ISBN 978-1-4377-2075-4.
- ^ A b C Thieme D, Hemmersbach P (18 December 2009). Doping in Sports. Springer Science & Business Media. pp. 470–. ISBN 978-3-540-79088-4.
- ^ A b Attardi BJ, Pham TC, Radler LC, Burgenson J, Hild SA, Reel JR (June 2008). "Dimethandrolone (7,11β-dimethyl-19-nortestosterone) and 11β-methyl-19-nortestosterone are not converted to aromatic A-ring products in the presence of recombinant human aromatase". The Journal of Steroid Biochemistry and Molecular Biology. 110 (3–5): 214–22. doi:10.1016/j.jsbmb.2007.11.009. PMC 2575079. PMID 18555683.
- ^ Llewellyn, William (2011). Anabolika. Molecular Nutrition LLC. pp. 533–, 402–412, 460–467. ISBN 978-0-9828280-1-4.
- ^ Suvisaari J (2000). 7α-Methyl-19-nortestosterone (MENT) Pharmacokinetics and Antigonadotropic Effects in Men (PDF). Helsinki: University of Helsinki. p. 14. ISBN 952-91-2950-5.
Androgens, estrogens and progestins exert a negative feedback effect on the secretion of GnRH and LH by their actions on the pituitary and the hypothalamus. Most of the negative feedback effect of androgens is caused by their estrogenic metabolites produced by aromatization. 5α-Reduction does not seem to be necessary for the negative feedback effect of testosterone. (Rittmaster et al, 1992; Kumar et al, 1995a; Hayes et al, 2000).
- ^ A b C d E Attardi BJ, Hild SA, Reel JR (June 2006). "Dimethandrolone undecanoate: a new potent orally active androgen with progestational activity". Endokrinologie. 147 (6): 3016–26. doi:10.1210/en.2005-1524. PMID 16497801.
- ^ Warren MP, Constantini NW (1 May 2000). Sports Endocrinology. Springer Science & Business Media. pp. 458–. ISBN 978-1-59259-016-2.
- ^ Haff GG, Triplett NT (23 September 2015). Essentials of Strength Training and Conditioning 4th Edition. Lidská kinetika. pp. 233–. ISBN 978-1-4925-0162-6.
- ^ Lemke TL, Williams DA (24. ledna 2012). Foyeho principy léčivé chemie. Lippincott Williams & Wilkins. pp. 1360–. ISBN 978-1-60913-345-0.
- ^ A b Karch SB, Drummer O (26 December 2001). Karch's Pathology of Drug Abuse, Third Edition. CRC Press. pp. 489–. ISBN 978-1-4200-4211-5.
- ^ A b van Amsterdam J, Opperhuizen A, Hartgens F (2010). "Adverse health effects of anabolic-androgenic steroids". Regul. Toxicol. Pharmacol. 57 (1): 117–23. doi:10.1016/j.yrtph.2010.02.001. PMID 20153798.
- ^ Wilson JD (1988). "Androgen abuse by athletes". Endocr. Rev. 9 (2): 181–99. doi:10.1210/edrv-9-2-181. PMID 3042375.
- ^ Jameson JL, De Groot LJ (25 February 2015). Endocrinology: Adult and Pediatric. Elsevier Health Sciences. pp. 2391–. ISBN 978-0-323-32195-2.
- ^ Nieschlag E, Behre HM, Nieschlag S (26. července 2012). Testosteron: Akce, nedostatek, substituce. Cambridge University Press. 374–. ISBN 978-1-107-01290-5.
- ^ Cameron R, Feuer G, de la Iglesia F (6. prosince 2012). Hepatotoxicita vyvolaná léky. Springer Science & Business Media. str. 166–. ISBN 978-3-642-61013-4.
- ^ Shahidi NT (2001). „Přehled chemie, biologického působení a klinických aplikací anabolicko-androgenních steroidů“. Clin Ther. 23 (9): 1355–90. doi:10.1016 / s0149-2918 (01) 80114-4. PMID 11589254.
- ^ A b Büttner A, Thieme D (2009). „Vedlejší účinky anabolických androgenních steroidů: patologické nálezy a vztahy mezi strukturou a aktivitou“. Příručka experimentální farmakologie. 195 (195): 459–84. doi:10.1007/978-3-540-79088-4_19. ISBN 978-3-540-79087-7. PMID 20020376. S2CID 30314430.
- ^ Mareck U, Geyer H, Opfermann G, Thevis M, Schänzer W (červenec 2008). "Faktory ovlivňující profil steroidů v analýze dopingové kontroly". J Hmotnostní spektrum. 43 (7): 877–91. Bibcode:2008JMSp ... 43..877M. doi:10,1002 / jms.1457. PMID 18570179.
- ^ Fragkaki AG, Angelis YS, Tsantili-Kakoulidou A, Koupparis M, Georgakopoulos C (květen 2009). "Schémata metabolických vzorců anabolických androgenních steroidů pro odhad metabolitů návrhových steroidů v lidské moči". J. Steroid Biochem. Mol. Biol. 115 (1–2): 44–61. doi:10.1016 / j.jsbmb.2009.02.016. PMID 19429460. S2CID 10051396.
- ^ Blackledge RD (srpen 2009). „Bad science: the instrumental data in the Floyd Landis case“. Clin. Chim. Acta. 406 (1–2): 8–13. doi:10.1016 / j.cca.2009.05.016. PMID 19465014.
- ^ Baselt, Randall Clint (2008). Dispozice toxických drog a chemických látek u člověka (8. vydání). Foster City, CA: Biomedical Publications. 95, 393, 403, 649, 695, 952, 962, 1078, 1156, 1170, 1442, 1501, 1581. ISBN 978-0-9626523-7-0.
- ^ A b C d E Hoberman JM, Yesalis CE (1995). "Historie syntetického testosteronu". Scientific American. 272 (2): 76–81. Bibcode:1995SciAm.272b..76H. doi:10.1038 / scientificamerican0295-76. PMID 7817189.
- ^ A b Freeman ER, Bloom DA, McGuire EJ (2001). "Stručná historie testosteronu". Journal of Urology. 165 (2): 371–373. doi:10.1097/00005392-200102000-00004. PMID 11176375.
- ^ David K, Dingemanse E, Freud J, Laqueur L (1935). „Uber krystallinisches mannliches Hormon aus Hoden (Testosteron) wirksamer als aus harn oder aus Cholesterin bereitetes Androsteron“. Hoppe-Seyler's Z Physiol Chem. 233 (5–6): 281–283. doi:10,1515 / bchm2.1935.233.5-6,281.
- ^ Butenandt A, Hanisch G (1935). „Über die Umwandlung des Dehydro-androsterons in Δ4-Androsten-ol- (17) -0n- (3) (Testosteron); ein Weg zur Darstellung des Testosterons aus Cholesterin (Vorläuf. Mitteil.)“ [O přeměně dehydro- Δ4-androsten androsterons in-ol (17) 0n (3) (testosteron), způsob reprezentace testosteronu z cholesterolu (Vorläuf. Msgs.)]. Berichte der Deutschen Chemischen Gesellschaft (řada A a B) (v němčině). 68 (9): 1859–62. doi:10,1002 / cber.1950680937.
- ^ Ruzicka L, Wettstein A (1935). „Sexualhormone VII. Uber die kunstliche Herstellung des Testikelhormons. Testosteron (Androsten-3-one-17-ol.)“ [Sexuální hormony VII. O umělé produkci testosteronu Testikelhormons (androsten-3-one-17-ol)]. Helvetica Chimica Acta (v němčině). 18: 1264–75. doi:10,1002 / hlca.193501801176.
- ^ A b Taylor WN (1. ledna 2009). Anabolické steroidy a sportovec. McFarland & Company. p. 181. ISBN 978-0-7864-1128-3.
- ^ Suarez R, hlavní korespondent, Kelman J, lékař (18. 11. 2002). „Tajemství zdraví prezidenta Kennedyho“. PBS NewsHour. Systém veřejného vysílání.
- ^ Calfee R, Fadale P (2006). „Populární ergogenní léky a doplňky u mladých sportovců“. Pediatrie. 117 (3): e577–89. doi:10.1542 / peds.2005-1429. PMID 16510635. S2CID 6559714.
- ^ Justin Peters Muž za džusem, Břidlice Pátek, 18. února 2005. Citováno 29. dubna 2008
- ^ A b Kochakian, Charles D. (1946). Anabolické účinky bílkovin na steroidní hormony. Vitamíny a hormony: pokrok ve výzkumu a aplikacích. Vitamíny a hormony. 4. 255–310. doi:10.1016 / S0083-6729 (08) 61085-7. ISBN 9780127098043. ISSN 0083-6729.
V posledních letech pobavilo několik laboratoří (Kochakian, Albright, Wilkins) naději na nalezení proteinového anabolického steroidu bez jakýchkoli sexuálních účinků nebo jen s malými účinky. Tyto studie získaly zvláštní podnět a povzbuzení z pozorování Kochakiana, že některé steroidy mají větší renotrofické (anabolické?) Než androgenní účinky.
- ^ A b C d E F Charles D. Kochakian (6. prosince 2012). Anabolicko-androgenní steroidy. Springer Science & Business Media. 370–373, 380. ISBN 978-3-642-66353-6.
- ^ Walter Sneader (23. června 2005). Objev drog: Historie. John Wiley & Sons. str. 206–. ISBN 978-0-471-89979-2.
- ^ A b Camille Georges Wermuth (2. května 2011). Praxe léčivé chemie. Akademický tisk. str. 34–. ISBN 978-0-08-056877-5.
- ^ A b James Edward Wright (1994). Změněné státy: Užívání a zneužívání anabolických steroidů. Masters Press. p. 33. ISBN 978-1-57028-013-9.
- ^ Spojené státy. Patentový úřad (1957). Úřední věstník Patentového úřadu Spojených států. Americký patentový úřad.
- ^ Mozayani A, Raymon L (18. září 2011). Příručka lékových interakcí: Klinický a forenzní průvodce. Springer Science & Business Media. str. 651–. ISBN 978-1-61779-222-9.
- ^ „Hlava 21 Zákon o regulovaných látkách v USA (USC)“. Americké ministerstvo spravedlnosti. Archivováno z původního dne 24. července 2009. Citováno 2009-09-07.
- ^ Zákon o kontrolovaných drogách a látkách, S.C. 1996, c. 19, s. 4 (7) (Zákon o kontrolovaných drogách a látkách at Department of Justice)
- ^ Deacon J (2. května 1994). „Biceps v láhvi“. Maclean: 52.
- ^ "Steroidy". Australský kriminologický institut. 2006. Archivovány od originál dne 05.04.2007. Citováno 2007-05-06.
- ^ HR 4658
- ^ „Zprávy z DEA, Kongresové svědectví, 16. 3. 2004“. Archivovány od originál 6. února 2007. Citováno 2007-04-24.
- ^ „Léky kontrolované pacientem.info“. Egton Medical Information Systems Limited. Citováno 8. srpna 2013.
- ^ „Anit-dopingové předpisy FIFA“ (PDF). FIFA. Citováno 2013-12-01.
- ^ „Antidopingový kodex olympijského hnutí“ (PDF). Mezinárodní olympijský výbor. 1999. Citováno 2007-05-06.
- ^ „Protidrogový program nba a nbpa“. Zásady NBA. findlaw.com. 1999. Citováno 2007-05-06.
- ^ „Přehled programů pro látky zvyšující výkon NHL / NHLPA“. nhlpa.com. Archivovány od originál dne 2. června 2007. Citováno 2007-05-06.
- ^ „Seznam zakázaných látek“ (PDF). nflpa.com. 2006. Archivovány od originál (PDF) dne 2007-06-20. Citováno 2007-05-06.
- ^ „Světový antidopingový kodex“ (PDF). WADA. 2003. Archivovány od originál (PDF) dne 7. srpna 2007. Citováno 2007-07-10.
- ^ „Zakázaný seznam roku 2005“ (PDF). WADA. 2005. Archivovány od originál (PDF) dne 2007-06-20. Citováno 2007-05-06.
- ^ „Španělský senát přijal antidopingový zákon“. Herald Tribune. Associated Press. 5. října 2006. Archivovány od originál 12. října 2006. Citováno 2007-05-06.
- ^ Johnson K (2006-02-20). „Italské antidopingové zákony mohou znamenat 3 roky vězení“. USA dnes. Citováno 2007-05-06.
- ^ „Zákon o podpoře sportu bez dopingu“ (PDF). kum.dk. 2004. Citováno 2016-09-04.
- ^ „Ochrana zdraví sportovců a boj proti dopingu“ (PDF). WADA. 2006. Archivovány od originál (PDF) dne 2007-06-20. Citováno 2007-05-06.
- ^ „Antidopingová legislativa v Nizozemsku“ (PDF). WADA. 2006. Archivovány od originál (PDF) dne 2007-06-20. Citováno 2007-05-06.
- ^ „Švédský zákon zakazující určité dopingové látky (1991: 1969)“ (PDF). WADA. 1991. Archivovány od originál (PDF) dne 2007-06-20. Citováno 2007-05-06.
- ^ Keeping J (27. prosince 2010). „Zneužívání steroidů mezi orgány činnými v trestním řízení problém na celostátní úrovni“. Ann Arbor News. Citováno 1. prosince 2013.
- ^ „Užívání a zneužívání anabolických steroidů ze strany policistů: politika a prevence“. Policejní šéf. Červen 2008. Citováno 1. prosince 2013.
- ^ Lockhart B (01.03.2010). „Vyšetřování steroidů WWE: Kontroverze, kterou McMahon 'nepotřebuje'". Střední greenwichský čas. Citováno 2010-03-01.
- ^ dokumenty Archivováno 24. prosince 2010, na Wayback Machine
- ^ "Podrobnosti o ukládání McMahon steroidní svědectví | Zprávy z jihovýchodního Connecticutu". Den. 2007-12-13. Citováno 2010-08-14.
- ^ Assael S (2007-09-24). "'Laboratoře společnosti Raw Deal v USA, z nichž mnohé dodávala Čína “. Časopis ESPN. Archivováno z původního dne 14. října 2007. Citováno 2007-09-24.
- ^ Yesalis C (2000). „Zdroj anabolických steroidů“. Anabolické steroidy ve sportu a cvičení. Champaign, Ill.: Kinetika člověka. ISBN 978-0-88011-786-9.
- ^ Black T (1996). „Zlepšuje zákaz drog ve sportu sociální blahobyt?“. International Review for the Sociology of Sport. Fakulta podnikání, Queensland University of Technology. 31 (4): 367–381. doi:10.1177/101269029603100402. S2CID 143442371.
- ^ Libra RW (2006). "Organizovaný zločin". Uvnitř drogy: jak jsou drogy největší hrozbou pro sport, proč by vám na nich mělo záležet a co se s nimi dá dělat. Mississaug, Ontario: Wiley. p.175. ISBN 978-0-470-83733-7.
- ^ Kanayama G, Hudson JI, papež HG (listopad 2008). „Dlouhodobé psychiatrické a lékařské důsledky zneužívání anabolicko-androgenních steroidů: hrozící obavy o veřejné zdraví?“. Závisí na alkoholu. 98 (1–2): 1–12. doi:10.1016 / j.drugalcdep.2008.05.004. PMC 2646607. PMID 18599224.
- ^ "Steroidy". Národní institut pro zneužívání drog. GDCADA. Archivováno z původního dne 2007-09-11. Citováno 2007-09-13.
- ^ „Mezinárodní operace Drug Enforcement Administration (Redigováno)“. Úřad generálního inspektora. USDOJ. Února 2007. Citováno 2014-01-02.
- ^ Nieschlag E, Kumar N, Sitruk-Ware R (2013). „7α-methyl-19-nortestosteron (MENTR): příspěvek rady obyvatelstva k výzkumu mužské antikoncepce a léčby hypogonadismu“. Antikoncepce. 87 (3): 288–95. doi:10.1016 / j. Antikoncepce.2012.08.036. PMID 23063338.
- ^ „Dimethandrolon undecanoate ukazuje slib jako mužskou antikoncepční pilulku | Endokrinní společnost“.
- ^ A b Gruber CJ, Wieser F, Gruber IM, Ferlitsch K, Gruber DM, Huber JC (prosinec 2002). "Současné koncepty v estetické endokrinologii". Gynecol. Endokrinol. 16 (6): 431–41. doi:10,1080 / gye.16.6.431.441. PMID 12626029. S2CID 37424524.
- ^ Sam S (únor 2015). "Adipozita a metabolická dysfunkce u syndromu polycystických vaječníků". Horm Mol Biol Clin Investig. 21 (2): 107–16. doi:10.1515 / hmbci-2015-0008. PMID 25781555. S2CID 23592351.
Další čtení
- Schänzer W (1996). "Metabolismus anabolických androgenních steroidů". Clin. Chem. 42 (7): 1001–20. doi:10.1093 / clinchem / 42.7.1001. PMID 8674183.
- Yesalis CE (2000). Anabolické steroidy ve sportu a cvičení. Lidská kinetika. ISBN 0-88011-786-9.
- Daniels RC (1. února 2003). Příručka anabolických steroidů. Knihy RCD. p. 80. ISBN 0-9548227-0-6.
- Gallaway S (15. ledna 1997). Steroidní Bible (3. Sprl ed.). Mezinárodní letiště Belle p. 125. ISBN 1-890342-00-9.
- Llewellyn W (28. ledna 2007). Anabolics 2007: Anabolic Steroid Reference Manual (6. vydání). Tělo vědy. p. 988. ISBN 978-0-9679304-6-6.
- Roberts A, Clapp B (leden 2006). Anabolické steroidy: Ultimate Research Guide. Anabolic Books, LLC. p. 394. ISBN 1-59975-100-3.
- Tygart TT (prosinec 2009). „Steroidy, média a mládež“. Prevence Researcher Integrated Research Services, Inc.. Výzkumník SIRS. 16 (7–9). Archivovány od originál dne 2014-11-29. Citováno 2013-11-24.
- Eisenhauer L (7. listopadu 2005). „Vypadám dobře?“. St. Louis Post-Dispatch (St. Louis, MO). Archivovány od originál 2. prosince 2013. Citováno 25. října 2010.
- Fragkaki AG, Angelis YS, Koupparis M, Tsantili-Kakoulidou A, Kokotos G, Georgakopoulos C (2009). "Strukturální charakteristiky anabolických androgenních steroidů přispívající k vazbě na androgenní receptor a k jejich anabolickým a androgenním aktivitám. Aplikované úpravy ve steroidní struktuře". Steroidy. 74 (2): 172–97. doi:10.1016 / j.steroids.2008.10.016. PMID 19028512. S2CID 41356223.
- McRobb L, Handelsman DJ, Kazlauskas R, Wilkinson S, McLeod MD, Heather AK (2008). "Vztahy mezi strukturou a aktivitou syntetických progestinů v kvasinkovém in vitro androgenním biologickém testu". J. Steroid Biochem. Mol. Biol. 110 (1–2): 39–47. doi:10.1016 / j.jsbmb.2007.10.008. PMID 18395441. S2CID 5612000.
externí odkazy
 Média související s Anabolicko-androgenní steroidy na Wikimedia Commons
Média související s Anabolicko-androgenní steroidy na Wikimedia Commons
