Kyselina ibotenová - Ibotenic acid
 | |
 | |
| Jména | |
|---|---|
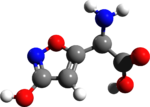
| Název IUPAC (S) -2-Amino-2- (3-hydroxyizoxazol-5-yl) octová kyselina | |
| Ostatní jména Kyselina ibotenová | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.151.170 |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C5H6N2Ó4 | |
| Molární hmotnost | 158.113 g · mol−1 |
| Bod tání | 151-152 ° C (bezvodý) 144-146 ° C (monohydrát) |
| H2O: 1 mg / ml 0,1 M NaOH: 10,7 mg / ml 0,1 M HCl: 4,7 mg / ml | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Kyselina ibotenová nebo (S) -2-amino-2- (3-hydroxyizoxazol-5-yl) octová kyselina, označovaný také jako ibotenát, je chemická sloučenina a psychoaktivní droga který se přirozeně vyskytuje v Amanita muscaria a příbuzné druhy houby obvykle se vyskytují v mírných a boreálních oblastech severní polokoule. Je to konformačně omezené analog z neurotransmiter glutamát, a díky své strukturální podobnosti s tímto neurotransmiterem působí jako neselektivní glutamátový receptor agonista.[1] Z tohoto důvodu může být kyselina ibotenová silná neurotoxin, a je zaměstnán jako „mozekpoškození agent "prostřednictvím lebečních injekcí v vědecký výzkum.[2][3]
Farmakologie

Kyselina ibotenová působí jako silná látka agonista z NMDA a skupina I (mGluR1 a mGluR5 ) a II (mGluR2 a mGluR3 ) metabotropní glutamátové receptory.[1][4] Je neaktivní v skupina III mGluRs.[5] Kyselina ibotenová také působí jako slabý agonista AMPA a kainátové receptory.[1][4] Navíc kvůli in vivo dekarboxylace do muscimol, působí nepřímo jako silný GABAA a GABAA-ρ receptor agonista.[4] Na rozdíl od muscimolu, hlavní psychoaktivní složky Amanita muscaria to je pochopitelné sedace a delirium „Psychoaktivní účinky kyseliny ibotenové nejsou známy, nezávisle na tom, že slouží jako a proléčivo na muscimol, lze však spekulovat, že by působil jako stimulant.[6][7]
Biologické vlastnosti
Mechanismus účinku
Kyselina ibotenová je agonista glutamátových receptorů, konkrétně jak na N-methyl-D-aspartátu, tak na NMDA a místa receptoru trans-ACPD v mnoha systémech v centrální nervový systém. Ibotenická neurotoxicita může být zvýšena glycinem a blokována dizocilpin. Dizocilpin působí jako nekonkurenční antagonista na NMDA receptory.[8]
Toxicita kyseliny ibotenové pochází z aktivace NMDA receptory. NMDA receptory jsou příbuzné synaptická plasticita a pracovat s metabotropní glutamátové receptory založit dlouhodobé potenciace nebo LTP. Předpokládá se, že proces dlouhodobého potenciace souvisí se získáváním informací. Receptor NMDA funguje správně, protože umožňuje Ca2+ ionty, které procházejí po aktivaci v místě receptoru.

Vazba kyseliny ibotenové umožňuje přebytek Ca2+ do systému, což má za následek smrt neuronových buněk. Ca.2+ také aktivuje CaM-KII nebo Ca2+/ Kalmodulin kináza, která fosforyluje více enzymů. Aktivované enzymy pak začnou produkovat reaktivní formy kyslíku který poškozuje okolní tkáň. Přebytek Ca2+ vede k posílení mitochondriálního elektronového transportního systému, který dále zvýší počet reaktivních forem kyslíku.[9]
Biologické účinky
Kyselina ibotenová typicky ovlivňuje receptory NMDA a trans-ACPD v centrálním nervovém systému.[8] Vzhledem k jejich cílení na tyto systémy jsou příznaky spojené s otravou kyselinou ibotenovou často spojeny s vnímáním a kontrolou.
Většina požité kyseliny ibotenové je pravděpodobně dekarboxylovaný do muscimol účinky požití kyseliny ibotenové jsou tedy podobné účinkům muscimolu.[10] Příznaky spojené s kyselinou ibotenovou se obvykle projeví během 30–60 minut a zahrnují řadu účinků na nervový systém. Mezi nejčastější příznaky patří nevolnost, zvracení a ospalost. Po první hodině však příznaky začnou zahrnovat zmatek, euforie, vizuální a sluchové zkreslení, pocity vznášení se a retrográdní amnézie.[11]
Příznaky se u dětí mírně liší, obvykle začínají po 30–180 minutách. Mezi dominantní příznaky u dětí patří ataxie, obtundace, a letargie. Záchvaty jsou občas hlášeny, častěji však u dětí.[11]
Léčba

Léčba otravy kyselinou ibotenovou je omezená a liší se v závislosti na toxické dávce sloučeniny od člověka k člověku. Pacientům přijatým do nemocnice pro otravu kyselinou ibotenovou se obvykle podává dřevěné uhlí, aby se zastavila absorpce sloučeniny a zabránilo se další intoxikaci. Po ošetření aktivním uhlím jsou sledovány vitální funkce pacienta a toxicita obvykle trvá 6 až 8 hodin; některé příznaky však mohou trvat až několik dní, než ustoupí. Občas, aby se snížilo nepohodlí spojené s příznaky, benzodiazepiny budou podávány za účelem kontroly záchvaty paniky a halucinace.
Zvláštní pozornost je třeba věnovat monitorování dýchání, kontrole dýchacích cest a oběhu. Pokud k léčbě dojde během první hodiny po požití výplach žaludku může být efektivní. Pokud zvracení začne být příliš intenzivní intravenózní tekutiny jsou podávány, může být poskytována také psychiatrická péče.
Ve vzácných případech anticholinergikum léky, jako např atropin, může být potřeba.[12]
Použití ve výzkumu
Kyselina ibotenová použitá k lézi mozků potkana se udržuje zmrazená ve fyziologickém roztoku pufrovaném fosfáty při pH 7,4 a může být udržována po dobu až jednoho roku bez ztráty toxicity. Injekce 0,05 - 0,1 mikrolitru kyseliny ibotenové do hipokampus rychlostí 0,1 mikrolitru / min vedlo k semeselektivnímu poškození. Hipokampální léze vedla ke značné ztrátě buněk v pyramidové buňky (CA1-CA3) a také granulované buňky v zubatý gyrus. Poškození kyselinou ibotenovou také způsobuje určité poškození axonů podél perforující cesta.
Když se léze provádí jinými chemickými látkami, subjekt se obvykle nemůže znovu naučit úkol. Avšak vzhledem k reaktivitě kyseliny ibotenové s glutamátovými receptory, jako je NMDA receptor, léze kyseliny ibotenové umožňuje subjektu znovu se naučit úkoly. Lézba kyselinou ibotenovou je tedy preferována ve studiích, kde je zásadní opětovné naučení se úkolu po lézi. Ve srovnání s jinými lézivými látkami je kyselina ibotenová jedním z nejvíce místně specifických; v současnosti se však hledají méně škodlivé alternativy.[13]
Biosyntéza
Kyselina ibotenová biosyntetický geny jsou organizovány ve fyzicky propojených biosyntetický genový klastr. Biosyntetická cesta je iniciována hydroxylací kyselina glutamová zasvěceným Fe (II) / 2-oxoglutarát-dependentní oxygenáza. Výtěžek reakce threoKyselina -3-hydroxyglutamová, která se přeměňuje na kyselinu ibotenovou, pravděpodobně enzymy kódovanými v biosyntetickém genovém klastru.[14]
Viz také
Reference
- ^ A b C Tommy Liljefors; Povl Krogsgaard-Larsen; Ulf Madsen (25. července 2002). Učebnice designu a objevu drog, třetí vydání. CRC Press. 263–. ISBN 978-0-415-28288-8.
- ^ Becker, A; Grecksch, G; Bernstein, HG; Höllt, V; Bogerts, B (1999). „Sociální chování u potkanů poškozených kyselinou ibotenovou v hipokampu: kvantitativní a kvalitativní analýza“. Psychofarmakologie. 144 (4): 333–8. doi:10.1007 / s002130051015. PMID 10435405. S2CID 25172395.
- ^ Isacson, O; Brundin, P; Kelly, PA; Gage, FH; Björklund, A (1984). „Funkční náhrada neuronů roubovanými striatálními neurony v striatu potkana s kyselinou ibotenovou“. Příroda. 311 (5985): 458–60. Bibcode:1984Natur.311..458I. doi:10.1038 / 311458a0. PMID 6482962. S2CID 4342937.
- ^ A b C Wantanabe (23. července 1999). Farmakologický výzkum tradičních bylinných léčiv. CRC Press. 107–. ISBN 978-90-5702-054-4.
- ^ Hermit MB, Greenwood JR, Nielsen B, Bunch L, Jørgensen CG, Vestergaard HT, Stensbøl TB, Sanchez C, Krogsgaard-Larsen P, Madsen U, Bräuner-Osborne H (2004). „Kyselina ibotenová a kyselina thioibotenová: pozoruhodný rozdíl v aktivitě na metabotropních glutamátových receptorech skupiny III“. Eur. J. Pharmacol. 486 (3): 241–50. doi:10.1016 / j.ejphar.2003.12.033. PMID 14985045.
- ^ Chilton 1975; Theobald a kol. 1968
- ^ Chilton 1975; Ott 1976a
- ^ A b Zinkand, William; Moore, W .; Thompson, Carolann; Salama, Andre; Patel, Jitendra (únor 1992). „Kyselina ibotenová zprostředkovává neurotoxicitu a hydrolýzu fosfoinositidů nezávislými mechanismy receptorů“. Molekulární a chemická neuropatologie. 16 (1–2): 1–10. doi:10.1007 / bf03159956. PMID 1325800.
- ^ Sureda, F. "Excitotoxicita a NMDA receptor". eurosiva. Citováno 30. dubna 2015.
- ^ Michelot, Didier; Melendez-Howell, Leda Maria (2003). „Amanita muscaria: chemistry, biology, toxicology, and ethnomycology“ (PDF). Mykologický výzkum. 107 (2): 131–146. doi:10.1017 / s0953756203007305. PMID 12747324.
- ^ A b Duffy, Thomas. "Příznaky otravy ibotenem / muscimolem (otrava isoxazolem)". Toxické houby západní Severní Ameriky. MykoWeb. Citováno 30. dubna 2015.
- ^ Rolston-Cregler, Louis. „Halucinogenní toxicita pro houby“. MedScape. Citováno 30. dubna 2015.
- ^ Jarrard, Leonard (2. února 1989). "O použití kyseliny ibotenové k lézi selektivně různých složek formace hipokampu". Journal of Neuroscience Methods. 29 (3): 251–259. doi:10.1016/0165-0270(89)90149-0. PMID 2477650. S2CID 3767525.
- ^ Obermaier, Sebastian; Müller, Michael (2020-03-31). „Biosyntéza kyseliny ibotenové v agarice mouchy je zahájena hydroxylamací glutamátu“. Angewandte Chemie International Edition. 59 (30): 12432–12435. doi:10.1002 / anie.202001870. PMC 7383597. PMID 32233056.


