Valinomycin - Valinomycin
 | |
 | |
| Jména | |
|---|---|
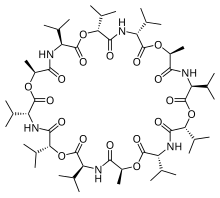
| Název IUPAC cyklo [N-oxa-D-alanyl-D-valyl-N-oxa-L-valyl-D-valyl-N-oxa-D-alanyl-D-valyl-N-oxa-L-valyl-L-valyl- N-oxa-L-alanyl-L-valyl-N-oxa-L-valyl-L-valyl | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.016.270 |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C54H90N6Ó18 | |
| Molární hmotnost | 1111,32 g / mol |
| Vzhled | Bílá pevná látka |
| Bod tání | 190 ° C (374 ° F; 463 K) |
| Rozpustnost | Metanol, ethanol, ethylacetát, benzín-ether, dichlormethan |
| UV-vis (λmax) | 220 nm |
| Nebezpečí | |
| Hlavní nebezpečí | Neurotoxický |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
LD50 (střední dávka ) | 4 mg / kg (orálně, potkan)[2] |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Valinomycin je přirozeně se vyskytující dodekadepsipeptid používané při přepravě draslík a jako antibiotikum. Valinomycin se získává z buněk několika Streptomyces druh, S. fulvissimus být pozoruhodný.
Je členem skupiny přirozeně neutrálních ionofory protože nemá zbytkový náboj. Skládá se z enantiomery D- a L-valin (Val), D-kyselina alfa-hydroxyisovalerová a L-kyselina mléčná. Struktury jsou střídavě vázány prostřednictvím amide a ester mosty. Valinomycin je vysoce selektivní pro draslík ionty nad sodík ionty uvnitř buněčná membrána.[3] Funguje jako transportér specifický pro draslík a usnadňuje pohyb iontů draslíku lipidovými membránami „dolů“ po gradientu elektrochemického potenciálu.[4] The konstanta stability K pro komplex draslík-valinomycin je téměř 100 000krát větší než pro komplex sodík-valinomycin.[5]Tento rozdíl je důležitý pro udržení selektivity valinomycinu pro transport iontů draslíku (a ne iontů sodíku) v biologických systémech.
Je klasifikován jako extrémně nebezpečná látka ve Spojených státech, jak je definováno v oddíle 302 USA Nouzové plánování a zákon o právu na znalost komunity (42 U.S.C. 11002) a podléhá přísným požadavkům na hlášení ze strany zařízení, která je vyrábějí, skladují nebo používají ve významných množstvích.[6]
Struktura
Valinomycin je dodekadepsipeptid, to znamená, že je vyroben z dvanácti střídajících se aminokyseliny a estery za vzniku makrocyklické molekuly. Dvanáct karbonyl skupiny jsou nezbytné pro vazbu kovových iontů a také pro solvatace v polární rozpouštědlo. The isopropyl a methyl skupiny jsou odpovědné za solvataci v nepolární rozpouštědla.[7] Spolu se svým tvarem a velikostí je tato molekulární dualita hlavním důvodem jeho vazebných vlastností. K ionty se musí vzdát své hydratační vody, aby mohly projít póry. K.+ ionty jsou oktaedricky koordinovány ve čtvercové bipyramidové geometrii 6 karbonylovými vazbami z Val. V tomto prostoru 1,33 Angstrom, Na+ se svým poloměrem 0,95 Angstromu je podstatně menší než kanál, což znamená, že Na+ nemůže vytvářet iontové vazby s aminokyselinami pórů při ekvivalentní energii, jaké se vzdává s molekulami vody. To vede k 10 000x selektivitě pro K.+ ionty nad Na+. U polárních rozpouštědel bude valinomycin vystavovat hlavně karbonyly rozpouštědlu a v nepolárních rozpouštědlech jsou isopropylové skupiny umístěny převážně na vnější straně molekuly. Tato konformace se mění, když je valinomycin vázán na iont draslíku. Molekula je „uzamčena“ do konformace s isopropylovými skupinami na vnější straně. Ve skutečnosti není uzamčen v konfiguraci, protože velikost molekuly ji činí vysoce flexibilní, ale draselný iont dává makromolekule určitý stupeň koordinace.
Aplikace
Nedávno se uvádí, že valinomycin je nejúčinnějším prostředkem proti těžkému akutnímu respiračnímu syndromu koronaviru (SARS-CoV) u infikovaných Buňky Vero E6.[Citace je zapotřebí ]
Valinomycin působí jako nekovové izoformační činidlo draslíkové selektivní elektrody.[8][9]
Tento ionofor se používá ke studiu membránové vezikuly, kde to může být selektivně aplikováno experimentálním designem ke snížení nebo eliminaci elektrochemického gradientu přes membránu.[Citace je zapotřebí ]
Reference
- ^ „ChemIDplus - 2001-95-8 - FCFNRCROJUBPLU-DNDCDFAISA-N - Valinomycin - Hledání podobných struktur, synonyma, vzorce, odkazy na zdroje a další chemické informace“.
- ^ „ChemIDplus - 2001-95-8 - FCFNRCROJUBPLU-DNDCDFAISA-N - Valinomycin - Hledání podobných struktur, synonyma, vzorce, odkazy na zdroje a další chemické informace“.
- ^ Lars, Rose; Jenkins ATA (2007). „Účinek ionoforu valinomycinu na biomimetické lipidy DPPTE / EPC na pevném nosiči“. Bioelektrochem. 70 (2): 387–393. doi:10.1016 / j.bioelechem.2006.05.009. PMID 16875886.
- ^ Cammann K (1985). "Iontově selektivní objemové membrány jako modely". Horní. Curr. Chem. Témata ze současné chemie. 128: 219–258. doi:10.1007/3-540-15136-2_8. ISBN 978-3-540-15136-4.
- ^ Rose, M.C .; Henkens, R.W. (1974). "Stabilita sodných a draselných komplexů valinomycinu". Biochimica et Biophysica Acta (BBA) - Obecné předměty. 372 (2): 426–435. doi:10.1016/0304-4165(74)90204-9.
- ^ „40 C.F.R .: Dodatek A k části 355 - Seznam extrémně nebezpečných látek a jejich mezní hodnoty pro plánování“ (PDF) (1. července 2008 ed.). Vládní tiskárna. Citováno 29. října 2011. Citovat deník vyžaduje
| deník =(Pomoc) - ^ Thompson M, Krull UJ (1982). „Elektroanalytická odpověď dvojvrstvé lipidové membrány na valinomycin: obsah cholesterolu v membráně“. Anální. Chim. Acta. 141: 33–47. doi:10.1016 / S0003-2670 (01) 95308-5.
- ^ Safiulina D, Veksler V, Zharkovsky A, Kaasik A (2006). „Ztráta potenciálu mitochondriální membrány je spojena se zvýšením objemu mitochondrií: fyziologická role v neuronech“. J. Cell. Physiol. 206 (2): 347–353. doi:10.1002 / jcp.20476. PMID 16110491.
- ^ Bulletin ionoforu draselného
externí odkazy
- Předpisy o chemické bezpečnosti z Ministerstvo zdravotnictví v New Jersey.
- Zdravotní informace na Scorecard.
- Valinomycin z Fermentek.
- Valinomycin v DataBase vlastností pesticidů (PPDB)
