Hadí jed - Snake venom
 Vipera berus - Přístroj pro dodávání jedu | |||||||||
| Identifikátory | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Symbol | Toxin_TOLIP | ||||||||
| Pfam | PF00087 | ||||||||
| InterPro | IPR003571 | ||||||||
| STRÁNKA | PDOC00245 | ||||||||
| SCOP2 | 2ctx / Rozsah / SUPFAM | ||||||||
| OPM nadčeleď | 53 | ||||||||
| OPM protein | 1txa | ||||||||
| |||||||||
Hadí jed je velmi upravený sliny[1] obsahující zootoxiny které usnadňují imobilizaci a trávení kořist a obrana proti hrozbám. Je vstřikován jedinečným tesáky během a kousat, a některé druhy jsou také schopné vyplivnout svůj jed.[2]
Žlázy, které vylučují zootoxiny, jsou modifikací příušní slinné žlázy nalezeno v jiných obratlovců, a jsou obvykle umístěny na každé straně hlavy, pod a za okem a zapouzdřeny ve svalové pochvě. Žlázy mají velké alveoly ve kterém se syntetizuje jed je uložen před tím, než je veden potrubím na základnu vedených nebo trubkových zubů, kterými je vyhozen.[3][4]
Jedy obsahují více než 20 různých sloučenin, většinou bílkovin a polypeptidů.[3] Složitá směs bílkovin, enzymů a různých dalších látek s toxickými a smrtícími vlastnostmi[2] slouží k znehybnění kořistního zvířete,[5] enzymy hrají důležitou roli při trávení kořisti,[4] a různé další látky jsou odpovědné za důležité, ale neletální biologické účinky.[2] Některé z proteinů v hadím jedu mají velmi specifické účinky na různé biologické funkce, včetně srážení krve, regulace krevního tlaku a přenosu nervových nebo svalových impulsů, a byly vyvinuty pro použití jako farmakologické nebo diagnostické nástroje a dokonce i jako užitečné léky.[2]
Chemie
Charles Lucien Bonaparte, syn Lucien Bonaparte, mladší bratr Napoleon Bonaparte, byl první, kdo v roce 1843 ustanovil bílkovinnou povahu hadího jedu.[Citace je zapotřebí ]
Proteiny tvoří 90-95% suché hmotnosti jedu a jsou zodpovědné za téměř všechny jeho biologické účinky. Mezi stovkami, dokonce tisíci bílkovin nalezenými v jedu jsou toxiny, neurotoxiny zejména netoxické proteiny (které mají také farmakologické vlastnosti) a mnoho enzymů, zejména hydrolytické.[2] Enzymy (molekulární váha 13-150 KDa) tvoří 80-90% viperidů a 25-70% elapidových jedů, včetně trávicích hydroláz, oxidázy L-aminokyselin, fosfolipáz, prokoagulantu podobného trombinu a serinových proteáz podobných kalikreinu a metaloproteinázy (hemoraginy), které poškozují vaskulární endotel. Polypeptid toxiny (molekulová hmotnost 5-10 KDa) zahrnují cytotoxiny, kardiotoxiny a postsynaptické neurotoxiny (jako např α-bungarotoxin a α-kobratoxin ), na které se váže acetylcholinové receptory na neuromuskulárních spojích. Mezi sloučeniny s nízkou molekulovou hmotností (do 1,5 KDa) patří kovy, peptidy, lipidy, nukleosidy, uhlohydráty, aminy a oligopeptidy, které inhibují angiotensin konvertující enzym (ACE) a potencují bradykinin (BPP). Mezidruhové a vnitrodruhové variace v chemickém složení jedu jsou geografické a ontogenní.[3] Fosfodiesterázy zasahovat do srdečního systému kořisti, hlavně ke snížení krevní tlak. Fosfolipáza A2 příčiny hemolýza lyžováním fosfolipid buněčné membrány z červené krvinky.[6] Aminokyselina oxidázy a proteázy se používají k trávení. Aminokyselinová oxidáza také spouští některé další enzymy a je zodpovědná za žlutou barvu jedu některých druhů. Hyaluronidáza zvyšuje permeabilitu tkání, aby se urychlila absorpce dalších enzymů do tkání. Některé hadí jedy nesou fasciculiny, jako mambas (Dendroaspis), které inhibují cholinesteráza aby kořist ztratila kontrolu nad svaly.[7]
| Typ | název | Původ |
|---|---|---|
| Oxydoreduktázy | laktát dehydrogenázy | Elapidae |
| L-aminokyselinová oxidáza | Všechny druhy | |
| Kataláza | Všechny druhy | |
| Transferázy | Alaninaminotransferáza | |
| Hydrolázy | Fosfolipáza A2 | Všechny druhy |
| Lysofosfolipáza | Elapidae, Viperidae | |
| Acetylcholinesteráza | Elapidae | |
| Alkalická fosfatáza | Bothrops atrox | |
| Kyselinová fosfatáza | Deinagkistrodon acutus | |
| 5'-nukleotidáza | Všechny druhy | |
| Fosfodiesteráza | Všechny druhy | |
| Deoxyribonukleáza | Všechny druhy | |
| Ribonukleáza 1 | Všechny druhy | |
| Adenosintrifosfatáza | Všechny druhy | |
| Amyláza | Všechny druhy | |
| Hyaluronidáza | Všechny druhy | |
| NAD-nukleotidáza | Všechny druhy | |
| Kininogenáza | Viperidae | |
| Aktivátor faktoru X | Viperidae, Crotalinae | |
| Heparináza | Crotalinae | |
| α-fibrinogenáza | Viperidae, Crotalinae | |
| β-fibrinogenáza | Viperidae, Crotalinae | |
| α-β-fibrinogenáza | Bitis gabonica | |
| Fibrinolytický enzym | Crotalinae | |
| Aktivátor protrombinu | Crotalinae | |
| Kolagenáza | Viperidae | |
| Elastáza | Viperidae | |
| Lyázy | Glukosamin amonná lyáza |
Hadové toxiny se velmi liší ve svých funkcích. Dvě široké skupiny toxinů nalezené v hadích jedech jsou neurotoxiny (většinou se vyskytují u elapidů) a hemotoxiny (většinou se vyskytují u viperidů). Vyskytují se však výjimky - jed kobra s černým hrdlem (Naja nigricollis), elapid, se skládá hlavně z cytotoxiny, zatímco to Mojave chřestýš (Crotalus scutulatus), viperid, je primárně neurotoxický. Elapidy i viperidy mohou nést řadu dalších druhů toxinů.
| α-neurotoxiny | α-bungarotoxin α-toxin, erabutoxin, kobratoxin |
|---|---|
| β-neurotoxiny (PLA2 ) | β-bungarotoxin, Notexin, ammodytoxin, krotoxin, taipoxin |
| κ-neurotoxiny | Kappa-bungarotoxin |
| Dendrotoxiny (Kunitz ) | Dendrotoxin toxiny I a K; případně β-bungarotoxinový řetězec B |
| Kardiotoxiny | Naja nigricollis y-toxin, kardiotoxin III (aka cytotoxiny) |
| Myotoxiny | Myotoxin -A, krotamin |
| Sarafotoxiny | Sarafotoxiny a, bac |
| Hemoraginy (metaloproteáza) | Mucrolysin, Atrolysiny, Akutolysiny, atd.[8] |
| Hemotoxiny (serinová proteáza) | Venombin A |
Toxiny
Neurotoxiny
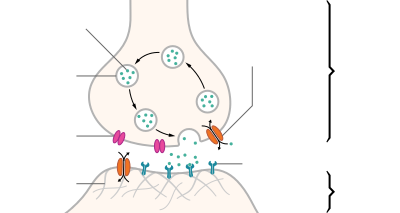
| Struktura typické chemická synapse |
|---|
Začátek nového nervového impulsu je následující:
- Výměna iontů (nabitých atomů) přes membránu nervových buněk vysílá depolarizační proud ke konci nervové buňky (terminus buňky).
- Když depolarizující proud dorazí na konec nervové buňky, neurotransmiter acetylcholin (ACh), který je držen ve váčcích, se uvolňuje do prostoru mezi dvěma nervy (synapse). Pohybuje se přes synapse k postsynaptickým receptorům.
- ACh se váže na receptory a přenáší signál do cílové buňky a po krátké době je zničen acetylcholinesterázou.
- Fasciculiny
- Tyto toxiny útočí na cholinergní neurony (ty, které používají ACh jako vysílač) ničením acetylcholinesterázy (AChE). ACh proto nelze rozložit a zůstává v receptoru. To způsobuje tetanii (nedobrovolnou kontrakci svalů), která může vést k smrti. Toxiny se od podání injekce nazývají fasciculiny myši, způsobují závažné, generalizované a dlouhotrvající (5-7 h) fascikulace (rychlé svalové kontrakce).
- Příklad hada: vyskytuje se většinou v jedu mambas (Dendroaspis spp.) a některé chřestýši (Crotalus spp.)
- Dendrotoxiny
- Dendrotoxiny inhibovat neurotransmise blokováním výměny pozitivních a negativních iontů přes neuronální membránu nevede k žádnému nervovému impulsu, čímž paralyzuje nervy.
- Příklad hada: mambas
- α-neurotoxiny
- Alfa-neurotoxiny jsou velkou skupinou s více než 100 postsynaptickými neurotoxiny, které byly identifikovány a sekvenovány.[9] α-neurotoxiny napadají Nikotinové acetylcholinové receptory cholinergních neuronů. Napodobují tvar molekuly acetylcholinu, takže zapadají do receptorů → blokují tok ACh → pocit necitlivosti a paralýzy.
- Příklady hadů: Král kobra (Ophiophagus hannah) (známý jako hannahtoxin obsahující α-neurotoxiny),[10] mořští hadi (Hydrophiinae) (známý jako erabutoxin), mnohopásý krait (Bungarus multicinctus) (známé jako α-bungarotoxin ), a kobry (Naja spp.) (známý jako kobratoxin )
Cytotoxiny
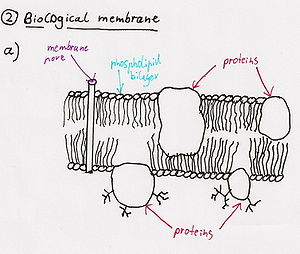

- Fosfolipázy
- Fosfolipáza je enzym, který transformuje molekulu fosfolipidů na lysofosfolipid (mýdlo) → nová molekula přitahuje a váže tuk a rozbíjí buněčné membrány. Fosfolipáza A2 je jeden specifický typ fosfolipáz nalezených v hadím jedu.
- Příklad hada: Okinawské habu (Trimeresurus flavoviridis)
- Kardiotoxiny / cytotoxiny
- Kardiotoxiny jsou složky, které jsou specificky toxické pro srdce. Váží se na konkrétní místa na povrchu svalových buněk a způsobují depolarizaci → toxin brání svalové kontrakci. Tyto toxiny mohou způsobit nepravidelný srdeční rytmus nebo přestat bít a způsobit smrt. Příkladem jsou tři prsty kardiotoxin III z kobry, příklad krátké tříprsté rodiny (InterPro: IPR003572 ).
- Příklad hada: mambas, a nějaký Naja druh
- Hemotoxiny
- Hemotoxiny způsobit hemolýzu, destrukci červených krvinek (erytrocytů) nebo vyvolat srážení krve (srážení krve, např. mucrocetin ). Běžná rodina hemotoxinů zahrnuje metaloproteinázy hadího jedu, jako je mucrolysin.[8][11]
- Příklady hadů: většina zmije a mnoho kobra druh: tropický chřestýš Crotalus durissus vyrábí konvulxin koagulant.[12]
Stanovení toxicity jedu (LD50)
Toxicita hadího jedu se hodnotí toxikologickým testem zvaným střední smrtelná dávka, LD50, (zkratka pro „smrtelnou dávku, 50%“), která určuje koncentraci toxinu potřebnou k usmrcení poloviny členů testované populace zvířat. Síla jedu divokých hadů se značně liší, dokonce iu jakéhokoli jednotlivého druhu, kvůli různým vlivům, jako je biofyzikální prostředí fyziologický stav, ekologické proměnné genetická variace (buď adaptivní nebo náhodné) a různé další molekulární a ekologické evoluční faktory. Taková variace je nutně menší u zajatých populací v kontrolovaných laboratorních podmínkách, i když ji nelze úplně vyloučit. Je však třeba navrhnout studie určující smrtelnost nebo účinnost hadího jedu, aby se minimalizovala variabilita, proto bylo za tímto účelem navrženo několik technik. Jedním z přístupů, který je považován za zvláště užitečný, je použití 0,1% hovězího sérového albuminu (také známého jako "frakce V" v Cohnův proces ) jako ředidlo při stanovení LD50 hodnoty pro různé druhy. Výsledkem je mnohem přesnější a konzistentnější LD50 stanovení, než například za použití 0,1% solného roztoku jako ředidla. Frakce V produkuje asi 95% čištěného albuminu, což je vysušený surový jed. Fyziologický roztok jako ředidlo trvale produkuje velmi proměnlivé LD50 výsledky pro téměř všechny jedovaté hady; produkuje nepředvídatelné rozdíly v čistotě sraženiny (rozmezí od 35 do 60%).[13] Frakce V je strukturálně stabilní, protože má sedmnáct disulfidové vazby; je jedinečný v tom, že má nejvyšší rozpustnost a nejnižší izoelektrický bod všech hlavních plazmatických proteinů. To z něj činí finální frakci, která se má vysrážet z roztoku. Hovězí sérový albumin je lokalizován ve frakci V. Srážení albuminu se provádí snížením pH na 4,8, což je blízké pí proteinů, a udržováním koncentrace ethanolu na 40%, s koncentrací proteinu 1%. V páté frakci tak zůstává pouze 1% původní plazmy.[14] Když je konečným cílem zpracování plazmy purifikovaná složka plazmy pro injekce nebo transfúze musí být složka plazmy vysoce čistá. První praktickou metodu frakcionace krevní plazmy ve velkém měřítku vyvinul Edwin J. Cohn v době druhá světová válka. To je známé jako Cohnův proces (nebo Cohnova metoda). Tento proces je také známý jako frakcionace studeným ethanolem, protože zahrnuje postupné zvyšování koncentrace z ethanol v řešení při 5 ° C a 3 ° C.[15] Cohnův proces využívá rozdíly ve vlastnostech různých plazmatických proteinů, konkrétně vysokých rozpustnost a nízko pI albuminu. Jak se koncentrace ethanolu zvyšuje ve stupních od 0 do 40%, snižuje se [pH] z neutrálního (pH ~ 7) na přibližně 4,8, což je blízko pl albuminu.[15] V každé fázi jsou určité bílkoviny vysráží se roztoku a odstraněn. Finále sraženina je čištěný albumin. Existuje několik variant tohoto procesu, včetně upravené metody Nitschmanna a Kistlera, která používá méně kroků, a nahrazuje ji centrifugace a hromadné zmrazení pomocí filtrace a diafiltrace.[15][16] Některé novější metody čištění albuminu přidávají k Cohnovu procesu a jeho variacím další kroky čištění. Chromatografické zpracování albuminu jako alternativa k Cohnovu procesu se objevilo počátkem 80. let, avšak široce bylo přijato až později kvůli nedostatečné dostupnosti velkého chromatografického zařízení. Metody, které začleňují chromatografii, obvykle začínají kryo-ochuzenou plazmou podstupující výměnu pufru buď diafiltrací nebo chromatografií na pufru, za účelem přípravy plazmy iontoměničová chromatografie kroky. Po iontové výměně obvykle probíhají další kroky chromatografického čištění a výměna pufru.[15]
Chromatografické metody pro separaci se však začaly přijímat počátkem 80. let. Vývoj probíhal v době mezi zahájením používání Cohnovy frakcionace, v roce 1946 a kdy chromatografie začal být používán v roce 1983. V roce 1962 byl vytvořen Kistlerův a Nistchmannův proces, který byl vedlejším produktem Cohnova procesu. Chromatografické procesy se začaly formovat v roce 1983. V 90. letech byly vytvořeny procesy Zenalb a CSL Albumex, které obsahovaly chromatografii s několika variantami. Obecný přístup k použití chromatografie pro frakcionaci plazmy pro albumin je: izolace supernatantu I, delipidace, aniontoměničová chromatografie, kationtoměničová chromatografie a gelová filtrační chromatografie. Získaný purifikovaný materiál je formulován s kombinací oktanoátu sodného a N-acetyl-tryptofanátu sodného a poté podroben postupům deaktivace viru, včetně pasterace při 60 ° C. Jedná se o efektivnější alternativu než Cohnův proces, a to ze čtyř hlavních důvodů: 1) byla nutná plynulá automatizace a bylo zapotřebí relativně levné zařízení, 2) snazší sterilizace zařízení a udržení dobrého výrobního prostředí, 3) chromatografické procesy méně poškozují albumin 4) lze dosáhnout úspěšnějšího konečného výsledku pro albumin. Ve srovnání s Cohnovým postupem se čistota albuminu zvýšila pomocí chromatografie z přibližně 95% na 98% a výtěžek se zvýšil z přibližně 65% na 85%. Malé procentuální zvýšení zvyšuje rozdíl v citlivých měřeních, jako je čistota. Jedna velká nevýhoda při použití chromatografie má co do činění s ekonomikou procesu. Ačkoli byla metoda z hlediska zpracování efektivní, získání potřebného vybavení je velkým úkolem. Je zapotřebí velké strojní zařízení a po dlouhou dobu nedostatečná dostupnost vybavení nepřispěla k jeho širokému použití. Komponenty jsou nyní snadněji dostupné, ale stále se jedná o nedokončenou výrobu.
Vývoj
Jed se mezi všemi vyvinul jen jednou Toxicofera asi před 170 miliony let a poté se diverzifikovala do obrovské rozmanitosti jedů, jaké dnes vidíme.[17] Původní toxikoferanový jed byl velmi jednoduchá sada bílkovin, které byly shromážděny ve dvojici žláz. Následně se tato sada proteinů vyvinula nezávisle v různých liniích toxikoferanů, včetně Serpentes, Anguimorpha, a Iguania.[18] Několik hadích linií od té doby ztratilo schopnost produkovat jed, často kvůli změně stravy nebo změně dravé taktiky.[17] Předpokládá se, že vývoj jedu je zodpovědný za enormní expanzi hadů po celém světě.[17][19]
Mechanismus evoluce ve většině případů byl genová duplikace v tkáních nesouvisejících s jedem, následovanou expresí nového proteinu v jedové žláze.[18] Poté následovalo přírodní výběr pro adaptivní vlastnosti podle modelu narození a smrti, kde po duplikaci následuje funkční diverzifikace, což vede k vytvoření strukturně příbuzných proteinů, které mají mírně odlišné funkce.[17][18][20] Studium vývoje jedu bylo pro vědce vysokou prioritou, pokud jde o vědecký výzkum, kvůli medicínskému významu hadího jedu, pokud jde o provádění výzkumu protijedů a rakoviny. Vědět více o složení jedu a způsobech, jak se může potenciálně vyvinout, je velmi prospěšné. Tři hlavní faktory ovlivňují vývoj jedu, které byly pečlivě studovány: predátoři hada, kteří jsou odolní vůči hadímu jedu, kořist, která je v evolučním závodě ve zbrojení s hady, a specifické stravy ovlivňující vnitrodruhový vývoj jedu. Jedy se nadále vyvíjejí jako specifické toxiny a jsou upraveny tak, aby cílily na konkrétní kořist, a u některých druhů se toxiny liší podle stravy.[21][22]
Rychlý vývoj jedu lze také vysvětlit zbrojním závodem mezi molekulami zaměřenými na jed u rezistentních predátorů, jako je například vačice a hadí jed, který cílí na molekuly. Vědci provedli experimenty na vačicích a zjistili, že několik pokusů ukázalo nahrazení tichými substitucemi ve von Willebrandově faktoru (vWf) gen, který kóduje hemostatický krevní protein zaměřený na jed. Předpokládá se, že tyto substituce oslabují spojení mezi vWf a toxickým ligandem hadího jedu (botrocetin), což mění čistý náboj a hydrofobicitu. Tyto výsledky jsou významné pro vývoj jedu, protože se jedná o první citaci rychlého vývoje v molekule zaměřené na jed. To ukazuje, že může dojít k evolučnímu závodu ve zbrojení, pokud jde o obranné účely. Alternativní hypotézy naznačují, že vývoj jedu je způsoben trofickou adaptací, zatímco tito vědci se domnívají, že v tomto případě by k výběru došlo na vlastnostech, které pomáhají s přežitím kořisti, pokud jde o vývoj jedu, místo úspěchu predace. Několik dalších predátorů zmije (mongoózy a ježci) vykazuje stejný typ vztahu mezi hady, což pomáhá podpořit hypotézu, že jed má spolu s trofickou roli velmi silnou obrannou roli. Což zase podporuje myšlenku, že predace hadů mohou být závody ve zbrojení, které produkují vývoj hadího jedu.[23]
Některé z různých adaptací produkovaných tímto procesem zahrnují jed toxičtější pro konkrétní kořist v několika liniích,[22][24][25] bílkoviny, které kořist tráví,[26] stejně jako metoda k vysledování kořisti po kousnutí.[27] Přítomnost někoho Trávicí enzymy u hadího jedu se kdysi věřilo, že je adaptací napomáhající trávení. Studie chřestýš západní diamantový (Crotalus atrox), had s vysoce proteolytický jed, ukažte, že jed nemá žádný vliv na dobu potřebnou k průchodu jídla skrz střevo.[28] Tyto různé úpravy jedu také vedly ke značné debatě o definici jedu a jedovatých hadů.[17]
Injekce
Zmije
V zmije, které mají nejrozvinutější aparát pro dodávání jedu, je jedová žláza velmi velká a je obklopena žloutek nebo spánkový sval, který se skládá ze dvou pásů, horní vycházející zpoza oka, spodní vyčnívající z žlázy do dolní čelisti. Potrubí nese jed z žlázy na tesák. U zmijí a elapidů je tato drážka zcela uzavřena a vytváří hypodermickou jehlovitou trubici. U jiných druhů nejsou drážky zakryty nebo jsou zakryty pouze částečně. Z předního konce žlázy kanál prochází pod okem a nad maxilární kost, k bazálnímu otvoru jedového tesáku, který je obalen hustým záhybem sliznice. Pomocí pohyblivé maxilární kosti zavěšené na prefrontální kosti a spojené s příčnou kostí, která je tlačena dopředu pomocí svalů aktivovaných otevřením úst, je vztyčen tesák a jed vypuštěn distálním otvorem. Když had kousne, čelisti se uzavřou a svaly obklopující žlázu se smrští, což způsobí vysunutí jedu pomocí zubů.
Elapids
V proteroglyphous elapids, tesáky jsou trubkovité, ale jsou krátké a nemají pohyblivost pozorovanou u zmijí.
Colubrids
Opisthoglyphous colubridy mají zvětšené, rýhované zuby umístěné na zadní končetině horní čelist, kde malá zadní část horní labiální nebo slinné žlázy produkuje jed.
Mechanika kousání

Několik rodů, včetně Asijské korálové hady (Calliophis), hrabat aspy (Atractaspis), a noční sčítače (Causus), jsou pozoruhodné tím, že mají výjimečně dlouhé jedové žlázy, rozprostírající se po každé straně těla, v některých případech zasahující až k srdci. Namísto svalů spánkové oblasti, které slouží k vytlačování jedu do potrubí, je tato akce prováděna těly na straně těla.
U hadů je patrná značná variabilita kousání. Při kousání viperidní hadi často rychle udeří, když tesáky proniknou kůží, vypustí jed a okamžitě se uvolní. Alternativně, jako v případě krmení, mohou být některé viperidy (např. Lachesis) kousnout a držet. A proteroglyf nebo opisthoglyph může po dlouhou dobu zavřít čelisti a kousat nebo pevně žvýkat.
Rozdíly v délce zubů mezi různými jedovatými hady jsou pravděpodobně způsobeny vývojem různých nápadných strategií.[29]
Mechanika plivání
Plivající kobry rodů Naja a Hemachatus, pokud jsou podrážděni nebo ohroženi, mohou vyvrhnout proudy nebo postřik jedem na vzdálenost 4 až 8 stop. Tesáky těchto hadů byly upraveny pro účely plivání; uvnitř tesáků kanál ohýbá 90 ° ke spodní přední části tesáku. Plivané mohou plivat opakovaně a stále mohou být smrtelní.
Plivání je pouze obranná reakce. Hadi mají tendenci mířit do očí vnímané hrozby. Přímý zásah může způsobit dočasný šok a slepotu zánět z rohovka a spojivka. I když obvykle nedojde k vážným příznakům, pokud je jed okamžitě vypláchnut velkým množstvím vody, slepota se může stát trvalou, pokud se neléčí. Krátký kontakt s pokožkou není bezprostředně nebezpečný, ale otevřené rány mohou být vektory pro envenomaci.
Fyziologické účinky
Čtyři odlišné druhy jedu působí na tělo odlišně:
- Proteolytické jed rozkládá molekulární okolí, včetně kousnutí.
- Hemotoxické jed působí na srdce a kardiovaskulární systém.
- Neurotoxický jed působí na nervový systém a mozek.
- Cytotoxický jed má lokalizovanou akci v místě kousnutí.
Proteroglyphous hadi
Účinek jedu proteroglyphous hadi (mořští hadi, kraits, mambas, černí hadi, tygří hadi, a přidavače smrti ) je hlavně na nervový systém, dýchací ochrnutí rychle se vytváří kontaktem jedu s mechanismem centrálního nervu, který řídí dýchání; bolest a místní otoky, které následují po kousnutí, nejsou obvykle závažné. Kousnutí všech proteroglyfických elapidů, dokonce i těch nejmenších a nejjemnějších, jako je korálové hady, je, pokud je známo, smrtící pro člověka. Některé mírně jedovaté elapidy však zůstávají, například hadi s kapucí (Parasuta ), bandy-bandies (Vermicella ), atd.
Zmije
Viper jed (Russellova zmije, zmije v měřítku, mistři keřů, a chřestýši ) působí více na cévní systém, vede ke srážení krve a srážení plicních tepen; jeho působení na nervový systém není velké, žádná jednotlivá skupina nervové buňky se zdá být vybrán a účinek na dýchání není tak přímý; vliv na oběh vysvětluje velkou depresi, která je příznakem eniperomace viperinu. Bolest rány je silná a rychle následuje otok a změna barvy. Příznaky způsobené kousnutím evropských zmijí jsou tak popsány Martinem a Beránkem:[30]
Po kousnutí bezprostředně následuje lokální bolest hořícího charakteru; končetina brzy nabobtná a zbarví se a během jedné až tří hodin dojde k velké pokoře doprovázené zvracení a často průjem, zapadá. Studený, vlhký pot je obvyklý. Pulz je extrémně slabý a mírný dušnost a může být vidět neklid. V závažných případech, které se vyskytují většinou u dětí, může být pulz nepostřehnutelný a končetiny studené; do kterého může pacient přejít kóma. Za dvanáct až dvacet čtyři hodin tyto závažné ústavní příznaky obvykle odezní; ale mezitím se otok a změna barvy enormně rozšířily. Končetina se stává flegmonózní a občas hnisá. Během několika dní se zotavení obvykle objeví poněkud náhle, ale smrt může být důsledkem těžké deprese nebo sekundárních účinků hnisání. V poslední kapitole tohoto úvodu je uvedeno, že případy úmrtí u dospělých i dětí nejsou v některých částech kontinentu neobvyklé.
Viperidae se mezi sebou velmi liší toxicitou svých jedů. Některé, například zmije indická Russell (Daboia russelli) a zmije v měřítku (E. carinatus); američtí chřestýši (Crotalus spp.), majitelé keřů (Lachesis spp.) a kopinaté hlavy (Bothrops spp.); a Africké přidávače (Bitis spp.), noční přidávače (Causus spp.) a rohaté zmije (Obilniny spp.), způsobí fatální výsledky, pokud není rychle aplikována náprava. Kousnutí větších evropských zmijí může být velmi nebezpečné a následovat budou fatální následky, zejména u dětí, přinejmenším v teplejších částech kontinentu; zatímco malé zmije luční (Vipera ursinii), který sotva někdy kousne, pokud není hrubě zacházen, se nezdá být posedlý velmi virulentním jedem, a přestože je v některých částech Rakousko a Maďarsko Není známo, že by někdy způsobil vážnou nehodu.
Opisthoglyphous colubrids
Biologové už dlouho věděli, že někteří hadi měli zadní zuby, „podřadné“ mechanismy vstřikování jedu, které by mohly znehybnit kořist; ačkoli bylo zaznamenáno několik úmrtí, až do roku 1957 se možnost, že by tito hadi byli pro člověka smrtelní, zdála nanejvýš vzdálená. Smrt dvou významných herpetologů, Robert Mertens a Karl Schmidt, od afrických colubridových kousnutí, změnilo toto hodnocení a nedávné události ukazují, že několik dalších druhů hadů se vzadu roztroušených má jedy, které jsou potenciálně smrtelné pro velké obratlovce.
Boomslang (Dispholidus typus) a větvička hada (Thelotornis spp.) jedy jsou toxické pro krevní buňky a ředí krev (hemotoxické, hemoragické). Mezi časné příznaky patří bolesti hlavy, nevolnost, průjem, letargie, duševní dezorientace, podlitiny a krvácení v místě a ve všech otvorech těla. Vykrvácení je hlavní příčinou smrti z takového kousnutí.
Jed boomslangu je nejúčinnější ze všech zadních hadů na světě založených na LD50. Ačkoli jeho jed může být účinnější než některé zmije a elapidy, způsobuje méně úmrtí v důsledku různých faktorů (například účinnost tesáků není vysoká ve srovnání s mnoha jinými hady, dodaná dávka jedu je nízká a boomslangs jsou obecně méně agresivní ve srovnání s jinými jedovatými hady, jako jsou kobry a mambové). Příznaky kousnutí od těchto hadů zahrnují nevolnost a vnitřní krvácení a člověk by mohl zemřít na krvácení do mozku a respirační kolaps.
Aglyphous hadi
Pokusy provedené s vylučováním příušní žláza z Rhabdophis a Zamenis ukázali, že dokonce aglyphous hadi nejsou úplně bez jedu, a poukazují na závěr, že fyziologický rozdíl mezi takzvanými neškodnými a jedovatými hady je pouze jeden stupeň, stejně jako existují různé kroky při transformaci obyčejné příušní žlázy na jedovou žlázu nebo pevný zub do trubkovitého nebo rýhovaného zubu.
Použití hadích jedů k léčbě nemocí
Vzhledem k tomu, že hadí jed obsahuje mnoho biologicky aktivních složek, mohou být některé užitečné při léčbě nemocí.[31]
Například, fosfolipázy typu A2 (PLA2s) od tuniských zmijí Cerastes cerastes a Macrovipera lebetina Bylo zjištěno, že mají protinádorovou aktivitu.[32] Protirakovinová aktivita byla také hlášena pro jiné sloučeniny v hadím jedu.[33][34] PLA2 hydrolyzují fosfolipidy, takže by mohly působit na povrch bakteriálních buněk a poskytovat nové antimikrobiální (antibiotické) aktivity.[35]
The analgetikum (zabíjení bolesti) aktivita mnoha proteinů hadího jedu je již dlouho známa.[36][37] Hlavní výzvou však je dodávat bílkoviny do nervových buněk, protože bílkoviny obvykle nelze použít jako pilulky.
Imunita
Mezi hady
Otázka, zda jsou jednotliví hadi imunní vůči svému vlastnímu jedu, ještě nebyla definitivně vyřešena, ačkoli je znám příklad kobry, která se sama uzdravila, což mělo za následek velkou absces vyžadující chirurgický zákrok, ale nevykazující žádný z dalších účinků, které by se rychle ukázaly jako smrtelné u druhů kořisti nebo u lidí.[38] Dále některé neškodné druhy, jako například severní Amerika obyčejný Kingsnake (Lampropeltis getula) a Centrální a jihoamerický mussurana (Clelia spp.), jsou důkazem proti jedu krotalinky, které navštěvují stejné okresy a které jsou schopné přemoci a živit se jimi. The kuřecí had (Spilotes pullatus) je nepřítelem zuřivost (Bothrops caribbaeus) na Svaté Lucii a při jejich setkáních je vždy vítězný kuřecí had. Opakované experimenty ukázaly Evropana užovka (Natrix natrix) nesmí být ovlivněn kousnutím Evropská zmije (Vipera berus) a Evropský asp (Vipera aspis), což je způsobeno přítomností toxických principů vylučovaných příušními a labiálními žlázami v krvi neškodného hada a obdobně jako u jedu těchto zmijí. Několik severoamerických druhů hadích krys, stejně jako královských hadů, se ukázalo jako imunní nebo vysoce odolné vůči jedu druhů chřestýšů. Královská kobra, která loví kobry, je prý imunní vůči jejich jedu.
Mezi jinými zvířaty
The ježek (Erinaceidae) mongoose (Herpestidae) Medojed (Mellivora capensis), vačice a několik dalších ptactvo které se živí hady, je známo, že jsou imunní vůči dávce hadího jedu.[Citace je zapotřebí ] Nedávno bylo zjištěno, že jezev medu a domácí prase konvergovaně vyvinuly náhrady aminokyselin ve svém nikotinovém acetylcholinovém receptoru, o kterém je známo, že u ježků vyvolává rezistenci na alfa-neurotoxiny.[39] Ať už prase lze považovat za imunní, je stále nejistá, i když rané studie ukazují endogenní rezistenci u prasat testovaných na neurotoxiny.[40] Ačkoli prase podkožní vrstva tuku ho může chránit před hadím jedem, většina jedů snadno prochází vaskulárními tukovými vrstvami, takže je nepravděpodobné, že by to přispělo k jeho schopnosti odolávat jedům. The plch zahradní (Eliomys quercinus) byl nedávno přidán na seznam zvířat odolných vůči zmiji. Některé populace Kalifornie sysel (Otospermophilus beecheyi) jsou alespoň částečně imunní vůči jedu chřestýšů jako dospělí.
Mezi lidmi
Získání lidské imunity proti hadímu jedu je prastaré (přibližně od roku 60 n. L. Psylli kmen). Probíhá výzkum vývoje vakcín, které povedou k imunitě. Bill Haast, majitel a ředitel Miami Serpentarium, si po většinu svého dospělého života injekčně podal hadí jed ve snaze vybudovat si imunitu vůči široké škále jedovatých hadů, v praxi známé jako mithridatism. Haast se dožil 100 let a přežil hlášených 172 hadích kousnutí. Daroval svou krev k léčbě obětí hadího kousnutí, když nebyl k dispozici vhodný protijed. Vyléčeno bylo více než 20 jedinců.[41][42][43] Amatérský výzkumník Tim Friede také nechává jedovaté hady kousat ho v naději, že bude vyvinuta vakcína proti hadímu jedu, a od ledna 2016 přežil více než 160 kousnutí od různých druhů.[44]
Tradiční léčba
The Světová zdravotnická organizace odhaduje, že 80% světové populace závisí na tradičních lécích, pokud jde o jejich primární potřeby zdravotní péče.[45] Metody tradičního léčení hadích kousnutí, i když mají spornou účinnost a možná i škodlivé, jsou nicméně relevantní.
Z rostlin používaných k ošetření hadích kousnutí v Trinidadu a Tobagu se vyrábějí tinktury s alkoholem nebo olivovým olejem a uchovávají se v rumových baňkách zvaných hadí lahve, které obsahují několik různých rostlin a / nebo hmyzu. Mezi použité rostliny patří réva zvaná opičí žebřík (Bauhinia cumanensis nebo Bauhinia excisa, Fabaceae), která se buší a kousne. Alternativně se vyrobí tinktura s kouskem vinné révy a uchovává se v hadí láhvi. Mezi další použité rostliny patří kořen mat (Aristolochia rugosa ), kočičí dráp (Pithecellobim unguis-cati ), tabák (Nicotiana tabacum ), hadí keř (Barleria lupulina ), obie semeno (Cola nitida ) a kořen divokého gri gri (Acrocomia aculeata ). Některé hadí lahve také obsahují housenky (Battus polydamas, Papilionidae), které jedí listy stromů (Aristolochia trilobata ). Léky na nouzové hady se získávají žvýkáním třípalcového kousku kořene bois canôt (Cecropia peltata ) a podávání tohoto žvýkacího roztoku kousnutému subjektu (obvykle loveckému psovi). Jedná se o běžnou původní rostlinu v Latinské Americe a Karibiku, což je vhodné jako nouzový prostředek. Další používanou původní rostlinou je mardi gras (Renealmia alpinia ) (bobule), které se drtí spolu se šťávou divoké třtiny (Costus scaber ) a dána kousnutému. Rychlé opravy zahrnovaly aplikaci žvýkaného tabáku z cigaret, doutníků nebo dýmek.[46] Dělání řezů kolem propíchnutí nebo vysávání jedu bylo v minulosti považováno za užitečné, ale od tohoto postupu léčby se nyní silně nedoporučuje, kvůli riziku sebenenergie při řezání nožem nebo řezáním v ústech (přísavky z hadího kousnutí) Lze použít soupravy, ale sání málokdy poskytuje jakoukoli měřitelnou výhodu).[47][48]
Séroterapie
Obzvláště pozoruhodný je pokrok, pokud jde o obrannou reakci, při které může být krev poskytnuta jako důkaz proti jedu, podobnými procesy jako očkování - antipoisonní seroterapie. Studie prokázaly, že antitoxický sera nepůsobí jako chemikálie protilátky při ničení jedu, ale jako fyziologické protilátky; že kromě jedových žláz mají hadi další žlázy zásobující svou krev látkami antagonistickými vůči jedu, jaké existují také u různých zvířat odolných vůči hadímu jedu ježek a mongoose například.
Regionální specifičnost jedu
Specifičnost různých hadích jedů je bohužel taková, že i když se fyziologický účinek jeví jako identický, sérové injekce nebo odstupňovaná přímá inokulace poskytují imunitu pouze jednomu druhu nebo několika příbuzným druhům.
Tak, a evropský v Austrálie kteří se stali imunní vůči jedu smrtícího Australana tygří had (Notechis scutatus), manipulating these snakes with impunity, and was under the impression that his immunity extended also to other species, when bitten by a nížina Copperhead (Austrelaps superbus), an allied elapine, died the following day.
v Indie, the serum prepared with the venom of monocled cobra Naja kaouthia has been found to be without effect on the venom of two species of kraits (Bungarus), Russell's viper (Daboia russelli), saw-scaled viper (Echis carinatus), a Pope's pit viper (Trimeresurus popeiorum). Russell's viper serum is without effect on colubrine venoms, or those of Echis a Trimeresurus.
v Brazílie, serum prepared with the venom of lanceheads (Bothrops spp.) is without action on rattlesnake (Crotalus spp.) venom.
Antivenom snakebite treatment must be matched as the type of envenomation that has occurred. In the Americas, polyvalent antivenoms are available that are effective against the bites of most pit vipers. Crofab is the antivenom developed to treat the bite of North American pit vipers.[49] These are not effective against korálový had envenomation, which requires a specific antivenom to their neurotoxic venom. The situation is even more complex in countries such as India, with its rich mix of vipers (Viperidae) and highly neurotoxic cobras and kraits of the Elapidae.
This article is based on the 1913 book Hadi Evropy, by G. A. Boulenger, which is now in the veřejná doména in the United States (and possibly elsewhere). Because of its age, the text in this article should not necessarily be viewed as reflecting the current knowledge of snake venom.
Viz také
Reference
- ^ "Reptile Venom Research". Park australských plazů. Archivovány od originál dne 2. února 2010. Citováno 21. prosince 2010.
- ^ A b C d E F Bauchot R (1994). Snakes: A Natural History. New York City, NY, USA: Sterling Publishing Co., Inc. pp.194–209. ISBN 978-1-4027-3181-5.
- ^ A b C Halliday A, Kraig T, eds. (2002). Firefly Encyclopedia of Reptiles and Amphibians. Toronto, Canada: Firefly Books Ltd. pp.202–203. ISBN 978-1-55297-613-5.
- ^ A b Bottrall JL, Madaras F, Biven CD, Venning MG, Mirtschin PJ (September 2010). "Proteolytic activity of Elapid and Viperid Snake venoms and its implication to digestion". Journal of Venom Research. 1 (3): 18–28. PMC 3086185. PMID 21544178.
- ^ Mattison C (2007). Nová encyklopedie hadů. New Jersey, USA (first published in the UK): Princeton University Press (Princeton and Oxford) first published in Blandford. p. 117. ISBN 978-0-691-13295-2.
- ^ Condrea E, Devries A, Mager J (February 1964). "Hemolysis and splitting of human erythrocyte phospholipids by snake venoms". Biochimica et Biophysica Acta (BBA) - Specialized Section on Lipids and Related Subjects. 84 (1): 60–73. doi:10.1016/0926-6542(64)90101-5. PMID 14124757.

- ^ Rodríguez-Ithurralde D, Silveira R, Barbeito L, Dajas F (1983). "Fasciculin, a powerful anticholinesterase polypeptide from Dendroaspis angusticeps venom". Neurochemistry International. 5 (3): 267–74. doi:10.1016/0197-0186(83)90028-1. PMID 20487949. S2CID 8952817.

- ^ A b "Keyword: Hemorrhagic toxin KW-1200". UniProt. Citováno 1. června 2019.
- ^ Hodgson WC, Wickramaratna JC (September 2002). "In vitro neuromuscular activity of snake venoms". Klinická a experimentální farmakologie a fyziologie. 29 (9): 807–14. doi:10.1046/j.1440-1681.2002.03740.x. PMID 12165047. S2CID 20158638.

- ^ He YY, Lee WH, Zhang Y (September 2004). "Cloning and purification of alpha-neurotoxins from king cobra (Ophiophagus hannah)". Toxicon. 44 (3): 295–303. doi:10.1016/j.toxicon.2004.06.003. PMID 15302536.

- ^ Bernardoni JL, Sousa LF, Wermelinger LS, Lopes AS, Prezoto BC, Serrano SM, Zingali RB, Moura-da-Silva AM (14 October 2014). "Functional variability of snake venom metalloproteinases: adaptive advantages in targeting different prey and implications for human envenomation". PLOS ONE. 9 (10): e109651. Bibcode:2014PLoSO...9j9651B. doi:10.1371/journal.pone.0109651. PMC 4196926. PMID 25313513.
- ^ Hermans C, Wittevrongel C, Thys C, Smethurst PA, Van Geet C, Freson K (August 2009). "A compound heterozygous mutation in glycoprotein VI in a patient with a bleeding disorder". Journal of trombózy a hemostázy. 7 (8): 1356–63. doi:10.1111/j.1538-7836.2009.03520.x. PMID 19552682. S2CID 205728095.

- ^ Broad AJ, Sutherland SK, Coulter AR (17 May 1979). "The lethality in mice of dangerous Australian and other snake venom" (PDF). Toxicon. 17 (6): 661–4. doi:10.1016/0041-0101(79)90245-9. PMID 524395.
- ^ Rosen FS (31 July 2003). "Edwin J. Cohn and the Development of Protein Chemistry". The New England Journal of Medicine. 349 (5): 511–512. doi:10.1056/NEJM200307313490522.
- ^ A b C d Matejtschuk P, Dash CH, Gascoigne EW (December 2000). "Production of human albumin solution: a continually developing colloid". British Journal of Anesthesia. 85 (6): 887–95. doi:10.1093/bja/85.6.887. PMID 11732525.
- ^ Brodniewicz-Proba T (December 1991). "Human plasma fractionation and the impact of new technologies on the use and quality of plasma-derived products". Blood Reviews. 5 (4): 245–57. doi:10.1016/0268-960x(91)90016-6. PMID 1782484.
- ^ A b C d E Fry BG, Casewell NR, Wüster W, Vidal N, Young B, Jackson TN (September 2012). "The structural and functional diversification of the Toxicofera reptile venom system". Toxicon. 60 (4): 434–48. doi:10.1016/j.toxicon.2012.02.013. PMID 22446061.
- ^ A b C Casewell NR, Wüster W, Vonk FJ, Harrison RA, Fry BG (April 2013). "Complex cocktails: the evolutionary novelty of venoms". Trendy v ekologii a evoluci. 28 (4): 219–29. doi:10.1016/j.tree.2012.10.020. PMID 23219381.
- ^ Lomonte B, Fernández J, Sanz L, Angulo Y, Sasa M, Gutiérrez JM, Calvete JJ (June 2014). "Venomous snakes of Costa Rica: biological and medical implications of their venom proteomic profiles analyzed through the strategy of snake venomics". Journal of Proteomics. 105: 323–39. doi:10.1016/j.jprot.2014.02.020. PMID 24576642.
- ^ Lynch VJ (January 2007). "Inventing an arsenal: adaptive evolution and neofunctionalization of snake venom phospholipase A2 genes". BMC Evoluční biologie. 7 (2): 2. doi:10.1186/1471-2148-7-2. PMC 1783844. PMID 17233905.

- ^ Pahari S, Bickford D, Fry BG, Kini RM (September 2007). "Expression pattern of three-finger toxin and phospholipase A2 genes in the venom glands of two sea snakes, Lapemis curtus and Acalyptophis peronii: comparison of evolution of these toxins in land snakes, sea kraits and sea snakes". BMC Evoluční biologie. 7: 175. doi:10.1186/1471-2148-7-175. PMC 2174459. PMID 17900344.

- ^ A b Barlow A, Pook CE, Harrison RA, Wüster W (July 2009). "Coevolution of diet and prey-specific venom activity supports the role of selection in snake venom evolution". Sborník: Biologické vědy. 276 (1666): 2443–9. doi:10.1098/rspb.2009.0048. JSTOR 30244073. PMC 2690460. PMID 19364745.

- ^ Jansa SA, Voss RS (22 June 2011). "Adaptive evolution of the venom-targeted vWF protein in opossums that eat pitvipers". PLOS ONE. 6 (6): e20997. Bibcode:2011PLoSO...620997J. doi:10.1371/journal.pone.0020997. PMC 3120824. PMID 21731638.
- ^ Calvete JJ, Ghezellou P, Paiva O, Matainaho T, Ghassempour A, Goudarzi H, Kraus F, Sanz L, Williams DJ (July 2012). "Snake venomics of two poorly known Hydrophiinae: Comparative proteomics of the venoms of terrestrial Toxicocalamus longissimus and marine Hydrophis cyanocinctus". Journal of Proteomics. 75 (13): 4091–101. doi:10.1016/j.jprot.2012.05.026. PMID 22643073.
- ^ Li M, Fry BG, Kini RM (January 2005). "Eggs-only diet: its implications for the toxin profile changes and ecology of the marbled sea snake (Aipysurus eydouxii)". Journal of Molecular Evolution. 60 (1): 81–9. Bibcode:2005JMolE..60...81L. doi:10.1007/s00239-004-0138-0. PMID 15696370. S2CID 17572816.
- ^ Mackessy SP (July 2010). "Evolutionary trends in venom composition in the western rattlesnakes (Crotalus viridis sensu lato): toxicity vs. tenderizers". Toxicon. 55 (8): 1463–74. doi:10.1016/j.toxicon.2010.02.028. PMID 20227433.
- ^ Saviola AJ, Chiszar D, Busch C, Mackessy SP (March 2013). "Molecular basis for prey relocation in viperid snakes". Biologie BMC. 11 (1): 20. doi:10.1186/1741-7007-11-20. PMC 3635877. PMID 23452837.
- ^ McCue MD (October 2007). "Prey envenomation does not improve digestive performance in western diamondback rattlesnakes (Crotalus atrox)". Journal of Experimental Zoology Part A. 307 (10): 568–77. doi:10.1002/jez.411. PMID 17671964.

- ^ Broeckhoven C, du Plessis A (August 2017). "Has snake fang evolution lost its bite? New insights from a structural mechanics viewpoint". Biologické dopisy. 13 (8): 20170293. doi:10.1098/rsbl.2017.0293. PMC 5582107. PMID 28768797.
- ^ Martin CJ, Lamb G (1907). "Snake-poison and Snake-bite". In Allbutt TC, Rolleston ND (eds.). Systém medicíny. Londýn: MacMillan. pp. 783–821.
- ^ McCleary RJ, Kini RM (February 2013). "Non-enzymatic proteins from snake venoms: a gold mine of pharmacological tools and drug leads". Toxicon. 62: 56–74. doi:10.1016/j.toxicon.2012.09.008. PMID 23058997.
- ^ Zouari-Kessentini R, Srairi-Abid N, Bazaa A, El Ayeb M, Luis J, Marrakchi N (2013). "Antitumoral potential of Tunisian snake venoms secreted phospholipases A2". BioMed Research International. 2013: 1–9. doi:10.1155/2013/391389. PMC 3581298. PMID 23509718.
- ^ Vyas VK, Brahmbhatt K, Bhatt H, Parmar U (February 2013). "Therapeutic potential of snake venom in cancer therapy: current perspectives". Asian Pacific Journal of Tropical Biomedicine. 3 (2): 156–62. doi:10.1016/S2221-1691(13)60042-8. PMC 3627178. PMID 23593597.
- ^ Jain D, Kumar S (2012). "Snake venom: a potent anticancer agent". Asian Pacific Journal of Cancer Prevention. 13 (10): 4855–60. doi:10.7314/apjcp.2012.13.10.4855. PMID 23244070.
- ^ de Oliveira Junior NG, e Silva Cardoso MH, Franco OL (December 2013). "Snake venoms: attractive antimicrobial proteinaceous compounds for therapeutic purposes". Buněčné a molekulární biologické vědy. 70 (24): 4645–58. doi:10.1007/s00018-013-1345-x. PMID 23657358. S2CID 15127065.
- ^ Woolf CJ (January 2013). "Pain: morphine, metabolites, mambas, and mutations". Lancet. Neurologie. 12 (1): 18–20. doi:10.1016/S1474-4422(12)70287-9. PMID 23237896. S2CID 8697382.
- ^ Osipov A, Utkin Y (December 2012). "Effects of snake venom polypeptides on central nervous system". Central Nervous System Agents in Medicinal Chemistry. 12 (4): 315–28. doi:10.2174/187152412803760618. PMID 23270323. S2CID 36274766.
- ^ "Sterile tail abscess in Naja annulifera - self-envenomation case". Archivovány od originál dne 27. října 2004. Citováno 2. dubna 2009.
- ^ Drabeck D, Jansa S (2015). "Why the Honey Badger Doesn't Care: Independent Evolution of Resistance to Three Finger Toxins in the Nicotinic Acetylcholine Receptor". Toxicon. 99: 68–72. doi:10.1016/j.toxicon.2015.03.007. PMID 25796346.
- ^ Grasset E, Zoutendykanda A, Schaafsma A (1935). "Studies on the toxic and antigenic properties of Southern African snake venoms with specialreference to the polyvalency of South African antivenene". Trans. R. Soc. Trop. Med. Hygiena. 28 (6): 601–612. doi:10.1016/S0035-9203(35)90031-1.
- ^ "Farewell to these famous Floridians". Florida Trend. 19. prosince 2011. Citováno 2. dubna 2012.
- ^ Rosenberg C (21 June 2011). "Bill Haast dies at 100; snakes were the charm for south Florida celebrity". Los Angeles Times. Citováno 16. října 2012.
- ^ Schudel M (18 June 2011). "Bill Haast dies at 100: Florida snake man provided venom for snakebite serum". The Washington Post. Citováno 16. října 2012.
- ^ "Man makes deadly snakes bite him 160 times in hunt for human antidote | Americas | News | The Independent". 21. ledna 2016. Citováno 7. července 2016.
- ^ Hiremath VT, Taranath TC (February 2010). "Traditional Phytotherapy for Snake bites by Tribes of Chitradurga District, Karnataka, India". Ethnobotanical Leaflets. 14 (2): 120–125.
- ^ Zethelius M, Balick MJ (March 1982). "Modern medicine and shamanistic ritual: a case of positive synergistic response in the treatment of a snakebite" (PDF). Journal of Ethnopharmacology. 5 (2): 181–5. doi:10.1016/0378-8741(82)90042-3. PMID 7057657.

- ^ "Treating Snake Bites". Ces.ncsu.edu. Citováno 16. října 2012.
- ^ "CDC - Venomous Snakes - NIOSH Workplace Safety and Health Topic". CDC.gov. 1. července 2016. Citováno 7. července 2016.
- ^ http://www.savagelabs.com/Products/CroFab/Home/crofab_frame.htm Link to PDF for full prescribing information, retrieved 11/12/12
Další čtení
- Jonassen I, Collins JF, Higgins DG (August 1995). "Finding flexible patterns in unaligned protein sequences". Věda o bílkovinách. 4 (8): 1587–95. doi:10.1002/pro.5560040817. PMC 2143188. PMID 8520485.
- Shaw IC (2007). "Chapter 19: Snake Toxins". In Waring RH, Steventon GB, Mitchell SC (eds.). Molecules of Death (Druhé vydání.). River Edge, N.J: Imperial College Press. str.329 –344. ISBN 978-1-86094-815-2.
externí odkazy
- An overview of the diversity and evolution of snake fangs.
- Snake VenomsUMich Orientace proteinů v membránách families/superfamily-55 - Calculated orientations of snake venom phospholipases A2 and myotoxins in the lipid bilayer.
- LD50's for most toxic venoms.
- Australian Venom Research Unit - a general source of information for venomous creatures in Australia.
- biomedcentral.com - Medicinal and ethnoveterinary remedies of hunters in Trinidad.
- reptilis.net - How venom works.
- snakevenom.net - Drying and storage of snake venom.