Tetanospasmin - Tetanospasmin
| Tetanospasmin | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Identifikátory | |||||||
| Organismus | |||||||
| Symbol | Stan | ||||||
| UniProt | P04958 | ||||||
| |||||||


Tetanový toxin je extrémně silný neurotoxin produkovaný vegetativní buňkou Clostridium tetani[1] v anaerobní podmínky, způsobující tetanus. Nemá žádnou známou funkci pro klostridie v půdním prostředí, kde se běžně vyskytují. Také se tomu říká spasmogenní toxinnebo Stan. LD50 tohoto toxinu bylo naměřeno přibližně 2,5-3 ng / kg,[2][3] takže je na druhém místě za související botulotoxin (LD50 2 ng / kg)[4] jako nejsmrtelnější toxin na světě. Tyto testy se však provádějí pouze na myších, které mohou reagovat na toxin odlišně od lidí a jiných zvířat.
C. tetani také vyrábí exotoxin tetanolysin hemolyzin, který způsobuje destrukci tkání.[5]
Rozdělení
Toxin tetanu se šíří tkáňovými prostory do lymfatický a cévní systémy. Vstupuje do nervového systému u neuromuskulární spojení a migruje nervovými kmeny do centrální nervový systém (CNS) retrográdním axonálním transportem pomocí dyneiny.[6][7]
Struktura
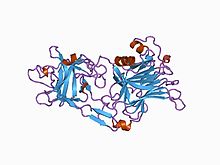
Toxin tetanu protein má molekulovou hmotnost 150kDa. Je přeložen z tetX Gen jako jeden protein, který se následně štěpí na dvě části: 100 kDa těžký nebo B-řetězec a 50 kDa lehký nebo A-řetězec. Řetězy jsou spojeny a disulfidová vazba.
- B-řetězec se váže na disialogangliosidy (GD2 a GD1b) na neuronální membráně a obsahuje translokační doménu, která napomáhá pohybu proteinu přes tuto membránu a do neuronu.
- Řetěz A, zinek rodiny M27 endopeptidáza, útočí na membránový protein spojený s vezikuly (VAMP).
Gen TetX kódující tento protein je umístěn na plazmidu PE88.[8][9]
Několik struktur vazebné domény a peptidázové domény bylo vyřešeno Rentgenová krystalografie a uloženy v PDB. Souhrn těchto struktur je k dispozici pomocí UniPDB přihláška na PDBe, například 1z7h nebo 3hmy.
Mechanismus účinku
Mechanismus působení TeNT lze rozdělit a diskutovat v těchto různých krocích:
- Doprava
- Specifická vazba v periferní neurony
- Retrográdní axonální transport do CNS inhibiční interneurony
- Transcytóza z axonu do inhibičních interneuronů
- Akce
- Translokace lehkého řetězce do cytosolu zprostředkovaná teplotou a pH
- Snížení disulfidového mostu do thioly, přerušení spojení mezi lehkým a těžkým řetězcem
- Štěpení synaptobrevinu
První tři kroky naznačují cestu tetanu z periferního nervového systému tam, kde je přenesen do CNS a má svůj konečný účinek. Poslední tři kroky dokumentují změny nezbytné pro finální mechanismus neurotoxinu.
Transport do CNS inhibujících interneuronů začíná B-řetězcem zprostředkujícím neurospecifickou vazbu TeNT na nervovou terminální membránu. Váže se na GT1b polysialogangliosidy, podobně jako C. botulinum neurotoxin. Rovněž se váže na jinou špatně charakterizovanou Protein ukotvený GPI receptor specifičtější pro TeNT.[10][11] Gangliozid i GPI ukotvený protein jsou umístěny v lipidové mikrodomény a oba jsou nezbytné pro konkrétní vazbu TeNT.[11] Jakmile je navázán, je neurotoxin poté endocytován do nervu a začne cestovat axonem k spinálním neuronům. Další krok, transcytóza z axonu do CNS inhibujícího interneuronu, je jednou z nejméně pochopených částí působení TeNT. Jsou zahrnuty alespoň dvě cesty, jedna se spoléhá na recyklaci systému synaptických vezikul 2 (SV2) a druhá nikoli.[12]
Jakmile je vezikul v inhibičním interneuronu, jeho translokace je zprostředkována pH a teplotou, konkrétně nízkým nebo kyselým pH ve vezikulu a standardními fyziologickými teplotami.[13][14] Jakmile je toxin translokován do cytosolu, dochází k chemické redukci disulfidové vazby na oddělené thioly, hlavně enzymem NADPH-thioredoxin reduktáza-thioredoxin. Lehký řetězec je potom volný k štěpení vazby Gln76-Phe77 synaptobrevinu.[15] Štěpení synaptobrevinu ovlivňuje stabilitu jádra SNARE omezením jeho vstupu do nízkoenergetické konformace, která je cílem pro vazbu NSF.[16] Synaptobrevin je integrální V-SNARE nezbytné pro fúzi vezikul na membrány. Konečným cílem TeNT je štěpení synaptobrevin a dokonce i v nízkých dávkách působí rušivě exocytóza z neurotransmitery z inhibičního interneurony. Blokování neurotransmiterů kyselina y-aminomáselná (GABA) a glycin je přímou příčinou fyziologických účinků, které TeNT vyvolává. GABA inhibuje motorické neurony, takže blokováním GABA toxin tetanu způsobuje prudkou spastickou paralýzu.[17] Působení A-řetězce také zastaví postižené neurony v uvolňování excitačních vysílačů,[18] degradací proteinu synaptobrevin 2.[19] Kombinovaným důsledkem je nebezpečná nadměrná aktivita v EU svaly z nejmenších smyslových podnětů, jako je tlumení motorické reflexy je inhibován, což vede ke generalizovaným kontrakcím muskulatury agonisty a antagonisty, označované jako „tetanický křeč“.
Klinický význam
Klinické projevy tetanu jsou způsobeny tím, že toxin tetanu blokuje inhibiční impulsy interferencí s uvolňováním neurotransmitery, počítaje v to glycin a kyselina gama-aminomáselná. Tyto inhibiční neurotransmitery inhibují alfa motorické neurony. Se sníženou inhibicí se zvyšuje klidová rychlost střelby alfa motorického neuronu, což způsobuje tuhost, bezporuchové svalové kontrakce a křeče. Charakteristické rysy jsou risus sardonicus (přísný úsměv), trismus (běžně známý jako "lock-jaw") a opisthotonus (tuhý, klenutý hřbet). Záchvaty může dojít, a autonomní nervový systém může být také ovlivněna. Zdá se, že tetanospasmin brání uvolňování neurotransmiterů selektivním štěpením složky synaptických vezikul zvané synaptobrevin II.[20] Ztráta inhibice také ovlivňuje preganglionové sympatické neurony v laterálním směru šedá hmota míchy a produkuje sympatickou hyperaktivitu a vysokou cirkulaci katecholamin úrovně. Hypertenze a tachykardie střídavě s hypotenze a bradykardie se může vyvinout.[21][22]
Tetanické křeče se mohou vyskytovat v charakteristické formě zvané opisthotonos a být dostatečně tvrdý, aby zlomil dlouhé kosti. Kratší nervy jsou inhibovány jako první, což vede k charakteristickým časným příznakům v obličeji a čelisti, risus sardonicus a kleště.
Toxin se váže na neurony je nevratný[6] a funkci nervů lze vrátit pouze růstem nových terminálů a synapsí.
Imunita a očkování
Díky své extrémní účinnosti nemusí být smrtelná dávka tetanospasminu dostatečná k vyvolání imunitní odpovědi. Přirozeně získané infekce tetanem tedy obvykle neposkytují imunitu vůči následným infekcím. Imunizace (která je nestálá a musí se pravidelně opakovat) používá méně smrtící toxoid odvozené od toxinu, jako v vakcína proti tetanu a nějaký kombinované vakcíny (jako DTP ).
Reference
- ^ "tetanospasmin " na Dorlandův lékařský slovník
- ^ "Pinkbook | Tetanus | Epidemiologie nemocí, kterým lze zabránit očkováním | CDC". www.cdc.gov. Citováno 2017-01-18.
- ^ "Tabulka toxinů» Zdraví a bezpečnost pro životní prostředí »University of Florida". www.ehs.ufl.edu. Citováno 2017-01-18.
- ^ "Botulismus". Světová zdravotnická organizace. Citováno 2017-01-18.
- ^ Willey, Joanne (2009). Prescottovy principy mikrobiologie. New York City, NY: McGraw-Hill. str.481. ISBN 978-0-07-337523-6.
- ^ A b Farrar JJ; Yen LM; Cook T; Fairweather N; Binh N; Parry J; Parry CM (září 2000). "Tetanus". Časopis neurologie, neurochirurgie a psychiatrie. 69 (3): 292–301. doi:10.1136 / jnnp.69.3.292. PMC 1737078. PMID 10945801.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ AU Lalli G, Gschmeissner S, Schiavo G (15. listopadu 2003). „Pro rychlý axonální retrográdní transport toxinu tetanu v motorických neuronech jsou vyžadovány motory na bázi myosinu Va a mikrotubulů“. Journal of Cell Science. 116 (22): 4639–50. doi:10.1242 / jcs.00727. PMID 14576357.
- ^ Eisel U, Jarausch W, Goretzki K, Henschen A, Engels J, Weller U, Hudel M, Habermann E, Niemann H (1986). „Tetanový toxin: primární struktura, exprese v E. coli a homologie s botulotoxiny“. EMBO J.. 5 (10): 2495–502. doi:10.1002 / j.1460-2075.1986.tb04527.x. PMC 1167145. PMID 3536478.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Popp D, Narita A, Lee LJ, Ghoshdastider U, Xue B, Srinivasan R, Balasubramanian MK, Tanaka T, Robinson RC (2012). „Nová struktura vlákna podobná aktinu z Clostridium tetani“. The Journal of Biological Chemistry. 287 (25): 21121–9. doi:10.1074 / jbc.M112.341016. PMC 3375535. PMID 22514279.CS1 maint: používá parametr autoři (odkaz)
- ^ Munro, P; Kojima, H; Dupont, JL; Bossu, JL; Poulain, B; Boquet, P (30. listopadu 2001). „Vysoká citlivost myších neuronálních buněk na tetanový toxin vyžaduje protein ukotvený GPI“. Sdělení o biochemickém a biofyzikálním výzkumu. 289 (2): 623–9. doi:10.1006 / bbrc.2001.6031. PMID 11716521.
- ^ A b Zima, A; Ulrich, WP; Wetterich, F; Weller, U; Galla, HJ (17. června 1996). „Gangliosidy ve fosfolipidových dvojvrstvých membránách: interakce s toxem tetanu“. Chemie a fyzika lipidů. 81 (1): 21–34. doi:10.1016/0009-3084(96)02529-7. PMID 9450318.
- ^ Yeh, FL; Dong, M; Yao, J; Tepp, WH; Lin, G; Johnson, EA; Chapman, ER (24. listopadu 2010). „SV2 zprostředkovává vstup neurotoxinu z tetanu do centrálních neuronů“ (PDF). PLOS patogeny. 6 (11): e1001207. doi:10.1371 / journal.ppat.1001207. PMC 2991259. PMID 21124874.
- ^ Pirazzini, M; Rossetto, O; Bertasio, C; Bordin, F; Shone, CC; Binz, T; Montecucco, C (4. ledna 2013). "Časový průběh a teplotní závislost membránové translokace tetanových a botulinových neurotoxinů C a D v neuronech". Sdělení o biochemickém a biofyzikálním výzkumu. 430 (1): 38–42. doi:10.1016 / j.bbrc.2012.11.048. PMID 23200837.
- ^ Burns, JR; Baldwin, MR (8. srpna 2014). „Neurotoxin tetanu využívá ke tvorbě kanálů dvě následné membránové interakce.“. The Journal of Biological Chemistry. 289 (32): 22450–8. doi:10.1074 / jbc.m114.559302. PMC 4139251. PMID 24973217.
- ^ Pirazzini, M; Bordin, F; Rossetto, O; Shone, CC; Binz, T; Montecucco, C (16. ledna 2013). „Systém thioredoxin reduktáza-thioredoxin se podílí na vstupu neurotoxinů tetanu a botulotoxinu do cytosolu nervových zakončení“. FEBS Dopisy. 587 (2): 150–5. doi:10.1016 / j.febslet.2012.11.007. PMID 23178719.
- ^ Pellegrini, LL; O'Connor, V; Lottspeich, F; Betz, H (2. října 1995). „Klostridiální neurotoxiny narušují stabilitu nízkoenergetického komplexu SNARE zprostředkujícího NSF aktivaci fúze synaptických vezikul“. Časopis EMBO. 14 (19): 4705–13. doi:10.1002 / j.1460-2075.1995.tb00152.x. PMC 394567. PMID 7588600.
- ^ Kumar, Vinay; Abbas, Abul K .; Fausto, Nelson; Aster, Jon (2009-05-28). Robbins and Cotran Pathologic Basis of Disease, Professional Edition: Expert Consult - Online (Robbins Pathology) (Kindle Locations 19359-19360). Elsevier zdraví. Kindle vydání.
- ^ Kanda K, Takano K (únor 1983). "Vliv tetanového toxinu na excitační a inhibiční postsynaptické potenciály v kočičím motoneuronu". J. Physiol. 335: 319–333. doi:10.1113 / jphysiol.1983.sp014536. PMC 1197355. PMID 6308220.
- ^ Schiavo G, Benfenati F, Poulain B, Rossetto O, Polverino de Laureto P, DasGupta BR, Montecucco C (29. října 1992). „Neurotoxiny tetanu a botulinum-B blokují uvolňování neurotransmiterů proteolytickým štěpením synaptobrevinu“. Příroda. 359 (6398): 832–5. Bibcode:1992 Natur.359..832S. doi:10.1038 / 359832a0. PMID 1331807.
- ^ Todar, Ken (2005). „Patogenní Clostridia, včetně botulismu a tetanu“. Todarova online učebnice bakteriologie. Citováno 24. června 2018.
- ^ Loscalzo, Joseph; Fauci, Anthony S .; Braunwald, Eugene; Dennis L. Kasper; Hauser, Stephen L; Longo, Dan L. (2008). Harrisonovy principy vnitřního lékařství. McGraw-Hill Medical. ISBN 978-0-07-146633-2.
- ^ „Tetanus v urgentní medicíně“. Emedicína. Citováno 2011-09-01.
externí odkazy
- tetanospasmin v americké národní lékařské knihovně Lékařské předměty (Pletivo)
- Pellizzari R, Rossetto O, Schiavo G, Montecucco C (1999). „Tetanus a botulinum neurotoxiny: mechanismus účinku a terapeutické použití“. Philos. Trans. R. Soc. Lond. B Biol. Sci. 354 (1381): 259–68. doi:10.1098 / rstb.1999.0377. PMC 1692495. PMID 10212474.CS1 maint: více jmen: seznam autorů (odkaz)
- Neurotoxin v toxikonu
- Cesta neurotoxinů tetanu a botulotoxinu v neuronech
- Jak se tetanové a botulotoxiny váží na neuronální membrány?
