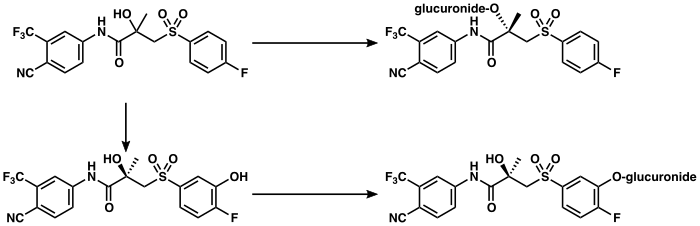
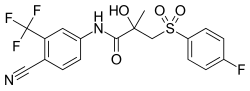
Farmakologie bikalutamidu - Pharmacology of bicalutamide
 | |
| Klinické údaje | |
|---|---|
| Trasy z správa | Pusou[1] |
| Třída drog | Nesteroidní antiandrogen |
| Farmakokinetické data | |
| Biologická dostupnost | Dobře se vstřebává; absolutní biologická dostupnost neznámý[2] |
| Vazba na bílkoviny | Racemate: 96.1%[1] (R) -Izomer: 99.6%[1] (Hlavně do albumin )[1] |
| Metabolismus | Játra (rozsáhle):[3][8] • Hydroxylace (CYP3A4 ) • Glukuronidace (UGT1A9 ) |
| Metabolity | • bikalutamid glukuronid • Hydroxybicalutamid • Hydroxybicalutamid gluc. (Vše neaktivní)[3][1][4][5] |
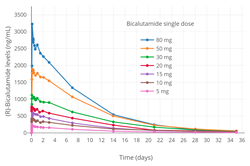
| Odstranění poločas rozpadu | Jedna dávka: 6 dní[6] Kontinuální: 7–10 dní[7] |
| Vylučování | Výkaly: 43%[3] Moč: 34%[3] |
The farmakologie z bikalutamid, a nesteroidní antiandrogen (NSAA), byl dobře charakterizován. Ve smyslu farmakodynamika, bikalutamid působí jako a selektivní antagonista z androgenní receptor (AR) biologický cíl z androgeny jako testosteron a dihydrotestosteron (DHT). Nemá kapacitu aktivovat the AR. Nesnižuje hladinu androgenu a nemá žádné další důležité hormonální aktivita. Lék má progonadotropní účinky kvůli AR antagonistická aktivita a může zvyšovat androgen, estrogen, a neurosteroid produkce a úrovně. To má za následek řadu rozdílů v monoterapii bikalutamidem ve srovnání s chirurgický a lékařská kastrace, například nepřímé estrogenní účinky a související výhody, jako je zachování sexuální funkce a nevýhody jako gynekomastie. Bicalutamid může paradoxně stimulují rakovinu prostaty v pozdním stadiu z důvodu akumulace mutace v rakovině. Při použití jako monoterapie může bikalutamid vyvolat vývoj prsou u mužů kvůli jeho estrogenním účinkům. Na rozdíl od jiných druhů antiandrogenů může mít méně nepříznivý efekt na testy a plodnost.
Ve smyslu farmakokinetika, bikalutamid je dobře vstřebává když se vezme pusou. Při vyšších dávkách však absorpce klesá. Dosahuje to maximální konstantní úrovně po 4 až 12 týdnech léčby. Bicalutamid vykazuje rozsáhlé výsledky vazba na plazmatické bílkoviny, hlavně do albumin. Překračuje to hematoencefalická bariéra a vykonává účinky v centrální nervový systém. Bicalutamid je metabolizován v játra podle hydroxylace a glukuronidace. The metabolity o bikalutamidu není známo aktivní. Léčba je velmi dlouhá biologický poločas 6 dnů s jednou dávkou a 7 až 10 dnů s opakovaným podáváním. Bicalutamid a jeho metabolity jsou vyloučeno v moč, výkaly, a žluč, hlavně ve formě konjugáty. Farmakokinetika bikalutamidu není ovlivněna jídlo, stáří, tělesná hmotnost, poškození ledvin nebo mírné až střední poškození jater, ale etnický původ může v některých případech ovlivnit jeho farmakokinetiku.
Farmakodynamika
| Antiandrogen | AR | PR-B | |||
|---|---|---|---|---|---|
| K.i (nM) | IC50 (nM) | Jámax (%) | IC50 (nM) | Jámax (%) | |
| Bikalutamid | 117 | 157 | 78 | 1,819 | 88 |
| Cyproteron-acetát | 14 | 26 | 48 | >10,000 | 12 |
| Hydroxyflutamid | 27 | 15 | 83 | 2,013 | 90 |
| Mifepriston | 22 | 5 | 75 | 0.18 | 96 |
| Poznámky: IC50 hodnoty jsou pro funkční antagonismus. Jámax je maximální inhibice. Zdroj: [9] | |||||
| Sloučenina | AR | PR | ER | GR | PAN |
|---|---|---|---|---|---|
| Bikalutamid | 14–54 | 3,500–7,200 | >1,000,000 | 44,000–320,000 | ≥360,000 |
| Dihydrotestosteron | 0.5–3.1 | 280–440 | 38,000–340,000 | 2,700–20,000 | 2,100–2,300 |
| Poznámky: Hodnoty jsou K.i nebo IC50 (nM) pro inhibici vazby (afinitu). Zdroje: [10][11][12][13] | |||||
Antiandrogenní aktivita

| Sloučenina | RBA[b] |
|---|---|
| Metribolon | 100 |
| Dihydrotestosteron | 85 |
| Cyproteron-acetát | 7.8 |
| Bikalutamid | 1.4 |
| Nilutamid | 0.9 |
| Hydroxyflutamid | 0.57 |
| Flutamid | <0.0057 |
Poznámky:
| |
| Antiandrogen | Relativní potence |
|---|---|
| Bikalutamid | 4.3 |
| Hydroxyflutamid | 3.5 |
| Flutamid | 3.3 |
| Cyproteron-acetát | 1.0 |
| Zanoteron | 0.4 |
| Popis: Relativní potence orálně antiandrogeny při antagonizaci 0,8 až 1,0 mg / kg s.c. testosteron propionát -indukovaný ventrální prostata přírůstek hmotnosti v kastrovaný nezralý samci krys. Zdroje: Viz šablona. | |
Bicalutamid působí jako vysoce účinná látka selektivní konkurenční tichý protivník z androgenní receptor (AR) (IC50 = 159–243 nM), hlavní biologický cíl androgenních pohlavních hormonů testosteron a dihydrotestosteron (DHT).[16][17][18][19] Nemá kapacitu aktivovat AR za normálních okolností fyziologický okolnosti.[20] Kromě konkurenčního antagonismu vůči ARBylo zjištěno, že bikalutamid urychluje degradace z AR, a tato akce může být také zapojena do její činnosti jako antiandrogen.[21] Aktivita bikalutamidu spočívá v (R)-izomer, který se váže na AR s afinita to je asi 30krát vyšší než u (S) -izomer.[22] Úrovně (R) -izomer také pozoruhodně stokrát vyšší než u (S) -izomer v ustáleném stavu.[23][24]
Ve vztahu k jeho selektivitě pro ARna rozdíl od steroidní antiandrogeny (DSP), jako je cyproteronacetát (CPA) a megestrol-acetát, bikalutamid neinteraguje důležitě s jinými receptory steroidních hormonů (včetně ER, PR, GR nebo PAN ) a v souladu s tím nemá žádný klinicky relevantní další, mimo cíl hormonální aktivita (estrogenní nebo antiestrogenní, progestogenní nebo antiprogestogenní, glukokortikoid nebo antiglukokortikoid nebo mineralokortikoid nebo antimineralokortikoid ).[25][26][22][27] Bylo však hlášeno, že bikalutamid má slabou afinitu k receptor progesteronu (PR) (~ 100- až 500krát nižší než u AR),[11][12][13][9] kde působí jako antagonista (pouze s ~ 12krát nižší funkční inhibicí ve srovnání s AR v jedné studii).[9][28] Proto může bikalutamid nějaké mít antiprogestogenní jeho klinická významnost není známa.[9][28] Bikalutamid neinhibuje 5α-reduktáza a není známo, že by inhiboval jiné enzymy podílející se na androgenu steroidogeneze (např., CYP17A1 ).[20] Ačkoli se bikalutamid neváže na ER, může sekundárně zvyšovat hladinu estrogenu k blokádě AR při použití jako monoterapie u mužů az tohoto důvodu může léčba nepřímo aktivovat ER do určité míry, a proto nějaké mají nepřímý estrogenní účinky u mužů.[29] Také na rozdíl od DSP, bikalutamid ani neinhibuje, ani nepotlačuje produkci androgenu v těle (tj. nepůsobí jako antigonadotropin nebo inhibitor steroidogeneze ),[2] a místo toho výhradně zprostředkovává své antiandrogenní účinky blokováním androgenu vazba a následující aktivace receptoru na úrovni AR.[25][22]
Kromě klasické jaderné AR, bikalutamid byl také identifikován jako silný antagonista ZIP9, a membránový androgenní receptor (mAR) a transportní protein zinku, s IC50 66,3 nM (vzhledem ke Kd = 17,9 nM pro testosteron).[30] Zdá se, že tento protein se podílí na rakovině prostaty a rakovina prsu.[31] Bikalutamid nedokázal ovlivnit signalizaci testosteronu zprostředkovanou GPRC6A, další mAR, na druhou stranu.[32]
| Antiandrogen | AR | PR | ER | GR | PAN |
|---|---|---|---|---|---|
| Cyproteron-acetát | 8–10 | 60 | <0.1 | 5 | 1 |
| Chlormadinonacetát | 5 | 175 | <0.1 | 38 | 1 |
| Megestrol-acetát | 5 | 152 | <0.1 | 50 | 3 |
| Spironolakton | 7 | 0.4A | <0.1 | 2A | 182 |
| Trimethyltrienolon | 3.6 | <1 | <1 | <1 | <1 |
| Inocoterone | 0.8 | <0.1 | <0.1 | <0.1 | <0.1 |
| Inocoteronacetát | <0.1 | <0.1 | <0.1 | <0.1 | <0.1 |
| Flutamid | <0.1 | <0.1 | <0.1 | <0.1 | <0.1 |
| Hydroxyflutamid | 0.5–0.8 | <0.1 | <0.1 | <0.1 | <0.1 |
| Nilutamid | 0.5–0.8 | <0.1 | <0.1 | <0.1 | <0.1 |
| Bikalutamid | 1.8 | <0.1 | <0.1 | <0.1 | <0.1 |
| Poznámky: (1): Odkaz ligandy (100%) byly testosteron pro AR, progesteron pro PR, estradiol pro ER, dexamethason pro GR, a aldosteron pro PAN. (2): Tkáně byla potkaní prostata (AR), králičí děloha (PR), myší děloha (ER), potkaní brzlík (GR) a krysí ledvina (MR). (3): Inkubační časy (0 ° C) byly 24 hodin (AR, A), 2 hodiny (PR, ER), 4 hodiny (GR) a 1 hodinu (MR). (4): Metody stanovení byly odlišné pro bikalutamid pro receptory kromě AR. Zdroje: Viz šablona. | |||||
| Druh | IC50 (nM) | RBA (poměr) | ||||
|---|---|---|---|---|---|---|
| Bikalutamid | 2-hydroxyflutamid | Nilutamid | Bica / 2-OH-chřipka | Bica / nilu | Čj | |
| Krysa | 190 | 700 | ND | 4.0 | ND | [33] |
| Krysa | ~400 | ~900 | ~900 | 2.3 | 2.3 | [34] |
| Krysa | ND | ND | ND | 3.3 | ND | [35] |
| KrysaA | 3595 | 4565 | 18620 | 1.3 | 5.2 | [36] |
| Člověk | ~300 | ~700 | ~500 | 2.5 | 1.6 | [15] |
| Člověk | ~100 | ~300 | ND | ~3.0 | ND | [37] |
| ČlověkA | 2490 | 2345 | 5300 | 1.0 | 2.1 | [36] |
| Poznámky pod čarou: A = Kontroverzní data. Zdroje: Viz šablona. | ||||||
Hladiny drog, hladiny androgenů a účinnost
Afinita bikalutamidu k AR je přibližně 30 až 100krát nižší než u DHT (IC50 ≈ 3,8 nM), hlavní endogenní ligand receptoru v prostatě.[38][19][1][39] Avšak dostatečně vysoké relativní koncentrace bikalutamidu (1 000 až 10 000násobný přebytek) jsou schopny aktivaci zcela zabránit AR androgeny jako DHT a testosteron a další upregulace z transkripce reagující na androgen geny a související efekty.[40][26][41][42] V ustáleném stavu, relativně k normálnímu rozmezí testosteronu u dospělých mužů (300–1 000 ng / dL),[43] cirkulující koncentrace bikalutamidu v dávce 50 mg / den jsou zhruba 600 až 2 500krát vyšší a při 150 mg / den přibližně 1 500 až 8 000krát vyšší než cirkulující hladiny testosteronu, zatímco koncentrace bikalutamidu v porovnání s průměrnými hladinami testosteronu přítomnými u mužů, kteří byli chirurgicky kastrovaný (15 ng / dL),[44] jsou přibližně 42 000krát vyšší než hladiny testosteronu při 50 mg / den.[45][46][47][48][49]

Zatímco testosteron je hlavním cirkulujícím androgenem, DHT je hlavním androgenem v prostatě.[51] DHT hladiny v oběhu jsou relativně nízké a pouze přibližně 10% hladin cirkulujících testosteronu.[51] Naopak místní koncentrace DHT v prostatě jsou 8 až 10krát vyšší než cirkulující hladiny DHT.[52][25] To je způsobeno vysokou expresí 5α-reduktázy v prostatické žláze, která velmi účinně katalyzuje tvorbu DHT z testosteronu[52] tak, že se přemění na více než 90% intraprostatického testosteronu DHT.[53][54] Ve vztahu k testosteronu, DHT je 2,5- až 10krát účinnější než AR agonista v biologické testy ve srovnání s tím je mnohem silnější androgen.[55] Jako takový, AR signalizace je v prostatě mimořádně vysoká a účinnost monoterapie bikalutamidem v léčbě rakoviny prostaty je zhruba ekvivalentní účinnosti analogy hormonu uvolňujícího gonadotropin (Analogy GnRH),[56][42][57][58] prokazuje schopnost bikalutamidu silně antagonizovat AR. Na druhou stranu, GnRH analogická monoterapie dosahuje pouze 50 až 60% snížení hladin DHT v prostatě,[19][59] a kombinovaná androgenní blokáda (CAB), kombinace chirurgické kastrace nebo a GnRH analog a bikalutamid, je při léčbě rakoviny prostaty významně účinnější než kterýkoli jiný způsob.[16][60] Bylo zjištěno, že monoterapie bikalutamidem snižuje cirkulující hladiny prostatický specifický antigen (PSA), marker růstu rakoviny prostaty, o 57% při 10 mg / den, 73% při 30 mg / den, 90% při 50 mg / den, 97% při 100 mg / den a 97% při 150 mg / den, zatímco u 50 mg / den bikalutamidu jako součásti CAB je pozorováno 97% snížení PSA.[19] Rovněž bylo hlášeno, že monoterapie bikalutamidem snižuje střední cirkulující hladiny PSA po 3 měsících o 86,7% při 100 mg / den, 91,1% při 150 mg / den a 93,8% při 200 mg / den.[50] Nad dávkou 200 mg / den monoterapie bikalutamidem, až do 600 mg / den, pokles hladiny PSA dosáhne plató.[28]
Navzdory vysokým hladinám léčby, kterých je dosaženo, vzhledem k jejich relativně nízké afinitě k AR, bylo navrženo, aby 5 až 10% DHT může zůstat odblokovaný v prostatě s KABINA pomocí standardních dávek první generace NSAA.[61][62][63] V souladu s druhou generací NSAA jako enzalutamid a apalutamid, které mají 5 až 10krát vyšší afinitu k AR než bikalutamid byly shledány účinnějšími než bikalutamid při léčbě rakoviny prostaty.[62] Ve studiích TERRAIN a STRIVE, které srovnávaly bikalutamid a enzalutamid jako složku KABINA a zjistili, že enzalutamid prodloužil životnost 3 až 4krát tolik času jako bikalutamid, byla dávka použitého enzalutamidu (160 mg) více než 3krát vyšší než dávka použitého bikalutamidu (50 mg).[64][65] Ve výsledku bylo navrženo, že dávka 50 mg / den bikalutamidu použitá v této studii a v KABINA obecně může být neoptimální.[28][65] To je v souladu s klinickými nálezy PSA klesá s KABINA pomocí platanu bikalutamidu v dávce bikalutamidu 150 až 200 mg / den.[28]
U žen jsou celkové hladiny testosteronu 20krát a hladiny volného testosteronu 40krát nižší ve srovnání s muži.[66] Vzhledem k tomu, že monoterapie bikalutamidem může u mužů zvýšit hladinu testosteronu až dvojnásobně,[58][67] léčba nezvyšuje hladinu testosteronu u žen.[68][69][70] Z těchto důvodů lze u žen s významnou antiandrogenní účinností použít mnohem nižší dávky bikalutamidu (např. 25 mg / den ve studiích hirsutismu).[71][72][73][74]
Vlivy na hladiny hormonů

| Dávkování | Před | PoA | Rozdíl | Změna |
|---|---|---|---|---|
| 10 mg / den | 400 ng / dl | 490–520 ng / dL | + 90–120 ng / dL | +21–29% |
| 30 mg / den | 320 ng / dL | 490–550 ng / dl | + 170–230 ng / dL | +55–73% |
| 50 mg / den | 370 ng / dl | 550–610 ng / dl | + 180–240 ng / dL | +46–62% |
| 100 mg / den | 320 ng / dL | 460–490 ng / dl | + 140–170 ng / dL | +45–55% |
| 150 mg / den | 290 ng / dl | 460–490 ng / dl | + 170–200 ng / dl | +60–70% |
| 200 mg / den | 320 ng / dL | 520–550 ng / dL | + 200–230 ng / dL | +64–73% |
| Poznámky pod čarou: A = Po 29 až 85 dnech léčby. Zdroje: [76] | ||||
U mužů blokáda AR bikalutamidem v hypofýza a hypotalamus brání negativní zpětná vazba androgenů na hypotalamus – hypofýza – gonadální (HPG) osa, což má za následek zvýšení luteinizační hormon (LH) sekrece a hladiny.[77] Folikulostimulační hormon Hladiny (FSH) naopak zůstávají v podstatě nezměněny.[78] Nárůst v LH hladiny vede ke zvýšení hladiny androgenu a estrogenu.[79] Při dávce 150 mg / den bylo zjištěno, že bikalutamid zvyšuje hladinu testosteronu přibližně 1,5krát až 2krát (59–97% nárůst) a hladiny estradiolu přibližně 1,5–2,5krát (65–146% nárůst) .[58][67][74] Úrovně DHT jsou také v menší míře zvýšeny (o 24–30%) a koncentrace globulin vázající pohlavní hormony (SHBG) a prolaktin se také zvyšuje (o 8–42%, respektive 40–65%) sekundárně ke zvýšení hladiny estradiolu.[74][80][81] Koncentrace estradiolu produkované u mužů monoterapií bikalutamidem se přibližují nízkým normálním hladinám estradiolu premenopauzální žena,[67] zatímco hladiny testosteronu obecně zůstávají na vyšší hranici normálního mužského rozmezí a zřídka ji překračují.[82][25] Bylo zjištěno, že dávky bikalutamidu 10 mg, 30 mg a 50 mg denně mají „mírný“ účinek na hladiny pohlavních hormonů u mužů s rakovinou prostaty (zejména poskytují indikaci, že lék má klinicky relevantní antiandrogenní účinky u mužů při dávka až 10 mg / den).[83][76] Zvýšené hladiny gonadotropinů a gonadálních steroidů spojené s NSAA monoterapie je jedinečný endokrinní stav, který lze popsat jako „hypergonadotropní hypergonadismus ".[84][85]
Bikalutamid zvyšuje hladinu androgenu a estrogenu pouze u mužů, u žen to tak není.[68][69][70] Je to proto, že hladiny androgenu jsou u žen poměrně daleko nižší a naopak nevykazují žádné nebo téměř žádné bazální potlačení HPG osa.[70] Minimální nebo žádné změny důležitosti hladin celkového testosteronu, volného testosteronu, dihydrotestosteronu, estradiolu, androstendion (A4), dehydroepiandrosteron (DHEA), dehydroepiandrosteron sulfát (DHEA-S), 3α-androstandiol glukuronid (3α-ADG), progesteron, 17a-hydroxyprogesteron (17α-OHP), LH, FSH, prolaktin nebo SHBG byly pozorovány u žen s hirsutismus s nebo bez syndrom polycystických vaječníků kteří byli léčeni 25 nebo 50 mg / den bikalutamidu po dobu 6 až 12 měsíců.[86][87] V jedné studii u žen s polycystickým ovariálním syndromem však 25 mg / den bikalutamid významně snížil hladiny celkového a volného testosteronu a významně zvýšil hladinu SHBG.[88] Kromě minimálních změn hladin hormonů u žen, i když monoterapie bikalutamidem zvyšuje hladiny gonadotropinu a pohlavních hormonů u mužů, nedojde k tomu, pokud je bikalutamid kombinován s antigonadotropinem, jako je GnRH analog, estrogen nebo progestogen, protože tyto léky udržují negativní zpětnou vazbu na ose HPG.[20][89][90][91]
Důvod, proč jsou hladiny testosteronu zvýšené, ale téměř vždy zůstávají v normálním rozmezí u mužů při monoterapii bikalutamidem, je považován za způsobený současně zvýšenými hladinami estradiolu, protože estradiol je silně antigonadotropní a omezuje sekreci LH.[77] Ve skutečnosti je estradiol mnohem silnějším inhibitorem sekrece gonadotropinu než testosteron, a přestože cirkulující koncentrace estradiolu jsou mnohem nižší než koncentrace testosteronu u mužů, říká se, že estradiol je přesto pravděpodobně hlavním regulátorem zpětné vazby sekrece gonadotropinu v tomto sex.[92] V souladu, klomifen, a selektivní modulátor estrogenových receptorů Bylo zjištěno, že s antiestrogenní aktivitou zvyšuje hladinu testosteronu až na 250% počátečních hodnot u mužů s hypogonadismus,[93] a studie léčby klomifenem u normálních mužů pozorovala zvýšení v FSH a LH hladiny 70–360%, respektive 200–700%, se zvýšením hladin testosteronu, které bylo podobné zvýšením pozorovaným u gonadotropinů.[94][95] Kromě systémového nebo cirkulujícího estradiolu může k potlačení sekrece gonadotropinu přispět i místní aromatizace testosteronu na estradiol v hypotalamu a hypofýze.[92]
Bikalutamid více než blokuje účinky zvýšené hladiny testosteronu, kterou vyvolává u mužů, o čemž svědčí skutečnost, že monoterapie tímto lékem je přibližně stejně účinná jako GnRH analogická terapie při léčbě rakoviny prostaty.[56] Naproti tomu účinky zvýšené hladiny estrogenu zůstávají bikalutamidem nevyvráceny, a to je do značné míry zodpovědné za feminizující vedlejší účinky (např. Gynekomastie) drogy u mužů.[96]
- Změny hladin hormonů s bikalutamid monoterapie
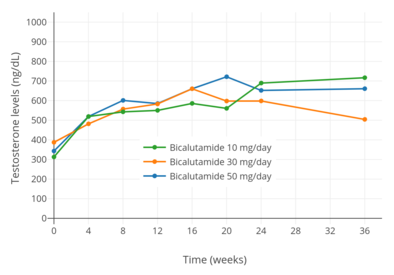
Hladiny testosteronu v monoterapii bikalutamidem 10, 30 a 50 mg / den u mužů s rakovinou prostaty.[97]

Hladiny testosteronu s monoterapií bikalutamidem 10 až 200 mg / den u mužů s rakovinou prostaty.[76]
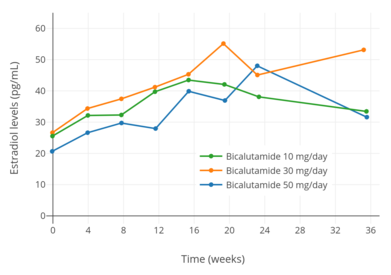
Hladiny estradiolu v monoterapii bikalutamidem 10, 30 a 50 mg / den u mužů s rakovinou prostaty.[97]

Hladiny estradiolu v monoterapii bikalutamidem 10 až 200 mg / den u mužů s rakovinou prostaty.[76]
Rozdíly od kastrace
Bylo navrženo, že zvýšení hladiny estrogenu způsobené NSAA jako bikalutamid kompenzuje blokování androgenů v mozku, což může vysvětlovat rozdíly v profilech vedlejších účinků těchto léků ve srovnání s GnRH analogy / kastrace, kombinovaná androgenní blokáda, a CPA (které naopak snižují hladinu androgenu i estrogenu).[98][99][100] V případě sexuálního zájmu a funkce je tato představa podporována řadou nálezů, včetně studií na zvířatech, které to dokazují nedostatek estrogenu má za následek snížené sexuální chování, léčba tamoxifenem vedoucí k významnému snížení libida u 30% mužů užívajících jej na rakovinu prsu u mužů a podávání estrogenu obnovující libido a frekvenci pohlavní styk u mužů s vrozený nedostatek estrogenu, mezi ostatními.[98][99][100][101]
Několik metabolitů testosteronu a DHT, včetně estradiolu, 3α-androstandiol, a 3β-androstandiol, jsou estrogeny (hlavně silné ERβ agonisté v případě posledních dvou) a 3α-androstandiol je navíc silný GABAA neurosteroid potencující receptory.[102][103] Vzhledem k tomu, že bikalutamid nesnižuje hladinu testosteronu, neočekává se, že by se snížily ani hladiny těchto metabolitů, na rozdíl od terapií, jako je GnRH analogy. (Opravdu, testosteron, DHTa hladiny estradiolu jsou ve skutečnosti zvýšeny léčbou bikalutamidem, a z tohoto důvodu mohou být hladiny 3α- a 3β-androstandiolu do určité míry zvýšeny podobně.) Bylo zjištěno, že tyto metabolity testosteronu mají AR-nezávislé pozitivní účinky na sexuální motivaci,[102][103][104][105] a může vysvětlovat zachování sexuálního zájmu a funkce bikalutamidem a dalšími NSAA.[98] Také mají antidepresivum, anxiolytikum, a kognitivní funkce efekty,[105][106][107][108] a může odpovídat za nižší výskyt deprese u bikalutamidu a dalších NSAA ve srovnání s jinými antiandrogenními terapiemi.
Studie zjistila, že kombinace bikalutamidu a dutasterid, a Inhibitor 5α-reduktázy a inhibitor biosyntézy neurosteroidů, produkoval méně sexuálních vedlejších účinků než GnRH analogická terapie, konkrétně naznačující úlohu estrogenů při zachování sexuálního zájmu a funkce monoterapií bikalutamidem.[109]
Uvádí se, že bikalutamid překvapivě nemá antianabolický vliv na testosteron propionát -indukované zvýšení v levator ani sval hmotnost v dávkách, které inhibují a dokonce zcela zabraňují růstu testosteronu propionátem indukovaného růstu prostaty a semenné váčky u potkanů.[110][111] Jako takové bylo řečeno, že na základě předklinický výzkum, bikalutamid nemá výrazné antianabolické účinky.[110] Vyšší dávky bikalutamidu jsou však schopné značně inhibovat růst svalu levator ani u potkanů.[112] V každém případě bylo zjištěno, že analogicky k nálezům na zvířatech monoterapie bikalutamidem významně zachovává svalové hmoty a svalová síla u starších mužů s rakovinou prostaty ve srovnání s agonisty GnRH.[81] Je pozoruhodné, že na rozdíl od kastrace bicalutamid zachovává a zvyšuje hladinu estrogenu a předpokládá se, že estrogeny mají pozitivní účinky na kosterní sval, včetně svalové hmoty.[113]
Paradoxní stimulace pozdního stadia rakoviny prostaty
Ačkoli čistý nebo tichý protivník AR za normálních okolností bylo zjištěno, že bikalutamid, stejně jako další dřívější antiandrogeny, jako je flutamid a nilutamid, mají slabé částečný agonista vlastnosti v nastavení AR nadměrná exprese a agonistická aktivita v případě určitých mutací v doména vázající ligand (LBD) AR.[114][115] Jelikož se obě tyto okolnosti mohou nakonec vyskytnout u rakoviny prostaty, obvykle se vyvíjí rezistence na bikalutamid a lék má potenciál paradoxně stimulovat růst nádoru, pokud k tomu dojde.[114][116] Toto je mechanismus jevu syndrom z vysazení antiandrogenu, kde vysazení antiandrogenu paradoxně zpomaluje rychlost růstu nádoru.[116] Ukázalo se, že novější lék enzalutamid nemá agonistické vlastnosti v souvislosti s nadměrnou expresí AR, ačkoli určité mutace v AR stále ji může převést z antagonisty na agonistu.[114]
Indukce vývoje prsu
U transgender žen vývoj prsou je požadovaným účinkem léčby antiandrogenem a / nebo estrogenem.[117][118] Bikalutamid vyvolává u jedinců vývoj prsu (nebo gynekomastie) přiřazený muž při narození dvěma mechanismy: 1) blokováním androgenní signalizace v prsní tkáni; a 2) zvýšení hladiny estrogenu.[119][120] Estrogen je za normálních okolností zodpovědný za indukci vývoje prsu, zatímco androgeny účinně potlačují růst prsu vyvolaný estrogenem.[121][122] Bylo zjištěno, že velmi nízké hladiny estrogenu mohou vyvolat vývoj prsu v přítomnosti nízké nebo žádné androgenní signalizace.[121][123][124] V souladu s tím nejen bikalutamid indukuje vysokou míru gynekomastie, pokud je podáván jako monoterapie mužům s rakovinou prostaty (47–85%; 66% v jedné velmi rozsáhlé studii),[120] podobně jako vysoká dávka estrogenu terapie s diethylstilbestrol (41–77%), NSAA Bylo zjištěno, že vedou k vyššímu výskytu gynekomastie v kombinaci s a GnRH analogický (13–25%) ve vztahu k GnRH samotná analogická terapie nebo kastrace (1–16%) (i přes přítomnost pouze kastrátových hladin estrogenu v obou případech).[125][29][126][50] Míra gynekomastie s KABINA je také vyšší než u CPA monoterapie (7%).[125]
Studie mužů léčených NSAA Monoterapie (flutamid nebo bikalutamid) pro rakovinu prostaty to zjistila NSAA indukované plné duktální vývoj a umírněný lobuloalveolární vývoj prsou od a histologické stanovisko.[127][128][129] Studie také zjistila, že na rozdíl od léčby transgender žen estrogeny a CPA (který je progestogenní kromě antiandrogenního, na rozdíl od NSAA) vedlo k plnému lobuloalevolarnímu vývoji i těhotenství hyperplazie prsu ve dvou z předmětů.[127][129] Kromě toho bylo pozorováno, že lobuloalveolární zrání se po ukončení léčby obrátilo CPA po chirurgická změna pohlaví (tj. chirurgická kastrace) u těchto jedinců.[127] Byl vyvozen závěr, že pro indukci úplného histologického vývoje prsu podobného ženám (tj. Který zahrnuje úplné lobuloalveolární zrání) je kromě léčby antiandrogenem / estrogenem nutný progestogen a pro udržení takového zrání je nutná další léčba progestogenem.[127][128] Je však třeba poznamenat, že ačkoli tato zjištění mohou mít důležité důsledky v kontextu laktace a kojení tvoří epiteliální tkáň přibližně pouze 10% objemu prsou (přičemž většinu prsou (80–90%) představuje stromální nebo tukové tkáň),[130][131][132][133] a není jisté, do jaké míry, pokud vůbec, došlo k rozvoji lobuloalveolárních struktur (forma epiteliální tkáň) přispívá k velikosti a / nebo tvaru prsou.[117]
| Studie | N | Dávkování | Gynekomastie | Něha prsou | Čj |
|---|---|---|---|---|---|
| Tyrrell a kol. (1998)A | 386 | 10 mg / den | 9% | 11% | [76] |
| 30 mg / den | 26% | 42% | |||
| 50 mg / den | 36% | 48% | |||
| 100 mg / den | 79% | 86% | |||
| 150 mg / den | 78% | 89% | |||
| 200 mg / den | 79% | 79% | |||
| Kennealey & Furr (1991)b | 210 | 10 mg / den | 29% | 38% | [97] |
| 30 mg / den | 60% | 64% | |||
| 50 mg / den | 52% | 60% | |||
| Zanardi a kol. (2006)C | 66 | 0 mg / týden (kontroly) | 0% | 0% | [134][135][136] |
| 50 mg / týden (~ 7 mg / den) | 44% | 32% | |||
| 100 mg / týden (~ 14 mg / den) | 50% | 64% | |||
| Poznámky pod čarou: A = Hladiny testosteronu se zvýšily na ~ 460–610 ng / dl a hladiny estradiolu na ~ 32–51 pg / ml. b = Hladiny testosteronu se zvýšily na ~ 505–715 ng / dL a hladiny estradiolu na ~ 32–53 pg / ml. C = Hladiny testosteronu se zvýšily na ~ 540–600 ng / dl a hladiny estradiolu na ~ 29–34 pg / ml. | |||||
Účinky na spermatogenezi a plodnost
Spermatogeneze a mužská plodnost jsou závislí na FSH, LHa vysoké hladiny testosteronu ve varlatech.[52][137] LH Nezdá se, že by se účastnil spermatogeneze mimo svoji roli při indukci produkce testosteronu Leydigovy buňky v semenonosné tubuly (které tvoří přibližně 80%[138] převážné části varlat),[139] vzhledem k tomu, že tomu tak není FSH, což je důležitě zapojeno.[140][141] V souladu se skutečností, že varlata jsou zdrojem 95% cirkulujícího testosteronu v těle, jsou místní hladiny testosteronu uvnitř varlat extrémně vysoké, pohybují se od 20 do 200krát vyšších než koncentrace v oběhu.[142][54] Kromě toho jsou pro spermatogenezi vyžadovány vysoké hladiny testosteronu ve varlatech,[137] i když se zdá, že pro spermatogenezi je ve skutečnosti nezbytná jen malá část (5–10%) normálních hladin.[54][143]
Na rozdíl od antigonadotropních antiandrogenů jako CPA a GnRH analogů, bylo hlášeno, že monoterapie bikalutamidem (v dávce 50 mg / den) má velmi malý nebo žádný účinek na ultrastruktura varlat a na spermatogenezi u mužů i po dlouhodobé léčbě (> 4 roky).[144][145] To lze vysvětlit extrémně vysokými místními hladinami testosteronu ve varlatech, protože je pravděpodobné, že systémová léčba bikalutamidem není schopna dosáhnout koncentrací léčiva ve varlatech, které jsou schopné značně blokovat androgenní signalizaci v této části těla. .[144] To platí zejména s ohledem na to, že bikalutamid zvyšuje hladinu testosteronu v oběhu a v širším smyslu produkci testosteronu gonadalů až dvojnásobně u mužů,[79] a že k udržení spermatogeneze se jeví jako nezbytná jen malá část normálních intratestikulárních hladin testosteronu a v širším smyslu působení androgenu.[54][143] Monoterapie bikalutamidem v dávce 50 mg / den nezpůsobuje žádné nebo klinicky nedůležité Hyperplázie Leydigových buněk.[145][146][147]
Na rozdíl od bikalutamidu a jiných čistých antiandrogenů nebo NSAAAntigonadotropní antiandrogeny potlačují sekreci gonadotropinů, což zase snižuje produkci testosteronu varlaty a také jejich udržování FSH, což má za následek atrofie a ztráta jejich funkce.[148] Jako takový, bikalutamid a další NSAA může jedinečně mít potenciál k zachování funkce varlat a spermatogeneze, a tedy mužské plodnosti ve srovnání s alternativními terapiemi.[144][149] V souladu s touto představou studie zjistila, že prodloužená léčba vysokými dávkami bikalutamidu měla minimální účinky na plodnost u samců potkanů.[150] Jiná studie však zjistila, že podávání nízkých dávek bikalutamidu vedlo k atrofii varlat a snížilo hladinu zárodečná buňka počítat ve varlatech samců potkanů o téměř 50%, i když míra úspěšnosti oplodnění a těhotenství následuje páření nebylo hodnoceno.[151] Další studie zjistily, že bikalutamid snížil hmotnosti varlat, změnil histologii varlat a snížil počet spermií u samců potkanů.[152][153][154] Ještě další studie zjistila, že bikalutamid nemá žádný účinek na hmotnosti varlat nebo spermatogenezi u samců potkanů.[155]
Zacházení s muži exogenní testosteron nebo jiné AAS vede k potlačení sekrece gonadotropinů a produkci testosteronu gonadal kvůli jejich antigonadotropním účinkům nebo aktivaci AR v hypofýze, což vede k inhibici nebo zrušení spermatogeneze a plodnosti:[156]
Léčba neplodného muže testosteronem nezlepšuje spermatogenezi, protože exogenně podávaný testosteron a jeho metabolit estrogen potlačuje jak GnRH produkci hypotalamu a luteinizačního hormonu produkci hypofýzy a následně potlačuje produkci testosteronu varlat. Ve varlatech je rovněž zapotřebí vysokých hladin testosteronu, čehož nikdy nelze dosáhnout orálním nebo parenterálním podáním androgenů. Potlačení produkce testosteronu leydigovými buňkami povede k nedostatečné spermatogenezi, jak je patrné u mužů užívajících anabolické androgenní steroidy.[156]
Naproti tomu čistý AR antagonisté by teoreticky vedli k opaku (i když může dojít ke snížení objemu spermatu a sexuální dysfunkci):[157]
Teoreticky jde o zdravou hypotézu, že spermatogenezi lze zvýšit nepřímou stimulací FSH a LH sekrece z hypofýzy. K tomu, aby se to uskutečnilo, však vyžaduje použití antagonisty testosteronu, aby se zrušil negativní zpětnovazebný účinek cirkulujícího testosteronu na uvolňování FSH a LH, čímž se zvyšuje sekrece testosteronu a spermatogeneze. Antagonista testosteronu bude pro muže bohužel nepřijatelný, protože může snížit sekundární sexuální funkce, včetně erekce a ejakulace, které jsou nezbytné pro úspěšné oplodnění.[157]
Přestože se zdá, že bikalutamid nepříznivě neovlivňuje spermatogenezi varlat a během monoterapie bikalutamidem lze ve varlatech produkovat zdravé spermie, AR antagonisté mohou být schopni interferovat s mužskou plodností prostřednictvím interference s androgenní signalizací mimo varlata.[158] K zrání a transportu spermií dochází nejen ve varlatech, ale i mimo varlata v epididymidy a vas deferens a tyto procesy v těchto tkáních jsou závislé na AR signalizace podobně jako testikulární spermatogeneze.[158] Avšak zatímco hladiny androgenu jsou ve varlatech extrémně vysoké, u epididymidů a chámovodu to neplatí.[158] Protože hladiny androgenu jsou v těchto tkáních relativně nízké, alespoň ve srovnání s varlaty může být bikalutamid schopen blokovat AR signalizace v těchto částech těla v rozsahu, který je dostatečný k narušení mužské plodnosti.[158] Opravdu AAS mesterolon byl použit ke zlepšení kvality a plodnosti spermií u mužů, protože, na rozdíl od jiných AAS, vykazuje minimální antigonadotropní účinky při typických klinických dávkách, ale aktivuje AR a tím podporuje zrání spermií v epididymidech.[159] Toto použití mesterolonu je však kontroverzní a jeho účinnost pro takové účely není zcela jistá.[159]
Ačkoli se zdá, že samotný bikalutamid má minimální nepříznivý účinek na spermatogenezi varlat, a tudíž na určité aspekty mužské plodnosti, je možné kombinovat další hormonální látky, s nimiž lze bikalutamid kombinovat, včetně GnRH analogy a zejména estrogeny (jako při léčbě transgenderovými hormony), mohou mít značný nepříznivý účinek na plodnost.[160][161] To je do značné míry důsledkem jejich antigonadotropní aktivity.[161] Antigonadotropní látky, jako jsou vysoké dávky CPA,[162][163] vysoké dávky androgenů (např. estery testosteronu ), a GnRH antagonisté (i když zejména ne GnRH agonisté v případě plodnosti) vyvolávají hypogonadismus a vysokou míru těžké nebo úplné neplodnosti (např. oligospermie nebo kompletní azoospermie ) u mužů.[161] Tyto účinky jsou však plně a často rychle reverzibilní s jejich vysazením, a to i po delší léčbě.[161][163] Naproti tomu, zatímco estrogeny v dostatečně vysokých dávkách jsou podobně schopné vyvolat hypogonadismus a zrušit nebo vážně narušit spermatogenezi,[160] v případě estrogenů to nemusí být nutně reverzibilní a po dlouhodobé expozici to může trvat dlouho.[161][164] Rozdíl je přičítán zdánlivě jedinečnému, přímému cytotoxický a nepříznivý účinek vysokých koncentrací estrogenů na Leydigovy buňky varlat.[161][164]
Další aktivity
Modulace cytochromu P450
Bylo hlášeno, že bikalutamid může mít potenciál inhibovat enzymy CYP3A4 a v menší míře CYP2C9, CYP2C19, a CYP2D6, na základě in vitro výzkum.[1] Nebyla však pozorována žádná relevantní inhibice CYP3A4 in vivo s bikalutamidem v dávce 150 mg (za použití midazolam jako specifický marker aktivity CYP3A4).[1] U zvířat bylo zjištěno, že bikalutamid je induktor jisté cytochrom P450 enzymy.[1] Dávky 150 mg / den nebo méně však u lidí neprokázaly žádný důkaz.[1]
Bikalutamid byl identifikován jako silný CYP27A1 (cholesterol 27-hydroxyláza) inhibitor in vitro.[165] Konverze CYP27A1 cholesterol do 27-hydroxycholesterol, an oxysterol který má více biologických funkcí včetně přímé tkáňově specifické aktivace ER (byl charakterizován jako selektivní modulátor estrogenových receptorů) a jaterní X receptor.[165] Bylo zjištěno, že 27-hydroxycholesterol roste ER-pozitivní růst buněk rakoviny prsu prostřednictvím jejich estrogenního působení, a proto bylo navrženo, že bikalutamid a další inhibitory CYP27A1 mohou být účinné jako adjuvantní terapie na inhibitory aromatázy při léčbě ER-pozitivní rakovina prsu.[165] Kromě CYP27A1 bylo zjištěno, že se bikalutamid váže na a inhibuje CYP46A1 (cholesterol 24-hydroxyláza) in vitro, ale toto ještě musí být posouzeno a potvrzeno in vivo.[166]
Inhibice P-glykoproteinu
Bylo zjištěno, že bikalutamid, stejně jako enzalutamid, působí jako inhibitory z P-glykoprotein výtok a ATPáza aktivita.[167][168][169] Tato akce se může obrátit docetaxel rezistence v buňkách rakoviny prostaty snížením doprava z těchto buněk.[167][168][169]
GABAA pozitivní modulace receptoru
Všechny NSAA Bylo zjištěno, že schválené pro léčbu rakoviny prostaty mají mimo cíl působící jako slabé nekompetitivní inhibitory lidské GABAA receptorové proudy in vitro v různé míře.[170][171] The IC50 hodnoty jsou 44 μM pro flutamid (jako hydroxyflutamid), 21 μM pro nilutamid, 5,2 μM pro bikalutamid a 3,6 μM pro enzalutamid.[170] Kromě toho bylo zjištěno, že flutamid, nilutamid a enzalutamid způsobují křeče a / nebo smrt u myší při dostatečně vysokých dávkách.[170] Bylo zjištěno, že bikalutamid to zejména neudělal, ale bylo to pravděpodobné jednoduše kvůli omezenosti centrální nervový systém penetrace bikalutamidu u tohoto druhu.[170] V každém případě je enzalutamid jediný schválený NSAA u kterého bylo shledáno, že je spojena s významně zvýšeným výskytem záchvatů a dalších souvisejících nežádoucích účinků klinicky, takže význam výše uvedených nálezů s ohledem na bikalutamid a další NSAA je nejasný.[170]
Smíšený
Bikalutamid byl identifikován jako silný antagonista receptor aktivovaný proteázou 2 (PAR-2) a jako a ligand a inhibitor z α2-makroglobulin.[172][173]
Farmakokinetika
| 50 mg / den | 150 mg / den | |
|---|---|---|
| Cmax | 0,77 μg / ml (1,8 μmol / L) | 1,4 μg / ml (3,3 μmol / L) |
| tmax | 31 hodin | 39 hodin |
| Css | 8,85 μg / ml (20,6 μmol / L) | 21,6–28,5 μg / ml (50,2–66,3 μmol / L) |
| tss | 4–12 týdnů | 4–12 týdnů |
| Poznámky: Všechny hodnoty jsou pro (R) -bicalutamid. Zdroje: [1][49] | ||
The farmakokinetika bikalutamidu nejsou ovlivněny jídlo, stáří, tělesná hmotnost, poškození ledvin a mírné až střední poškození jater.[1][47] Bylo však pozorováno, že koncentrace bikalutamidu v ustáleném stavu jsou vyšší u Japonští jednotlivci než v Běloši, což naznačuje etnický původ může v některých případech souviset s rozdíly ve farmakokinetice bikalutamidu.[1]
Vstřebávání
Bikalutamid je značně a dobře absorbován ústní podání,[1] a jeho absorpce není ovlivněna jídlem.[2][174] The absolutní biologická dostupnost bikalutamidu u lidí není znám kvůli jeho velmi nízkému obsahu rozpustnost ve vodě a tudíž nedostatek hodnotitelnosti intravenózní formulace.[1][2] Bylo však zjištěno, že absolutní biologická dostupnost bikalutamidu je u zvířat při nízkých dávkách vysoká (109% u myší při 10 mg / kg; 72% u potkanů při 1 mg / kg; 100% u psů při 0,1 mg / kg), ale klesá s rostoucími dávkami, takže biologická dostupnost bikalutamidu je při vysokých dávkách nízká (10% u potkanů při 250 mg / kg; 31% u psů při 100 mg / kg).[1][175][176] V souladu, vstřebávání z (R) -bicalutamid u lidí je pomalý a rozsáhlý, ale saturovatelný,[48] s hladinami v ustáleném stavu lineárně stoupajícími při dávce až 150 mg / den a nelineárně při vyšších dávkách.[1]
Při vyšších dávkách 100 až 200 mg / den je absorpce bikalutamidu přibližně lineární, s malým, ale rostoucím odklonem od linearity nad 150 mg / den.[177] Ve smyslu geometrický průměr ustálené koncentrace (R) -bicalutamid, odchylky od linearity byly 4%, 13%, 17% a 32% při dávkách 100, 150, 200 a 300 mg / den.[1] V ustáleném stavu je náhorní plošina (R) -bicalutamid s dávkami bikalutamidu nad 300 mg / den, a proto dávky bikalutamidu od 300 do 600 mg / den vedou k podobným cirkulujícím koncentracím (R) -bicalutamid a podobné stupně klinicky účinnosti, snášenlivosti a toxicity.[1][178] Ve vztahu k 150 mg / den bikalutamidu, hladiny (R) -bicalutamid je asi o 15% vyšší při dávce 200 mg / den a asi o 50% vyšší při dávce 300 mg / den.[178] Na rozdíl od (R) -bicalutamid, neaktivní enantiomer (S) -bicalutamid se mnohem rychleji vstřebává (a také se vylučuje z oběhu).[1]
Rovnovážných koncentrací léčiva je dosaženo po 4 až 12 týdnech podávání nezávisle na dávce, s přibližně 10 až 20násobnou progresivní akumulací hladin v oběhu (R) -bicalutamid.[48][179][78][47] Navzdory relativně dlouhé době dosažení ustáleného stavu (což je produkt jeho dlouhého eliminačního poločasu),[47] there is indication that the achieved AR blockade of bicalutamide is equivalent to that of flutamide by the end of the first day of treatment.[179] With single 50 mg and 150 mg doses of bicalutamide, mean peak concentrations (Cmax) of (R)-bicalutamide are 0.77 μg/mL (1.8 μmol/L) (at 31 hours) and 1.4 μg/mL (3.3 μmol/L) (at 39 hours), respectively.[48][45] At steady-state, mean circulating concentrations (Css) of (R)-bicalutamide with 50 mg/day and 150 mg/day bicalutamide are 8.85 μg/mL (20.6 μmol/L) and 21.6 μg/mL (50.2 μmol/L), respectively.[48][45][46][47] In another 150 mg/day bicalutamide study, mean circulating concentrations of (R)-bicalutamide were 19.4 μg/mL (45.1 μmol/L) and 28.5 μg/mL (66.3 μmol/L) on days 28 and 84 (weeks 4 and 12) of treatment, respectively.[49]
Rozdělení
The apparent oral volume of distribution (PROTISS/F) at steady state of (R)-bicalutamide with oral administration of a single 5 to 80 mg dose of (R)-bicalutamide in a novel solid disperze s polymerní matice hydroxypropyl methylcellulose ftalát (HP55S) (also known as (R)-bicalutamide/HP55S) ranges from 22.53 ± 3.71 L to 25.38 ± 2.69 L.[180] Bicalutamide is highly protein-bound (96.1% for racemic bicalutamide, 99.6% for (R)-bicalutamide)), mainly to albumin.[3][1][181] It has negligible affinity for SHBG and no affinity for globulin vázající kortikosteroidy.[20]
The tkáň rozdělení of bicalutamide is not well-characterized.[181] However, it has been reported that distribution studies with bicalutamide have shown that preferential (i.e., tkáňově selektivní ) accumulation in anabolický (např., sval ) tissues does not occur.[182] There are no available data on hepatic bicalutamide concentrations in humans, but a rat study found that oral bicalutamide treatment resulted in 4-fold higher concentrations of the drug in the liver relative to plasma (a common finding with orally administered drugs, due to transfer through the jaterní portál před dosažením oběh ).[1][183] In men receiving 150 mg/day bicalutamide, concentrations of (R)-bicalutamide in semen were 4.9 μg/mL (11 μmol/L), and the amount of the drug that could potentially be delivered to a female partner during pohlavní styk is regarded as low (estimated at 0.3 μg/kg) and below the amount that is required to induce changes in the offspring of laboratory animals.[46]
Na základě výzkum na zvířatech, it was initially thought that bicalutamide was unable to cross the hematoencefalická bariéra into the central nervous system and hence would be a peripherally-selective antiandrogen in humans.[184][26] This conclusion was drawn from the finding that bicalutamide does not increase LH or testosterone levels in multiple tested animal species (including rats and dogs).[184][26][185][186] AR antagonists like flutamide normally do this by blocking AR in the pituitary gland and hypothalamus in the brain and thereby disinhibiting the HPG osa.[77] In humans however, bicalutamide has been found to increase LH and testosterone levels, and to a comparable extent relative to flutamide and nilutamide.[1][77][187][188] This occurs to a significant extent at even a very low dosage of 10 mg/day bicalutamide.[76] As such, it appears that there are species differences in the central penetration of bicalutamide and that the medication does indeed cross the blood–brain barrier and affect central function in humans.[1][188] This is supported by potential side effects of bicalutamide, in spite of increased testosterone levels, like hot flashes and decreased sexual interest in men.[189] Novější NSAA, darolutamid, has been found to negligibly cross the blood–brain barrier in both animals a humans, and in accordance, unlike bicalutamide, does not increase LH or testosterone levels in humans.[190]
Metabolismus
The metabolismus of bicalutamide is jaterní a stereoselektivní.[3][174] Neaktivní (S)-enantiomer is metabolized mainly by glukuronidace and is rapidly vymazáno from circulation, while the active (R)-isomer is slowly hydroxylovaný and then glucuronidated.[174] In accordance, the active (R)-enantiomer has a far longer elimination half-life than the (S)-isomer,[22] and circulating levels of (R)-bicalutamide are 10- to 20-fold[48] and 100-fold higher than those of (S)-bicalutamide after a single dose and at steady-state, respectively.[23][24] (R)-Bicalutamide is almost exclusively metabolizován via hydroxylation into (R)-hydroxybicalutamide by the cytochrom P450 enzym CYP3A4.[1][3][23] Bicalutamide is also glucuronidated by UGT1A9, a UDP-glukuronyltransferáza,[8] into bicalutamide glucuronide, and (R)-hydroxybicalutamide glucuronide is formed from the metabolism of (R)-hydroxybicalutamide by UGT1A9.[1][8][5] Similar to the inactive (S)-enantiomer of bicalutamide, (R)-hydroxybicalutamide is glucuronidated and rapidly cleared from circulation.[191] None of the metabolites of bicalutamide are known to be active.[3][4] Following administration of bicalutamide, only low concentrations of the metabolites are detectable in krevní plazma, while unchanged bicalutamide predominates.[1] (R)-Bicalutamide has a long eliminační poločas of 5.8 days with a single dose,[6][82] and an elimination half-life of 7 to 10 days with repeated administration, which allows for convenient once-daily dosing of bicalutamide.[7]
Odstranění
Bicalutamide is vyloučeno v výkaly (43%) a moč (34%),[3][174] whereas its metabolites are eliminated in approximately equal proportions in urine and žluč.[75][176] It is excreted to a substantial extent in its unmetabolized form, with both bicalutamide and its metabolites excreted mainly as glukuronid konjugáty.[22]
Grafy
- Bicalutamide levels during therapy with bicalutamide
Reference
- ^ A b C d E F G h i j k l m n Ó p q r s t u proti w X y z aa Cockshott ID (2004). „Bicalutamid: klinická farmakokinetika a metabolismus“. Klinická farmakokinetika. 43 (13): 855–878. doi:10.2165/00003088-200443130-00003. PMID 15509184.
Tyto údaje naznačují, že přímá glukuronidace je hlavní metabolickou cestou pro rychle vyčištěné (S) -bicalutamid, zatímco hydroxylace následovaná glukuronidací je hlavní metabolickou cestou pro pomalu vylučované (R) -bicalutamid.
- ^ A b C d Dart RC (2004). Lékařská toxikologie. Lippincott Williams & Wilkins. 497, 521. ISBN 978-0-7817-2845-4. Archivováno z původního dne 11. května 2016.
- ^ A b C d E F G h i Lemke TL, Williams DA (2008). Foyeho principy léčivé chemie. Lippincott Williams & Wilkins. 121, 1288, 1290. ISBN 978-0-7817-6879-5. Archivováno z původního dne 8. září 2017.
- ^ A b Dole EJ, Holdsworth MT (1997). „Nilutamid: antiandrogen pro léčbu rakoviny prostaty“. The Annals of Pharmacotherapy. 31 (1): 65–75. doi:10.1177/106002809703100112. PMID 8997470. S2CID 20347526.
page 67: Currently, information is not available regarding the activity of the major urinary metabolites of bicalutamide, bicalutamide glucuronide, and hydroxybicalutamide glucuronide.
- ^ A b Schellhammer PF (September 2002). "An evaluation of bicalutamide in the treatment of prostate cancer". Znalecký posudek na farmakoterapii. 3 (9): 1313–28. doi:10.1517/14656566.3.9.1313. PMID 12186624. S2CID 32216411.
The clearance of bicalutamide occurs pre- dominantly by hepatic metabolism and glucuronidation, with excretion of the resulting inactive metabolites in the urine and faces.
- ^ A b Skidmore-Roth L (17. dubna 2013). Mosby's 2014 Nursing Drug Reference - Elsevieron VitalSource. Elsevier Health Sciences. 193–194. ISBN 978-0-323-22267-9.
- ^ A b Jordan VC, Furr BJ (5 February 2010). Hormonální terapie u rakoviny prsu a prostaty. Springer Science & Business Media. str. 350–. ISBN 978-1-59259-152-7. Archivováno z původního dne 29. května 2016.
- ^ A b C Grosse L, Campeau AS, Caron S, Morin FA, Meunier K, Trottier J, Caron P, Verreault M, Barbier O (August 2013). "Enantiomer selective glucuronidation of the non-steroidal pure anti-androgen bicalutamide by human liver and kidney: role of the human UDP-glucuronosyltransferase (UGT)1A9 enzyme". Základní a klinická farmakologie a toxikologie. 113 (2): 92–102. doi:10.1111/bcpt.12071. PMC 3815647. PMID 23527766.
- ^ A b C d Hamann LG, Higuchi RI, Zhi L, Edwards JP, Wang XN, Marschke KB, Kong JW, Farmer LJ, Jones TK (1998). "Synthesis and biological activity of a novel series of nonsteroidal, peripherally selective androgen receptor antagonists derived from 1,2-dihydropyridono[5,6-g]quinolines". J. Med. Chem. 41 (4): 623–39. doi:10.1021/jm970699s. PMID 9484511.
- ^ Hanada K, Furuya K, Yamamoto N, Nejishima H, Ichikawa K, Nakamura T, Miyakawa M, Amano S, Sumita Y, Oguro N (November 2003). "Bone anabolic effects of S-40503, a novel nonsteroidal selective androgen receptor modulator (SARM), in rat models of osteoporosis". Biol. Pharm. Býk. 26 (11): 1563–9. doi:10.1248/bpb.26.1563. PMID 14600402.
- ^ A b Nagata N, Miyakawa M, Amano S, Furuya K, Yamamoto N, Nejishima H, Inoguchi K (2011). "Tetrahydroquinolines as a novel series of nonsteroidal selective androgen receptor modulators: structural requirements for better physicochemical and biological properties". Bioorg. Med. Chem. Lett. 21 (21): 6310–3. doi:10.1016/j.bmcl.2011.08.118. PMID 21944856.
- ^ A b Nagata N, Miyakawa M, Amano S, Furuya K, Yamamoto N, Inoguchi K (2011). "Design and synthesis of tricyclic tetrahydroquinolines as a new series of nonsteroidal selective androgen receptor modulators (SARMs)". Bioorg. Med. Chem. Lett. 21 (6): 1744–7. doi:10.1016/j.bmcl.2011.01.073. PMID 21349712.
- ^ A b Kinoyama I, Taniguchi N, Toyoshima A, Nozawa E, Kamikubo T, Imamura M, Matsuhisa A, Samizu K, Kawanimani E, Niimi T, Hamada N, Koutoku H, Furutani T, Kudoh M, Okada M, Ohta M, Tsukamoto S (2006). "(+)-(2R,5S)-4-[4-cyano-3-(trifluoromethyl)phenyl]-2,5-dimethyl-N-[6-(trifluoromethyl)pyridin-3- yl]piperazine-1-carboxamide (YM580) as an orally potent and peripherally selective nonsteroidal androgen receptor antagonist". J. Med. Chem. 49 (2): 716–26. doi:10.1021/jm050293c. PMID 16420057.
- ^ Bohl CE, Gao W, Miller DD, Bell CE, Dalton JT (April 2005). "Strukturální základ pro antagonismus a rezistenci bikalutamidu u rakoviny prostaty". Sborník Národní akademie věd Spojených států amerických. 102 (17): 6201–6. Bibcode:2005PNAS..102.6201B. doi:10.1073 / pnas.0500381102. PMC 1087923. PMID 15833816.
- ^ A b Ayub M, Levell MJ (srpen 1989). „Účinek imidazolových léčiv a antiandrogenů souvisejících s ketokonazolem na vazbu [3H] R 1881 na prostatický androgenní receptor a [3H] 5 alfa-dihydrotestosteron a [3H] kortizol na vazbu na plazmatické proteiny.“ J. Steroid Biochem. 33 (2): 251–5. doi:10.1016/0022-4731(89)90301-4. PMID 2788775.
- ^ A b Singh SM, Gauthier S, Labrie F (únor 2000). "Antagonisté androgenových receptorů (antiandrogeny): vztahy mezi strukturou a aktivitou". Současná léčivá chemie. 7 (2): 211–47. doi:10.2174/0929867003375371. PMID 10637363.
- ^ Balaj K (25. dubna 2016). Řízení metastatického karcinomu prostaty ve vaší urologické onkologické praxi. Springer. str. 24–25. ISBN 978-3-319-31341-2. Archivováno z původního dne 8. září 2017.
- ^ Masiello D, Cheng S, Bubley GJ, Lu ML, Balk SP (July 2002). „Bicalutamid funguje jako antagonista androgenového receptoru sestavením transkripčně neaktivního receptoru“. The Journal of Biological Chemistry. 277 (29): 26321–6. doi:10,1074 / jbc.M203310200. PMID 12015321.
- ^ A b C d Denis L (6. prosince 2012). Antiandrogeny u rakoviny prostaty: klíč k endokrinní léčbě na míru. Springer Science & Business Media. pp. 128, 158, 203, 231–232. ISBN 978-3-642-45745-6.
At daily doses of 10, 30 and 50 mg decreases of this range were noted in 33%, 53% and 83% of treated patients. [% PSA decline: 10 mg: 57%; 30 mg: 73%; 50 mg: 90%; 100 mg: 97%; 150 mg: 97%; CAS: 97%.]
- ^ A b C d Furr BJ (červen 1995). „Casodex: předklinické studie a diskuse“. Annals of the New York Academy of Sciences. 761 (1): 79–96. Bibcode:1995NYASA.761...79F. doi:10.1111 / j.1749-6632.1995.tb31371.x. PMID 7625752. S2CID 37242269.
It is suggested that the resulting increase in output of androgen by the testis requires an increased dose of antiandrogen to neutralize any stimulatory effect on the prostate gland. This is a controversial topic [...], but when given in combination with medical or surgical castration, any rise in serum LH becomes irrelevant to clinical outcome.
- ^ Waller AS, Sharrard RM, Berthon P, Maitland NJ (June 2000). "Androgen receptor localisation and turnover in human prostate epithelium treated with the antiandrogen, casodex". Journal of Molecular Endocrinology. 24 (3): 339–51. CiteSeerX 10.1.1.499.7722. doi:10.1677/jme.0.0240339. PMID 10828827.
- ^ A b C d E Schellens JH, McLeod HL, Newell DR (5 May 2005). Cancer Clinical Pharmacology. OUP Oxford. str. 229–230. ISBN 978-0-19-262966-1. Archivováno z původního dne 10. června 2016.
- ^ A b C Lemke TL, Williams DA (24. ledna 2012). Foyeho principy léčivé chemie. Lippincott Williams & Wilkins. str. 1372–1373. ISBN 978-1-60913-345-0. Archivováno z původního dne 3. května 2016.
- ^ A b Butler SK, Govindan R (25 October 2010). Essential Cancer Pharmacology: The Prescriber's Guide. Lippincott Williams & Wilkins. str. 49–. ISBN 978-1-60913-704-5.
- ^ A b C d Becker KL (2001). Principy a praxe endokrinologie a metabolismu. Lippincott Williams & Wilkins. str. 1119, 1196, 1208. ISBN 978-0-7817-1750-2. Archivováno z původního dne 8. září 2017.
- ^ A b C d Furr BJ, Tucker H (leden 1996). „Preklinický vývoj bikalutamidu: farmakodynamika a mechanismus účinku“. Urologie. 47 (1A Suppl): 13–25, diskuse 29–32. doi:10.1016 / S0090-4295 (96) 80003-3. PMID 8560673.
- ^ Bagatelle C, Bremner WJ (27. května 2003). Androgeny ve zdraví a nemoci. Springer Science & Business Media. str. 25–. ISBN 978-1-59259-388-0.
- ^ A b C d E Ito Y, Sadar MD (2018). "Enzalutamide and blocking androgen receptor in advanced prostate cancer: lessons learnt from the history of drug development of antiandrogens". Res Rep Urol. 10: 23–32. doi:10.2147/RRU.S157116. PMC 5818862. PMID 29497605.
- ^ A b Guise TA, Oefelein MG, Eastham JA, Cookson MS, Higano CS, Smith MR (2007). „Estrogenní vedlejší účinky androgenní deprivační terapie“. Recenze v urologii. 9 (4): 163–80. PMC 2213888. PMID 18231613.
The incidence of gynecomastia varies with the type and duration of ADT.65,83 For example, it is reported in 40% to 80% of men on estrogen therapy (eg, DES), 40% to 70% of men on antiandrogens (bicalutamide, flutamide, or nilutamide, including > 50% with high-dose bicalutamide [150 mg]), 25% of men on combined androgen blockade (LHRH with an antiandrogen), and 10% to 15% of men on LHRH alone or after orchiectomy.66
- ^ Bulldan A, Malviya VN, Upmanyu N, Konrad L, Scheiner-Bobis G (2017). "Testosterone/bicalutamide antagonism at the predicted extracellular androgen binding site of ZIP9". Biochim. Biophys. Acta. 1864 (12): 2402–2414. doi:10.1016/j.bbamcr.2017.09.012. PMID 28943399.
- ^ Thomas P, Converse A, Berg HA (2017). "ZIP9, a novel membrane androgen receptor and zinc transporter protein". Gen. Comp. Endokrinol. 257: 130–136. doi:10.1016/j.ygcen.2017.04.016. PMID 28479083.
- ^ Pi M, Parrill AL, Quarles LD (2010). "GPRC6A mediates the non-genomic effects of steroids". J. Biol. Chem. 285 (51): 39953–64. doi:10.1074/jbc.M110.158063. PMC 3000977. PMID 20947496.
- ^ Furr BJ, Valcaccia B, Curry B, Woodburn JR, Chesterson G, Tucker H (červen 1987). „ICI 176 334: nový nesteroidní, periferně selektivní antiandrogen“. J. Endocrinol. 113 (3): R7–9. doi:10.1677 / joe.0.113R007. PMID 3625091.
- ^ Teutsch G, Goubet F, Battmann T, Bonfils A, Bouchoux F, Cerede E, Gofflo D, Gaillard-Kelly M, Philibert D (leden 1994). "Nesteroidní antiandrogeny: syntéza a biologický profil vysokoafinitních ligandů pro androgenní receptor". J. Steroid Biochem. Mol. Biol. 48 (1): 111–9. doi:10.1016/0960-0760(94)90257-7. PMID 8136296.
- ^ Winneker RC, Wagner MM, Batzold FH (prosinec 1989). "Studie o mechanismu účinku Win 49596: antagonista steroidních androgenových receptorů". J. Steroid Biochem. 33 (6): 1133–8. doi:10.1016/0022-4731(89)90420-2. PMID 2615358.
- ^ A b Luo, S; Martel, C; LeBlanc, G; Candas, B; Singh, SM; Labrie, C; Simard, J; Belanger, A; Labrie, F (1996). "Relativní potence Flutamidu a Casodexu: preklinické studie". Rakovina související s endokrinním systémem. 3 (3): 229–241. doi:10.1677 / erc.0.0030229. ISSN 1351-0088.
- ^ Kemppainen JA, Wilson EM (červenec 1996). „Agonistické a antagonistické aktivity hydroxyflutamidu a Casodexu se týkají stabilizace androgenových receptorů“. Urologie. 48 (1): 157–63. doi:10.1016 / S0090-4295 (96) 00117-3. PMID 8693644.
- ^ Furr BJ (2009). „Výzkum reprodukční medicíny ve farmaceutickém průmyslu“. Human Fertility. 1 (1): 56–63. doi:10.1080/1464727982000198131. PMID 11844311.
- ^ Tran C, Ouk S, Clegg NJ, Chen Y, Watson PA, Arora V, Wongvipat J, Smith-Jones PM, Yoo D, Kwon A, Wasielewska T, Welsbie D, Chen CD, Higano CS, Beer TM, Hung DT, Scher HI, Jung ME, Sawyers CL (2009). „Vývoj antiandrogenu druhé generace pro léčbu pokročilého karcinomu prostaty“. Věda. 324 (5928): 787–90. Bibcode:2009Sci...324..787T. doi:10.1126 / science.1168175. PMC 2981508. PMID 19359544.
[...] bicalutamide has relatively low affinity for AR (at least 30-fold reduced relative to the natural ligand dihydrotestosterone (DHT)) (7), [...]
- ^ Furr, B J A (1997). "Relative potencies of flutamide and 'Casodex'". Rakovina související s endokrinním systémem. 4 (2): 197–202. doi:10.1677/erc.0.0040197. ISSN 1351-0088.
'Casodex' has been used in both models; in the Shionogi mammary tumour, an independent study by Darbre & King (1990) shows that a 1000-fold excess of 'Casodex' completely inhibits the response to 5α-DHT. Inspection of the data shown by Luo et al. suggests that at least a 10 000-fold excess of 'Casodex' and around a 3500-fold excess of hydroxyflutamide is required to achieve complete inhibition of 5α-DHT-stimulated growth.
- ^ Furr BJ (1996). "The development of Casodex (bicalutamide): preclinical studies". Evropská urologie. 29 Suppl 2 (2): 83–95. doi:10.1159/000473846. PMID 8717469.
- ^ A b Figg W, Chau CH, Small EJ (14. září 2010). Léčba rakoviny prostaty. Springer Science & Business Media. 56, 71–72, 75, 93. ISBN 978-1-60327-829-4.
- ^ Chapple CR, Steers WD (10 May 2011). Practical Urology: Essential Principles and Practice: Essential Principles and Practice. Springer Science & Business Media. str. 225–. ISBN 978-1-84882-034-0.
Normal reference ranges for serum total testosterone in adult men is generally considered to be 300–1,000 ng/dL (10–35 nmol/L).
- ^ Gentile V, Panebianco V, Sciarra A (11 April 2014). Multidisciplinary Management of Prostate Cancer: The Role of the Prostate Cancer Unit. Springer Science & Business Media. 106–. ISBN 978-3-319-04385-2.
The standard castrate level is <50 ng/dl. It was defined more than 40 years ago, when testosterone level testing was limited. However, current testing methods using chemiluminescence have found that the mean value of testosterone after surgical castration is 15 ng/dL.
- ^ A b C „Tablety Casodex® (bikalutamid)“ (PDF). FDA. Archivováno (PDF) z původního dne 27. února 2017.
- ^ A b C "COSUDEX® (bicalutamide) 150 mg tablets". TGA. Archivováno from the original on 14 September 2016.
- ^ A b C d E Denis L, Mahler C (January 1996). "Pharmacodynamics and pharmacokinetics of bicalutamide: defining an active dosing regimen". Urologie. 47 (1A Suppl): 26–8, discussion 29–32. doi:10.1016/S0090-4295(96)80004-5. PMID 8560674.
- ^ A b C d E F Wellington K, Keam SJ (2006). „Bicalutamid 150mg: přehled jeho použití při léčbě lokálně pokročilého karcinomu prostaty“ (PDF). Drogy. 66 (6): 837–50. doi:10.2165/00003495-200666060-00007. PMID 16706554. S2CID 46966712. Archivovány od originál (PDF) dne 28. srpna 2016. Citováno 23. listopadu 2017.
- ^ A b C Boccardo F, Rubagotti A, Conti G, Potenzoni D, Manganelli A, Del Monaco D (2005). "Exploratory study of drug plasma levels during bicalutamide 150 mg therapy co-administered with tamoxifen or anastrozole for prophylaxis of gynecomastia and breast pain in men with prostate cancer". Chemoterapie rakoviny a farmakologie. 56 (4): 415–20. doi:10.1007/s00280-005-1016-1. PMID 15838655. S2CID 23014567.
- ^ A b C Kolvenbag GJ, Nash A (April 1999). "Bicalutamide dosages used in the treatment of prostate cancer". Prostata. 39 (1): 47–53. doi:10.1002/(SICI)1097-0045(19990401)39:1<47::AID-PROS8>3.0.CO;2-X. PMID 10221266.
- ^ A b Chung LW, Isaacs WB, Simons JW (10 November 2007). Prostate Cancer: Biology, Genetics, and the New Therapeutics. Springer Science & Business Media. str. 365–. ISBN 978-1-59745-224-3. Archivováno z původního dne 20. května 2016.
- ^ A b C Melmed S, Polonsky KS, Reed Larsen P, Kronenberg HM (30 November 2015). Williamsova učebnice endokrinologie. Elsevier Health Sciences. pp. 704–708, 711, 1104. ISBN 978-0-323-29738-7.
- ^ Bruskewitz R (6. prosince 2012). Atlas prostaty. Springer Science & Business Media. 5, 190. ISBN 978-1-4615-6505-5.
- ^ A b C d Nieschlag E, Behre HM (6. prosince 2012). Testosterone: Action – Deficiency – Substitution. Springer Science & Business Media. pp. 130, 276. ISBN 978-3-642-72185-4.
- ^ Mozayani A, Raymon L (18. září 2011). Příručka lékových interakcí: Klinický a forenzní průvodce. Springer Science & Business Media. str. 656–. ISBN 978-1-61779-222-9.
- ^ A b Chabner BA, Longo DL (8. listopadu 2010). Chemoterapie a bioterapie rakoviny: principy a praxe. Lippincott Williams & Wilkins. 679–680. ISBN 978-1-60547-431-1.
Ze strukturálního hlediska jsou antiandrogeny klasifikovány jako steroidní, včetně cyproteron [acetátu] (Androcur) a megestrol [acetátu], nebo nesteroidní, včetně flutamidu (Eulexin atd.), Bikalutamidu (Casodex) a nilutamidu (Nilandron). Steroidní antiandrogeny se používají jen zřídka.
- ^ Mydlo JH, Godec CJ (29. září 2015). Rakovina prostaty: Věda a klinická praxe. Elsevierova věda. str. 516–521, 534–540. ISBN 978-0-12-800592-7. Archivováno z původního dne 8. září 2017.
- ^ A b C Strauss III JF, Barbieri RL (28. srpna 2013). Yen & Jaffe's Reprodukční endokrinologie: fyziologie, patofyziologie a klinické řízení. Elsevier Health Sciences. str. 688–. ISBN 978-1-4557-5972-9.
Hustota kostí se zlepšuje u mužů užívajících bikalutamid, pravděpodobně sekundárně po 146% zvýšení estradiolu a skutečnosti, že estradiol je hlavním mediátorem kostní hustoty u mužů.
- ^ Luo S, Martel C, Chen C, Labrie C, Candas B, Singh SM, Labrie F (prosinec 1997). "Denní dávkování flutamidu nebo Casodexu vykazuje maximální antiandrogenní aktivitu." Urologie. 50 (6): 913–9. doi:10.1016 / S0090-4295 (97) 00393-2. PMID 9426723.
- ^ Wirth MP, Hakenberg OW, Froehner M (únor 2007). "Antiandrogeny v léčbě rakoviny prostaty". Evropská urologie. 51 (2): 306–13, diskuse 314. doi:10.1016 / j.eururo.2006.08.043. PMID 17007995.
- ^ Labrie F (January 2015). "Combined blockade of testicular and locally made androgens in prostate cancer: a highly significant medical progress based upon intracrinology". J. Steroid Biochem. Mol. Biol. 145: 144–56. doi:10.1016/j.jsbmb.2014.05.012. PMID 24925260. S2CID 23102323.
- ^ A b Crawford ED, Schellhammer PF, McLeod DG, Moul JW, Higano CS, Shore N, Denis L, Iversen P, Eisenberger MA, Labrie F (May 2018). "Androgen Receptor-Targeted Treatments for Prostate Cancer: 35 Years' Progress with Antiandrogens". J. Urol. 200 (5): 956–966. doi:10.1016/j.juro.2018.04.083. PMID 29730201. S2CID 19162538.
- ^ Student, Sebastian; Hejmo, Tomasz; Poterała-Hejmo, Aleksandra; Leśniak, Aleksandra; Bułdak, Rafał (2019). „Antiandrogenní hormonální léčba rakoviny a dalších nemocí“. European Journal of Pharmacology. 866: 172783. doi:10.1016 / j.ejphar.2019.172783. ISSN 0014-2999. PMID 31712062.
- ^ Nadal R, Bellmunt J (March 2016). "The evolving role of enzalutamide on the treatment of prostate cancer". Future Oncol. 12 (5): 607–16. doi:10.2217/fon.15.351. PMC 5551941. PMID 26839021.
- ^ A b Stein MN, Jang TL (June 2016). "Striving Toward a Cure for Prostate Cancer". J. Clin. Oncol. 34 (18): 2075–8. doi:10.1200/JCO.2015.66.3146. PMID 27022121.
- ^ Styne, D. M. (6. prosince 2019). "Fyziologie a poruchy puberty". In Melmed, S .; Koenig, R. J .; Rosen, C. J.; Auchus, R. J.; Goldfine, A. B .; Williams, R. H. (eds.). Williamsova učebnice endokrinologie (14 ed.). Philadelphia, PA: Elsevier. str. 1023–1164. ISBN 9780323555968.
- ^ A b C Marcus R, Feldman D, Nelson D, Rosen CJ (8 November 2007). Osteoporóza. Akademický tisk. str. 1354–. ISBN 978-0-08-055347-4. Archivováno z původního dne 11. června 2016.
- ^ A b Diamanti-Kandarakis E, Nestler JE, Pandas D, Pasquale R (21. prosince 2009). Inzulínová rezistence a syndrom polycystických vaječníků: patogeneze, hodnocení a léčba. Springer Science & Business Media. str. 75–. ISBN 978-1-59745-310-3. Archivováno z původního dne 19. května 2016.
- ^ A b Carrell DT, Peterson CM (23 March 2010). Reprodukční endokrinologie a neplodnost: integrace moderní klinické a laboratorní praxe. Springer Science & Business Media. str. 163–. ISBN 978-1-4419-1436-1. Archivováno z původního dne 4. července 2014.
- ^ A b C Bouchard P, Caraty A (15. listopadu 1993). GnRH, analogy GnRH, gonadotropiny a peptidy gonadalů. CRC Press. 455–456. ISBN 978-0-203-09205-7.
[...] když jsou mužské hladiny androgenů dosaženy v plazmě, jsou jejich účinky na sekreci gonadotropinů podobné u žen i mužů. [...] podávání flutamidu skupině normálně cyklujících žen vedlo ke klinickému zlepšení akné a hirsutismu bez významné hormonální změny. [...] Všechna tato data zdůrazňují, že fyziologické hladiny androgenů nemají žádný vliv na regulaci gonadotropinů u normálních žen. [...] Androgeny nehrají přímo roli v regulaci gonadotropinů [u žen].
- ^ Williams H, Bigby M, Diepgen T, Herxheimer A, Naldi L, Rzany B (22. ledna 2009). Dermatologie založená na důkazech. John Wiley & Sons. str. 529–. ISBN 978-1-4443-0017-8. Archivováno z původního dne 2. května 2016.
- ^ Erem C (2013). "Aktualizace idiopatického hirsutismu: diagnóza a léčba". Acta Clinica Belgica. 68 (4): 268–74. doi:10.2143 / ACB.3267. PMID 24455796. S2CID 39120534.
- ^ Costanzo Giulio Moretti, Laura Guccione, Paola Di Giacinto, Amalia Cannuccia, Chiara Meleca, Giulia Lanzolla, Aikaterini Andreadi, Davide Lauro (2016), Účinnost a bezpečnost suplementace myo-inozitolem při léčbě obézních chlupatých PCOS žen: srovnávací hodnocení s terapií OCP + bikalutamidem, doi:10.1210 / endo-meeting.2016.RE.5.SUN-153 (neaktivní 2020-10-05)CS1 maint: používá parametr autoři (odkaz) CS1 maint: DOI neaktivní od října 2020 (odkaz)
- ^ A b C Mahler C, Verhelst J, Denis L (květen 1998). „Klinická farmakokinetika antiandrogenů a jejich účinnost při rakovině prostaty“. Klinická farmakokinetika. 34 (5): 405–17. doi:10.2165/00003088-199834050-00005. PMID 9592622. S2CID 25200595.
- ^ A b Fradet Y (únor 2004). „Bicalutamid (Casodex) při léčbě rakoviny prostaty“. Odborná recenze protinádorové terapie. 4 (1): 37–48. doi:10.1586/14737140.4.1.37. PMID 14748655. S2CID 34153031.
Naproti tomu byl výskyt průjmu ve skupině s bikalutamidem srovnatelný (6,3 vs. 6,4%) v programu EPC [71].
- ^ A b C d E F G h Tyrrell CJ, Denis L, Newling D, Soloway M, Channer K, Cockshott ID (1998). „Casodex 10–200 mg denně, používaný jako monoterapie k léčbě pacientů s pokročilým karcinomem prostaty. Přehled účinnosti, snášenlivosti a farmakokinetiky ze tří studií rozsahu dávek fáze II. Casodex Study Group“. Eur. Urol. 33 (1): 39–53. doi:10.1159/000019526. PMID 9471040. S2CID 71758492.
- ^ A b C d Iversen P, Melezinek I, Schmidt A (leden 2001). „Nesteroidní antiandrogeny: terapeutická možnost pro pacienty s pokročilým karcinomem prostaty, kteří si chtějí zachovat sexuální zájem a funkci“. BJU International. 87 (1): 47–56. doi:10.1046 / j.1464-410x.2001.00988.x. PMID 11121992. S2CID 28215804.
- ^ A b DeVita Jr VT, Lawrence TS, Rosenberg SA (7. ledna 2015). DeVita, Hellman a Rosenberg's Cancer: Principles & Practice of Oncology. Wolters Kluwer Health. str. 1142–. ISBN 978-1-4698-9455-3.
- ^ A b Eri LM, Haug E, Tveter KJ (březen 1995). „Účinky dlouhodobé léčby nesteroidním antiandrogenem Casodex na endokrinní systém u pacientů s benigní hyperplazií prostaty“. British Journal of Urology. 75 (3): 335–40. doi:10.1111 / j.1464-410X.1995.tb07345.x. PMID 7537602.
- ^ Verhelst J, Denis L, Van Vliet P, Van Poppel H, Braeckman J, Van Cangh P, Mattelaer J, D'Hulster D, Mahler C (říjen 1994). „Endokrinní profily během podávání nového nesteroidního antiandrogenního Casodexu u rakoviny prostaty“. Clin. Endokrinol. (Oxf). 41 (4): 525–30. doi:10.1111 / j.1365-2265.1994.tb02585.x. PMID 7525125. S2CID 7880831.
- ^ A b Wadhwa VK, Weston R, Parr NJ (červen 2011). „Monoterapie bikalutamidem zachovává kostní minerální hustotu, svalovou sílu a má významné přínosy pro kvalitu života související se zdravím pro osteoporotické muže s rakovinou prostaty.“ BJU Int. 107 (12): 1923–9. doi:10.1111 / j.1464-410X.2010.09726.x. PMID 20950306. S2CID 205543615.
- ^ A b Wein AJ, Kavoussi LR, Novick AC, Partin AW, Peters CA (25. srpna 2011). Campbell-Walsh Urology: Expert Consult Premium Edition: Enhanced Online Features and Print, 4-Volume Set. Elsevier Health Sciences. 2938–2939, 2946. ISBN 978-1-4160-6911-9. Archivováno z původního dne 5. května 2016.
- ^ Lunglmayr G (1989). „Casodex (ICI 176 334), nový nesteroidní antiandrogen. Včasné klinické výsledky“. Výzkum hormonů. 32 Suppl 1: 77–81. doi:10.1159/000181316. PMID 2515147.
- ^ E.E. Müller (6. prosince 2012). Peptidy a nepeptidy s onkologickým a neuroendokrinním významem: od základního po klinický výzkum. Springer Science & Business Media. str. 231–. ISBN 978-88-470-2085-6.
Čisté antiandrogeny lze podávat jako monoterapii ve snaze vyhnout se vedlejším účinkům způsobeným terapiemi potlačujícími androgen (ztráta libida, impotence, osteoporóza, patologické zlomeniny, úbytek svalové hmoty a tónu, progresivní anémie, astenie a deprese). (Tyrrell, 1992). Použití těchto sloučenin u pacientů s intaktními pohlavními žlázami vyvolává stav hypergonadotropního hypergonadismu, který umožňuje udržovat vysoké hladiny testosteronu v oběhu.
- ^ Knuth UA, Hano R, Nieschlag E (listopad 1984). „Vliv flutamidu nebo cyproteron-acetátu na hormony hypofýzy a varlat u normálních mužů“. J. Clin. Endokrinol. Metab. 59 (5): 963–9. doi:10.1210 / jcem-59-5-963. PMID 6237116.
Protože FLU postrádá vnitřní hormonální aktivitu, její antiandrogenní vlastnost vede ke zvýšeným hladinám testosteronu (T) v séru a ke zvýšeným hodnotám gonadotropinu. Účinek této jedinečné endokrinní situace, kterou lze popsat jako „hypergonadotropní hypergonadismus“.
- ^ Müderris II, Bayram F, Ozçelik B, Güven M (únor 2002). „Nová alternativní léčba hirzutismu: bikalutamid 25 mg / den“. Gynecol. Endokrinol. 16 (1): 63–6. doi:10,1080 / gye.16.1.63.66. PMID 11915584. S2CID 6942048.
- ^ Moretti C, Guccione L, Di Giacinto P, Simonelli I, Exacoustos C, Toscano V, Motta C, De Leo V, Petraglia F, Lenzi A (březen 2018). „Kombinovaná orální antikoncepce a bikalutamid u syndromu polycystických vaječníků a závažného hirsutismu: dvojitě zaslepená randomizovaná kontrolovaná studie“. J. Clin. Endokrinol. Metab. 103 (3): 824–838. doi:10.1210 / jc.2017-01186. PMID 29211888.
- ^ Bahceci M, Tuzcu A, Canoruc N, Tuzun Y, Kidir V, Aslan C (2004). „Hladiny sérového C-reaktivního proteinu (CRP) a inzulínová rezistence u neobézních žen se syndromem polycystických vaječníků a účinek bikalutamidu na hirzutismus, hladiny CRP a inzulínovou rezistenci“. Horm. Res. 62 (6): 283–7. doi:10.1159/000081973. PMID 15542929. S2CID 46261843.
- ^ Shlomo Melmed (1. ledna 2016). Williamsova učebnice endokrinologie. Elsevier Health Sciences. str. 752–. ISBN 978-0-323-29738-7.
Analogy GnRH, jak agonisté, tak antagonisté, silně potlačují produkci endogenního gonadotropinu a testosteronu [...] Podávání agonistů GnRH (např. Leuprolid, goserelin) produkuje počáteční stimulaci sekrece gonadotropinu a testosteronu (známou jako „vzplanutí“), která po 1 až 2 týdnech následuje downregulace receptoru GnRH a výrazné potlačení gonadotropinů a testosteronu na kastrační hladiny. [...] Aby se zabránilo možným komplikacím spojeným s vzplanutím testosteronu, antagonisté AR (např. Bikalutamid) se obvykle podávají spolu s agonistou GnRH u mužů s metastatickým karcinomem prostaty.399
- ^ Asscheman H, Gooren LJ, Peereboom-Wynia JD (1989). „Snížení nežádoucího sexuálního růstu vlasů s anandronem u transsexuálů muž-žena - zkušenosti s novým blokátorem androgenních receptorů“. Klinická a experimentální dermatologie. 14 (5): 361–3. doi:10.1111 / j.1365-2230.1989.tb02585.x. PMID 2612040. S2CID 45303518.
- ^ Rao BR, de Voogt HJ, Geldof AA, Gooren LJ, Bouman FG (1988). „Přednosti a úvahy při užívání antiandrogenu“. Journal of Steroid Biochemistry. 31 (4B): 731–7. doi:10.1016/0022-4731(88)90024-6. PMID 3143862.
- ^ A b Jameson JL, de Kretser DM, Marshall JC, De Groot LJ (7. května 2013). Endokrinologie pro dospělé a děti: Reprodukční endokrinologie. Elsevier Health Sciences. ISBN 978-0-323-22152-8. Archivováno z původního dne 25. července 2014.
Používají se také nesteroidní antiandrogeny (např. Flutamid a nilutamid), ale zvyšují sekreci gonadotropinů, což způsobuje zvýšenou sekreci testosteronu a estradiolu.119 Ten je v tomto kontextu žádoucí, protože má feminizující účinky.
- ^ Bach PV, Najari BB, Kashanian JA (2016). "Doplňkové řízení mužského hypogonadismu". Aktuální zprávy o sexuálním zdraví. 8 (4): 231–239. doi:10.1007 / s11930-016-0089-7. ISSN 1548-3584. S2CID 79220716.
- ^ Santen RJ, Leonard JM, Sherins RJ, Gandy HM, Paulsen CA (1971). „Krátkodobé a dlouhodobé účinky klomifen citrátu na osu hypofýza-varlata“. J. Clin. Endokrinol. Metab. 33 (6): 970–9. doi:10.1210 / jcem-33-6-970. PMID 5135636.
Zvýšení sérových hladin LH se pohybovalo v rozmezí 200–700% během prvních 21 dnů podávání klomifenu, ale poté dosáhlo plató. Hladiny FSH v séru vykazovaly podobné plató po 35 dnech, s maximálními titry 70–360% nad kontrolou. Rozsah přírůstků testosteronu v séru po 7 a 51 dnech podávání klomifenu byl podobný rozsahu pozorovanému v hladinách gonadotropinu v séru.
- ^ Martini L (2. prosince 2012). Klinická neuroendokrinologie. Elsevier. str. 239. ISBN 978-0-323-14429-2.
Ze studií Santen et al. (1971) se zdá, že delší období podávání (v jejich studii 51 dní) by způsobilo ještě větší nárůst FSH a LH (70–360%, respektive 200–700%).
- ^ Sieber PR (prosinec 2007). "Léčba bikalutamidem vyvolaných příhod prsu". Odborná recenze protinádorové terapie. 7 (12): 1773–9. doi:10.1586/14737140.7.12.1773. PMID 18062751. S2CID 40410461.
- ^ A b C Kennealey GT, Furr BJ (únor 1991). „Použití nesteroidního antiandrogenního Casodexu u pokročilého karcinomu prostaty“. Urol. Clin. North Am. 18 (1): 99–110. PMID 1992575.
- ^ A b C Wibowo E, Schellhammer P, Wassersug RJ (leden 2011). „Role estrogenu v normální mužské funkci: klinické důsledky pro pacienty s rakovinou prostaty na androgenní deprivační terapii“. The Journal of Urology. 185 (1): 17–23. doi:10.1016 / j.juro.2010.08.094. PMID 21074215.
- ^ A b Motofei IG, Rowland DL, Popa F, Kreienkamp D, Paunica S (červenec 2011). „Předběžná studie s bikalutamidem u heterosexuálních a homosexuálních pacientů s rakovinou prostaty: možné důsledky androgenů v mužském homosexuálním vzrušení“. BJU International. 108 (1): 110–5. doi:10.1111 / j.1464-410X.2010.09764.x. PMID 20955264. S2CID 45482984.
- ^ A b Wibowo E, Wassersug RJ (září 2013). "Vliv estrogenu na sexuální zájem kastrovaných mužů: Důsledky pro pacienty s rakovinou prostaty na androgenní deprivační terapii". Kritické recenze v onkologii / hematologii. 87 (3): 224–38. doi:10.1016 / j.critrevonc.2013.01.006. PMID 23484454.
- ^ Simpson ER, Jones ME (2007). „Z myší a mužů: mnoho podob estrogenu“. Tkáňově specifická estrogenová akce. Sborník sympozia Ernsta Scheringa. 2006/1. str. 45–67. doi:10.1007/2789_2006_016. ISBN 978-3-540-49547-5. PMID 17824171.
- ^ A b Král SR (2008). "Vznikající role neurosteroidů v sexuálním chování a funkci". Journal of Andrology. 29 (5): 524–33. doi:10.2164 / jandrol.108.005660. PMID 18567641.
- ^ A b Morali G, Oropeza MV, Lemus AE, Perez-Palacios G (září 1994). „Mechanismy regulující mužské sexuální chování u potkanů: role 3 alfa- a 3 beta-androstandiolů“. Biologie reprodukce. 51 (3): 562–71. doi:10.1095 / biolreprod51.3.562. PMID 7803627.
- ^ Sánchez Montoya EL, Hernández L, Barreto-Estrada JL, Ortiz JG, Jorge JC (listopad 2010). „Metabolit testosteronu 3α-diol zvyšuje sexuální motivaci samic potkanů, pokud je aplikován do skořápky nucleus accumbens“. The Journal of Sexual Medicine. 7 (11): 3598–609. doi:10.1111 / j.1743-6109.2010.01937.x. PMC 4360968. PMID 20646182.
- ^ A b Chedrese PJ (13. června 2009). Reprodukční endokrinologie: Molekulární přístup. Springer Science & Business Media. 233–. ISBN 978-0-387-88186-7. Archivováno z původního dne 5. září 2017.
- ^ Frye CA, Edinger KL, Lephart ED, Walf AA (2010). „3alfa-androstandiol, ale ne testosteron, tlumí s věkem související snížení kognitivního, úzkostného a depresivního chování samců potkanů“. Frontiers in Aging Neuroscience. 2: 15. doi:10.3389 / fnagi.2010.000.000. PMC 2874398. PMID 20552051.
- ^ Huang Q, Zhu H, Fischer DF, Zhou JN (červen 2008). „Estrogenní účinek 5alfa-androstan-3beta, 17beta-diolu na behaviorální reakci na stres a na regulaci CRH.“ Neurofarmakologie. 54 (8): 1233–8. doi:10.1016 / j.neuropharm.2008.03.016. PMID 18457850. S2CID 9052079.
- ^ Frye CA, Koonce CJ, Edinger KL, Osborne DM, Walf AA (listopad 2008). „Androgeny s aktivitou na estrogenovém receptoru beta mají anxiolytické a kognitivní účinky u samců potkanů a myší“. Hormony a chování. 54 (5): 726–34. doi:10.1016 / j.yhbeh.2008.07.013. PMC 3623974. PMID 18775724.
- ^ Gaudet M, Vigneault É, Foster W, Meyer F, Martin AG (leden 2016). „Randomizovaná studie non-inferiority s bikalutamidem a dutasteridem versus agonisty LHRH pro snížení objemu prostaty před brachyterapií I-125 s permanentním implantátem pro rakovinu prostaty“. Radiother Oncol. 118 (1): 141–7. doi:10.1016 / j.radonc.2015.11.022. PMID 26702991.
Dutasterid a bikalutamid jsou režimem, který nemá horší účinnost než režimy založené na agonistech LHRH pro snížení objemu prostaty před trvalou implantací brachyterapie prostaty. D + B má nižší sexuální toxicitu ve srovnání s agonisty LHRH před implantací a prvních 6 měsíců po implantaci. D + B je proto možnost, kterou je třeba zvážit pro snížení objemu prostaty před PIPB.
- ^ A b Furr BJ, Tucker H (leden 1996). „Preklinický vývoj bikalutamidu: farmakodynamika a mechanismus účinku“. Urologie. 47 (1A Suppl): 13–25, diskuse 29–32. doi:10.1016 / S0090-4295 (96) 80003-3. PMID 8560673.
- ^ Kolvenbag, G. J. C. M. (2001). „Kontinuum rakoviny prostaty: role bikalutamidu (CasodexR)“. Prostata Journal. 3 (1): 2–13. doi:10.1046 / j.1525-1411.2001.003001002.x. ISSN 1095-5100.
- ^ Zhang X, Li X, Allan GF, Sbriscia T, Linton O, Lundeen SG, Sui Z (srpen 2007). "Design, syntéza a in vivo SAR nové řady pyrazolinů jako účinných selektivních modulátorů androgenových receptorů". J. Med. Chem. 50 (16): 3857–69. doi:10.1021 / jm0613976. PMID 17636947.
Pro srovnání, androgenní antagonisté flutamid a bikalutamid snižovali jak hmotnost prostaty, tak levator ani o 30 až 67% při 30 mg / kg.
- ^ Ikeda, Kazuhiro; Horie-Inoue, Kuniko; Inoue, Satoshi (2019). "Funkce estrogenu a signalizace estrogenových receptorů na kosterním svalu". The Journal of Steroid Biochemistry and Molecular Biology. 191: 105375. doi:10.1016 / j.jsbmb.2019.105375. ISSN 0960-0760. PMID 31067490. S2CID 145024087.
- ^ A b C Bambury RM, Scher HI (červen 2015). „Enzalutamid: vývoj od lavice po postel“. Urologická onkologie. 33 (6): 280–8. doi:10.1016 / j.urolonc.2014.12.017. PMID 25797385.
- ^ Bambury RM, Rathkopf DE (srpen 2016). „Nové a další generace terapií zaměřených na androgenní receptory pro rakovinu prostaty: Kromě abirateronu a enzalutamidu“. Urologická onkologie. 34 (8): 348–55. doi:10.1016 / j.urolonc.2015.05.025. PMID 26162486.
- ^ A b Pinto Á (únor 2014). „Kromě abirateronu: nové hormonální terapie pro metastatický karcinom prostaty rezistentní na kastraci“. Biologie a terapie rakoviny. 15 (2): 149–55. doi:10,4161 / cbt.26724. PMC 3928129. PMID 24100689.
- ^ A b Wierckx K, Gooren L, T'Sjoen G (květen 2014). „Klinický přehled: Vývoj prsu u trans-žen užívajících hormony křížového pohlaví“. The Journal of Sexual Medicine. 11 (5): 1240–7. doi:10.1111 / jsm.12487. PMID 24618412.
Dalšími látkami s antiandrogenními vlastnostmi používanými [při léčbě transgender žen] jsou nesteroidní blokátory androgenních receptorů, jako jsou flutamid a bikalutamid [...]
- ^ Orentreich N, Durr NP (1974). „Mamogeneze u transsexuálů“. Journal of Investigative Dermatology. 63 (1): 142–6. doi:10.1111 / 1523-1747.ep12678272. PMID 4365991.
- ^ Anderson J (2003). „Úloha antiandrogenní monoterapie v léčbě rakoviny prostaty“. BJU Int. 91 (5): 455–61. doi:10.1046 / j.1464-410X.2003.04026.x. PMID 12603397. S2CID 8639102.
Gynekomastie je očekávaným farmakologickým účinkem nesteroidní antiandrogenní monoterapie a je způsobena nerovnováhou v normálním poměru androgenní a estrogenní aktivity [32]. Je to důsledek zvýšení hladin estrogenu (po periferní aromatizaci zvýšené hladiny testosteronu v séru) a přímého antagonismu působení androgenu v prsní tkáni.
- ^ A b Jameson JL, De Groot LJ (25. února 2015). Edndocrinology: Adult and Pediatric. Elsevier Health Sciences. str. 2425–2426, 2139. ISBN 978-0-323-32195-2.
- ^ A b Strauss III JF, Barbieri RL (13. září 2013). Yen and Jaffe's Reprodukční endokrinologie. Elsevier Health Sciences. 236–237. ISBN 978-1-4557-2758-2. Archivováno z původního dne 14. ledna 2017.
- ^ Wilson CB, Nizet V, Maldonado Y, Klein JO, Remington JS (2015). Remingtonovy a Kleinovy infekční nemoci plodu a novorozence. Elsevier Health Sciences. str. 190–. ISBN 978-0-323-24147-2. Archivováno z původního dne 14. ledna 2017.
- ^ Yen SS, Jaffe RB, Barbieri RL (2001). Endocrinología de la reproducción: fisiología, fisiopatología y manejo clínico. Vyd. Medic Panamericana. 303–. ISBN 978-950-06-2538-8.
- ^ Pinsky L, Ericsson RP, Schimke RN (1999). Genetické poruchy lidského sexuálního vývoje. Oxford University Press. 215–. ISBN 978-0-19-510907-8.
- ^ A b Di Lorenzo G, Autorino R, Perdonà S, De Placido S (2005). „Řízení gynekomastie u pacientů s rakovinou prostaty: systematický přehled“. Lancet Oncol. 6 (12): 972–9. doi:10.1016 / S1470-2045 (05) 70464-2. PMID 16321765.
- ^ Wassersug RJ, Oliffe JL (duben 2009). „Sociální kontext pro psychické potíže z iatrogenní gynekomastie s návrhy na její zvládnutí“. The Journal of Sexual Medicine. 6 (4): 989–1000. doi:10.1111 / j.1743-6109.2008.01053.x. PMID 19175864.
Agonisté LH-RH samy o sobě neprodukují mnoho gynekomastie (tj. Odhadují se na pouhých 4,4%) [13], ale ve spojení s typicky předepisovanými antiandrogeny (flutamid, bikalutamid a nilutamid) je gynekomastie častější (49) –68%) [13].
- ^ A b C d Kanhai RC, Hage JJ, van Diest PJ, Bloemena E, Mulder JW (leden 2000). „Krátkodobé a dlouhodobé histologické účinky kastrace a léčby estrogeny na prsní tkáň 14 transsexuálů mezi muži a ženami ve srovnání se dvěma chemicky kastrovanými muži“. American Journal of Surgical Pathology. 24 (1): 74–80. doi:10.1097/00000478-200001000-00009. PMID 10632490.
- ^ A b Lawrence AA (2006). „Transgender Health Concerns“. V Meyer IH, Northridge ME (eds.). Zdraví sexuálních menšin Perspektivy veřejného zdraví v populacích lesbiček, gayů, bisexuálů a transsexuálů. New York: Springer. 473–505. doi:10.1007/978-0-387-31334-4_19. ISBN 978-0-387-28871-0.
- ^ A b Rosen PP (2009). Rosenova patologie prsu (3. vyd.). Philadelphia: Lippincott Williams & Wilkins. str. 31–. ISBN 978-0-7817-7137-5.
- ^ Lorincz AM, Sukumar S (2006). „Molekulární vazby mezi obezitou a rakovinou prsu“. Rakovina související s endokrinním systémem. 13 (2): 279–92. doi:10.1677 / erc.1.00729. PMID 16728564.
Adipocyty tvoří převážnou část lidského prsu, přičemž epiteliální buňky tvoří pouze přibližně 10% objemu lidského prsu.
- ^ Howard BA, Gusterson BA (2000). "Vývoj lidského prsu". Journal of Mammary Gland Biology and Neoplasia. 5 (2): 119–37. doi:10.1023 / A: 1026487120779. PMID 11149569. S2CID 10819224.
Ve stromatu dochází ke zvýšení množství vláknité a tukové tkáně, přičemž dospělá nelaktující prsa sestává z 80% nebo více ze stromatu.
- ^ Sperling MA (10. dubna 2014). Dětská endokrinologie. Elsevier Health Sciences. str. 598–. ISBN 978-1-4557-5973-6.
Estrogen stimuluje růst bradavek, rozvětvování terminálních kanálků mléčné žlázy pro postup do stadia, ve kterém se tvoří duktuly, a růst mastného stromatu se zvyšuje, dokud netvoří asi 85% hmotnosti prsu. [...] Lobulace se objevuje kolem menarché, kdy se rozvětvením koncových kanálků vytvoří několik slepých vakovitých pupenů. Tyto účinky jsou způsobeny přítomností progesteronu. [...] K plnému alveolárnímu vývoji obvykle dochází pouze během těhotenství pod vlivem dalšího progesteronu a prolaktinu.
- ^ Hagisawa S, Shimura N, Arisaka O (2012). „Vliv přebytku estrogenu na vývoj prsu a vnějších genitálií při nedostatku růstového hormonu“. Journal of Pediatric and Adolescent Gynecology. 25 (3): e61–3. doi:10.1016 / j.jpag.2011.11.005. PMID 22206682.
Estrogen stimuluje růst bradavek, progresi větvení mléčného kanálu do stádia, ve kterém se tvoří duktily, a růst mastného stromatu, dokud netvoří asi 85% hmotnosti prsu.
- ^ Zanardi S, Puntoni M, Maffezzini M, Bandelloni R, Branchi D, Argusti A, Campodonico F, Turbino L, Mori M, Decensi A (1. prosince 2006). „Biomarkerová studie s přerušovaným podáváním nízkých dávek bikalutamidu u subjektů s vysokým rizikem rakoviny prostaty: aktualizované výsledky“. Biomarkery proti rakovině Epidemiol Předchozí. 15 (12 dodatek): A145.
Hladiny testosteronu (T), LH, E2 a SHBG se zvýšily u Bic, i když pouze změny T u obou dávek a změny LH u Bic 100 mg se významně lišily od kontrol (p <0,001). Změny cirkulujících hormonů a biomarkerů byly patrné po 3 měsících a přetrvávaly až do 6. měsíce léčby. V kontrolní skupině nebyla pozorována žádná změna cirkulujících hormonů nebo biomarkerů. [...] Léčba byla dobře snášena, i když bolest prsu byla zaznamenána u 0/19 (0%), 8/25 (32%) a 14/22 (64%) a gynekomastie u 0/19 (0%) 11/25 (44%) a 11/22 (50%) subjektů bez léčby, Bic 50 nebo 100 mg.
- ^ Zanardi, S .; Puntoni, M .; Maffezzini, M .; Bandelloni, R .; Mori, M .; Argusti, A .; Campodonico, F .; Turbino, L .; Branchi, D .; Montironi, R .; Decensi, A. (2009). „Fáze I-II Zkouška týdenního bikalutamidu u mužů se zvýšeným prostatickým specifickým antigenem a negativními biopsiemi prostaty“. Výzkum prevence rakoviny. 2 (4): 377–384. doi:10.1158 / 1940-6207.CAPR-08-0205. ISSN 1940-6207. PMID 19336728.
- ^ Decensi A, Zanardi S, Puntoni M, Bandelloni R, Branchi D, Argusti A, Campodonico F, Turbino L, Mori M, Maffezzini M (20. června 2007). „Fáze I-II studie týdenního bikalutamidu u mužů s vysokým PSA a negativní biopsií“. Journal of Clinical Oncology. 25 (18_suppl): 1500. doi:10.1200 / jco.2007.25.18_suppl.1500.
T, LH, estradiol a SHBG vzrostly na Bic o 50–60%. [...] Léčba byla dobře tolerována, mírná (G1) bolest prsu a gynekomastie byly zaznamenány u 40% léčených subjektů.
- ^ A b J. Aiman (6. prosince 2012). Neplodnost: Diagnostika a řízení. Springer Science & Business Media. str. 182–. ISBN 978-1-4613-8265-2.
- ^ Kroemer RW (2009). Reprodukční systém. Publikování na Infobase. str. 51–. ISBN 978-1-4381-3083-5.
- ^ Fody EP, Walker EM (1985). "Účinky léků na mužský a ženský reprodukční systém". Ann. Clin. Laboratoř. Sci. 15 (6): 451–8. PMID 4062226.
- ^ Liu YX (2005). "Kontrola spermatogeneze u primátů a vyhlídka na mužskou antikoncepci". Oblouk. Androl. 51 (2): 77–92. doi:10.1080/01485010490485768. PMID 15804862. S2CID 25411118.
- ^ Cheng CY, Wong EW, Yan HH, Mruk DD (2010). „Regulace spermatogeneze v mikroprostředí semenonosného epitelu: nové poznatky a pokroky“. Mol. Buňka. Endokrinol. 315 (1–2): 49–56. doi:10.1016 / j.mce.2009.08.004. PMC 3516447. PMID 19682538.
- ^ Schill W, Comhaire FH, Hargreave TB (26. srpna 2006). Andrologie pro lékaře. Springer Science & Business Media. str. 76–. ISBN 978-3-540-33713-3. Archivováno z původního dne 26. května 2016.
- ^ A b Cheng C (24. října 2009). Molekulární mechanismy ve spermatogenezi. Springer Science & Business Media. str. 258–. ISBN 978-0-387-09597-4.
- ^ A b C Morgante E, Gradini R, Realacci M, Sale P, D'Eramo G, Perrone GA, Cardillo MR, Petrangeli E, Russo M, Di Silverio F (březen 2001). „Účinky dlouhodobé léčby antiandrogenním bikalutamidem na lidská varlata: ultrastrukturální a morfometrická studie“. Histopatologie. 38 (3): 195–201. doi:10.1046 / j.1365-2559.2001.01077.x. PMID 11260298. S2CID 36892099.
- ^ A b Bjerklund Johansen TE, Majak M, Nesland JM (březen 1994). "Testikulární histologie po léčbě novým antiandrogenem Casodex pro karcinom prostaty. Předběžná zpráva". Scand. J. Urol. Nephrol. 28 (1): 67–70. doi:10.3109/00365599409180473. PMID 8009196.
- ^ Jones HB, Betton GR, Bowdler AL, McFarquhar RL, Middleton BJ, Lunglmayr G (1994). „Patologické a morfometrické hodnocení parametrů varlat u pacientů s metastatickým karcinomem prostaty po léčbě buď antiandrogenním Casodexem (ZM176,334) nebo bilaterální orchidektomií“. Urol. Res. 22 (3): 191–5. doi:10.1007 / BF00571849. PMID 7992465. S2CID 19540140.
- ^ Lunglmayr G, Girsch E, Kuber W, Biegelmayr C (1988). Vliv nového nesteroidního antiandrogenu (ICI 176 334) na hladiny hormonů a morfologii varlat u pacientů s pokročilým karcinomem prostaty (abstrakt 583). Sborník z 21. kongresu Mezinárodní urologické společnosti, 9. – 14. Října 1988, Buenos Aires, Argentina.
- ^ Johnson LR (14. října 2003). Základní lékařská fyziologie. Akademický tisk. str. 731–. ISBN 978-0-08-047270-6. Archivováno z původního dne 15. února 2017.
- ^ Mulhall JP (21. února 2013). Zachování plodnosti u pacientů s rakovinou mužského pohlaví. Cambridge University Press. str. 84–. ISBN 978-1-139-61952-3. Archivováno z původního dne 29. dubna 2016.
- ^ Iswaran TJ, Imai M, Betton GR, Siddall RA (květen 1997). „Přehled toxikologických studií na zvířatech s bikalutamidem (ICI 176 334)“. The Journal of Toxicological Sciences. 22 (2): 75 - 88. doi:10.2131 / jts.22.2_75. PMID 9198005.
- ^ Khursheed A, Minhas LA, Diaz WA (září 2011). "Histomorfometrická studie účinků bikalutamidu na spermatogenezi u samců potkanů" (PDF). Pákistán ozbrojené síly Medical Journal (3). Archivováno (PDF) z původního dne 23. června 2016.
- ^ Khurshid A, Hamid S, Niaz WA (2014). „Účinek bikalutamidu; antiandrogen, na hmotnost varlat u dospělých potkanů“. Pak Armed Forces Med J. 64 (2): 204–07. ISSN 0030-9648.
- ^ Abdulrahman AS, Mustafa IA (2019). „Dopad bikalutamidu, antiandrogenu na varlata potkana“. ZANCO Journal of Pure and Applied Sciences. 31 (2). doi:10.21271 / ZJPAS.31.2.12. ISSN 2218-0230.
- ^ Chandolia RK, Weinbauer GF, Behre HM, Nieschlag E (březen 1991). „Hodnocení periferně selektivního antiandrogenu (Casodex) jako nástroje pro studium vztahu mezi testosteronem a spermatogenezí u krysy“. J. Steroid Biochem. Mol. Biol. 38 (3): 367–75. doi:10.1016 / 0960-0760 (91) 90109-I. PMID 1848993. S2CID 19423860.
- ^ Chandolia RK, Weinbauer GF, Simoni M, Behre HM, Nieschlag E (listopad 1991). „Srovnávací účinky chronického podávání nesteroidních antiandrogenů flutamidu a Casodexu na reprodukční systém dospělého samce krysy“. Acta Endocrinol. 125 (5): 547–55. doi:10.1530 / acta.0.1250547. PMID 1759544.
- ^ A b Dohle GR, Smit M, Weber RF (listopad 2003). "Androgeny a mužská plodnost". World Journal of Urology. 21 (5): 341–5. doi:10.1007 / s00345-003-0365-9. PMID 14566423. S2CID 29032693.
- ^ A b Basu SC (15. prosince 2011). Mužská reprodukční dysfunkce. Jaypee Brothers Medical Publishers Pvt. Ltd. str. 323–. ISBN 978-93-5025-703-6.
- ^ A b C d Neumann, F .; Schenck, B. (1980). „Antiandrogeny: základní koncepty a klinické studie“. Regulace mužské plodnosti. 93–106. doi:10.1007/978-94-009-8875-0_10. ISBN 978-94-009-8877-4.
- ^ A b William Llewellyn (2011). Anabolika. Molecular Nutrition LLC. 642–643. ISBN 978-0-9828280-1-4.
- ^ A b Jones CA, Reiter L, Greenblatt E (2016). "Zachování plodnosti u transgender pacientů". International Journal of Transgenderism. 17 (2): 76–82. doi:10.1080/15532739.2016.1153992. ISSN 1553-2739. S2CID 58849546.
Tradičně bylo pacientům doporučeno kryokonzervovat spermie před zahájením hormonální léčby křížového pohlaví, protože existuje potenciál pro snížení motility spermií při vysoké dávce estrogenové terapie v průběhu času (Lubbert et al., 1992). Tento pokles plodnosti v důsledku léčby estrogeny je však kontroverzní kvůli omezeným studiím.
- ^ A b C d E F Payne AH, Hardy MP (28. října 2007). Leydigova buňka ve zdraví a nemocech. Springer Science & Business Media. str. 422–431. ISBN 978-1-59745-453-7.
Estrogeny jsou vysoce účinné inhibitory osy hypotalamus-hypofýza-varlat (212–214). Kromě jejich negativní zpětné vazby na úrovni hypotalamu a hypofýzy jsou pravděpodobné přímé inhibiční účinky na varlata (215 216). [...] Histologie varlat [s léčbou estrogeny] ukázala dezorganizaci semenných tubulů, vakuolizaci a absenci lumenu a kompartmentalizaci spermatogeneze.
- ^ Wakelin SH, Maibach HI, Archer CB (1. června 2002). Systémová léčba drogami v dermatologii: Příručka. CRC Press. str. 32–. ISBN 978-1-84076-013-2. Archivováno z původního dne 25. července 2014.
[Cyproteron-acetát] inhibuje spermatogenezi a způsobuje reverzibilní neplodnost (nejedná se však o mužskou antikoncepci).
- ^ A b Neumann F (1994). „Antiandrogen cyproteronacetát: objev, chemie, základní farmakologie, klinické použití a nástroj v základním výzkumu“. Exp. Clin. Endokrinol. 102 (1): 1–32. doi:10.1055 / s-0029-1211261. PMID 8005205.
Spermatogeneze je také závislá na androgenech a je inhibována CPA, což znamená, že pacienti léčení vysokými dávkami CPA jsou sterilní (obrázek 23). Všechny účinky CPA jsou plně reverzibilní.
- ^ A b Salam MA (2003). Principy a praxe urologie: Komplexní text. Universal-Publishers. str. 684–. ISBN 978-1-58112-412-5.
Estrogeny působí primárně prostřednictvím negativní zpětné vazby na úrovni hypotalamus-hypofýza, aby snížily sekreci LH a syntézu androgenů ve varlatech. [...] Je zajímavé, že pokud je léčba estrogeny přerušena po 3 letech. nepřerušované expozice může testosteron v séru zůstat na kastračních úrovních po dobu dalších 3 let. Předpokládá se, že toto prodloužené potlačení je výsledkem přímého účinku estrogenů na Leydigovy buňky.
- ^ A b C Mast N, Lin JB, Pikuleva IA (září 2015). „Léky na trhu mohou inhibovat cytochrom P450 27A1, potenciální nový cíl pro adjuvantní léčbu rakoviny prsu“. Molekulární farmakologie. 88 (3): 428–36. doi:10,1124 / mol. 115,099598. PMC 4551053. PMID 26082378.
- ^ Mast N, Zheng W, Stout CD, Pikuleva IA (únor 2013). „Vazba léčiva bikalutamidu obsahujícího kyano a fluor na cytochrom P450 46A1: neobvyklé vlastnosti a spektrální odezva“. The Journal of Biological Chemistry. 288 (7): 4613–24. doi:10,1074 / jbc.M112.438754. PMC 3576067. PMID 23288837.
- ^ A b Zhu Y, Liu C, Armstrong C, Lou W, Sandher A, Gao AC (září 2015). „Antiandrogeny inhibují odtok ABCB1 a aktivitu ATPázy a reverzní rezistenci na docetaxel u pokročilého karcinomu prostaty“. Klinický výzkum rakoviny. 21 (18): 4133–42. doi:10.1158 / 1078-0432.CCR-15-0269. PMC 4573793. PMID 25995342.
- ^ A b Fenner A (červenec 2015). "Rakovina prostaty: Antiandrogeny zvracejí rezistenci na docetaxel prostřednictvím inhibice ABCB1". Recenze přírody. Urologie. 12 (7): 361. doi:10.1038 / nrurol.2015.135. PMID 26057062. S2CID 29729317.
- ^ A b Armstrong CM, Gao AC (2015). „Léková rezistence u kastračně rezistentního karcinomu prostaty: mechanismy rezistence a nové strategie léčby. American Journal of Clinical and Experimental Urology. 3 (2): 64–76. PMC 4539108. PMID 26309896.
- ^ A b C d E Foster WR, Car BD, Shi H, Levesque PC, Obermeier MT, Gan J, Arezzo JC, Powlin SS, Dinchuk JE, Balog A, Salvati ME, Attar RM, Gottardis MM (duben 2011). „Bezpečnost léčiv je překážkou objevu a vývoji nových antagonistů androgenových receptorů“. Prostata. 71 (5): 480–8. doi:10.1002 / pros.21263. PMID 20878947.
- ^ Barrish J, Carter P, Cheng P (2010). Účty v oblasti objevování drog: případové studie v medicinální chemii. Royal Society of Chemistry. str. 127–. ISBN 978-1-84973-126-3.
- ^ Saqib U, Savai R, Liu D, Banerjee S, Baig MS (říjen 2018). "Repozice léku jako účinná terapie pro inhibici receptoru 2 aktivovanou proteázou". J. Cell. Biochem. 120 (2): 1522–1526. doi:10.1002 / jcb.27334. PMID 30370939. S2CID 53099338.
- ^ Zia MK, Siddiqui T, Ali SS, Ahsan H, Khan FH (prosinec 2018). „Zkoumání interakce antiandrogenního léčiva-bikalutamidu s lidským alfa-2-makroglobulinem: biofyzikální vyšetření“. Int. J. Biol. Makromol. 120 (Pt B): 2285–2292. doi:10.1016 / j.ijbiomac.2018.08.117. PMID 30149080.
- ^ A b C d Weber GF (22. července 2015). Molekulární terapie rakoviny. Springer. 318–. ISBN 978-3-319-13278-5.
Ve srovnání s flutamidem a nilutamidem má bikalutamid dvojnásobně zvýšenou afinitu k androgennímu receptoru, delší poločas a podstatně sníženou toxicitu. Na základě příznivějšího bezpečnostního profilu ve srovnání s flutamidem je bikalutamid indikován k použití v kombinované terapii s analogem hormonu uvolňujícího gonadotropin k léčbě pokročilého metastatického karcinomu prostaty.
- ^ Cockshott ID, Plummer GF, Cooper KJ, Warwick MJ (říjen 1991). "Farmakokinetika Casodexu u laboratorních zvířat". Xenobiotica. 21 (10): 1347–55. doi:10.3109/00498259109043209. PMID 1796611.
- ^ A b Sharma K, Pawar GV, Giri S, Rajagopal S, Mullangi R (prosinec 2012). „Vývoj a validace vysoce citlivé metody LC-MS / MS-ESI pro stanovení bikalutamidu v myší plazmě: aplikace na farmakokinetickou studii“. Biomed Chromatogr. 26 (12): 1589–95. doi:10,1002 / bmc.2736. PMID 22495777.
- ^ Kolvenbag GJ, Blackledge GR, Gotting-Smith K (leden 1998). „Bicalutamid (Casodex) v léčbě rakoviny prostaty: historie klinického vývoje“. Prostata. 34 (1): 61–72. doi:10.1002 / (SICI) 1097-0045 (19980101) 34: 1 <61 :: AID-PROS8> 3.0.CO; 2-N. PMID 9428389.
- ^ A b Tyrrell CJ, Iversen P, Tammela T, Anderson J, Björk T, Kaisary AV, Morris T (září 2006). „Tolerance, účinnost a farmakokinetika bikalutamidu 300 mg, 450 mg nebo 600 mg v monoterapii u pacientů s lokálně pokročilým nebo metastazujícím karcinomem prostaty ve srovnání s kastrací“. BJU International. 98 (3): 563–72. doi:10.1111 / j.1464-410X.2006.06275.x. PMID 16771791. S2CID 41672303.
- ^ A b Blackledge GR (1996). "Klinický pokrok s novým antiandrogenem, Casodex (bikalutamid)". Eur. Urol. 29 Suppl 2 (2): 96–104. doi:10.1159/000473847. PMID 8717470.
- ^ A b C Cantarini M, Fuhr R, Morris T (2006). "Farmakokinetika dvou nových formulací bikalutamidu u zdravých mužských dobrovolníků". Farmakologie. 77 (4): 171–8. doi:10.1159/000094599. PMID 16847400. S2CID 35010482.
- ^ A b Chu E, DeVita Jr VT (28. prosince 2012). Příručka k lékům na chemoterapii proti rakovině lékařů 2013. Vydavatelé Jones & Bartlett. str. 51–. ISBN 978-1-284-04039-5.
- ^ Bunce CM, Campbell MJ (11. března 2010). Jaderné receptory: současné koncepty a budoucí výzvy. Springer Science & Business Media. 160, 167. ISBN 978-90-481-3303-1. Archivováno z původního dne 10. června 2016.
- ^ Beale C, Collins P (15. května 1996). Kardioprotektivní role HRT: Klinická aktualizace. CRC Press. str. 14–. ISBN 978-1-85070-740-0.
- ^ A b Helsen C, Van den Broeck T, Voet A, Prekovic S, Van Poppel H, Joniau S, Claessens F (srpen 2014). „Antagonisté receptoru androgenu pro léčbu rakoviny prostaty“. Rakovina související s endokrinním systémem. 21 (4): T105–18. doi:10.1530 / ERC-13-0545. PMID 24639562.
- ^ Furr BJ (1989). ""Casodex „(ICI 176 334) - nový, čistý, periferně selektivní antiandrogen: preklinické studie“. Výzkum hormonů. 32 Suppl 1 (1): 69–76. doi:10.1159/000181315. PMID 2533159.
- ^ Furr BJ, Valcaccia B, Curry B, Woodburn JR, Chesterson G, Tucker H (červen 1987). „ICI 176 334: nový nesteroidní, periferně selektivní antiandrogen“. The Journal of Endocrinology. 113 (3): R7–9. doi:10.1677 / joe.0.113R007. PMID 3625091.
- ^ Soloway MS, Schellhammer PF, Smith JA, Chodak GW, Vogelzang NJ, Kennealey GT (prosinec 1995). „Bicalutamid v léčbě pokročilého karcinomu prostaty: nekomparativní multicentrická studie fáze II hodnotící bezpečnost, účinnost a dlouhodobé endokrinní účinky monoterapie“. The Journal of Urology. 154 (6): 2110–4. doi:10.1016 / S0022-5347 (01) 66709-0. PMID 7500470.
- ^ A b Gao W, Dalton JT (březen 2007). „Rozšíření terapeutického využití androgenů prostřednictvím selektivních modulátorů androgenních receptorů (SARM)“. Objev drog dnes. 12 (5–6): 241–8. doi:10.1016 / j.drudis.2007.01.003. PMC 2072879. PMID 17331889.
- ^ Mason M (srpen 2006). „Jaké důsledky mají profily snášenlivosti antiandrogenů a dalších běžně používaných způsobů léčby rakoviny prostaty na péči o pacienty?“. Journal of Cancer Research and Clinical Oncology. 132 Příloha 1: S27–35. doi:10.1007 / s00432-006-0134-4. PMID 16896883. S2CID 19685819.
- ^ Moilanen AM, Riikonen R, Oksala R, Ravanti L, Aho E, Wohlfahrt G, Nykänen PS, Törmäkangas OP, Palvimo JJ, Kallio PJ (2015). „Objev ODM-201, inhibitoru androgenního receptoru nové generace zaměřeného na rezistenční mechanismy k terapii rakoviny prostaty zaměřené na androgenní signalizaci“. Vědecké zprávy. 5: 12007. Bibcode:2015NatSR ... 512007M. doi:10.1038 / srep12007. PMC 4490394. PMID 26137992.
- ^ Anderson PO, Knoben JE, Troutman WG (22. srpna 2001). Příručka o datech klinických léků. Canadian Medical Association Journal. 128. McGraw Hill Professional. str. 245. ISBN 978-0-07-138942-6. PMC 1875767. PMID 20313924.
Při perorální dávce 50 mg / den dosahuje bikalutamid maximální sérové hladiny 8,9 mg / l (21 μmol / l) 31 hodin po podání dávky v ustáleném stavu. CI (R) -bicalutamidu je 0,32 l / hod. Aktivní (R) -enantiomer bikalutamidu se oxiduje na neaktivní metabolit, který je stejně jako inaktivní (S) -enantiomer glukuronidován a rychle vylučován močí a stolicí.
- ^ Cockshott ID (2004). „Bicalutamid: klinická farmakokinetika a metabolismus“. Klinická farmakokinetika. 43 (13): 855–878. doi:10.2165/00003088-200443130-00003. PMID 15509184.
Tyto údaje naznačují, že přímá glukuronidace je hlavní metabolickou cestou pro rychle vyčištěné (S) -bicalutamid, zatímco hydroxylace následovaná glukuronidací je hlavní metabolickou cestou pro pomalu vylučované (R) -bicalutamid.
- ^ Grosse L, Campeau AS, Caron S, Morin FA, Meunier K, Trottier J, Caron P, Verreault M, Barbier O (srpen 2013). „Enantiomerová selektivní glukuronidace nesteroidního čistého antiandrogenního bikalutamidu lidskými játry a ledvinami: role lidského enzymu UDP-glukuronosyltransferáza (UGT) 1A9“. Základní a klinická farmakologie a toxikologie. 113 (2): 92–102. doi:10.1111 / bcpt.12071. PMC 3815647. PMID 23527766.
- ^ A b McKillop, D .; Boyle, G. W .; Cockshott, I.D .; Jones, D. C .; Phillips, P. J .; Yates, R. A. (1993). "Metabolismus a enantioselektivní farmakokinetika casodexu u člověka". Xenobiotica. 23 (11): 1241–1253. doi:10.3109/00498259309059435. ISSN 0049-8254. PMID 8310708.
- ^ A b Cockshott, I.D .; Cooper, K.J .; Sweetmore, D.S .; Blacklock, N.J .; Denis, L. (1990). "Farmakokinetika kasodexu u pacientů s rakovinou prostaty po jednorázovém a vícečetném dávkování". Evropská urologie. 18 (3): 10–17. doi:10.1159/000463972. ISSN 0302-2838. PMID 2094606.
- ^ A b Tyrrell CJ, Iversen P, Tammela T, Anderson J, Björk T, Kaisary AV, Morris T (září 2006). „Tolerance, účinnost a farmakokinetika bikalutamidu 300 mg, 450 mg nebo 600 mg v monoterapii u pacientů s lokálně pokročilým nebo metastazujícím karcinomem prostaty ve srovnání s kastrací“. BJU International. 98 (3): 563–72. doi:10.1111 / j.1464-410X.2006.06275.x. PMID 16771791. S2CID 41672303.
- ^ A b C Cockshott ID (2004). „Bicalutamid: klinická farmakokinetika a metabolismus“. Klinická farmakokinetika. 43 (13): 855–878. doi:10.2165/00003088-200443130-00003. PMID 15509184.