CYP17A1 - CYP17A1
| Steroid 17-alfa-hydroxyláza / 17,20 lyáza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifikátory | |||||||||
| EC číslo | 1.14.14.19 | ||||||||
| Číslo CAS | 9029-67-8 | ||||||||
| Alt. jména | P450c17, CYP17A1, steroid 17-alfa-hydroxyláza / 17,20 lyáza, CYPXVII, cytochrom P450 17A1, cytochrom p450 XVIIA1, cytochrom P450-C17, cytochrom P450, rodina 17, podčeleď A, polypeptid 1, steroid 17-alfa-monooxygenáza, cytochrom P450c17, 4.1.2.30, 17-alfa-hydroxyprogesteron aldoláza, cytochrom P450, podčeleď XVII (steroid 17-alfa-hydroxyláza), steroid 17 alfa-hydroxyláza / 17,20 lyáza, IPR033282 | ||||||||
| Databáze | |||||||||
| IntEnz | IntEnz pohled | ||||||||
| BRENDA | Vstup BRENDA | ||||||||
| EXPASY | Pohled NiceZyme | ||||||||
| KEGG | Vstup KEGG | ||||||||
| MetaCyc | metabolická cesta | ||||||||
| PRIAM | profil | ||||||||
| PDB struktur | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
Cytochrom P450 17A1, také zvaný steroid 17α-monooxygenáza, 17a-hydroxyláza, 17,20-lyázanebo 17,20-desmoláza, je enzym z hydroxyláza typ, který je u lidí kódován CYP17A1 gen na chromozom 10.[5] Je všudypřítomně exprimován v mnoha tkáních a typech buněk, včetně zona reticularis a zona fasciculata z kůra nadledvin stejně jako gonadal papírové kapesníky.[6][7] Má aktivity 17α-hydroxylázy i 17,20-lyázy a je klíčovým enzymem v steroidogenní cestě, která produkuje progestiny, mineralokortikoidy, glukokortikoidy, androgeny, a estrogeny. Přesněji řečeno, enzym působí pregnenolon a progesteron přidat a hydroxyl (-OH) skupina v poloze uhlíku 17 (C17) steroidního D kruhu (aktivita 17α-hydroxylázy, ES 1.14.14.19 ), nebo jedná podle 17a-hydroxyprogesteron a 17a-hydroxypregnenolon rozdělit postranní řetězec od steroidního jádra (17,20-lyáza aktivita, ES 1.14.14.32 ).[7]
Struktura
Gen
The CYP17A1 Gen leží na chromozomu 10 v pásmu 10q24.3 a obsahuje 8 exony.[5] The cDNA tohoto genu zabírá délku 1527 bp.[8] Tento gen kóduje člena cytochrom P450 nadrodina enzymů. Za proteiny cytochromu P450 se obecně považuje monooxygenázy které katalyzují mnoho reakcí zapojených do metabolismu léčiv a syntézy cholesterol, steroidy, a další lipidy, včetně pozoruhodného štěpení vazby uhlík-uhlík katalyzovaného tímto enzymem.
The CYP17A1 Gen může také obsahovat varianty spojené se zvýšeným rizikem ischemická choroba srdeční.[9][není nutný primární zdroj ]
Protein
CYP17A1 je 57,4 kDa protein, který patří do rodiny cytochromu P450.[10][11] Protein kódovaný jeho cDNA se skládá z 508 aminokyselinové zbytky. Jako enzym obsahuje CYP17A1 Aktivní stránky který se sdružuje s a heme protetická skupina katalyzující biosyntetické reakce.[8] Na základě jeho známých struktur, zatímco je vázán na dva steroidní inhibitory, abirateron a galeteron, CYP17A1 má kanonický cytochrom P450 násobně přítomný v jiných komplexních enzymech P450, které se účastní steroidogeneze nebo cholesterol metabolismus, i když orientuje steroidní ligandy směrem k helixům F a G, kolmo na skupinu hemu, spíše než k listu β1.[12][13]
Výraz
Výraz CYP17A1 byl nalezen ve všech tradičních steroidogenní papírové kapesníky kromě placenta, včetně zona reticularis a zona fasciculata z kůra nadledvin, Leydigovy buňky z testy, thecal buňky z vaječníky, a v poslední době v luteinizováno granulózní buňky v ovariální folikuly.[14] Kromě klasické steroidogenní tkáně byl v buňce detekován také CYP17A1 srdce, ledviny, a tuková tkáň.[14] V plod „V ledvinách byl hlášen CYP17A1, brzlík, a slezina.[14]
Funkce
CYP17A1 je členem cytochrom P450 nadrodina enzymů lokalizovaných v endoplazmatické retikulum. Proteiny v této rodině jsou monooxygenázy, které katalyzují syntézu cholesterol, steroidy a další lipidy a podílejí se na metabolismu léků.[5] CYP17A1 má jak aktivitu 17α-hydroxylázy (ES 1.14.14.19 ) a aktivita 17,20-lyázy (ES 1.14.14.32 ). Aktivita 17α-hydroxylázy CYP17A1 je vyžadována pro generování glukokortikoidy jako je kortizol, ale pro produkci enzymu CYP17A1 jsou vyžadovány aktivity hydroxylázy a 17,20-lyázy. androgenní a estrogenní sexuální steroidy převodem 17a-hydroxypregnenolon na dehydroepiandrosteron (DHEA).[15] Mutace v tomto genu jsou spojeny s izolovaným nedostatkem steroid-17α-hydroxylázy, nedostatkem 17α-hydroxylázy / 17,20-lyázy, pseudohermafroditismus, a adrenální hyperplazie.[5]
Dále je aktivita 17,20-lyázy závislá na cytochromu Oxidoreduktáza P450 (POR) cytochrom b5 (CYB5) a fosforylace.[16][17][18] Cytochrom b5 působí jako zprostředkovatel aktivity 17,20 lyázy CYP17A1 a může darovat druhý elektron některým P450. U lidí výroba testosteron prostřednictvím pregnenolonu to17-OHPreg a DHEA pomocí CYP17A1 vyžaduje POR.[19] Lidský protein CYP17A1 je fosforylovaný na serinových a threoninových zbytcích a cAMP-dependentní protein kináza. Fosforylace proteinu zvyšuje aktivitu 17,20-lyázy, zatímco defosforylace tuto aktivitu prakticky eliminuje.[18]
Klinický význam
Mutace v tomto genu jsou spojeny se vzácnými formami vrozená hyperplázie nadledvin konkrétně Nedostatek 17α-hydroxylázy / nedostatek 17,20-lyázy a izolovaný nedostatek 17,20-lyázy.[20]
U lidí je gen CYP17A1 do značné míry spojen s endokrinními účinky a metabolizmem steroidních hormonů.[21][22][23] Kromě toho jsou mutace v genu CYP17A1 spojeny se vzácnými formami vrozená hyperplázie nadledvin zejména nedostatek 17a-hydroxylázy / nedostatek 17,20-lyázy a izolovaný nedostatek 17,20-lyázy. Celkově je CYP17A1 důležitým cílem pro inhibici v léčbě rakoviny prostaty, protože produkuje androgen, který je nezbytný pro růst nádorových buněk.[24][25] Snížená aktivita enzymu CYP17A1 souvisí s neplodností v důsledku hypogonadotropního hypogonadismu. U žen je zastavena folikulogeneze, u mužů atrofie varlat s proliferací intersticiálních buněk a zastavená spermatogeneze. Ačkoli jsou obecně anovulační, existují případové zprávy o ženách s nedostatkem 17α-hydroxylázy, které podstoupily spontánní menarche s cyklickým menstruačním cyklem.[26]
Klinický marker
Studie multi-lokusového skóre genetického rizika založená na kombinaci 27 lokusů, včetně genu CYP17A1, identifikovala jedince se zvýšeným rizikem jak příhodných, tak rekurentních příhod ischemické choroby srdeční, stejně jako zvýšený klinický přínos léčby statiny. Studie byla založena na komunitní kohortní studii (Malmova dieta a rakovina) a čtyřech dalších randomizovaných kontrolovaných studiích kohort primární prevence (JUPITER a ASCOT) a kohort sekundární prevence (CARE a PROVE IT-TIMI 22).[9]
Jako drogový cíl
Inhibitory CYP17A1
V současné době,[když? ] FDA schválila pouze jeden inhibitor CYP17A1, abirateron, který obsahuje steroidní lešení podobné endogenním substrátům CYP17A1. Abirateron je strukturně podobný substrátům jiných enzymů cytochromu P450 zapojených do steroidogeneze a interference může představovat odpovědnost z hlediska vedlejších účinků. Použitím nesteroidní lešení předpokládá, že umožní návrh sloučenin, které selektivněji interagují s CYP17A1.[25] Silné inhibitory enzymu CYP17A1 poskytují poslední linii obrany proti ektopické androgenezi u pokročilého karcinomu prostaty.[27]
Droga abirateronacetát, který se používá k léčbě rakovina prostaty rezistentní na kastraci, blokuje biosyntézu androgenů inhibicí enzymu CYP17A1. Abirateronacetát se váže na aktivní místo enzymu[28] a koordinuje heme železo přes jeho pyridinový dusík, napodobující substrát.[29]
Od roku 2014 galeteron byl v fáze III klinické testy pro rakovina prostaty rezistentní na kastraci.[30]
Ketokonazol je starší Inhibitor CYP17A1 to je nyní málo používané. Ketokonazol však kompetitivně inhibuje CYP17A1, proto jeho účinnost bude záviset na koncentraci ketokonazolu. To je na rozdíl od abirateronacetát, který trvale (spíše než kompetitivně) deaktivuje CYP17A1, jakmile se na něj naváže.
Seviteronel (VT-464) je román Inhibitor CYP17A1 jehož cílem je vyhnout se souběžnému podávání glukokortoidové terapie.[31] V roce 2010 prošla různými fázemi klinických studií a preklinických modelů jako lék proti rakovině prostaty nebo rakovině prsu.[32][33][34]
Steroidogeneze
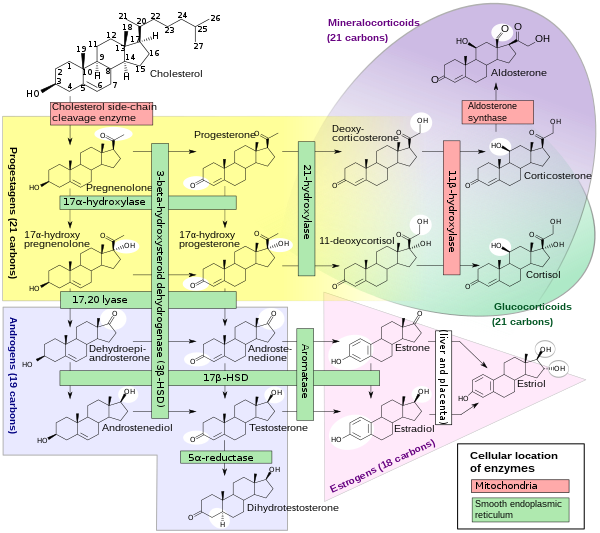 Steroidogeneze, zobrazující na levé straně obě reakce 17a-hydroxylázy a obě akce 17, 20 lyázy. |
Další obrázky

Číslování steroidů
Viz také
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000148795 - Ensembl, Květen 2017
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000003555 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ A b C d „CYP17A1 cytochrom P450 rodina 17 podrodina A člen 1 [Homo sapiens (člověk)] - gen - NCBI“. www.ncbi.nlm.nih.gov. Citováno 2016-09-27.
- ^ „BioGPS - váš systém genového portálu“. biogps.org. Citováno 2016-10-11.
- ^ A b Boulpaep EL; Boron, WF (2005). Lékařská fyziologie: buněčný a molekulární přístup. St. Louis, Mo: Elsevier Saunders. str. 1180. ISBN 1-4160-2328-3.
- ^ A b Vasaitis TS, Bruno RD, Njar VC (květen 2011). „Inhibitory CYP17 pro léčbu rakoviny prostaty“. The Journal of Steroid Biochemistry and Molecular Biology. 125 (1–2): 23–31. doi:10.1016 / j.jsbmb.2010.11.005. PMC 3047603. PMID 21092758.
- ^ A b Mega JL, Stitziel NO, Smith JG, Chasman DI, Caulfield MJ, Devlin JJ, Nordio F, Hyde CL, Cannon CP, Sacks FM, Poulter NR, Sever PS, Ridker PM, Braunwald E, Melander O, Kathiresan S, Sabatine MS (Červen 2015). „Genetické riziko, příhody ischemické choroby srdeční a klinický přínos léčby statiny: analýza studií primární a sekundární prevence“. Lanceta. 385 (9984): 2264–71. doi:10.1016 / S0140-6736 (14) 61730-X. PMC 4608367. PMID 25748612.
- ^ „CYP17A1 - steroid 17-alfa-hydroxyláza / 17,20 lyáza - Homo sapiens (člověk) - gen a protein CYP17A1“. www.uniprot.org. Citováno 2016-10-11.
- ^ Estrada DF, Laurence JS, Scott EE (únor 2016). „Interakce cytochromu P450 17A1 s doménou FMN jeho reduktázy charakterizované NMR“. The Journal of Biological Chemistry. 291 (8): 3990–4003. doi:10,1074 / jbc.M115,677294. PMC 4759177. PMID 26719338.
- ^ DeVore NM, Scott EE (únor 2012). „Struktury cytochromu P450 17A1 s léky proti rakovině prostaty abirateron a TOK-001“. Příroda. 482 (7383): 116–9. Bibcode:2012Natur.482..116D. doi:10.1038 / příroda10743. PMC 3271139. PMID 22266943.
- ^ Petrunak EM, DeVore NM, Porubsky PR, Scott EE (listopad 2014). "Struktury lidského steroidogenního cytochromu P450 17A1 se substráty". The Journal of Biological Chemistry. 289 (47): 32952–64. doi:10.1074 / jbc.M114.610998. PMC 4239641. PMID 25301938.
- ^ A b C Storbeck KH, Swart P, Africander D, Conradie R, Louw R, Swart AC (2011). „16α-hydroxyprogesteron: původ, biosyntéza a interakce s receptory“. Mol. Buňka. Endokrinol. 336 (1–2): 92–101. doi:10.1016 / j.mce.2010.11.016. PMID 21095220. S2CID 5503049.
- ^ DeVore NM, Scott EE (únor 2012). „Struktury cytochromu P450 17A1 s léky proti rakovině prostaty abirateron a TOK-001“. Příroda. 482 (7383): 116–9. Bibcode:2012Natur.482..116D. doi:10.1038 / příroda10743. PMC 3271139. PMID 22266943.
- ^ Udhane SS, Dick B, Hu Q, Hartmann RW, Pandey AV (září 2016). „Specifičnost inhibitorů CYP prostaty rakoviny prostaty na biosyntézu androgenu“. Sdělení o biochemickém a biofyzikálním výzkumu. 477 (4): 1005–10. doi:10.1016 / j.bbrc.2016.07.019. PMID 27395338.
- ^ Pandey AV, Miller WL (duben 2005). „Regulace aktivity 17,20 lyázy cytochromem b5 a serinovou fosforylací P450c17“. The Journal of Biological Chemistry. 280 (14): 13265–71. doi:10,1074 / jbc.M414673200. PMID 15687493.
- ^ A b Zhang LH, Rodriguez H, Ohno S, Miller WL (listopad 1995). "Serinová fosforylace lidského P450c17 zvyšuje aktivitu 17,20-lyázy: důsledky pro adrenarche a syndrom polycystických vaječníků". Sborník Národní akademie věd Spojených států amerických. 92 (23): 10619–23. Bibcode:1995PNAS ... 9210619Z. doi:10.1073 / pnas.92.23.10619. PMC 40663. PMID 7479852.
- ^ Fukami M, Homma K, Hasegawa T, Ogata T (duben 2013). „Backdoor pathway for dihydrotestosterone biosynthesis: implications for normal and abnormal human sex development“. Dynamika vývoje. 242 (4): 320–9. doi:10.1002 / dvdy.23892. PMID 23073980. S2CID 44702659.
- ^ „Entrez Gene: CYP17A1 cytochrom P450, rodina 17, podčeleď A, polypeptid 1“.
- ^ Ma YN, Cao CY, Wang QW, Gui WJ, Zhu GN (říjen 2016). "Účinky azocyklotinu na genovou transkripci a steroidní metabolom osy hypotalamus-hypofýza-gonáda a jejich důsledky pro reprodukci u zebrafish (Danio rerio)". Vodní toxikologie. 179: 55–64. doi:10.1016 / j.aquatox.2016.08.006. PMID 27571716.
- ^ Legendre A, Elie C, Ramambason C, Manens L, Souidi M, Froment P, Tack K (srpen 2016). "Endokrinní účinky celoživotního vystavení nízkodávkovanému ochuzenému uranu na funkce varlat u dospělých krys". Toxikologie. 368-369: 58–68. doi:10.1016 / j.tox.2016.08.014. PMID 27544493.
- ^ Yadav R, Petrunak EM, Estrada DF, Scott EE (srpen 2016). „Strukturální pohledy na funkci steroidogenního cytochromu P450 17A1“. Molekulární a buněčná endokrinologie. 441: 68–75. doi:10.1016 / j.mce.2016.08.035. PMC 5235955. PMID 27566228.
- ^ Kostin VA, Zolottsev VA, Kuzikov AV, Masamrekh RA, Shumyantseva VV, Veselovsky AV, Stulov SV, Novikov RA, Timofeev VP, Misharin AY (listopad 2016). "Oxazolinylové deriváty [17 (20) E] -21-norpregnenu lišící se strukturou kruhů A a B. Facilová syntéza a inhibice katalytické aktivity CYP17A1". Steroidy. 115: 114–122. doi:10.1016 / j.steroids.2016.06.002. PMID 27505042. S2CID 205256638.
- ^ A b Bonomo S, Hansen CH, Petrunak EM, Scott EE, Styrishave B, Jørgensen FS, Olsen L (2016-01-01). „Slibné nástroje ve výzkumu rakoviny prostaty: selektivní nesteroidní inhibitory cytochromu P450 17A1“. Vědecké zprávy. 6: 29468. Bibcode:2016NatSR ... 629468B. doi:10.1038 / srep29468. PMC 4942611. PMID 27406023.
- ^ Acién P, Acién M (listopad 2020). „Poruchy pohlavního vývoje: klasifikace, hodnocení a dopad na plodnost“. Journal of Clinical Medicine. 9 (11). doi:10,3390 / jcm9113555. PMID 33158283.
- ^ Bordeau BM, Ciulla DA, Callahan BP (září 2016). „Ježkové proteiny konzumují steroidní antagonisty CYP17A1: potenciální terapeutický význam u pokročilého karcinomu prostaty“. ChemMedChem. 11 (18): 1983–6. doi:10.1002 / cmdc.201600238. PMC 5588864. PMID 27435344.
- ^ Fernández-Cancio, Mónica; Camats, Núria; Flück, Christa E .; Zalewski, Adam; Dick, Bernhard; Frey, Brigitte M .; Monné, Raquel; Torán, Núria; Audí, Laura (29.04.2018). „Mechanismus dvojí činnosti lidského CYP17A1 a vazby na lék proti rakovině prostaty Abirateron odhalen novou mutací V366M způsobující nedostatek 17,20 lyázy“. Léčiva. 11 (2): 37. doi:10,3390 / ph11020037. PMC 6027421. PMID 29710837.
- ^ PDB: 3ruk; DeVore NM, Scott EE (únor 2012). „Struktury cytochromu P450 17A1 s léky proti rakovině prostaty abirateron a TOK-001“. Příroda. 482 (7383): 116–9. Bibcode:2012Natur.482..116D. doi:10.1038 / příroda 10743. PMC 3271139. PMID 22266943.
- ^ „Reformulovaný galeteron společnosti Tokai Pharmaceuticals prokazuje výrazné snížení PSA u pacientů s pokročilým karcinomem prostaty“ (Tisková zpráva). Tokai Pharmaceuticals. 29. ledna 2014.
- ^ Bird IM, Abbott DH (říjen 2016). „Honba za selektivním inhibitorem lyázy 17,20; poučení z přírody“. The Journal of Steroid Biochemistry and Molecular Biology. 163: 136–46. doi:10.1016 / j.jsbmb.2016.04.021. PMC 5046225. PMID 27154414.
VT464 je další nedávno vyvinutá sloučenina navržená tak, aby působila jako selektivní inhibitor lyázy, a na podporu tohoto tvrzení jsou ve veřejné doméně k dispozici úplnější údaje. Přezkoumání zveřejněných předběžných údajů naznačuje, že IC50 pro aktivitu lidské CYP17 lyázy je desetkrát nižší než u hydroxylázy 15 a u nelidských primátů byl VT464 schopen potlačit cirkulující testosteron stejně účinně jako abirateron, ale s minimálně depresivním kortizolem (zbývající při 82% kontrole ve srovnání pouze s 9% u aberateronu) a bez souvisejícího zvýšení pregnenolonu, progesteronu a mineralokortikoidů, které bylo jinak pozorováno u abirateronu. Stejně jako Galateron se i VT464 používá v klinických studiích bez současného podávání prednisonu. Spolu s jasným nedostatkem potlačení cirkulujícího kortizolu u primátů jiných než lidská tato data tvrdí, že VT464 může být skutečně selektivním inhibitorem 17,20 lyázy.
- ^ Sharma VR, Sharma DK, Navnit M, Anil KS, Batra N (2010). „Nové a možné terapie léčby rakoviny prsu: aktualizace pro onkology“. Rakovina prsu. 2. doi:10.2147 / ECTTS71781.
- ^ Madan RA, Schmidt KT, Karzai F, Peer CJ, Cordes LM, Chau CH, Steinberg SM, Owens H, Eisner J, Moore WR, Dahut WL, Gulley JL, Figg WD (srpen 2020). „Fáze 2 Studie seviteronelu (INO-464) u pacientů s metastatickým kastrací rezistentním karcinomem prostaty po léčbě enzalutamidem“. Klinická urogenitální rakovina. 18 (4): 258–267.e1. doi:10.1016 / j.clgc.2019.11.002. PMID 32327394.
- ^ Peer CJ, Schmidt KT, Kindrick JD, Eisner JR, Brown VV, Baskin-Bey E, Madan R, Figg WD (říjen 2019). „Populační farmakokinetická analýza perorálního CYP17 lyázy a inhibitoru androgenního receptoru seviteronelu u pacientů s pokročilým / metastatickým kastrací rezistentním karcinomem prostaty nebo karcinomem prsu“. Chemoterapie rakoviny a farmakologie. 84 (4): 759–770. doi:10.1007 / s00280-019-03908-0. PMID 31367790.
Další čtení
- Miura K, Yasuda K, Yanase T, Yamakita N, Sasano H, Nawata H, Inoue M, Fukaya T, Shizuta Y (říjen 1996). „Mutace genu pro cytochrom P-45017 alfa (CYP17) u japonského pacienta, u kterého bylo dříve hlášeno, že má hyperaldosteronismus reagující na glukokortikoidy: s přehledem japonských pacientů s mutacemi CYP17“. The Journal of Clinical Endocrinology and Metabolism. 81 (10): 3797–801. doi:10.1210 / jcem.81.10.8855840. PMID 8855840.
- Miller WL, Geller DH, Auchus RJ (1999). "Molekulární základ izolovaného nedostatku 17,20 lyázy". Endokrinní výzkum. 24 (3–4): 817–25. doi:10.3109/07435809809032692. PMID 9888582.
- Strauss JF (listopad 2003). "Některé nové myšlenky na patofyziologii a genetiku syndromu polycystických vaječníků". Annals of the New York Academy of Sciences. 997 (1): 42–8. Bibcode:2003NYASA.997 ... 42S. doi:10.1196 / annals.1290.005. PMID 14644808. S2CID 23559461.
- Haider SM, Patel JS, Poojari CS, Neidle S (červenec 2010). „Molekulární modelování na inhibičních komplexech a dynamika aktivního místa cytochromu P450 C17, cíl léčby rakoviny prostaty“. Journal of Molecular Biology. 400 (5): 1078–98. doi:10.1016 / j.jmb.2010.05.069. PMID 20595043.
externí odkazy
- CYP17A1 + protein, + člověk v americké národní lékařské knihovně Lékařské předměty (Pletivo)
- Člověk CYP17A1 umístění genomu a CYP17A1 stránka s podrobnostmi o genu v UCSC Genome Browser.