TRPM8 - TRPM8
Přechodný kanál potenciálního kationového kanálu podčeleď M (melastatin) člen 8 (TRPM8), také známý jako studený a mentolový receptor 1 (CMR1), je a protein že u lidí je kódován TRPM8 gen.[5][6] Kanál TRPM8 je primárním molekulárním měničem studené somatosenzace u lidí.[5][7] Mentol je slabý agonista KOR[8] kvůli jeho antinociceptivní nebo blokování bolesti, účinky u potkanů. Kromě toho mohou mincovny znecitlivět oblast aktivací TRPM8 receptory („studený“ / mentolový receptor).[9]
Struktura
Kanál TRPM8 je homotetramer, složený ze čtyř identických podjednotek s a transmembránová doména se šesti šroubovicemi (S1–6). První čtyři, S1–4, fungují jako napěťový senzor a povolit vazbu mentol, icilin a podobný kanál agonisté. S5 a S6 a spojovací smyčka, která je také součástí struktury, tvoří póry, neselektivní kationtový kanál, který se skládá z vysoce konzervativního hydrofobní region, Pro vysokou úroveň specificity při reakci na výsledný tok iontů na chladné a mentolové podněty je zapotřebí řada různých složek.[10][11]
Funkce
TRPM8 je iontový kanál: při aktivaci umožňuje zadání Na+ a Ca.2+ ionty do buňky, což vede k depolarizaci a generování akčního potenciálu. Signál je veden primárními aferenty (delta typu C a A), což nakonec vede k pocitu chladu a bolesti za studena.[5]
Protein TRPM8 je exprimován v senzorických neuronech a je aktivován nízkými teplotami a chladicími činidly, jako jsou mentol a icilin zatímco WS-12 a CPS-369 jsou nejselektivnějšími agonisty TRPM8.[12][13]
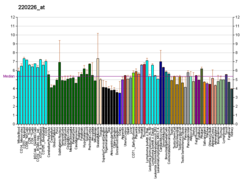
TRPM8 je také vyjádřen v prostata, plíce a močový měchýř, kde jeho funkce není dobře známa.
Role v nervovém systému
The přechodný kanál potenciálního receptoru (TRP) nadčeleď, která zahrnuje mentol (TRPM8) a kapsaicin receptory (TRPV1 ), slouží různým funkcím v obvodový a centrální nervové systémy. V periferním nervovém systému reagují TRP na podněty z teplota, tlak, zánětlivé látky, a receptor aktivace. Role centrálního nervového systému receptorů zahrnují růst neuritů, signalizaci receptorů a smrt excitoxických buněk v důsledku škodlivých podnětů.[14]
McKemy et al., 2002 poskytl některé z prvních důkazů o existenci chladu aktivovaného receptoru v celém somatosenzorickém systému savců.[5] Použitím zobrazování vápníku a svorka na základě přístupů vykázaly odezvu v hřbetní kořenový ganglion (DRG) neurony vystavení chladu, teplotě 20 ° C nebo nižší teplotě, vede k reakci na příliv vápníku. Ukázalo se, že tento receptor reaguje jak na nízké teploty, tak na mentol a podobné nyní známé agonisty receptoru TRPM8. Funguje ve spojení s TRPV1 Receptor udržuje udržovatelný prahový teplotní rozsah, ve kterém jsou naše buňky pohodlné a naše vnímání těchto stimulů nastává v míše a mozku, které integrují signály z různých vláken různé citlivosti na teplotu. Aplikace mentolu na kůži nebo sliznice vede přímo k membráně depolarizace, následovaný přílivem vápníku přes napěťově závislé vápníkové kanály, poskytující důkazy o úloze TRPM8 a dalších TRP receptorů při zprostředkování naší smyslové interakce s prostředím v reakci na chlad stejným způsobem jako v reakci na mentol.[15]
Vlastnosti
citlivost na pH
Na rozdíl od TRPV1 (kapsaicin ) receptor, který je potencován nízkým pH, kyselé Bylo prokázáno, že podmínky inhibují TRPM8 Ca.2+ reakce na mentol a icilin (an agonista receptoru mentolu). Předpokládá se TRPV1 a receptory TRPM8 působí společně v reakci na zánětlivé stavy: TRPV1 působením protonů zvyšuje pocit pálení bolesti, zatímco kyselost inhibuje TRPM8, aby blokovala příjemnější pocit chladu ve zoufalejších případech bolesti.[16]
Senzibilizace
Byly publikovány četné studie zkoumající účinek aplikace L-mentolu jako modelu pro senzibilizaci TRPM8.[5][17] Primární shoda bylo zjištěno, že senzibilizace TRPM8 zvyšuje pocit bolesti za studena, také známý jako chlad hyperalgezie.[5] Experiment byl proveden v dvojitě zaslepený obousměrná zkřížená studie pomocí aplikace 40% L-mentolu na předloktí s použitím ethanolu jako kontroly. Aktivace TRPM8-receptorového kanálu (primární mentolový receptorový kanál) vedla ke zvýšené senzibilizaci na mentolový stimul. Wasner, aby prozkoumal mechanismy této senzibilizace et al., 2004, provedeno Vlákno blokáda vedení povrchového radiálního nervu u jiné skupiny subjektů. To nakonec snížilo pocit chladu a hyperalgezie vyvolaný mentolem, protože blokování vedení vlákna A mělo za následek inhibici třídy nervové vlákno skupiny C. nociceptory potřebné k přenosu pocitu bolesti. Došli k závěru, že mentol senzitizuje periferní C nociceptory citlivé na chlad a aktivuje delta vlákna specifická pro chlad.[5][7][18]
Desenzibilizace
Jak je běžné v reakci na mnoho dalších smyslových stimulů, existuje mnoho experimentálních důkazů o desenzibilizaci lidské reakce receptorů TRPM8 na mentol.[5] Testování zahrnující podávání mentolu a nikotin - cigarety obsahující nekuřáky, které po počáteční senzibilizaci vyvolaly to, co klasifikovaly jako dráždivou reakci, vykazovaly u subjektů v průběhu času klesající reakci, což vedlo k výskytu desenzibilizace. Ethanol, s podobnými dráždivými a desenzibilizačními vlastnostmi, byl použit jako kontrola pro nikotin, aby se odlišil od reakce vyvolané mentolem. Bylo pozorováno, že mentolový receptor senzibilizuje nebo desenzibilizuje na základě buněčných podmínek a mentol produkuje zvýšenou aktivitu v Ca2+- napěťově řízené kanály, které nejsou v ethanolu vidět, cyklohexanol a další dráždivé kontroly naznačující specifický molekulární receptor. Dessirier et al., 2001, také tvrdí, že ke křížové desenzibilizaci mentolových receptorů může dojít neznámými molekulárními mechanismy, i když předpokládají význam Ca2 + při snižování excitability buněk podobným způsobem jako v kapsaicin receptor.[19]
Mutageneze protein kináza C. fosforylační místa v TRPM8 (seriny a threoniny divokého typu nahrazené v mutantech alaninem) snižují desenzibilizující odpověď.[20]
Křížová desenzibilizace
Útes et al., 1994, provedli studii, jejímž cílem bylo zjistit více o vlastnostech receptoru mentolu a o tom, zda má mentol schopnost křížové desenzitizace s jinými receptory dráždivých chemických látek. Kapsaicin bylo známo, že zkříženě znecitlivuje s jinými dráždivými agonisty, kde o mentolu nebyly známy stejné informace. Studie zahrnovala subjekty, které delší dobu hledaly mentol nebo kapsaicin v pravidelných intervalech. O křížové desenzibilizaci došlo ke třem významným závěrům: 1) Obě chemikálie samy desenzibilizují, 2) receptory mentolu mohou znecitlivit v reakci na kapsaicin a nejnověji 3) receptory kapsaicinu jsou senzibilizovány v reakci na mentol.[21]
Ligandy
Agonisté
Při hledání sloučenin, které aktivovaly chladný receptor TRPM8, byly z odvětví vonných látek vyhledávány sloučeniny, které vyvolávají pocit ochlazení. Ze 70 relevantních sloučenin následujících 10 vyvolalo související [Ca2 +] - zvýšení odpovědi v buňkách HEK293 transfekovaných mTRPM8 použitých k identifikaci agonistů. Mezi experimentálně identifikované a běžně používané agonisty receptoru mentolu patří linalool, geraniol, hydroxy-citronellal, icilin, WS-12, Frescolat MGA, Frescolat ML, PMD 38, Coolact P, M8-Ag a Chladicí agent 10.[16][17]
Antagonisté
BCTC, thio-BCTC, kapsazepin a M8-An[22] byly identifikovány jako antagonisté receptoru TRPM8. Tito antagonisté fyzicky blokují receptor pro chlad a mentol vazbou na S1-S4 snímání napětí doména, která brání reakci.[16]
- PF 05105679 cas: [1398583-31-7].
- M8 B
- AMTB
- 5-benzyloxytryptamin[23]
Klinický význam
K vyvolání se tradičně používají studené záplaty analgezie nebo úleva od bolesti způsobené traumatickým zraněním.[24] Základní mechanismus analgezie vyvolané chladem zůstal nejasný až do objevení TRPM8.
Jedna výzkumná skupina uvedla, že TRPM8 je aktivován chemickými chladicími činidly (např mentol ) nebo když okolní teploty klesnou pod přibližně 26 ° C, což naznačuje, že zprostředkovává detekci chladných tepelných stimulů primárními aferentními senzorickými neurony aferentní nervová vlákna.[25]
Tři nezávislé výzkumné skupiny uvedly, že myši, kterým chybí funkční genová exprese TRPM8, mají vážnou poruchu v schopnosti detekovat Studený teploty.[26] Je pozoruhodné, že tato zvířata mají nedostatek mnoha různých aspektů signalizace chladu, včetně vnímání chladu a škodlivého chladu, senzibilizace vyvolané zraněním na chlad a analgezie vyvolané ochlazením. Tato zvířata poskytují velký přehled o molekulárních signálních drahách, které se účastní detekce chladných a bolestivých podnětů. Mnoho výzkumných skupin, ať už na univerzitách nebo ve farmaceutických společnostech, se nyní aktivně podílí na hledání selektivního TRPM8 ligandy být použit jako nová generace neuropatický analgetika.[17][22]
Nízké koncentrace agonistů TRPM8, jako je mentol (nebo icilin), byly za určitých podmínek shledány jako antihyperalgetické,[27] zatímco vysoké koncentrace mentolu způsobily u zdravých dobrovolníků studenou i mechanickou hyperalgezii.[18]
TRPM8 knockout myši nejen naznačil, že TRPM8 je vyžadován pro pocit chladu, ale také odhalil, že TRPM8 zprostředkovává jak chlad, tak mechanické alodynie na modelech neuropatické bolesti u hlodavců.[28] Dále se nedávno ukázalo, že antagonisté TRPM8 jsou účinní při zvrácení zavedené bolesti v modelech neuropatické a viscerální bolesti.[29][22]
Upregulace TRPM8 v tkáních močového měchýře koreluje s bolestí u pacientů s bolestivými syndromy močového měchýře.[30] Kromě toho je TRPM8 upregulován v mnoha buněčných liniích rakoviny prostaty a Dendreon / Genentech usilují o agonistický přístup k indukci apoptózy a smrti buněk rakoviny prostaty.[31]
Role v rakovině
Kanály TRPM8 mohou být cílem léčby rakovina prostaty. TRPM8 je androgen závislý Ca2+ kanál nutný pro rakovina prostaty buňky přežít a růst. Imunfluorescence ukázala expresi proteinu TRPM8 v ER a plazmatické membráně reagující na androgen LNCaP buněčná linie. TRPM8 byl exprimován v buňkách necitlivých na androgeny, ale nebylo prokázáno, že je to nutné pro jejich přežití. Vyřazením TRPM8 s siRNA cílení TRPM8 mRNA nezbytnost receptoru TRPM8 byla prokázána v rakovinných buňkách závislých na androgenu. To má užitečné důsledky, pokud jde o genová terapie, protože u mužů s rakovinou prostaty je tak málo možností léčby. Jako androgenem regulovaný protein, jehož funkce se ztrácí při vývoji rakoviny v buňkách, se protein TRPM8 zdá být obzvláště důležitý při regulaci hladin vápníku a nedávno byl navržen jako zaměření nových léků používaných k léčbě rakoviny prostaty.[32]
Viz také
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000144481 - Ensembl, Květen 2017
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000036251 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ A b C d E F G h Andersen HH, Møller G, Winter R, Eskelund P, Arendt-Nielsen L (srpen 2013). "Přehled topického vysoce koncentrovaného L-mentolu jako translačního modelu studené alodýnie a hyperalgezie". European Journal of Pain. 18 (3): 315–325. doi:10.1002 / j.1532-2149.2013.00380.x. PMID 23963768. S2CID 35385748.
- ^ Clapham DE, Julius D, Montell C, Schultz G (prosinec 2005). „International Union of Pharmacology. XLIX. Nomenklatura a vztahy struktury a funkce přechodných kanálů potenciálních receptorů“. Farmakologické recenze. 57 (4): 427–50. doi:10.1124 / pr.57.4.6. PMID 16382100. S2CID 17936350.
- ^ A b Olsen RV, Andersen HH, Møller HG, Eskelund PW, Arendt-Nielsen L (2014). „Somatosenzorické a vazomotorické projevy individuální a kombinované stimulace TRPM8 a TRPA1 pomocí topického L-mentolu a trans-cinnamaldehydu u zdravých dobrovolníků“. Eur J Pain. 18 (9): 1333–42. doi:10.1002 / j.1532-2149.2014.494.x. PMID 24664788. S2CID 34286049.
- ^ Galeotti N, Di Cesare Mannelli L, Mazzanti G, Bartolini A, Ghelardini C (duben 2002). "Mentol: přírodní analgetická sloučenina". Neurovědy Dopisy. 322 (3): 145–8. doi:10.1016 / S0304-3940 (01) 02527-7. PMID 11897159. S2CID 33979563.
- ^ Werkheiser JL, Rawls SM, Cowan A (říjen 2006). „Agonisté opioidního receptoru Mu a kappa antagonizují otřesy mokrého psa vyvolané icilinem u potkanů“. European Journal of Pharmacology. 547 (1–3): 101–5. doi:10.1016 / j.ejphar.2006.07.026. PMID 16945367.
- ^ Pedretti A, Marconi C, Bettinelli I, Vistoli G (květen 2009). "Srovnávací modelování kvartérní struktury pro lidský kanál TRPM8 a analýza jeho vazebných vlastností". Biochim. Biophys. Acta. 1788 (5): 973–82. doi:10.1016 / j.bbamem.2009.02.007. PMID 19230823.
- ^ Diver MM, Cheng Y, Julius D (September 2019). „Strukturální pohledy na inhibici a desenzibilizaci TRPM8“. Věda. 365 (6460): 1434–1440. doi:10.1126 / science.aax6672. PMC 7262954. PMID 31488702.
- ^ Sherkheli M.A .; et al. (2007). „Selektivní agonisté TRPM8: nová skupina neurofatických analgetik“. FEBS Journal. 274 (s1): 232. doi:10.1111 / j.0014-2956.2007.05861_4.x. PMC 7163963.
- ^ Sherkheli M.A .; G G; Ak VE; Jf D; H H (říjen 2008). „Derivát mentolu WS-12 selektivně aktivuje iontové kanály přechodného receptorového potenciálu melastatin-8 (TRPM8)“. Pak J Pharm Sci. 21 (4): 370–8. PMID 18930858.
- ^ Moran MM, Xu H, Clapham DE (červen 2004). "TRP iontové kanály v nervovém systému". Curr. Opin. Neurobiol. 14 (3): 362–9. doi:10.1016 / j.conb.2004.05.003. PMID 15194117. S2CID 2410787.
- ^ McKemy DD, Neuhausser WM, Julius D (březen 2002). „Identifikace studeného receptoru odhaluje obecnou roli kanálů TRP v termosenzaci.“ Příroda. 416 (6876): 52–8. doi:10.1038 / příroda719. PMID 11882888. S2CID 4340358.
- ^ A b C Behrendt HJ, Germann T, Gillen C, Hatt H, Jostock R (únor 2004). „Charakterizace myšího studeného-mentolového receptoru TRPM8 a vaniloidního receptoru typu 1 VR1 pomocí testu čtečky fluorometrických zobrazovacích desek (FLIPR)“. Br. J. Pharmacol. 141 (4): 737–45. doi:10.1038 / sj.bjp.0705652. PMC 1574235. PMID 14757700.
- ^ A b C Patel R, Gonçalves L, Leveridge M, Mack SR, Hendrick A, Brice NL, Dickenson AH (říjen 2014). „Antihyperalgetické účinky nového agonisty TRPM8 u neuropatických potkanů: srovnání s topickým mentolem“. Bolest. 155 (10): 2097–107. doi:10.1016 / j.pain.2014.07.022. PMC 4220012. PMID 25083927.
- ^ A b Wasner G, Schattschneider J, Binder A, Baron R (květen 2004). „Aktuální mentol - lidský model bolesti za studena aktivací a senzibilizací C nociceptorů“. Brain: Journal of Neurology. 127 (Pt 5): 1159–71. doi:10.1093 / mozek / awh134. PMID 14985268.
- ^ Dessirier JM, O'Mahony M, Carstens E (květen 2001). „Orální dráždivé vlastnosti mentolu: senzibilizující a desenzibilizující účinky opakované aplikace a křížová desenzibilizace na nikotin“. Physiol. Chovat se. 73 (1–2): 25–36. doi:10.1016 / S0031-9384 (01) 00431-0. PMID 11399291. S2CID 11433605.
- ^ Abe J, Hosokawa H, Sawada Y, Matsumura K, Kobayashi S (2006). „Aktivace PKC závislá na Ca2 + zprostředkovává mentolem indukovanou desenzibilizaci přechodného potenciálu receptoru M8“. Neurosci. Lett. 397 (1–2): 140–4. doi:10.1016 / j.neulet.2005.12.005. PMID 16380208. S2CID 23638727.
- ^ Cliff MA, Green BG (březen 1996). "Senzibilizace a desenzibilizace vůči kapsaicinu a mentolu v ústní dutině: interakce a individuální rozdíly". Physiol. Chovat se. 59 (3): 487–94. doi:10.1016/0031-9384(95)02089-6. PMID 8700951. S2CID 45406823.
- ^ A b C Patel R, Gonçalves L, Newman R, Jiang FL, Goldby A, Reeve J, Hendrick A, Teall M, Hannah D, Almond S, Brice N, Dickenson AH (duben 2014). „Nový antagonista TRPM8 tlumí přecitlivělost na chlad po poranění periferních nervů u potkanů“. The Journal of Pharmacology and Experimental Therapeutics. 349 (1): 47–55. doi:10.1124 / jpet.113.211243. PMID 24472724. S2CID 10407715.
- ^ DeFalco, Jeff; Steiger, Daniel; Dourado, Michelle; Emerling, Daniel; Duncton, Matthew A.J. (Prosinec 2010). „5-Benzyloxytryptamin jako antagonista TRPM8“. Dopisy o bioorganické a léčivé chemii. 20 (23): 7076–7079. doi:10.1016 / j.bmcl.2010.09.099. PMID 20965726.
- ^ Sikandar S, Patel R, Patel S, Sikander S, Bennett DL, Dickenson AH (září 2013). „Geny, molekuly a pacienti - nově se objevující témata pro vedení výzkumu klinické bolesti“. European Journal of Pharmacology. 716 (1–3): 188–202. doi:10.1016 / j.ejphar.2013.01.069. PMC 3793871. PMID 23500200.
- ^ Bautista DM, Siemens J, Glazer JM, Tsuruda PR, Basbaum AI, Stucky CL, Jordt SE, Julius D (2007). „Mentolový receptor TRPM8 je hlavním detektorem chladného prostředí“. Příroda. 448 (7150): 204–208. doi:10.1038 / nature05910. PMID 17538622. S2CID 4427901.
- ^ Daniels RL, McKemy DD (2007). „Myši vynechány v chladu: komentář k fenotypu TRPM8-null“. Mol Pain. 3 (1): 23. doi:10.1186/1744-8069-3-23. PMC 1988789. PMID 17705869.
- ^ Proudfoot CJ, Garry EM, Cottrell DF, Rosie R, Anderson H, Robertson DC, Fleetwood-Walker SM, Mitchell R (srpen 2006). „Analgezie zprostředkovaná studeným receptorem TRPM8 u chronické neuropatické bolesti“. Aktuální biologie. 16 (16): 1591–605. doi:10.1016 / j.cub.2006.07.061. PMID 16920620. S2CID 18467791.
- ^ Colburn RW, Lubin ML, Stone DJ Jr, Wang Y, Lawrence D, D'Andrea MR, Brandt MR, Liu Y, Flores CM, Qin N (květen 2007). "Oslabená citlivost na chlad u myší s nulovou hodnotou TRPM8". Neuron. 54 (3): 379–86. doi:10.1016 / j.neuron.2007.04.017. PMID 17481392. S2CID 17703702.
- ^ Lashinger ES, Steiginga MS, Hieble JP, Leon LA, Gardner SD, Nagilla R, Davenport EA, Hoffman BE, Laping NJ, Su X (září 2008). „AMTB, blokátor kanálů TRPM8: důkazy o aktivitě u potkanů u hyperaktivního močového měchýře a syndromu bolestivého močového měchýře“. American Journal of Physiology. Fyziologie ledvin. 295 (3): F803–10. doi:10.1152 / ajprenal.90269.2008. PMID 18562636.
- ^ Mukerji G, Yiangou Y, Corcoran SL, Selmer IS, Smith GD, Benham CD, Bountra C, Agarwal SK, Anand P (2006). „Chladný a mentolový receptor TRPM8 u lidských poruch močového měchýře a klinické korelace“. BMC urologie. 6: 6. doi:10.1186/1471-2490-6-6. PMC 1420318. PMID 16519806.
- ^ „Dendreon: Cílení na rakovinu, transformace životů“. Dendreon Corporation. 2005-09-21. Archivovány od originál 28. října 2008. Citováno 2008-10-31.
- ^ Zhang L, Barritt GJ (listopad 2004). „Důkazy, že TRPM8 je androgen-dependentní kanál Ca2 +, který je nutný pro přežití buněk rakoviny prostaty“. Cancer Res. 64 (22): 8365–73. doi:10.1158 / 0008-5472.CAN-04-2146. PMID 15548706.
Další čtení
- Clapham DE, Julius D, Montell C, Schultz G (2006). „International Union of Pharmacology. XLIX. Nomenklatura a vztahy struktury a funkce přechodných kanálů potenciálních receptorů“. Pharmacol. Rev. 57 (4): 427–50. doi:10.1124 / pr.57.4.6. PMID 16382100. S2CID 17936350.
- Voets T, Owsianik G, Nilius B (2007). "TRPM8". Handb Exp Pharmacol. Příručka experimentální farmakologie. 179 (179): 329–44. doi:10.1007/978-3-540-34891-7_20. ISBN 978-3-540-34889-4. PMID 17217067.
externí odkazy
- TRPM8 + protein, + člověk v americké národní lékařské knihovně Lékařské předměty (Pletivo)
Tento článek včlení text z United States National Library of Medicine, který je v veřejná doména.