Eluxadolin - Eluxadoline
tento článek potřebuje další citace pro ověření. (Červen 2015) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
 | |
 | |
| Klinické údaje | |
|---|---|
| Výslovnost | Viberzi (/protiaɪˈb.rzi/ vy-BUR-zee |
| Obchodní názvy | Viberzi, Truberzi |
| Ostatní jména | JNJ-27018966 |
| Licenční údaje | |
| Trasy z správa | Pusou |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Vazba na bílkoviny | 81% |
| Odstranění poločas rozpadu | 3,7–6 hodin |
| Vylučování | 82,2% (výkaly), <1% (moč)[1] |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| ChemSpider | |
| UNII | |
| KEGG | |
| Řídicí panel CompTox (EPA) | |
| Chemické a fyzikální údaje | |
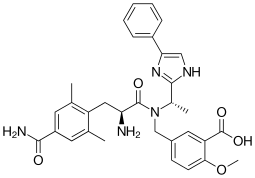
| Vzorec | C32H35N5Ó5 |
| Molární hmotnost | 569.662 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
Eluxadolin, prodávané pod obchodními názvy Viberzi a Truberzi,[2] je lék užívaný ústy k léčbě průjem a bolest břicha u jedinců s převládajícím průjmem syndrom dráždivého tračníku (IBS-D).[3] Bylo schváleno pro použití v EU Spojené státy v roce 2015.[4] The lék původem z Janssen Pharmaceutica a byl vyvinut Actavis.
Kontraindikace
Tento lék je kontraindikován v případě, že:
- Blokování žlučník nebo a Oddiho svěrače problém
- Problémy se zneužíváním alkoholu
- Pankreatitida
- Problémy s játry
- Chronická nebo těžká zácpa[5]
Nepříznivé účinky
Časté nežádoucí účinky jsou zácpa a nevolnost, ale míra přerušení léčby v důsledku zácpy byla nízká jak u eluxadolinu, tak u placeba. Vzácné nežádoucí účinky: únava, bronchitida, virová gastroenteritida. Mezi vzácné závažné nežádoucí účinky patří pankreatitida s obecným výskytem 0,3% - vyšší výskyt u dávky 100 mg (0,3%) než u dávky 75 mg (0,2%).[6] Riziko je ještě větší u těch, kteří nemají žlučník a léčba se v této skupině nedoporučuje.[7]
V březnu 2017 US Food and Drug Administration vydal bezpečnostní varování pro eluxadolin týkající se zvýšeného rizika závažné pankreatitidy u pacientů bez žlučníku.[8] Přezkoumání FDA zjistilo, že u těchto pacientů dochází k křečím Oddiho svěrače může vést k závažné pankreatitidě.[9] FDA uvádí, že v některých případech se u pacientů bez žlučníku (75 mg) vyskytly příznaky pouze s jednou nebo dvěma dávkami v doporučené dávce.[9] Ze dvou úmrtí souvisejících s eluxadolinem hlášených do února 2017 došlo k oběma u pacientů bez žlučníku.[8]
Interakce
Při současném podávání inhibitorů transportního proteinu byly pozorovány zvýšené koncentrace eluxadolinu OATP1B1, jako:
Rovněž není upřednostňováno současné užívání jiných léků, které způsobují zácpu, například:
- Opioidy
- Alosetron
- Anticholinergika
- Subsalicylát vizmutu potenciálně nebezpečná synergie.[10]
Eluxadolin zvyšuje koncentrace léčiv, které jsou substráty OATP1B1 a BCRP. Současné podávání eluxadolinu s rosuvastatin může zvýšit riziko rhabdomyolýza.[1]
Farmakologie
Mechanismus účinku
Eluxadolin je a μ- a κ-opioidní receptor agonista a 5-opioidní receptor antagonista [11] který působí lokálně v střevní nervový systém, případně snižující nepříznivé účinky na EU centrální nervový systém.[12][13]
Farmakokinetika
V in vitro studiích bylo zjištěno, že eluxadolin je transportován OAT3 (SLC22A8 ), OATP1B1 (SLCO1B1 ) a BSEP (ABCB11 ) při nejvyšších testovaných koncentracích (400 ng / ml, což je 162krát více než pozorovaná Cmax nejvyšší terapeutické dávky 100 mg). Ale bylo ne k přepravě OCT1 POU2F1, OAT1 Transportér organických aniontů 1, OCT2, OATP1B3 (SLCO1B3 ), P-gp (P-glykoprotein ) nebo BCRP (ABCG2 ).
Protein související s rezistencí na více léků 2 Byla pozorována (MRP2) -vesikulární akumulace eluxadolinu, což naznačuje, že léčivo je substrátem MRP2. Nebylo zjištěno, že by eluxadolin inhiboval transport substrátů zprostředkovaný sondou BCRP-, BSEP-, MRP2-, OCT1-, OCT2-, OAT1-, OAT3- nebo OATP1B3, ale inhiboval transport substrátů sondy OATP1B1 a P-gp. Také v in vitro studie, bylo pozorováno, že eluxadolin je in vivo substrát OATP1B1, OAT3 a MRP2. Nakonec žádná inhibice nebo indukce cytochrom P450 byly pozorovány enzymy.[14]
Po 100mg dávce eluxadolinu se Cmax byla asi 2 až 4 ng / ml a AUC byla 12-22 ng.h / ml. Eluxadolin má lineární farmakokinetiku bez akumulace při opakovaném podávání dvakrát denně. Užívání eluxadolinu s jídlem s vysokým obsahem tuku snížilo Cmax o 50% a AUC o 60%.[1]
Chemie
Syntéza
Syntéza eluxadolinu byla rozsáhle diskutována v patentu č. W02006099060 A2 s názvem: „Proces přípravy opioidních modulátorů“, který byl zveřejněn v září 2006.[15]
Viz také
Reference
- ^ A b C "Tablety Viberzi (eluxadolin) pro orální podání, CIV. Úplné informace o předepisování". Actavis Pharma, Inc. Parsippany, NJ 07054 USA. Archivovány od originál dne 27. prosince 2015. Citováno 26. prosince 2015.
- ^ "Truberzi". Evropská agentura pro léčivé přípravky. 29. září 2016.
- ^ Fragkos KC (2017-09-25). „Pozornost na eluxadolin pro léčbu pacientů se syndromem dráždivého tračníku s průjmem“. Klinická a experimentální gastroenterologie. 10: 229–240. doi:10,2147 / ceg.s123621. PMC 5624596. PMID 28989282.
- ^ „FDA schvaluje dvě terapie k léčbě IBS-D“. www.fda.gov. Citováno 2015-06-01.
- ^ „Informace společnosti Viberzi z webu Drugs.com“. www.drugs.com. Citováno 2015-06-01.
- ^ Lembo AJ, Lacy BE, Zuckerman MJ, Schey R, Dove LS, Andrae DA a kol. (Leden 2016). "Eluxadolin pro syndrom dráždivého tračníku s průjmem". The New England Journal of Medicine. 374 (3): 242–53. doi:10.1056 / NEJMoa1505180. PMID 26789872. S2CID 205098220.
- ^ Úřad komisaře (15. března 2017). „Bezpečnostní upozornění na humánní léčivé přípravky - Viberzi (eluxadolin): Komunikace o bezpečnosti léčiv - zvýšené riziko závažné pankreatitidy u pacientů bez žlučníku“. www.fda.gov. Citováno 19. března 2017.
- ^ A b Brooks M (březen 2017). "FDA: Vyvarujte se IBS Drug Viberzi u pacientů bez žlučníku". www.medscape.com. Citováno 2017-09-18.
- ^ A b Úřad komisaře. „Bezpečnostní upozornění na humánní léčivé přípravky - Viberzi (eluxadolin): Komunikace o bezpečnosti léčiv - zvýšené riziko závažné pankreatitidy u pacientů bez žlučníku“. www.fda.gov. Citováno 2017-09-18.
- ^ "subsalicylát bismutu". reference.medscape.com. Citováno 2016-05-10.
- ^ Levy-Cooperman N, McIntyre G, Bonifacio L, McDonnell M, Davenport JM, Covington PS a kol. (Prosinec 2016). „Potenciál zneužívání a farmakodynamické vlastnosti orálního a intranasálního eluxadolinu, agonisty smíšeného μ- a κ-opioidního receptoru a δ-opioidního receptoru“. The Journal of Pharmacology and Experimental Therapeutics. 359 (3): 471–481. doi:10.1124 / jpet.116.236547. PMC 5118645. PMID 27647873.
- ^ „Actavis oznamuje přijetí FDA pro podání NDA pro eluxadolin“. www.drugs.com. Citováno 2015-06-01.
- ^ „FDA schvaluje Viberzi (eluxadolin) pro syndrom dráždivého tračníku s průjmem (IBS-D) u dospělých“. www.drugs.com. Citováno 2015-06-01.
- ^ Davenport JM, Covington P, Bonifacio L, McIntyre G, Venitz J (květen 2015). „Účinek absorpčních transportérů OAT3 a OATP1B1 a efluxních transportérů MRP2 na farmakokinetiku eluxadolinu“. Journal of Clinical Pharmacology. 55 (5): 534–42. doi:10,1002 / jcph.442. PMC 4402028. PMID 25491493.
- ^ [1] „Proces přípravy opioidních modulátorů.
