Acetyl-CoA - Acetyl-CoA
tento článek má nejasný styl citace. (Srpna 2017) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC S-[2-[3-[[(2R)-4-[[[(2R,3S,4R,5R) -5- (6-aminopurin-9-yl) -4-hydroxy-3-fosfonooxyoxolan-2-yl] methoxy-hydroxyfosforyl] oxy-hydroxyfosforyl] oxy-2-hydroxy-3,3-dimethylbutanoyl] amino] propanoylamino] ethyl] ethanethioát | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.000.719 |
| KEGG | |
| Pletivo | Acetyl + koenzym + A |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C23H38N7Ó17P3S | |
| Molární hmotnost | 809.57 g · mol−1 |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
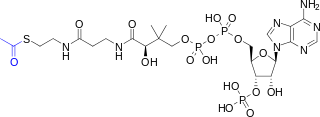
Acetyl-CoA (acetyl koenzym A) je molekula, která se účastní mnoha biochemické reakce v bílkovinách, sacharidech a lipidech metabolismus.[1] Jeho hlavní funkcí je dodávat acetyl skupina do cyklus kyseliny citronové (Krebsův cyklus) být oxidovaný pro výrobu energie. Koenzym A (CoASH nebo CoA) se skládá z a β-merkaptoethylaminová skupina spojené s vitaminem kyselina pantothenová (B5) prostřednictvím amidová vazba [2] a 3'-fosforylovaný ADP. Acetyl skupina (označená modře ve strukturním diagramu vpravo) acetyl-CoA je spojena s sulfhydryl substituent p-merkaptoethylaminové skupiny. Tento thioester vazba je „vysokoenergetická“ vazba, která je zvláště reaktivní. Hydrolýza thioesterové vazby je exergonický (-31,5 kJ / mol).
CoA je acetylován na acetyl-CoA rozkladem sacharidy přes glykolýza a členěním mastné kyseliny přes β-oxidace. Acetyl-CoA poté vstupuje do cyklu kyseliny citronové, kde se acetylová skupina oxiduje na oxid uhličitý a vodu a uvolněná energie je zachycena ve formě 11 ATP a jeden GTP na acetylovou skupinu.
Konrad Bloch a Feodor Lynen byly uděleny v roce 1964 Nobelova cena za fyziologii a medicínu za jejich objevy spojující acetyl-CoA a metabolismus mastných kyselin. Fritz Lipmann získal Nobelovu cenu v roce 1953 za objev kofaktoru koenzym A.
Přímá syntéza
Acetylace CoA je určena zdroji uhlíku.[3][4]
Extramitochondriální
- Vysoko glukóza úrovně, glykolýza probíhá rychle, čímž se zvyšuje množství citrát vyrobený z cyklu trikarboxylové kyseliny. Tento citrát se poté exportuje do jiných organely mimo mitochondrie, které mají být rozděleny na acetyl-CoA a oxaloacetát podle enzym ATP citrát lyáza (ACL). Tato hlavní reakce je spojena s hydrolýzou ATP.[5][6]
- Při nízké hladině glukózy:
- CoA je acetylován pomocí acetát podle acetyl-CoA syntetáza (ACS), také ve spojení s ATP hydrolýza.[7]
- Ethanol slouží také jako zdroj uhlíku pro acetylaci CoA s využitím enzymu alkohol dehydrogenáza.[8]
- Degradace rozvětveného řetězce ketogenní aminokyseliny jako valin, leucin, a isoleucin dojde. Tyto aminokyseliny se převádějí na α-ketokyseliny pomocí transaminace a nakonec na isovaleryl-CoA prostřednictvím oxidativní dekarboxylace komplexem a-ketoaciddehydrogenázy. Isovaleryl-CoA prochází dehydrogenace, karboxylace a hydratace za vzniku dalšího meziproduktu derivátu CoA před jeho štěpením na acetyl-CoA a acetoacetát.[9][stránka potřebná ]
Intramitochondriální

- Při vysokých hladinách glukózy se acetyl-CoA produkuje prostřednictvím glykolýza.[10] Pyruvát prochází oxidační dekarboxylací, při které ztrácí svoji karboxyl skupina (jako oxid uhličitý ) za vzniku acetyl-CoA, vydávajícího 33,5 kJ / mol energie. Oxidační přeměna pyruvátu na acetyl-CoA se označuje jako pyruvátdehydrogenázová reakce. Je katalyzován komplex pyruvátdehydrogenázy. Další přeměny mezi pyruvátem a acetyl-CoA jsou možné. Například, pyruvátformiát lyáza disproporcionuje pyruvát na acetyl-CoA a kyselina mravenčí.
- Při nízkých hladinách glukózy je spojena produkce acetyl-CoA β-oxidace z mastné kyseliny. Mastné kyseliny se nejprve převádějí na acyl-CoA. Acyl-CoA se poté degraduje ve čtyřstupňovém cyklu oxidace, hydratace, oxidace a thiolýza katalyzováno čtyřmi příslušnými enzymy, a to acyl-CoA dehydrogenáza, enoyl-CoA hydratáza, 3-hydroxyacyl-CoA dehydrogenáza, a thioláza. Cyklus produkuje nový řetězec mastných kyselin se dvěma méně uhlíky a acetyl-CoA jako vedlejším produktem.[11]
Funkce
Meziprodukty v různých cestách
- V buněčném dýchání
- Cyklus kyseliny citronové:
- Prostřednictvím řady chemických reakcí se akumulovaná energie uvolňuje oxidací acetyl-CoA získaného ze sacharidů, tuků a bílkovin na adenosintrifosfát (ATP) a oxid uhličitý.
- Metabolismus mastných kyselin
- Acetyl-CoA se vyrábí rozpadem obou sacharidy (podle glykolýza ) a lipidy (podle β-oxidace ). Poté vstupuje do cyklu kyseliny citronové v mitochondriích kombinací s oxaloacetát tvořit citrát.[12][13]
- Dvě molekuly acetyl-CoA kondenzují za vzniku acetoacetyl-CoA, což vede k tvorbě acetoacetát a p-hydroxybutyrát.[12] Acetoacetát, β-hydroxybutyrát a jejich produkt spontánního rozkladu aceton[14] jsou často, ale matoucí, známé jako ketolátky (protože to vůbec nejsou „těla“, ale chemické látky rozpustné ve vodě). Ketonová tělíska jsou uvolňována játra do krve. Všechny buňky s mitochondriemi mohou přijímat ketolátky z krve a přeměnit je na acetyl-CoA, který lze poté použít jako palivo v cyklech kyseliny citronové, protože žádná jiná tkáň nedokáže odklonit svůj oxaloacetát na glukoneogenní cesta tak, jak to dělají játra. Na rozdíl od volných mastných kyselin mohou ketolátky procházet hematoencefalická bariéra a jsou proto k dispozici jako palivo pro články palivové nádrže centrální nervový systém, působící jako náhrada za glukózu, na které tyto buňky normálně přežívají.[12] Výskyt vysokých hladin ketonů v krvi během hladovění, a nízkosacharidová strava, prodloužené těžké cvičení a nekontrolované diabetes mellitus 1. typu je známý jako ketóza, a v extrémní formě u diabetes mellitus 1. typu mimo kontrolu, as ketoacidóza.
- Na druhou stranu, když inzulín koncentrace v krvi je vysoká, a to glukagon je nízký (tj. po jídle), acetyl-CoA produkovaný glykolýzou kondenzuje jako obvykle s oxaloacetátem za vzniku citrátu v mitochondrii. Avšak místo toho, aby v cyklu kyseliny citronové pokračoval v přeměnu na oxid uhličitý a vodu, je citrát odstraněn z mitochondrie do cytoplazma.[12] Tam to štěpí ATP citrát lyáza na acetyl-CoA a oxaloacetát. Oxaloacetát se vrací do mitochondrií jako malát (a poté se převede zpět na oxaloacetát, aby se z mitochondrií přeneslo více acetyl-CoA).[15] Tento cytosolický acetyl-CoA lze poté použít k syntéze mastných kyselin karboxylací pomocí acetyl-CoA karboxyláza do malonyl CoA, první spáchaný krok v syntéze mastných kyselin.[15][16] K této přeměně dochází primárně v játrech, tuková tkáň a kojící mléčné žlázy, kde jsou mastné kyseliny kombinovány s glycerol tvořit triglyceridy, hlavní zásobník paliva většiny zvířat. Mastné kyseliny jsou také součástí fosfolipidy které tvoří většinu lipidové dvojvrstvy ze všech buněčné membrány.[12]
- V rostlinách de novo syntéza mastných kyselin se vyskytuje v plastidy. Mnoho semena akumulovat velké rezervy semenných olejů na podporu klíčení a časný růst sazenice, než bude síť fotosyntetický organismus.
- The cytosolický acetyl-CoA může také kondenzovat s acetoacetyl-CoA za vzniku 3-hydroxy-3-methylglutaryl-CoA (HMG-CoA ), což je krok omezující rychlost ovládající syntéza cholesterolu.[12] Cholesterol může být použit jako takový, jako strukturní složka buněčných membrán, nebo může být použit k syntéze steroidní hormony, žlučové soli, a Vitamín D.[12][16]
- Acetyl-CoA může být karboxylovaný v cytosolu acetyl-CoA karboxyláza, což vede k malonyl-CoA, substrát potřebný pro syntézu flavonoidy a související polyketidy pro prodloužení produkce mastných kyselin vosky, pokožka a oleje ze semen u členů Brassica rodina a pro mallonace bílkovin a dalších fytochemikálií.[17] V rostlinách to zahrnuje seskviterpeny, brassinosteroidy (hormony) a membrány steroly.
- Syntéza steroidů:
- Acetyl-CoA se účastní mevalonátová cesta účastí na syntéze hydroxymethyl glutaryl-CoA.
- Acetylcholin syntéza:
- Acetyl-CoA je také důležitou složkou v biogenní syntéze neurotransmiter acetylcholin. Cholin, v kombinaci s acetyl-CoA, je katalyzován enzymem cholin acetyltransferáza k výrobě acetylcholinu a koenzym A jako vedlejší produkt.
- Melatonin syntéza
- Acetylace
- Acetyl-CoA je také zdrojem acetylové skupiny zabudované do určité skupiny lysin zbytky histon a nonhistonové proteiny v posttranslační modifikace acetylace. Tato acetylace je katalyzována acetyltransferázy. Tato acetylace ovlivňuje růst buněk, mitóza, a apoptóza.[18]
- Allosterický regulátor
- Acetyl-CoA slouží jako alosterický regulátor z pyruvátdehydrogenáza kináza (PDK). Reguluje prostřednictvím poměru acetyl-CoA k CoA. Zvýšená koncentrace acetyl-CoA aktivuje PDK.[19]
- Acetyl-CoA je také alosterickým aktivátorem pyruvátkarboxyláza.[20]
Interaktivní mapa cest
Kliknutím na níže uvedené geny, proteiny a metabolity navštívíte Gene Wiki stránky a související články z Wikipedie. Cestu lze stáhnout a upravit na WikiPathways.
TCA cyklus Upravit | Statinová cesta Upravit |
Viz také
Reference
- ^ „Křižovatka acetyl CoA“. chemistry.elmhurst.edu. Citováno 2016-11-08.
- ^ "Mastné kyseliny - struktura acetyl CoA". knihovna.med.utah.edu. Citováno 2017-06-02.
- ^ Hynes, Michael J .; Murray, Sandra L. (01.07.2010). „ATP-citrát-lyáza je vyžadována pro produkci cytosolického acetyl koenzymu A a vývoj u Aspergillus nidulans“. Eukaryotická buňka. 9 (7): 1039–1048. doi:10.1128 / EC.00080-10. ISSN 1535-9778. PMC 2901662. PMID 20495057.
- ^ Wellen, Kathryn E .; Thompson, Craig B. (01.04.2012). „Obousměrná ulice: vzájemná regulace metabolismu a signalizace“. Nature Reviews Molecular Cell Biology. 13 (4): 270–276. doi:10.1038 / nrm3305. ISSN 1471-0072. PMID 22395772. S2CID 244613.
- ^ Storey, Kenneth B. (2005-02-25). Funkční metabolismus: regulace a adaptace. John Wiley & Sons. ISBN 9780471675570.
- ^ "ACLY ATP citrát lyáza [Homo sapiens (člověk)] - gen - NCBI". www.ncbi.nlm.nih.gov. Citováno 2016-11-06.
- ^ Ragsdale, S. W. (2004). "Život s oxidem uhelnatým". CRC kritické recenze v biochemii a molekulární biologii. 39 (3): 165–195. doi:10.1080/10409230490496577. PMID 15596550. S2CID 16194968.
- ^ Chatterjea (01.01.2004). Učebnice biochemie pro studenty zubního lékařství / ošetřovatelství / farmacie. Vydavatelé Jaypee Brothers. ISBN 9788180612046.
- ^ Berg, Jeremy M .; Tymoczko, John L .; Stryer, Lubert (2002). Biochemie (5. vydání). W. H. Freeman. ISBN 978-0716730514.
- ^ Blackstock, James C. (2014-06-28). Průvodce po biochemii. Butterworth-Heinemann. ISBN 9781483183671.
- ^ Houten, Sander Michel; Wanders, Ronald J. A. (2010-03-02). „Obecný úvod do biochemie β-oxidace mitochondriálních mastných kyselin“. Journal of Inherited Metabolic Disease. 33 (5): 469–477. doi:10.1007 / s10545-010-9061-2. ISSN 0141-8955. PMC 2950079. PMID 20195903.
- ^ A b C d E F G Stryer, Lubert (1995). Biochemie (Čtvrté vydání). New York: W.H. Freeman a společnost. str. 510–515, 559–565, 581–613, 614–623, 775–778. ISBN 978-0-7167-2009-6.
- ^ „Oxidace mastných kyselin“. 2013-10-11.
- ^ "Ketonový metabolismus těla". University of Waterloo.
- ^ A b Ferre, P .; F. Foufelle (2007). „Transkripční faktor SREBP-1c a homeostáza lipidů: klinická perspektiva“. Výzkum hormonů. 68 (2): 72–82. doi:10.1159/000100426. PMID 17344645.
tento proces je graficky načrtnut na straně 73
- ^ A b Voet, Donald; Judith G. Voet; Charlotte W. Pratt (2006). Základy biochemie, 2. vydání. John Wiley and Sons, Inc. str.547, 556. ISBN 978-0-471-21495-3.
- ^ Fatland, B.L. (2005). „Reverzní genetická charakterizace tvorby cytosolického acetyl-CoA pomocí ATP-citrát-lyázy u Arabidopsis“. Rostlinná buňka online. 17 (1): 182–203. doi:10.1105 / tpc.104.026211. PMC 544498. PMID 15608338.
- ^ Yi, C.H .; Vakifahmetoglu-Norberg, H .; Yuan, J. (01.01.2011). „Integrace apoptózy a metabolismu“. Cold Spring Harbor Symposia o kvantitativní biologii. 76: 375–387. doi:10.1101 / sqb.2011.76.010777. ISSN 0091-7451. PMID 22089928.
- ^ Pettit, Flora H .; Pelley, John W .; Reed, Lester J. (1975-07-22). "Regulace pyruvátdehydrogenázové kinázy a fosfatázy poměrem acetyl-CoA / CoA a NADH / NAD". Sdělení o biochemickém a biofyzikálním výzkumu. 65 (2): 575–582. doi:10.1016 / S0006-291X (75) 80185-9. PMID 167775.
- ^ Jitrapakdee, Sarawut; Maurice, Martin St .; Rayment, Ivan; Cleland, W. Wallace; Wallace, John C .; Attwood, Paul V. (2008-08-01). "Struktura, mechanismus a regulace pyruvátkarboxylázy". The Biochemical Journal. 413 (3): 369–387. doi:10.1042 / BJ20080709. ISSN 0264-6021. PMC 2859305. PMID 18613815.
externí odkazy
- Acetyl + koenzym + A v americké národní lékařské knihovně Lékařské předměty (Pletivo)
ATP ADP ATP ADP + + 2 ×  2 ×  2 × 3-fosfoglycerát 2 ×  2 × 2-fosfoglycerát 2 ×  2 × Fosfoenolpyruvát 2 ×  ADP ATP 2 × Pyruvát 2 × |
| + H 2Ó | |||
| NADH + H+ + CO 2 | |||
| CoA | NAD+ | ||


















