Karboxylace - Carboxylation
Karboxylace je chemická reakce ve kterém a karboxylová kyselina skupina se vyrábí zpracováním a Podklad s oxid uhličitý.[1] Opačná reakce je dekarboxylace. v chemie, termín karbonatace se někdy používá synonymně s karboxylací, zvláště když se použije na reakci karbaniontový činidla s CO2. Obecněji karbonatace obvykle popisuje produkci uhličitany.[2]
Organická chemie
Karboxylace je standardní přeměna na organická chemie.[3] Konkrétně karbonace (tj. Karboxylace) Grignardova činidla a organolithné sloučeniny je klasický způsob převodu organických halogenidů na karboxylové kyseliny.[4]
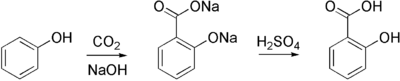
Salicylát sodný, předchůdce aspirin, je komerčně připraven zpracováním fenolát sodný (sodná sůl fenol ) s oxid uhličitý při vysokém tlaku (100 atm) a vysoké teplotě (390 K) - metoda známá jako Kolbe-Schmittova reakce. Okyselením výsledné salicylátové soli se získá kyselina salicylová.
Mnoho podrobných postupů je popsáno v časopise Organické syntézy.[5][6][7]
Karboxylační katalyzátory zahrnují N-Heterocyklické karbeny [8] a katalyzátory na bázi stříbra.[9]
Karboxylace v biochemii
Život na bázi uhlíku pochází z karboxylace, která spojuje atmosférický oxid uhličitý s cukrem. Proces je obvykle katalyzovaný enzymem RuBisCO. Ribulóza-1,5-bisfosfátkarboxyláza / oxygenáza Enzym, který katalyzuje tuto karboxylaci, je pravděpodobně nejhojnější protein na Zemi.[10][11][12]


Mnoho karboxyláz, včetně Acetyl-CoA karboxyláza, Methylcrotonyl-CoA karboxyláza, Propionyl-CoA karboxyláza, a Pyruvátkarboxyláza vyžadovat biotin jako kofaktor. Tyto enzymy se účastní různých biogenních drah.[13] Ve schématu EC jsou takové karboxylázy klasifikovány podle EC 6.3.4, „Ostatní uhlík - dusíkaté ligázy“.
Dalším příkladem je posttranslační modifikace z glutamát zbytky, do y-karboxyglutamát v bílkovinách. Vyskytuje se primárně v proteinech podílejících se na srážení krve kaskáda, konkrétně faktory II, VII, IX a X, protein C a protein S a také v některých kostních proteinech. Tato modifikace je nutná pro fungování těchto proteinů. Karboxylace probíhá v játra a provádí ji y-glutamylkarboxyláza (GGCX).[14] GGCX vyžaduje vitamin K. jako kofaktor a provádí reakci procesivním způsobem.[15] γ-karboxyglutamát váže vápník, který je nezbytný pro jeho aktivitu.[16] Například v protrombin vazba vápníku umožňuje, aby se protein asocioval s plazmatická membrána v krevní destičky, čímž se dostává do těsné blízkosti s proteiny, které štěpí protrombin na aktivní trombin po zranění.[17]
Viz také
Reference
- ^ „Karboxylace: Zavedení karboxylové skupiny do molekuly nebo sloučeniny za vzniku karboxylové kyseliny nebo karboxylátu; příklad toho.“Oxfordský anglický slovník. Oxford University Press. 2018.
- ^ „Karbonatace: Impregnace nebo úprava oxidem uhličitým; přeměna na uhličitan.“Oxfordský anglický slovník. Oxford University Press. 2018.
- ^ Braunstein, Pierre; Matt, Dominique; Nobel, Dominique (srpen 1988). „Reakce oxidu uhličitého s tvorbou vazby uhlík-uhlík katalyzovanou komplexy přechod-kov“. Chemické recenze. 88 (5): 747–764. doi:10.1021 / cr00087a003.
- ^ A. M. Appel; et al. (2013). „Hranice, příležitosti a výzvy v biochemické a chemické katalýze CO2 Fixace ". Chem. Rev. 113 (8): 6621–6658. doi:10.1021 / cr300463y. PMC 3895110. PMID 23767781.
- ^ Akira Yanagisawa; Katsutaka Yasue; Hisashi Yamamoto (1997). "Regio- a stereoselektivní karboxylace allylického barnatého činidla: (E) -4,8-dimethyl-3,7-nonadienová kyselina". Organické syntézy. 74: 178. doi:10.15227 / orgsyn.074.0178.
- ^ H. Koch; W. Haaf (1964). „Kyselina 1-adamantankarboxylová“. Organické syntézy. 44: 1. doi:10.15227 / orgsyn.044.0001.
- ^ W. Haaf (1966). „Kyselina 1-methylcyklohexankarboxylová“. Organické syntézy. 46: 72. doi:10.15227 / orgsyn.046.0072.
- ^ Zhang Liang (2013). „N-Heterocyklický karben (NHC) - transformace oxidu uhličitého katalyzovaná mědí“. Chemická věda. 4: 3395. doi:10.1039 / C3SC51070K.
- ^ K. Sekine; T. Yamada (2016). „Karboxylace katalyzovaná stříbrem“. Chem. Soc. Rev. 45 (16): 4524–4532. doi:10.1039 / C5CS00895F.
- ^ Dhingra A, Portis AR, Daniell H (duben 2004). „Vylepšený překlad genu RbcS exprimovaného chloroplasty obnovuje malé hladiny podjednotky a fotosyntézu v jaderných rostlinách RbcS antisense“. Proc. Natl. Acad. Sci. USA. 101 (16): 6315–20. Bibcode:2004PNAS..101,6315D. doi:10.1073 / pnas.0400981101. PMC 395966. PMID 15067115.
(Rubisco) je nejrozšířenějším enzymem na této planetě a představuje 30–50% celkového rozpustného proteinu v chloroplastu;
- ^ Feller U, Anders I, Mae T (2008). „Rubiscolytics: osud Rubisco po ukončení jeho enzymatické funkce v buňce“ (PDF). J. Exp. Bot. 59 (7): 1615–24. doi:10.1093 / jxb / erm242. PMID 17975207.
- ^ Raven, John A. (duben 2013). „Rubisco: stále nejhojnější protein na Zemi?“. Nový fytolog. 198 (1): 1–3. doi:10.1111 / nph.12197.
- ^ „Biotin - informační list pro zdravotnické pracovníky“. Úřad doplňků stravy, USA Národní institut zdraví. 8. prosince 2017. Citováno 25. února 2018.
- ^ OMIM - gama-glutamylkarboxyláza, přispěla společnost McKusick VA, naposledy aktualizovaná v říjnu 2004 [1]
- ^ Morris DP, Stevens RD, Wright DJ, Stafford DW (1995). "Procesní posttranslační modifikace. Karboxylace peptidového substrátu závislá na vitaminu K". J. Biol. Chem. 270 (51): 30491–8. doi:10.1074 / jbc.270.51.30491. PMID 8530480.
- ^ Hauschka PV, Lian JB, Gallop PM (1975). „Přímá identifikace aminokyseliny vázající vápník, gama-karboxyglutamátu, v mineralizované tkáni“. Proc. Natl. Acad. Sci. USA. 72 (10): 3925–9. Bibcode:1975PNAS ... 72,3925H. doi:10.1073 / pnas.72.10.3925. PMC 433109. PMID 1060074.
- ^ Berg JM, Tymoczko JL, Stryer L. Biochemie, 5. vyd. New York: W. H. Freeman and Company, 2002.