Kyselina oxalooctová - Oxaloacetic acid
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Kyselina 2-oxobutandiová | |
| Ostatní jména Kyselina oxalooctová Kyselina oxalactová Kyselina 2-oxosukcinová Kyselina ketosukcinová | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.005.755 |
| Číslo ES |
|
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C4H4Ó5 | |
| Molární hmotnost | 132,07 g / mol |
| Hustota | 0,18 g / cm3 |
| Bod tání | 161 ° C (322 ° F; 434 K) |
| Termochemie | |
Std entalpie of formace (ΔFH⦵298) | -943,21 kJ / mol |
Std entalpie of spalování (ΔCH⦵298) | -1205,58 kJ / mol |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Kyselina oxalooctová (také známý jako kyselina oxalactová nebo OAA) je krystalický organická sloučenina s chemický vzorec HO2CC (O) CH2CO2H. Kyselina oxaloctová, ve formě své konjugovaná báze oxaloacetát, je metabolický meziprodukt v mnoha procesech, které se vyskytují u zvířat. Účastní se glukoneogeneze, močovinový cyklus, glyoxylátový cyklus, syntéza aminokyselin, syntéza mastných kyselin a cyklus kyseliny citronové.[1]
Vlastnosti
Kyselina oxalooctová prochází postupnými deprotonacemi, aby poskytla dianion:
- HO2CC (O) CH2CO2H ⇌ −Ó2CC (O) CH2CO2H + H+ pKA = 2.22
- −Ó2CC (O) CH2CO2H ⇌ −Ó2CC (O) CH2CO2− + H+, pKA = 3.89
Při vysokém pH je enolizovatelný proton ionizován:
- −Ó2CC (O) CH2CO2− ⇌ −Ó2CC (O.−) CHCO2− + H+, pKA = 13.03
The enol formy kyseliny oxalooctové jsou zvláště stabilní, a to natolik, že tyto dvě tautomery mají různé teploty tání (152 ° C pro cis izoforma a 184 ° C pro trans izoforma).
Biosyntéza
Oxaloacetát se v přírodě tvoří několika způsoby. Hlavní cesta je na cestě oxidace z L-malát, katalyzováno malát dehydrogenáza v cyklu kyseliny citronové. Malát je také oxidován sukcinát dehydrogenáza v pomalé reakci s počátečním produktem, kterým je enol-oxaloacetát.[2]
Vyplývá to také z kondenzace pyruvát s kyselinou uhličitou, poháněnou hydrolýzou ATP:
- CH3KOKOS2− + HCO3− + ATP → −Ó2CCH2KOKOS2− + ADP + Pi
Vyskytující se v mezofyl rostlin, tento proces probíhá prostřednictvím fosfoenolpyruvát, katalyzováno fosfoenolpyruvátkarboxyláza.
Oxaloacetát může také vzniknout z trans- nebo určení kyselina asparagová.
Biochemické funkce
Oxaloacetát je meziproduktem cyklus kyseliny citronové, kde reaguje s acetyl-CoA tvořit citrát, katalyzováno citrát syntáza. Rovněž se podílí na glukoneogeneze, močovinový cyklus, glyoxylátový cyklus, syntéza aminokyselin, a syntéza mastných kyselin. Oxaloacetát je také silným inhibitorem komplex II.
Glukoneogeneze
Glukoneogeneze[1] je metabolická cesta skládající se z řady jedenácti enzymem katalyzovaných reakcí, které vedou k tvorbě glukóza z nesacharidových substrátů. Začátek tohoto procesu probíhá v mitochondriální matici, kde pyruvát molekuly jsou nalezeny. Molekula pyruvátu je karboxylována a pyruvátkarboxyláza enzym, aktivovaný každou z molekul ATP a voda. Tato reakce vede k tvorbě oxaloacetátu. NADH redukuje oxaloacetát na malát. Tato transformace je nutná k transportu molekuly ven mitochondrie. Jednou v cytosol, malát se znovu oxiduje na oxaloacetát pomocí NAD +. Poté oxaloacetát zůstane v cytosolu, kde proběhne zbytek reakcí. Oxaloacetát je později dekarboxylován a fosforylován fosfoenolpyruvátkarboxykináza a stává se 2-fosfoenolpyruvát použitím guanosin trifosfát (GTP) jako zdroj fosfátů. Glukóza se získává po dalším následném zpracování.
Cyklus močoviny
The močovinový cyklus je metabolická cesta, která vede k tvorbě močovina pomocí dvou molekul amonného a jedné molekuly hydrogenuhličitanu.[1] Tato trasa se běžně vyskytuje v hepatocyty. Vyvolávají se reakce související s cyklem močoviny NADH ) a NADH lze vyrobit dvěma různými způsoby. Jedno z těchto použití oxaloacetát. V cytosolu jsou fumarát molekuly. Fumarát lze přeměnit na malát působením enzymu fumarázy. Na malát působí malát dehydrogenáza, aby se stal oxaloacetátem, čímž se vytvoří molekula NADH. Poté bude oxaloacetát recyklován na aspartát, protože transaminázy preferují tyto ketokyseliny před ostatními. Tato recyklace udržuje tok dusík do cely.

Glyoxylátový cyklus
The glyoxylátový cyklus je variantou cyklu kyseliny citronové.[3] Je to anabolický cesta vyskytující se v rostliny a bakterie s využitím enzymů isocitrát lyáza a malát syntáza. Některé mezikroky cyklu se mírně liší od cyklu kyseliny citronové; oxaloacetát má nicméně v obou procesech stejnou funkci.[1] To znamená, že oxaloacetát v tomto cyklu působí také jako primární reaktant a konečný produkt. Oxaloacetát je ve skutečnosti čistým produktem glyoxylátový cyklus protože jeho smyčka cyklu zahrnuje dvě molekuly acetyl-CoA.
Syntéza mastných kyselin
V předchozích fázích se acetyl-CoA přenáší z mitochondrií do cytoplazmy, kde syntáza mastných kyselin bydlí. Acetyl-CoA je transportován jako citrát, který byl dříve vytvořen v mitochondriální matrici z acetyl-CoA a oxaloacetátu. Tato reakce obvykle iniciuje cyklus kyseliny citronové, ale když není potřeba energie, je transportována do cytoplazmy, kde je rozložena na cytoplazmatický acetyl-CoA a oxaloacetát.
Další část cyklu vyžaduje NADPH pro syntézu mastných kyselin.[4] Část této redukční energie se generuje, když se cytosolický oxaloacetát vrací do mitochondrií, pokud je vnitřní mitochondriální vrstva pro oxaloacetát nepropustná. Nejprve se oxaloacetát redukuje na malát pomocí NADH. Potom je malát dekarboxylován na pyruvát. Nyní může tento pyruvát snadno vstoupit do mitochondrií, kde je znovu karboxylován na oxaloacetát pyruvátkarboxylázou. Tímto způsobem přenos acetyl-CoA, který je z mitochondrií do cytoplazmy, produkuje molekulu NADH. Celková reakce, která je spontánní, lze shrnout jako:
- HCO3– + ATP + acetyl-CoA → ADP + Pi + malonyl-CoA
Syntéza aminokyselin
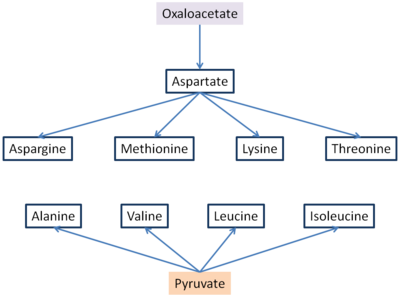
Syntetizuje se šest esenciálních aminokyselin a tři neesenciální oxaloacetát a pyruvát.[5] Aspartát a alanin se tvoří z oxaloacetátu, respektive pyruvátu, transaminací z glutamátu. Asparagin, methionin, lysin a threonin jsou syntetizovány aspartátem, a proto je oxaloacetátu dán význam, protože bez něj by nevznikl žádný aspartát a nebyly by produkovány ani další aminokyseliny.
Biosyntéza oxalátu
Oxaloacetát produkuje oxalát hydrolýzou.[6]
- oxaloacetát + H2Oxalát + octan
Tento proces je katalyzován enzym oxaloacetáza. Tento enzym je vidět v rostlinách, ale není znám v živočišné říši. [7]
Interaktivní mapa cest
| Kliknutím na geny, proteiny a metabolity níže můžete odkazovat na příslušné články.[§ 1] Glykolýza a glukoneogeneze Upravit
| Kliknutím na geny, proteiny a metabolity níže můžete odkazovat na příslušné články. [§ 1] TCA cyklus Upravit
|
Viz také
Reference
- ^ A b C d Nelson, David L .; Cox, Michael M. (2005). Principy biochemie (4. vydání). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ^ M.V. Panchenko; A.D. Vinogradov (1991). „Přímé prokázání enol-oxaloacetátu jako okamžitého produktu oxidace malátu savčí sukcinátdehydrogenázou“. FEBS Dopisy. 286 (1–2): 76–78. doi:10.1016 / 0014-5793 (91) 80944-X.
- ^ „Vítejte v Chemistry Place“. www.pearsonhighered.com. Citováno 5. dubna 2018.
- ^ "syntéza mastných kyselin". http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb2/part1/fasynthesis.htm. Externí odkaz v
| vydavatel =(Pomoc); Chybějící nebo prázdný| url =(Pomoc) - ^ „http://faculty.ksu.edu.sa/69436/Documents/lecture-15-aa_from_oxaloacetate_and_pyruvate.pptx“. Archivovány od originál dne 21.10.2013. Citováno 2013-10-21. Externí odkaz v
| název =(Pomoc) - ^ Gadd, Geoffrey M. „Plísňová produkce kyseliny citronové a šťavelové: význam ve speciaci kovů, fyziologii a biogeochemických procesech“ Advances in Microbial Physiology (1999), 41, 47-92.
- ^ Xu, Hua-Wei. „Akumulace a regulace oxalátu je nezávislá na glykolát oxidáze v rýžových listech“ Journal of Experimental Botany, sv. 57, č. 9, str. 1899-1908, 2006
| + H 2Ó | |||
| NADH + H+ + CO 2 | |||
| CoA | NAD+ | ||












