Kyselina pyrohroznová - Pyruvic acid - Wikipedia
| |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC Kyselina 2-oxopropanová[1] | |||
| Ostatní jména | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| Zkratky | Pyr | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Informační karta ECHA | 100.004.387 | ||
| KEGG | |||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C3H4Ó3 | |||
| Molární hmotnost | 88.06 g / mol | ||
| Hustota | 1.250 g / cm3 | ||
| Bod tání | 11,8 ° C (53,2 ° F; 284,9 K) | ||
| Bod varu | 165 ° C (329 ° F; 438 K) | ||
| Kyselost (strK.A) | 2.50[2] | ||
| Související sloučeniny | |||
jiný anionty | Pyruvátový ion  | ||
Příbuzný ketokyseliny, karboxylové kyseliny | |||
Související sloučeniny | |||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Kyselina pyrohroznová (CH3COCOOH) je nejjednodušší z alfa-ketokyseliny, s karboxylová kyselina a a keton funkční skupina. Pyruvát (/paɪˈruːprotieɪt/), konjugovaná báze, CH3KOKOS−, je klíčovým prostředníkem v několika metabolické cesty v celé buňce.
Kyselina pyrohroznová může být vyrobena z glukóza přes glykolýza, převedeno zpět na sacharidy (jako je glukóza) prostřednictvím glukoneogeneze nebo mastné kyseliny prostřednictvím reakce s acetyl-CoA.[3] Může se také použít ke konstrukci aminokyseliny alanin a lze je převést na ethanol nebo kyselina mléčná přes kvašení.
Kyselina pyrohroznová dodává energii buňky skrz cyklus kyseliny citronové (také známý jako Krebsův cyklus), když je přítomen kyslík (aerobní dýchání ) a alternativně fermentuje k výrobě laktát když chybí kyslík (kyselina mléčná ).[4]
Chemie
V roce 1834 Théophile-Jules Pelouze destilovaný kyselina vinná a izolovaný kyselina glutarová a další neznámá organická kyselina. Jöns Jacob Berzelius charakterizoval tuto další kyselinu v následujícím roce a pojmenoval kyselinu pyrohroznovou, protože byla destilována pomocí tepla.[5][6] Kyselina pyrohroznová je bezbarvá kapalina s vůní podobnou vůni octová kyselina a je mísitelný s vodou.[7] V laboratoři lze kyselinu pyrohroznovou připravit zahřátím směsi kyselina vinná a hydrogensíran draselný,[8] podle oxidace z propylenglykol silným oxidačním činidlem (např. manganistan draselný nebo bělidlo ), nebo hydrolýzou acetylkyanid, vytvořený reakcí acetylchlorid s kyanid draselný:
- CH3COCl + KCN → CH3COCN + KCl
- CH3COCN → CH3COCOOH
Biochemie
Pyruvát je důležitý chemická sloučenina v biochemie. Je to výstup metabolismu glukóza známý jako glykolýza.[9] Jedna molekula glukóza rozpadá se na dvě molekuly pyruvátu,[9] které se poté používají k poskytnutí další energie jedním ze dvou způsobů. Pyruvát se převádí na acetyl-koenzym A, což je hlavní vstup pro řadu reakcí známých jako Krebsův cyklus (také známý jako cyklus kyseliny citronové nebo cyklus trikarboxylové kyseliny). Pyruvát se také převádí na oxaloacetát podle anaplerotická reakce, který doplňuje Krebsův cyklus meziprodukty; oxaloacetát se také používá pro glukoneogeneze. Tyto reakce jsou pojmenovány po Hans Adolf Krebs, biochemik udělil 1953 Nobelova cena pro fyziologii, společně s Fritz Lipmann, pro výzkum metabolických procesů. Cyklus je také známý jako cyklus kyseliny citronové nebo cyklus trikarboxylové kyseliny, protože kyselina citronová je jednou z meziproduktů vznikajících během reakcí.
Pokud není k dispozici dostatek kyslíku, kyselina se rozloží anaerobně, vytváření laktát u zvířat a ethanol v rostlinách a mikroorganismech (a kapr[10]). Pyruvát z glykolýzy se převádí na kvašení na laktát za použití enzym laktátdehydrogenáza a koenzym NADH v laktátu kvašení nebo acetaldehyd (s enzymem pyruvát dekarboxyláza ) a poté na ethanol v alkoholové kvašení.
Pyruvát je klíčovou křižovatkou v síti metabolické cesty. Pyruvát lze převést na sacharidy přes glukoneogeneze, do mastné kyseliny nebo skrz energii acetyl-CoA, do aminokyselina alanin a do ethanol. Proto spojuje několik klíčových metabolických procesů.

Produkce kyseliny pyrohroznové glykolýzou
v glykolýza, fosfoenolpyruvát (PEP) se převede na pyruvát pyruvátkináza. Tato reakce je silně exergonická a nevratná; v glukoneogeneze, to vyžaduje dva enzymy, pyruvátkarboxyláza a PEP karboxykináza, pro katalyzování reverzní transformace pyruvátu na PEP.
| fosfoenolpyruvát | pyruvátkináza | pyruvát | |
 |  | ||
| ADP | ATP | ||
 | |||
| ADP | ATP | ||
| pyruvátkarboxyláza a PEP karboxykináza | |||
Sloučenina C00074 na KEGG Databáze cest. Enzym 2.7.1.40 na KEGG Databáze cest. Sloučenina C00022 na KEGG Databáze cest.
Kliknutím na geny, proteiny a metabolity níže můžete odkazovat na příslušné články.[§ 1]
- ^ Interaktivní mapu cest lze upravit na WikiPathways: „GlycolysisGluconeogenesis_WP534“.
Dekarboxylace na acetyl CoA
Dekarboxylace pyruvátu podle komplex pyruvátdehydrogenázy vyrábí acetyl-CoA.
| pyruvát | komplex pyruvátdehydrogenázy | acetyl-CoA | |
 |  | ||
| CoA + NAD+ | CO2 + NADH + H+ | ||
 | |||
Karboxylace na oxaloacetát
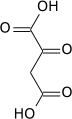
Karboxylace pomocí pyruvátkarboxyláza vyrábí oxaloacetát.
| pyruvát | pyruvátkarboxyláza | oxaloacetát | |
 |  | ||
| ATP + CO2 | ADP + Pi | ||
 | |||
Transaminace na alanin
Transaminace alanin transamináza vyrábí alanin.
| pyruvát | alanin transamináza | alanin | |
 |  | ||
| glutamát | α-ketoglutarát | ||
 | |||
| glutamát | α-ketoglutarát | ||
Redukce na laktát
Snížení o laktátdehydrogenáza vyrábí laktát.
| pyruvát | laktátdehydrogenáza | laktát | |
 |  | ||
| NADH | NAD+ | ||
 | |||
| NADH | NAD+ | ||
Použití
Pyruvát se prodává jako doplněk na hubnutí, ačkoli důvěryhodná věda toto tvrzení ještě musí podpořit. A systematický přehled ze šesti pokusy našel statisticky významný rozdíl v tělesné hmotnosti u pyruvátu ve srovnání s placebo. Všechny pokusy však měly metodologické nedostatky a rozsah účinku byl malý. Přezkum rovněž zjistil nežádoucí účinky spojené s pyruvátem, jako je průjem, nadýmání, plynatost a zvýšení lipoprotein s nízkou hustotou (LDL) cholesterol. Autoři dospěli k závěru, že neexistují dostatečné důkazy na podporu použití pyruvátu pro hubnutí.[11]
K dispozici je také in vitro stejně jako in vivo důkazy v srdcích, že pyruvát zlepšuje metabolismus stimulací produkce NADH a zvyšuje srdeční funkce.[12][13]
Viz také
Poznámky
- ^ A b Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 748. doi:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ Dawson, R. M. C .; et al. (1959). Data pro biochemický výzkum. Oxford: Clarendon Press.
- ^ Fox, Stuart Ira (2011). Fyziologie člověka (12. vydání). McGraw = Hill. str. 146.[ISBN chybí ]
- ^ Ophardt, Charles E. "Kyselina pyrohroznová - směs silnic". Virtuální chembook. Elmhurst College. Citováno 7. dubna 2017.
- ^ Thomson, Thomas (1838). „Kapitola II. Sekce fixovaných kyselin“. Chemie organických těl, zelenina. London: J. B. Baillière. str. 65. Citováno 1. prosince 2010.
- ^ Berzelius, J. (1835). „Ueber eine neue, durch Destilace von Wein-und Traubensäure erhaltene Säure“. Annalen der Pharmacie. 13 (1): 61–63. doi:10,1002 / jlac.18350130109.
- ^ "Kyselina pyrohroznová". ChemSpider. Royal Society of Chemistry. Citováno 21. dubna 2017.
- ^ Howard, J. W .; Fraser, W. A. "Kyselina pyrohroznová". Organické syntézy. 4: 63.; Kolektivní objem, 1, str. 475
- ^ A b Lehninger, Albert L .; Nelson, David L .; Cox, Michael M. (2008). Principy biochemie (5. vydání). New York, NY: W. H. Freeman and Company. str.528. ISBN 978-0-7167-7108-1.
- ^ Aren van Waarde; G. Van den Thillart; Maria Verhagen (1993). „Tvorba ethanolu a regulace pH u ryb“. Přežívající hypoxie. str. 157–170. hdl:11370 / 3196a88e-a978-4293-8f6f-cd6876d8c428. ISBN 0-8493-4226-0.
- ^ Onakpoya, I .; Hunt, K .; Širší, B .; Ernst, E. (2014). „Suplementace pyruvátem pro hubnutí: systematický přehled a metaanalýza randomizovaných klinických studií“. Krit. Rev. Food Sci. Nutr. 54 (1): 17–23. doi:10.1080/10408398.2011.565890. PMID 24188231. S2CID 20241217.
- ^ Jaimes, R., III (červenec 2015). „Funkční odpověď izolovaného, perfundovaného normoxického srdce na aktivaci pyruvátdehydrogenázy pomocí dichloracetátu a pyruvátu“. Pflügers Arch. 468 (1): 131–42. doi:10.1007 / s00424-015-1717-1. PMC 4701640. PMID 26142699.
- ^ Hermann, H. P .; Pieske, B .; Schwarzmüller, E .; Keul, J .; Jen, H .; Hasenfuss, G. (1999-04-17). „Hemodynamické účinky intrakoronárního pyruvátu u pacientů s městnavým srdečním selháním: otevřená studie“. Lanceta. 353 (9161): 1321–1323. doi:10.1016 / s0140-6736 (98) 06423-x. ISSN 0140-6736. PMID 10218531. S2CID 25126646.
Reference
- Cody, G. D .; Boctor, N.Z .; Filley, T. R .; Hazen, R. M .; Scott, J. H .; Sharma, A .; Yoder, H. S., Jr. (2000). „Prvotní karbonylované sloučeniny železa a síry a syntéza pyruvátu“. Věda. 289 (5483): 1337–1340. Bibcode:2000Sci ... 289.1337C. doi:10.1126 / science.289.5483.1337. PMID 10958777. S2CID 14911449.
externí odkazy
ATP ADP ATP ADP + + 2 ×  2 ×  2 × 3-fosfoglycerát 2 ×  2 × 2-fosfoglycerát 2 ×  2 × Fosfoenolpyruvát 2 ×  ADP ATP 2 × Pyruvát 2 × |