RTI-274 - RTI-274
 | |
| Identifikátory | |
|---|---|
| |
| Chemické a fyzikální údaje | |
| Vzorec | C21H22FNÓ3 |
| Molární hmotnost | 355.409 g · mol−1 |
| 3D model (JSmol ) | |
| |
| (ověřit) | |
RTI (-4229)-274nebo 2β - ((3,4-methyl
Úvod
Ve skutečnosti je známo velmi málo esterů fenyltropanů.
NS2330 a NS2359 oba mají α, β stereochemii.
NS2214 se zdá být nyní opuštěný, RTI-336 byla jejich poslední sloučenina.
RTI se rozhodli, že chtějí vyrobit všech 8 stereoizomerů fenyltropanu paroxetin homolog.[1]
| ROHOŽ IC50 (nM) Nor / tropan-paroxetinové hybridy | ||||
| Sloučenina | [3H] CFT | [3H] paroxetin | [3H] nisoxetin | |
| Paroxetin | ? → 623 | ? → 0.28 | ? → 535 | |
| R | „β, β“ | 308 → 835 | 294 → 480 | 5,300 → 37,400 |
| α, β | 172 → 142 | 52.9 → 90 | 26,600 → 2,500 | |
| β, α | 3.01 → 3.86 | 422 → 5.62 | 123 → 14.4 | |
| S | „β, β“ | 1,050 → 1,210 | 88.1 → 424 | 27,600 → 17,300 |
| α, β | 1,500 → 27.6 | 447→ 55.8 | 2,916 → 1,690 | |
| β, α | 298 → 407 | 178 → 19 | 12,400 → 1,990 | |
- N- demetylovat S-α, β (1S, 2S, 3R) izomer vedl k 54násobnému zvýšení DAT IC50.
V případě nocain rozumí se, že SR enantiomer je ten, který by měl být demethylován, pokud má zlepšit afinitu DAT.
Jedná se o stejný enantiomer, který se používá při výrobě paroxetinu.
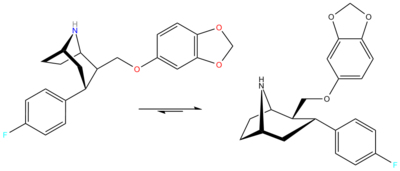
Kosterní přesmyk

O čtyři roky později to někteří nesouvisející autoři uvedli jako kosterní přesmyk.[2] Diagram[mrtvý odkaz ]
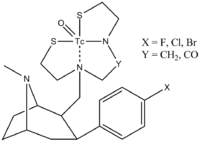
Všimněte si, že se nezajímají jen o ethery, ale o dusíkaté látky obsahující Nu („TRODAT ")[3]
Kov se nazývá „Technecium "a je vázán a chelátování činidlo.
Autoři uvádějí, že nejprve je kyselina halogenována, amid je připraven a redukován.
Tisková chyba

(a) (1) 1-chlorethylchlorformiát, 1,2-dichlorethan, reflux; (2) MeOH reflux; b) str-toluensulfonylchlorid, triethylamin; (c) LiAlH4, THF, rt; (d) anhydrid kyseliny trifluormethansulfonové, pyridin, CH2Cl2; (e) Na, sesamol, THF; (f) 5% Na / Hg amalgám, Na2HPO4, MeOH.
| ROHOŽ IC50 (K.i) N-Metyl → De-methyl | |||
| Sloučenina | [3H] CFT | [3H] nisoxetin | [3H] paroxetin |
| R-β, β | ? → 3 | ? → 2 (0.2) | ? → 6 (4) |
| S-β, β | ? → ? | ? → ? (?) | ? → ? (?) |
| R- "nonan" | 308 → 835 | 294 (27) → 480 (44) | 5,300 (3200) → 37,400 (22,500) |
| S- "nonan" | 1050 → 1210 | 88 (8) → 424 (39) | 27,600 (16,600) → 17,300 (10,400) |

Aby se vyřešil problém neočekávaného aza-bicyklo [3.2.2] nonanového přesmykového produktu, musela být původní syntéza upravena následujícím způsobem;[4] VYHRAJ 35428 byl N-demethylován a potom NH amin reagoval s vhodným chránící skupina takže N již není nukleofilní. V jejich případě použili tosyl.[3]
Viz také
Reference
- ^ A b Keverline-Frantz KI, Boja JW, Kuhar MJ, Abraham P, Burgess JP, Lewin AH, Carroll FI (leden 1998). "Syntéza a vazba ligandu analogů tropanového kruhu paroxetinu". Journal of Medicinal Chemistry. 41 (2): 247–57. doi:10.1021 / jm970669p. PMID 9457247.
- ^ Ogier L, Turpin F, Baldwin RM, Riché F, Law H, Innis RB, Tamagnan G (květen 2002). „Přesmyk mezylát-tropanového meziproduktu v nukleofilních substitučních reakcích. Syntéza aza-bicyklo [3.2.1] oktanu a aza-bicyklo [3.2.2] nonanetherů, imidů a aminů.“ The Journal of Organic Chemistry. 67 (11): 3637–42. doi:10.1021 / jo010973x. PMID 12027674.
- ^ A b Singh S (březen 2000). "Chemie, design a vztah mezi strukturou a aktivitou kokainových antagonistů". Chemické recenze. 100 (3): 925–1024. doi:10.1021 / cr9700538. PMID 11749256. S2CID 36764655.
- ^ Runyon SP, Burgess JP, Abraham P, Keverline-Frantz KI, Flippen-Anderson J, Deschamps J a kol. (Duben 2005). „Syntéza, strukturní identifikace a vazba ligandu analogů tropanového kruhu paroxetinu a neočekávaného produktu přesmyku aza-bicyklo [3.2.2] nonanu“. Bioorganická a léčivá chemie. 13 (7): 2439–49. doi:10.1016 / j.bmc.2005.01.046. PMID 15755646.
