Itoprid - Itopride
 | |
 | |
| Klinické údaje | |
|---|---|
| AHFS /Drugs.com | Mezinárodní názvy drog |
| Trasy z správa | Orální (potažené filmem tablety ) |
| ATC kód |
|
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Biologická dostupnost | ~60% (Tmax = 35 ± 5 min) |
| Vazba na bílkoviny | 96% |
| Metabolismus | Rozsáhlé jaterní (FMO1 a FMO3 ), především N-oxidace[2] |
| Odstranění poločas rozpadu | 5,7 ± 0,3 hodiny |
| Vylučování | Renální (3,7–4,1% jako nezměněný itoprid, 75,4–89,4% jako itoprid-N-kysličník)[1] |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.222.888 |
| Chemické a fyzikální údaje | |
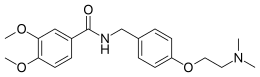
| Vzorec | C20H26N2Ó4 |
| Molární hmotnost | 358.438 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| | |
Itoprid (HOSPODA ) (jméno značky Ganaton) je prokinetický benzamid derivát. Tyto léky inhibují dopamin a enzym acetylcholinesterázy a mají a gastrokinetický účinek.[3] Itoprid je indikován k léčbě funkční dyspepsie a další gastrointestinální stavy.[4] Je to kombinovaná D2 receptor antagonista a inhibitor acetylcholinesterázy.[5][6]
Itoprid není v současné době schválen US Food and Drug Administration (FDA) pro použití v Spojené státy, ani to ještě není schváleno v EU Spojené království. To může vysvětlovat zjevný nedostatek informací o pacientech dostupných v Angličtina ve srovnání s jinými podobnými skupinami léků.
Lékařské použití

Typicky je itoprid indikován k léčbě GI symptomů způsobených sníženou GI motilitou:
- dyspepsie typu bez vředů / dysmotility (žaludeční „plnost“, nepohodlí a možná bolest)[7][8]
- gastroparéza (opožděné vyprazdňování žaludku)[9]
- anorexie
- pálení žáhy
- regurgitace
- nadýmání
- nevolnost a zvracení
- další možné stavy související se žaludkem, prolaktinem nebo dopaminem
Itoprid se obvykle užívá třikrát denně. Dávka se obvykle užívá nalačno asi hodinu před jídlem. Dávkování a podrobnosti podání se však mohou lišit v závislosti na věku pacienta, jeho příznacích a dalších faktorech.
V placebem kontrolovaných studiích bylo prokázáno, že Itoprid významně zlepšuje příznaky u pacientů s funkční dyspepsií a poruchami motility.
Tyto studie dospěly k závěru, že snížení závažnosti příznaků funkční dyspepsie po 8 týdnech léčby itopridem naznačuje, že itoprid byl významně lepší než placebo a že itoprid významně snižoval bolest a plnost ve srovnání s placebem.[10]
Kontraindikace a bezpečnostní opatření
Itoprid je relativně nový lék a v současné době není schválen ani pro běžné předepsané použití OTC použití v USA ani ve Velké Británii. To však nemusí nutně znamenat, že itoprid není účinný nebo bezpečný.
Pacienti užívající itoprid by měli hlásit jakékoli nežádoucí účinky svému ošetřujícímu lékaři.
Itoprid je kontraindikován při přecitlivělosti na itoprid nebo benzamidy; laktace GI krvácení, překážka nebo perforace. Itoprid nemusí být indikován u pacientů trpících Parkinsonova choroba nebo jiné podmínky zahrnující dopamin otázky regulace. Itoprid by měl být používán se zvláštní opatrností u mladých a starších osob. V současné době není k dispozici dostatek informací o bezpečném užívání itopridu během těhotenství.
Nežádoucí účinky
Mezi nejčastější vedlejší účinky itopridu patří mírné až středně silné bolesti břicha a průjem.[7] Některé další nežádoucí účinky, které se mohou objevit, zahrnují: vyrážka závratě, vyčerpání, bolesti zad nebo hrudníku, zvýšené slinění, zácpa, bolest hlavy poruchy spánku, závratě, galaktorea, a gynekomastie.
Mohou být přítomny i další nežádoucí účinky.
Leukopenie, snížení normální hladiny bílých krvinek, může být potenciálně život ohrožující reakcí na itoprid.
Nežádoucí účinky na centrální nervový systém nemají tendenci se vyskytovat kvůli špatnému průniku přes hematoencefalickou bariéru, i když může dojít k mírnému zvýšení hladin prolaktinu.[7] Zvyšování hladin prolaktinu je častější u režimů vysokých dávek itopridu.[11]
Srdeční studie
Itoprid patří do stejné skupiny benzamid seskupit jako cisaprid, lék, o kterém bylo zjištěno, že ovlivňuje QT interval a možná předisponovat ty, kteří jej používají, na srdce arytmie. Itoprid však nemá žádný nepříznivý účinek na QT interval.[7]
Později se ve studii provedené se zdravými dospělými dobrovolníky ukázalo, že je nepravděpodobné, že by itoprid způsoboval srdeční arytmie nebo změny EKG částečně kvůli nedostatku významné interakce a metabolismu prostřednictvím cytochrom P450 enzymová cesta, na rozdíl od cisaprid a mosaprid, protože je metabolizován jinou sadou enzymů. Nové molekulární studie na komorových morčatech myocyty také podporoval srdeční bezpečnostní profil itopridu, protože neovlivňoval určité mechanismy draslíku, které mohly být ovlivněny cisapridem nebo mosapridem. Itoprid navíc nemá žádnou afinitu k 5-HT4 receptory, na rozdíl od jiných benzamidy jako je cisaprid a mosaprid, což jsou 5-HT4 agonisté. Afinita cisapridu k 5-HT4 receptory v srdci se podílejí na nežádoucích srdečních účincích samotného cisapridu.
Závěr této studie ukázal, že itoprid nemá žádný abnormální účinek na QT interval. Je proto možné, že itoprid lze považovat za lepší a určitě bezpečnější prokinetické činidlo než kterýkoli z nich cisaprid nebo mosaprid a itoprid by měl být také považován za vítaný doplněk léčby symptomatické neulcerózní dyspepsie a dalších poruch motility žaludku.[12]
Farmakologie
Itoprid působí jako selektivní dvojník D2 receptor antagonista a inhibitor acetylcholinesterázy.[5][6]
Existují důkazy, že itoprid může mít prokinetické účinky v celém gastrointestinálním traktu od žaludku po konec tlustého střeva.[13] Zdá se, že farmakokinetika itopridu se u asijské a bělošské populace liší, přičemž běloši mají po perorálním podání o 30–50 procent nižší hladiny itopridu v krvi.[14] Itoprid špatně proniká přes hematoencefalickou bariéru kvůli své vysoké polaritě, a proto itoprid nemá tendenci způsobovat žádné centrální nervový systém nepříznivé účinky.[7] Itoprid nemá žádný účinek na draslíkové kanály.[15]
Podobně jako ostatní D2 antagonisté receptoru, bylo zjištěno, že itoprid se zvyšuje v závislosti na dávce prolaktin úrovně.[6]
Farmakokinetika
Po perorálním podání prochází itoprid rychlou a rozsáhlou absorpcí, přičemž hladiny itopridu vrcholí v krevní plazmě po pouhých 35 minutách. Itoprid je primárně vylučován ledvinami, které mají eliminační poločas přibližně 6 hodin.[16]
Mechanismus účinku

Itoprid se zvyšuje acetylcholin koncentrace inhibicí receptory dopaminu D2 a acetylcholinesteráza. Vyšší acetylcholin zvyšuje GI peristaltika, zvyšuje tlak dolního jícnového svěrače, stimuluje žaludeční motilitu, urychluje vyprazdňování žaludku a zlepšuje gastro-duodenální koordinaci.[7]
Itoprid podávaný ve studii s jednou dávkou zjistil, že také zvyšuje hladinu motilin, somatostatin a snižuje úroveň cholecystokinin, stejně jako adrenokortikotropní hormon. Tyto účinky mohou také přispívat k farmakologii itopridu.[17]
Interakce
Anticholinergikum látky snižují účinek itopridu. Je třeba poznamenat, že itoprid je relativně nový lék, a proto je možné, že s itopridem mohou interagovat jiné léky, které způsobují kontraindikace nebo vedlejší účinky, které nejsou v současné době známy.
Obchodní názvy
Itopride je dostupný pod obchodními názvy Ganaton ((JP, CZ, RU), Abbott Laboratories ), Itomed ((RU, KR, UA, MD), PRO.MED.CS Praha a.s.), Itogarda (Apex Pharmaceuticals, Nepál) a další. V Mexiku prodává itoprid (50 mg) společnost Takeda Laboratories pod značkou Dagla. V Bulharsku a dalších východoevropských zemích prodává itoprid (50 mg) společnost Zentiva pod značkou Zirid [18]
Viz také
Reference
- ^ "Tablety Ganaton (itoprid hydrochlorid) 50 mg. Informace o předepisování" (PDF). Abbott Japan Co., Ltd. Archivováno od originál (PDF) dne 11. prosince 2015. Citováno 9. prosince 2015.
- ^ Smith, Dennis A .; Allerton, Charlotte; Kubinyi, Hugo; van de Waterbeemd, Han; Walker, Don K., eds. (Duben 2012). Farmakokinetika a metabolismus v designu léčiv (3. vyd.). Weinheim: Wiley-VCH. p. 132. ISBN 978-3-527-32954-0.
- ^ Iwanaga Y, Miyashita N, Saito T, Morikawa K, Itoh Z (červen 1996). „Gastroprokinetický účinek nového benzamidového derivátu itopridu a jeho mechanismy působení u psů při vědomí“. Jpn. J. Pharmacol. 71 (2): 129–37. doi:10,1254 / jjp.71.129. PMID 8835639.
- ^ Holtmann G, Talley NJ, Liebregts T, Adam B, Parow C (únor 2006). „Placebem kontrolovaná studie itopridu s funkční dyspepsií“. N. Engl. J. Med. 354 (8): 832–40. doi:10.1056 / NEJMoa052639. PMID 16495395.
- ^ A b Henry P. Parkman; Richard W. McCallum (5. října 2011). Gastroparéza: Patofyziologie, prezentace a léčba. Springer. 264–. ISBN 978-1-60761-552-1.
- ^ A b C William Y. Chey; William D. Chey (2011). Syndrom dráždivého tračníku, problém gastroenterologických klinik. Elsevier Health Sciences. str. 232–. ISBN 978-1-4557-0450-7.
- ^ A b C d E F Huang, X .; Lv, B .; Zhang, S .; Fan, YH .; Meng, LN. (Prosinec 2012). „Itopridová terapie funkční dyspepsie: metaanalýza“. Svět J Gastroenterol. 18 (48): 7371–7. doi:10,3748 / wjg.v18.i48.7371. PMC 3544044. PMID 23326147.
- ^ Chiba, T .; Tokunaga, Y .; Ikeda, K .; Takagi, R .; Chishima, R .; Terui, T .; Kudara, N .; Endo, M .; et al. (Září 2007). „Účinky itopridiumchloridu a ranitidinu u pacientů s funkční dyspepsií: srovnání mezi prokinetickou a kyselinou potlačující terapií“. Hepatogastroenterologie. 54 (78): 1878–81. PMID 18019739.
- ^ Keil, R. (květen 2004). „[Prokinetika a diabetes mellitus]“. Vnitr Lek. 50 (5): 358, 360–2. PMID 15305632.
- ^ Holtmann, Gerald; Talley, Nicholas J .; Liebregts, Tobias; Adam, Birgit; Parow, Christopher (2006). „Placebem kontrolovaná studie s itopridem při funkční dyspepsii“. New England Journal of Medicine. 354 (8): 832–40. doi:10.1056 / NEJMoa052639. PMID 16495395.
- ^ Kim, YS .; Kim, TH .; Choi, CS .; Shon, YW .; Kim, SW .; Seo, GS .; Nah, YH .; Choi, MG .; Choi, SC. (Červenec 2005). „Účinek itopridu, nového prokinetika, u pacientů s mírnou GERD: pilotní studie“ (PDF). Svět J Gastroenterol. 11 (27): 4210–4. doi:10,3748 / wjg.v11.i27.4210. PMC 4615444. PMID 16015691. Archivovány od originál (PDF) dne 05.10.2013.
- ^ Gupta, Seema; Kapoor, Vinod; Gupta, B. M .; Kapoor, B .; Verma, Ujala; Gupta, Vikram (2005). „Vliv ittopridiumchloridu na QT interval u dospělých zdravých dobrovolníků“ (PDF). Praktik JK. 12 (4): 207–10.
- ^ Lim, HC .; Kim, YG .; Lim, JH .; Kim, HS .; Park, H. (červen 2008). „Účinek itopridiumchloridu na ileální a tlustou střevu morčat in vitro“. Yonsei Med J. 49 (3): 472–8. doi:10,3349 / ymj.2008.49.3.472. PMC 2615341. PMID 18581598.
- ^ Stevens, JE .; Russo, A .; Maddox, AF .; Rayner, CK .; Phillips, L .; Talley, NJ .; Giguère, M .; Horowitz, M .; Jones, KL. (Květen 2008). "Účinek itopridu na vyprazdňování žaludku u dlouhodobého diabetes mellitus". Neurogastroenterol Motil. 20 (5): 456–63. doi:10.1111 / j.1365-2982.2007.01058.x. PMID 18179609.
- ^ Morisawa, T .; Hasegawa, J .; Hama, R .; Kitano, M .; Kishimoto, Y .; Kawasaki, H. (1999). "Účinky hydrochloridu itopridu na zpožděné proudy usměrňovače K + a L2 typu v komorových myocytech morčat". Res Commun Mol Pathol Pharmacol. 106 (1–2): 37–45. PMID 11127807.
- ^ Bose, A .; Wong, TW .; Singh, N. (duben 2013). „Vývoj formulace a optimalizace tablety matrice s prodlouženým uvolňováním Itopride HCl metodou povrchové odezvy a jejím hodnocením kinetiky uvolňování“. Saudi Pharm J. 21 (2): 201–13. doi:10.1016 / j.jsps.2012.03.006. PMC 3744972. PMID 23960836.
- ^ Katagiri, F .; Shiga, T .; Inoue, S .; Sato, Y .; Itoh, H .; Takeyama, M. (2006). „Účinky hydrochloridu itopridu na plazmatické regulační peptidy a hladiny hormonů souvisejících se stresem u zdravých lidských subjektů“. Farmakologie. 77 (3): 115–21. doi:10.1159/000093485. PMID 16717477.
- ^ http://www.bda.bg/images/stories/documents/bdias/Z-1.htm
