Arytmogenní kardiomyopatie - Arrhythmogenic cardiomyopathy
tento článek potřebuje další citace pro ověření. (Únor 2009) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
| Arytmogenní kardiomyopatie | |
|---|---|
| Ostatní jména | arytmogenní kardiomyopatie pravé komory (ARVC), arytmogenní dysplázie pravé komory / kardiomyopatie (ARVD / C), dysplazie pravé komory |
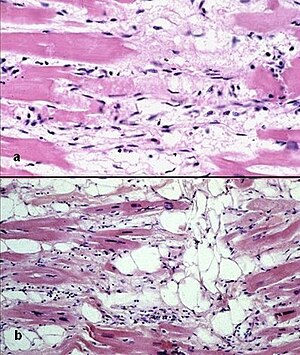 | |
| Mikrofotografie srdce ACM. | |
| Specialita | Kardiologie |
Arytmogenní kardiomyopatie (ACM), arytmogenní dysplázie pravé komory (ARVD), nebo arytmogenní kardiomyopatie pravé komory (ARVC), je zděděný srdeční choroba.[1]
ACM je způsobeno genetické vady částí srdeční sval (také zvaný myokard nebo srdeční sval) známý jako desmosomy, oblasti na povrchu buněk srdečního svalu, které spojují buňky dohromady. Desmosomy se skládají z několika bílkoviny a mnoho z těchto proteinů může mít škodlivé účinky mutace.
Nemoc je typem neischemické kardiomyopatie který zahrnuje především pravá komora, ačkoli byly hlášeny případy výlučného onemocnění levé komory. Vyznačuje se hypokinetický oblasti zahrnující volnou stěnu komory s fibrofatózní náhradou myokardu, s přidruženými arytmie často pocházející z pravé komory. Názvosloví ARVD je v současné době považováno za nevhodné a zavádějící, protože ACM nezahrnuje dysplázii komorové stěny. Případy ACM pocházející z levé komory vedly k opuštění názvu ARVC.
ACM lze nalézt ve spojení s difúzní palmoplantární keratoderma, a vlněné vlasy, v autosomálně recesivním stavu zvaném Naxosova choroba, protože tato genetická abnormalita může také ovlivnit integritu povrchových vrstev kůže nejvíce vystavených tlakovému stresu.[2]:513[3]
ACM je důležitou příčinou komorových arytmií u dětí a mladých dospělých. Vyskytuje se převážně u mužů a 30–50% případů má rodinnou distribuci.
Příznaky a symptomy
Ti, kteří jsou postiženi arytmogenní kardiomyopatií, nemusí mít vůbec žádné příznaky, přestože mají významné abnormality ve struktuře srdce.[4] Pokud se příznaky objeví, je počáteční projev často způsoben abnormálními srdečními rytmy (arytmie), které při arytmogenní kardiomyopatii mohou mít formu bušení srdce nebo výpadků proudu.[5] Náhlá smrt může být prvním projevem ACM bez jakýchkoli předchozích příznaků.[4] Tyto příznaky se často vyskytují během dospívání a časná dospělost, ale známky ACM se u kojenců vyskytují jen zřídka.
Jak ACM postupuje, svalová tkáň v komorách se může dilatovat a oslabovat. Pravá komora obvykle nejprve oslabuje, což vede k únavě a otoku kotníku. V pozdějších stadiích onemocnění, při nichž jsou zapojeny obě komory, se může objevit dušnost, zvláště když ležíte naplocho.[4]
První klinické příznaky ACM jsou obvykle během dospívání a raná dospělost. U kojenců však byly známky ACM prokázány zřídka.
Genetika
ACM se obvykle dědí v autosomálně dominantní vzor s variabilním výrazem. Pouze 30% až 50% jedinců postižených ACM bude mít pozitivní test na jednu ze známých genetických mutací chromozomální loci spojené s nemocí.[6][7] Nové studie ukázaly, že mutace (bodové mutace) v genech kódujících desmosomální proteiny (viz vložený disk ) jsou hlavními původci vzniku tohoto onemocnění. Nedávno se ukázalo, že mutace v desmin Gen DES může způsobit ACM.[8] Desmin je meziproduktový vláknitý protein, který je spojen s desmosomy. Odlišný DES mutace způsobují abnormální agregaci desminu a asociovaných proteinů.[9] The pronikavost je 20–35% obecně, ale v Itálii výrazně vyšší. Sedm genových lokusů bylo zapojeno do ACM. Není jasné, zda se patogeneze mění s různými zúčastněnými lokusy. Standardní genetické screeningové testy jsou v současné době testovány a hodnoceny v různých nejmodernějších kardiovaskulárních výzkumných centrech a nemocnicích. Typy zahrnují:
| Typ | OMIM | Gen | Místo | Odkaz |
|---|---|---|---|---|
| ARVD1lpl | 107970 | TGFB3 | 14q23-q24 | [10] |
| ARVD2 | 600996 | RYR2 | 1q42-q43 | [11] |
| ARVD3 | 602086 | ? | 14q12-q22 | |
| ARVD4 | 602087 | ? | 2q32.1-q32.3 | |
| ARVD5 | 604400 | TMEM43 | 3p23 | [12][13] |
| ARVD6 | 604401 | ? | 10p14-p12 | |
| ARVD7 | 609160 | DES | 10q22.3 | [14][15] |
| ARVD8 | 607450 | DSP | 6p24 | [16] |
| ARVD9 | 609040 | PKP2 | 12p11 | [17] |
| ARVD10 | 610193 | DSG2 | 18q12.1-q12 | [18][19] |
| ARVD11 | 610476 | DSC2 | 18q12.1 | [20][21] |
| ARVD12 | 611528 | JUP | 17q21 | [22][23] |
| ILK | 11p15.4 | [24] | ||
| LMNA | [25] |
Patogeneze
The patogeneze ACM je do značné míry neznámý. Apoptóza (programovaná buněčná smrt) zřejmě hraje velkou roli. Dříve se předpokládalo, že se jedná pouze o pravou komoru, ale nedávné kohorty ukázaly mnoho případů onemocnění levé komory a biventrikulární choroby. Proces nemoci začíná v subepikardiální oblasti a postupuje směrem k povrchu endokardu, což vede k transmurálnímu postižení (což pravděpodobně odpovídá za aneuryzmatickou dilataci komor). Zbytkový myokard je omezen na subendokardiální oblast a trabekuly komor. Tyto trabekuly mohou být hypertrofovány.
Aneuryzmatická dilatace je při pitvě pozorována v 50% případů. Obvykle se vyskytuje v brániční, apikální a infundibulární oblasti (známé jako trojúhelník dysplazie). Levá komora je zapojena u 50–67% jedinců. Pokud je postižena levá komora, je to obvykle pozdě v průběhu onemocnění a přináší špatnou prognózu.
Existují dva patologické vzorce pozorované u ACM, mastná infiltrace a fibro-mastná infiltrace.
Mastná infiltrace
První, mastná infiltrace, je omezena na pravou komoru. To zahrnuje částečnou nebo téměř úplnou substituci myokardu tukovou tkání bez ztenčení stěny. Jedná se převážně o apikální a infundibulární oblasti RV. Levá komora a komorové septum jsou obvykle ušetřeny. U mastné infiltrace nejsou vidět žádné zánětlivé infiltráty. Existují důkazy o myocyt degenerace a smrt (buňky myokardu) pozorována u 50% případů infiltrace tuků.
Fibro-mastná infiltrace
Druhá, fibrotučná infiltrace, zahrnuje nahrazení myocytů fibrofatní tkání. Skvrnitá myokarditida se vyskytuje až ve 2/3 případů se zánětlivými infiltráty (většinou T buňky ) viděný mikroskopem. Atrofie myokardu je důsledkem poranění a apoptóza. To vede ke ztenčení stěny bez RV (do tloušťky <3 mm). Myocyty jsou nahrazeny fibrofatní tkání. Mezi regiony, které jsou přednostně zapojeny, patří přítokový trakt RV, výtokový trakt RV a vrchol RV. V některých případech však může být zapojena stěna bez LV. Zapojení komorového septa je vzácné. Zúčastněné oblasti jsou náchylné k tvorbě aneuryzmatu.
Role cvičení
V poslední době některé studie identifikovaly namáhavé cvičení jako nové riziko pro zrychlenou progresi onemocnění. Jedna retrospektivní studie na 301 pacientech přesvědčivě prokázala, že subpopulace účastnící se namáhavé fyzické aktivity (například profesionální sportovci) měly ve srovnání s jinými populacemi dřívější nástup příznaků a dřívější úmrtnost.[26]
Komorové arytmie

Komorové arytmie způsobené ACM obvykle vznikají z nemocné pravé komory. Typ arytmie se pohybuje od častých předčasné komorové komplexy (PVC) do ventrikulární tachykardie (VT) do ventrikulární fibrilace (VF).
I když je iniciační faktor komorových arytmií nejasný, může to být způsobeno spuštěnou aktivitou nebo reentry.
Ventrikulární arytmie obvykle souvisejí s cvičením, což naznačuje, že jsou citlivé na katecholaminy. Komorové rytmy mají obvykle odchylku pravé osy. U jednoho jedince může být přítomno více morfologií komorové tachykardie, což naznačuje více arytmogenní ohniska nebo cesty.
Tachykardie pravého komorového výtokového traktu (RVOT) je nejčastější VT pozorovanou u jedinců s ACM. V tomto případě EKG ukazuje a blok levé větve svazku (LBBB) morfologie s dolní osou.
Diagnóza
The diferenciální diagnostika pro komorovou tachykardii způsobenou ACM zahrnují:
- Vrozená srdeční choroba
- Opraveno Fallotova tetralogie
- Ebsteinova anomálie
- Uhlova anomálie
- Porucha síňového septa
- Částečný anomální žilní návrat
- Získané srdeční choroby
- Onemocnění trikuspidální chlopně
- Plicní Hypertenze
- Infarkt pravé komory
- Tachykardie s opakovaným vstupem do svazku větví
- Smíšený
- Pre-vzrušená AV re-entry tachykardie
- Idiopatická RVOT tachykardie
- Sarkoidóza
Pro stanovení diagnózy ACM se používá řada klinických testů, včetně elektrokardiogram (EKG), echokardiografie, angiografie pravé komory, srdeční MRI a genetické testování.
Elektrokardiogram
90% jedinců s ARVD má nějakou abnormalitu EKG. Nejběžnější abnormalitou EKG pozorovanou v ACM je inverze vlny T ve svodech V1 do V3. Jedná se však o nespecifický nález a lze jej považovat za normální variantu v pravý blok větve svazku (RBBB), ženy a děti do 12 let.
Samotný RBBB se často vyskytuje u jedinců s ACM. To může být způsobeno opožděnou aktivací pravé komory, spíše než jakoukoli vnitřní abnormalitou ve větvi pravého svazku.

Vlna epsilon se vyskytuje asi u 50% pacientů s ACM. Toto je popsáno jako koncový zářez v komplexu QRS. Je to způsobeno zpomaleným intraventrikulárním vedením. Vlnu epsilon lze vidět na povrchovém EKG; je to však častěji vidět na EKG průměrovaných signálem.
Ventrikulární ektopie viděný na povrchu EKG v nastavení ACM je typicky blok levé větve svazku (LBBB) morfologie, s osou QRS -90 až +110 stupňů. Původ ektopických tepů obvykle pochází z jedné ze tří oblastí tukové degenerace („trojúhelník dysplazie“): odtokový trakt RV, přítokový trakt RV a vrchol RV.
Průměrný signál EKG (SAECG ) se používá k detekci pozdních potenciálů a vln epsilon u jedinců s ACM.
Echokardiografie
Echokardiografie může odhalit zvětšenou hypokinetickou pravou komoru s papírově tenkou stěnou bez RV. Dilatace RV způsobí dilataci mezikruží trikuspidální chlopně s následnou trikuspidální regurgitace. Může být také přítomen paradoxní septální pohyb.
MRI

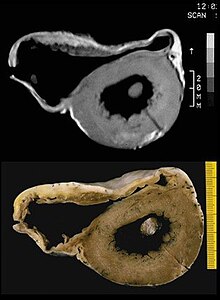
Mastná infiltrace stěny bez RV může být viditelná na srdečním MRI. Tuk zvýšil na obrázcích vážených pomocí T1 intenzitu. Může však být obtížné rozlišit intramyokardiální tuk a epikardiální tuk, který se běžně vyskytuje v sousedství normálního srdce. Subtricuspidální oblast může být také obtížně odlišitelná od atrioventrikulárního sulku, který je bohatý na tuk.
Srdeční MRI dokáže vizualizovat extrémní ztenčení a akinezi stěny bez RV. Normální stěna bez RV však může mít tloušťku asi 3 mm, což činí test méně citlivým.
Angiografie
Angiografie pravé komory je považována za Zlatý standard pro diagnostiku ACM. Nálezy shodné s ACM jsou akinetické nebo dyskinetické vyboulení lokalizované do infundibulárních, apikálních a subtricuspidálních oblastí RV. Specificita je 90%; test je však závislý na pozorovateli.
Biopsie
Transvenózní biopsie pravé komory může být vysoce specifická pro ACM, ale má nízkou citlivost. Falešné pozitivity zahrnují další stavy s mastnou infiltrací komory, jako je chronické zneužívání alkoholu a Duchenne / Beckerova svalová dystrofie.
Falešné negativy jsou běžné, nicméně, protože onemocnění postupuje typicky z epikardu do endokardu (s bioptickým vzorkem pocházejícím z endokardu) a segmentální povahou onemocnění. Také kvůli papírové tenké volné komoře pravé komory, která je běžná v tomto procesu onemocnění, se většina bioptických vzorků odebírá z komorového septa, které je obvykle ne podílející se na chorobném procesu.
Vzorek biopsie, který odpovídá ACM, by měl> 3% tuku,> 40% vláknité tkáně a <45% myocytů.
Post mortem histologická demonstrace plné tloušťky substituce RV myokardu mastnou nebo fibro-mastnou tkání je v souladu s ACM.
Genetické testování
ACM je autosomálně dominantní vlastnost se sníženou pronikavost. Přibližně 40–50% pacientů s ACM má mutaci identifikovanou v jednom z několika genů kódujících složky desmosome, což může pomoci potvrdit diagnózu ACM.[27] Vzhledem k tomu, že ACM je autosomálně dominantní znak, mají děti pacienta s ACM 50% pravděpodobnost, že zdědí mutaci způsobující onemocnění. Kdykoli je mutace identifikována genetickým testováním, lze použít genetické testování specifické pro rodinu k rozlišení mezi příbuznými, kteří jsou vystaveni riziku onemocnění, a těmi, kteří nejsou. Genetické testování ACM je klinicky dostupné.[28]
Diagnostická kritéria
ACM nemá žádnou patognomonickou vlastnost. Diagnóza ACM je založena na kombinaci hlavních a vedlejších kritérií. Stanovení diagnózy ACM vyžaduje buď 2 hlavní kritéria nebo 1 hlavní a 2 menší kritéria nebo 4 menší kritéria.[29]
Hlavní kritéria
- Dysfunkce pravé komory
- Silná dilatace a redukce RV ejekční frakce s malým nebo žádným postižením LV
- Lokalizované aneuryzma RV
- Silná segmentová dilatace RV
- Charakterizace tkáně
- Fibrofatická náhrada myokardu při endomyokardiální biopsii
- Elektrokardiografické abnormality
- Epsilonové vlny ve V.1 - V3
- Lokalizované prodloužení (> 110 ms) QRS ve V.1 - V3
- Invertované T vlny ve V1 -V3 u jednotlivce staršího 12 let, v nepřítomnosti a pravý blok větve svazku (RBBB)
- Komorová tachykardie s a blok levé větve svazku (LBBB) morfologie s nadřazenou osou
- Rodinná historie
- Familiární onemocnění se potvrdilo buď klinicky, nebo při pitvě nebo chirurgickém zákroku
Drobná kritéria
- Dysfunkce pravé komory
- Mírná globální dilatace RV a / nebo snížená ejekční frakce s normální LV.
- Mírná segmentová dilatace RV
- Regionální hypokineze RV
- Charakterizace tkáně
- Elektrokardiografické abnormality
- Pozdní potenciály na signálu byly v průměru EKG.
- Komorová tachykardie s a blok levé větve svazku (LBBB) morfologie, s nižší nebo neznámou osou
- Časté PVC (> 500 PVC / 24 hodin)
Řízení
Cílem léčby ACM je snížit výskyt náhlé srdeční smrti. To vyvolává klinické dilema: Jak profylakticky léčit asymptomatického pacienta, který byl diagnostikován během rodinného screeningu.
Určitá podskupina jedinců s ACM je považována za vysoce rizikovou pro náhlou srdeční smrt. Přidružené vlastnosti zahrnují:
- Mladý věk
- Soutěžní sportovní aktivita
- Maligní rodinná historie
- Rozsáhlé onemocnění RV se sníženou ejekční frakcí pravé komory.
- Postižení levé komory
- Synkopa
- Epizoda komorové arytmie
Možnosti léčby zahrnují farmakologické, chirurgické, katetrizační ablace a umístění an implantovatelný kardioverter-defibrilátor.
Před rozhodnutím o možnosti léčby naprogramovaná elektrická stimulace v elektrofyziologie laboratoř může být provedena pro další prognostické informace. Mezi cíle naprogramované stimulace patří:
- Posouzení arytmogenního potenciálu nemoci
- Vyhodnoťte hemodynamické důsledky trvalé VT
- Určete, zda lze VT přerušit pomocí antitachykardické stimulace.
Bez ohledu na zvolenou možnost léčby se jednotlivci obvykle doporučuje podstoupit úpravu životního stylu, včetně vyhýbání se namáhavému cvičení, stimulantům srdce (tj .: kofeinu, nikotinu, pseudoefedrinu) a alkoholu.
Pokud jde o fyzickou aktivitu a cvičení, pacienti s ARVC a nositelé genů patogenních desmosomálních mutací spojených s ARVC by se neměli účastnit závodních sportů. Tito pacienti by měli být poučeni, aby své cvičební programy omezili na volnočasové aktivity a zůstali pod klinickým dohledem.[30]
Léky
Farmakologická léčba ACM zahrnuje potlačení arytmie a prevenci tvorby trombů.
Sotalol, a beta blokátor a třída III antiarytmikum, je nejúčinnějším antiarytmickým činidlem v ACM. Mezi další použitá antiarytmická činidla patří amiodaron a konvenční beta blokátory (tj .: metoprolol). Pokud se používají antiarytmika, měla by se jejich účinnost řídit sledováním sériového ambulantního holteru, aby se prokázalo snížení arytmických příhod.
Zatímco inhibitory angiotenzin konvertujícího enzymu (ACE inhibitory) jsou dobře známé pro zpomalení progrese u jiných kardiomyopatií, neprokázalo se, že by byly užitečné při ACM.
Jedinci se sníženou ejekční frakcí RV s dyskinetickými částmi pravé komory mohou mít prospěch z dlouhodobé antikoagulace s warfarin aby se zabránilo tvorbě trombu a následně plicní embolie.
Ablace katétru
Katetrizační ablace může být použita k léčbě nepoddajné ventrikulární tachykardie. Má 60–90% úspěšnost.[31] Bohužel vzhledem k progresivní povaze onemocnění je recidiva častá (60% míra recidivy) s vytvářením nových arytmogenních ložisek. Indikace pro katetrizační ablaci zahrnují KT refrakterní na léky a častou recidivu KT po ICD umístění, což způsobuje časté výboje ICD.
Implantovatelný kardioverter-defibrilátor
An ICD je nejúčinnější prevencí proti náhlé srdeční smrti. Vzhledem k neúnosným nákladům na ICD nejsou rutinně umisťovány u všech jedinců s ACM.
Indikace pro umístění ICD v prostředí ACM zahrnují:
- Srdeční zástava v důsledku VT nebo VF
- Symptomatická KT, která není indukovatelná během naprogramovaná stimulace
- Neúspěšná naprogramovaná léková terapie vedená stimulací
- Těžké zapojení RV se špatnou tolerancí VT
- Náhlá smrt přímého člena rodiny
Vzhledem k tomu, že ICD jsou obvykle umístěny transvenózním přístupem do pravé komory, existují komplikace spojené s umístěním ICD a následným sledováním.
Kvůli extrémnímu ztenčení stěny bez RV je možné během implantace RV perforovat, což může způsobit perikardiální tamponáda. Z tohoto důvodu je proveden každý pokus o umístění elektrody defibrilátoru na komorové septum.
Po úspěšné implantaci může progresivní povaha onemocnění vést k fibro-mastné náhradě myokardu v místě umístění elektrody. To může vést k nedostatečnému snímání elektrické aktivity jednotlivce (potenciálně způsobující neschopnost snímat VT nebo VF) a neschopnosti tempu komory.
Transplantace srdce
Transplantace srdce lze provádět v ACM. Může to být indikováno, pokud jsou arytmie spojené s onemocněním nekontrolovatelné nebo pokud existuje závažné dvouventrikulární srdeční selhání, které nelze pomocí farmakologické léčby zvládnout.
Rodinné promítání
Všichni členové rodiny prvního stupně postižené osoby by měli být vyšetřeni na ACM. To se používá k vytvoření vzorce dědičnosti. Screening by měl začít během dospívání, pokud není uvedeno jinak. Screeningové testy zahrnují:
Prognóza
U jedinců s ACM existuje dlouhá asymptomatická dodací lhůta. I když se jedná o geneticky přenosnou nemoc, jedinci v jejich mladistvém věku nemusí mít při screeningových testech žádné vlastnosti ACM.
Mnoho jedinců má příznaky spojené s komorovou tachykardií, jako je bušení srdce, točení hlavy nebo synkopa. Jiné mohou mít příznaky a příznaky související se selháním pravé komory, jako je edém dolních končetin nebo ucpání jater se zvýšenými jaterními enzymy.
ACM je progresivní onemocnění. Postupem času se více zapojuje pravá komora, což vede k selhání pravé komory. Pravá komora selže dříve, než dojde k dysfunkci levé komory. Avšak v době, kdy bude mít jedinec známky zjevného selhání pravé komory, dojde k histologickému postižení levé komory. Nakonec se zapojí také levá komora, což povede k selhání dvou komor. Mohou se projevit známky a příznaky selhání levé komory, včetně městnavého srdečního selhání, fibrilace síní a zvýšeného výskytu tromboembolických příhod.
Epidemiologie
Prevalence ACM je asi 1/10 000 v běžné populaci v EU Spojené státy, ačkoli některé studie naznačují, že to může být stejně běžné jako 1/1 000. Nedávno bylo zjištěno, že 1/200 jsou nositeli mutací, které predisponují k ACM.[32] Na základě těchto zjištění a dalších důkazů se má za to, že u většiny pacientů mohou být u pacienta nakonec vyžadovány další faktory, jako jsou jiné geny, atletický životní styl, expozice určitým virům atd., Aby se u něj nakonec vyvinuly příznaky a příznaky ACM.[33] Představuje až 17% všech náhlých srdečních úmrtí u mladých lidí. v Itálie, prevalence je 40/10 000, což je nejčastější příčinou náhlé srdeční smrti u mladé populace.[34]
Pozoruhodné případy
- Columbus Crew záložník Kirk Urso se zhroutil s přáteli 5. srpna 2012 a o hodinu později byl prohlášen za mrtvého. Pitva později odhalila, že nemoc je pravděpodobným viníkem.[35][36]
- Sevilla FC a španělský mezinárodní levý křídel Antonio Puerta zemřel na tento stav ve věku 22 let dne 28. srpna 2007, tři dny poté, co utrpěl několik srdečních zástav, zatímco zpochybňoval La Liga hra proti Getafe CF.[37][38]
- Angličan Matt Gadsby také zemřel na tento stav poté, co se zhroutil na hřišti dne 9. září 2006, když hrál za Hinckley United v Conference North hra proti Harrogate Town.[39][40]
- Suzanne Crough, americká dětská herečka nejlépe známá pro svou roli v Rodina Partridge, zemřel náhle na tento stav v roce 2015 ve věku 52 let.[41]
- James Taylor Anglický mezinárodní hráč kriketu, důchod v dubnu 2016.[42]
- Krissy Taylor, americká modelka, zemřela 2. července 1995 v rodinném domě na Floridě. Její oficiální příčinou smrti byla srdeční arytmie a těžké astma, u nichž jí nikdy nebyla diagnostikována. Její rodina nechala nezávislé odborníky prozkoumat vzorky tkáně jejího srdečního svalu a dospěli k závěru, že nejpravděpodobnější příčinou smrti byla zmeškaná diagnóza ACM.
- Jordan Boyd (1997-2013), kanadský juniorský hokejista. On byl posmrtně diagnostikován s onemocněním poté, co odešel z kolapsu z výcvikového tábora v roce 2013.[43]
Viz také
Reference
- ^ Pilichou, Kalliopi; Thiene, Gaetano; Bauce, Barbara; Rigato, Ilaria; Lazzarini, Elisabetta; Migliore, Federico; Perazzolo Marra, Martina; Rizzo, Stefania; Zorzi, Alessandro; Daliento, Luciano; Corrado, Domenico; Basso, Cristina (2. dubna 2016). „Arytmogenní kardiomyopatie“. Orphanet Journal of Rare Diseases. 11 (1): 33. doi:10.1186 / s13023-016-0407-1. PMC 4818879. PMID 27038780.
- ^ Freedberg IM, Fitzpatrick TB (2003). Fitzpatrickova dermatologie ve všeobecném lékařství (6. vydání). McGraw-Hill. ISBN 978-0-07-138076-8.
- ^ James WD, Berger TG, Elston DM, Odom RB (2006). Andrewsovy choroby kůže: Klinická dermatologie (10. vydání). Saunders. ISBN 978-0-7216-2921-6.
- ^ A b C Corrado, Domenico; Basso, Cristina; Soudce Daniel P. (2017-09-15). „Arytmogenní kardiomyopatie“. Výzkum oběhu. 121 (7): 784–802. doi:10.1161 / CIRCRESAHA.117.309345. ISSN 1524-4571. PMC 4818879. PMID 28912183.
- ^ Corrado, Domenico; Link, Mark S .; Calkins, Hugh (05.01.2017). „Arytmogenní kardiomyopatie pravé komory“. The New England Journal of Medicine. 376 (1): 61–72. doi:10.1056 / NEJMra1509267. ISSN 1533-4406. PMID 28052233.
- ^ Cox MG, van der Zwaag PA, van der Werf C, van der Smagt JJ, Noorman M, Bhuiyan ZA, Wiesfeld AC, Volders PG, van Langen IM, Atsma DE, Dooijes D, van den Wijngaard A, Houweling AC, Jongbloed JD Jordaens L, Cramer MJ, Doevendans PA, de Bakker JM, Wilde AA, van Tintelen JP, Hauer RN (červen 2011). „Arytmogenní dysplázie pravé komory / kardiomyopatie: patogenní desmosomové mutace u pacientů s indexem předpovídají výsledek rodinného screeningu: Holandská arytmogenní dysplázie pravé komory / kardiomyopatie následná studie genotyp-fenotyp. Oběh. 123 (23): 2690–700. doi:10.1161 / oběhaha.110.988287. PMID 21606396.
- ^ Fressart V, Duthoit G, Donal E, Probst V, Deharo JC, Chevalier P, Klug D, Dubourg O, Delacretaz E, Cosnay P, Scanu P, Extramiana F, Keller D, Hidden-Lucet F, Simon F, Bessirard V, Roux-Buisson N, Hebert JL, Azarine A, Casset-Senon D, Rouzet F, Lecarpentier Y, Fontaine G, Coirault C, Frank R, Hainque B, Charron P (červen 2010). „Desmosomální genová analýza u arytmogenní dysplázie / komorové kardiomyopatie pravé komory: spektrum mutací a klinický dopad v praxi“. Europace. 12 (6): 861–8. doi:10.1093 / europace / euq104. PMID 20400443.
- ^ Klauke B, Kossmann S, Gaertner A, Brand K, Stork I, Brodehl A, Dieding M, Walhorn V, Anselmetti D, Gerdes D, Bohms B, Schulz U, Zu Knyphausen E, Vorgerd M, Gummert J, Milting H (prosinec 2010). „De novo desmin-mutace N116S je spojena s arytmogenní kardiomyopatií pravé komory“. Lidská molekulární genetika. 19 (23): 4595–607. doi:10,1093 / hmg / ddq387. PMID 20829228.
- ^ Brodehl A, Hedde PN, Dieding M, Fatima A, Walhorn V, Gayda S, Šarić T, Klauke B, Gummert J, Anselmetti D, Heilemann M, Nienhaus GU, Milting H (květen 2012). „Dvoubarevná fotoaktivační lokalizační mikroskopie desminových mutantů spojených s kardiomyopatií“. The Journal of Biological Chemistry. 287 (19): 16047–57. doi:10.1074 / jbc.M111.313841. PMC 3346104. PMID 22403400.
- ^ Beffagna G, Occhi G, Nava A, Vitiello L, Ditadi A, Basso C, Bauce B, Carraro G, Thiene G, Towbin JA, Danieli GA, Rampazzo A (únor 2005). "Regulační mutace v transformujícím genu pro růstový faktor-beta3 způsobují arytmogenní kardiomyopatii pravé komory typu 1". Kardiovaskulární výzkum. 65 (2): 366–73. doi:10.1016 / j.cardiores.2004.10.005. PMID 15639475.
- ^ Milting H, Lukas N, Klauke B, Körfer R, Perrot A, Osterziel KJ, Vogt J, Peters S, Thieleczek R, Varsányi M (srpen 2006). "Složené polymorfismy v genu pro ryanodinový receptor 2 spojené s arytmogenní pravou komorovou kardiomyopatií". Kardiovaskulární výzkum. 71 (3): 496–505. doi:10.1016 / j.cardiores.2006.04.004. PMID 16769042.
- ^ Merner ND, Hodgkinson KA, Haywood AF, Connors S, French VM, Drenckhahn JD, Kupprion C, Ramadanova K, Thierfelder L, McKenna W, Gallagher B, Morris-Larkin L, Bassett AS, Parfrey PS, Young TL (duben 2008) . „Arytmogenní kardiomyopatie pravé srdeční komory typu 5 je plně penetrantní, smrtelná arytmická porucha způsobená missense mutací v genu TMEM43“. American Journal of Human Genetics. 82 (4): 809–21. doi:10.1016 / j.ajhg.2008.01.010. PMC 2427209. PMID 18313022.
- ^ Christensen AH, Andersen CB, Tybjaerg-Hansen A, Haunso S, Svendsen JH (září 2011). "Mutační analýza a vyhodnocení srdeční lokalizace TMEM43 při arytmogenní kardiomyopatii pravé komory". Klinická genetika. 80 (3): 256–64. doi:10.1111 / j.1399-0004.2011.01623.x. PMID 21214875.
- ^ Klauke B, Kossmann S, Gaertner A, Brand K, Stork I, Brodehl A, Dieding M, Walhorn V, Anselmetti D, Gerdes D, Bohms B, Schulz U, Zu Knyphausen E, Vorgerd M, Gummert J, Milting H (prosinec 2010). „De novo desmin-mutace N116S je spojena s arytmogenní kardiomyopatií pravé komory“. Lidská molekulární genetika. 19 (23): 4595–607. doi:10,1093 / hmg / ddq387. PMID 20829228.
- ^ Bermúdez-Jiménez FJ, Carriel V, Brodehl A, Alaminos M, Campos A, Schirmer I, Milting H, Abril BÁ, Álvarez M, López-Fernández S, García-Giustiniani D, Monserrat L, Tercedor L, Jiménez-Jáimez J ( Dubna 2018). „Nová desminutová mutace p.Glu401Asp narušuje formování vláken, narušuje integritu buněčné membrány a způsobuje těžkou arytmogenní kardiomyopatii / dysplázii levé komory“. Oběh. 137 (15): 1595–1610. doi:10.1161 / CIRCULATIONAHA.117.028719. PMID 29212896.
- ^ Bauce B, Basso C, Rampazzo A, Beffagna G, Daliento L, Frigo G, Malacrida S, Settimo L, Danieli G, Thiene G, Nava A (srpen 2005). „Klinický profil čtyř rodin s arytmogenní kardiomyopatií pravé komory způsobenou dominantními desmoplakinovými mutacemi“. European Heart Journal. 26 (16): 1666–75. doi:10.1093 / eurheartj / ehi341. PMID 15941723.
- ^ Gerull B, Heuser A, Wichter T, Paul M, Basson CT, McDermott DA, Lerman BB, Markowitz SM, Ellinor PT, MacRae CA, Peters S, Grossmann KS, Drenckhahn J, Michely B, Sasse-Klaassen S, Birchmeier W, Dietz R, Breithardt G, Schulze-Bahr E, Thierfelder L (listopad 2004). „Mutace v desmosomálním proteinu plakofilinu-2 jsou běžné u arytmogenní kardiomyopatie pravé komory“. Genetika přírody. 36 (11): 1162–4. doi:10.1038 / ng1461. PMID 15489853.
- ^ Pilichou K, Nava A, Basso C, Beffagna G, Bauce B, Lorenzon A, Frigo G, Vettori A, Valente M, Towbin J, Thiene G, Danieli GA, Rampazzo A (březen 2006). „Mutace v genu desmogleinu-2 jsou spojeny s arytmogenní kardiomyopatií pravé komory“. Oběh. 113 (9): 1171–9. doi:10.1161 / CIRCULATIONAHA.105.583674. PMID 16505173.
- ^ Awad MM, Dalal D, Cho E, Amat-Alarcon N, James C, Tichnell C, Tucker A, Russell SD, Bluemke DA, Dietz HC, Calkins H, soudce DP (červenec 2006). „Mutace DSG2 přispívají k arytmogenní dysplázii / kardiomyopatii pravé komory“. American Journal of Human Genetics. 79 (1): 136–42. doi:10.1086/504393. PMC 1474134. PMID 16773573.
- ^ Heuser A, Plovie ER, Ellinor PT, Grossmann KS, Shin JT, Wichter T, Basson CT, Lerman BB, Sasse-Klaassen S, Thierfelder L, MacRae CA, Gerull B (prosinec 2006). „Mutantní desmocollin-2 způsobuje arytmogenní kardiomyopatii pravé komory“. American Journal of Human Genetics. 79 (6): 1081–8. doi:10.1086/509044. PMC 1698714. PMID 17186466.
- ^ Syrris P, Ward D, Evans A, Asimaki A, Gandjbakhch E, Sen-Chowdhry S, McKenna WJ (listopad 2006). „Arytmogenní dysplázie / kardiomyopatie pravé komory spojená s mutacemi v desmosomálním genu desmocollin-2“. American Journal of Human Genetics. 79 (5): 978–84. doi:10.1086/509122. PMC 1698574. PMID 17033975.
- ^ Antoniades L, Tsatsopoulou A, Anastasakis A, Syrris P, Asimaki A, Panagiotakos D, Zambartas C, Stefanadis C, McKenna WJ, Protonotarios N (září 2006). „Arytmogenní kardiomyopatie pravé komory způsobená delecemi v plakofilinu-2 a plakoglobinu (Naxosova choroba) v rodinách z Řecka a Kypru: vztahy genotyp-fenotyp, diagnostické rysy a prognóza“. European Heart Journal. 27 (18): 2208–16. doi:10.1093 / eurheartj / ehl184. PMID 16893920.
- ^ Asimaki A, Syrris P, Wichter T, Matthias P, Saffitz JE, McKenna WJ (listopad 2007). „Nová dominantní mutace v plakoglobinu způsobuje arytmogenní kardiomyopatii pravé komory“. American Journal of Human Genetics. 81 (5): 964–73. doi:10.1086/521633. PMC 2265660. PMID 17924338.
- ^ Brodehl A, Rezazadeh S, Williams T, Munsie NM, Liedtke D, Oh T, Ferrier R, Shen Y, Jones SJ, Stiegler AL, Boggon TJ, Duff HJ, Friedman JM, Gibson WT, Childs SJ, Gerull B (únor 2019 ). „Mutace v ILK kódující kinázu spojenou s integrinem jsou spojeny s arytmogenní kardiomyopatií“. Translační výzkum. 208: 15–29. doi:10.1016 / j.trsl.2019.02.004. PMC 7412573. PMID 30802431.
- ^ Forleo C, Carmosino M, Resta N, Rampazzo A, Valecce R, Sorrentino S, Iacoviello M, Pisani F, Procino G, Gerbino A, Scardapane A, Simone C, Calore M, Torretta S, Svelto M, Favale S (2015) . „Klinická a funkční charakterizace nové mutace v genu lamin a / c ve vícegenerační rodině s arytmogenní srdeční laminopatií“. PLOS ONE. 10 (4): e0121723. Bibcode:2015PLoSO..1021723F. doi:10.1371 / journal.pone.0121723. PMC 4383583. PMID 25837155.
- ^ Mazzanti, Andrea; Ng, Kevin; Faragli, Alessandro; Maragna, Riccardo; Chiodaroli, Elena; Orphanou, Nicoletta; Monteforte, Nicola; Memmi, Mirella; Gambelli, Patrick (prosinec 2016). „Arytmogenní kardiomyopatie pravé komory“. Journal of the American College of Cardiology. 68 (23): 2540–2550. doi:10.1016 / j.jacc.2016.09.951. PMID 27931611.
- ^ Sen-Chowdhry S, Syrris P, McKenna WJ (listopad 2007). "Role genetické analýzy při léčbě pacientů s arytmogenní dysplázií / kardiomyopatií pravé komory". Journal of the American College of Cardiology. 50 (19): 1813–21. doi:10.1016 / j.jacc.2007.08.008. PMID 17980246.
- ^ Přehled genetického testování ARVD / C
- ^ Marcus, Frank I. (2010). „Diagnóza arytmogenní kardiomyopatie pravé komory / dysplazie Navrhovaná úprava kritérií pracovní skupiny“. Oběh.
- ^ Pelliccia, A (2019). „Doporučení pro účast na sportu ve volném čase a ve volném čase u sportovců s kardiomyopatií, myokarditidou a perikarditidou: prohlášení o postoji sekce sportovní kardiologie Evropské asociace pro preventivní kardiologii (EAPC)“. European Heart Journal. 40: 19–33.
- ^ Fontaine G, Tonet J, Gallais Y, Lascault G, Hidden-Lucet F, Aouate P, Halimi F, Poulain F, Johnson N, Charfeddine H, Frank R (listopad 2000). „Ablace katetrizační tachykardie katétrem při arytmogenní dysplazii pravé komory: 16letá zkušenost“. Aktuální zprávy o kardiologii. 2 (6): 498–506. doi:10.1007 / s11886-000-0034-1. PMID 11203287.
- ^ Lahtinen AM, Lehtonen E, Marjamaa A, Kaartinen M, Heliö T, Porthan K, Oikarinen L, Toivonen L, Swan H, Jula A, Peltonen L, Palotie A, Salomaa V, Kontula K (srpen 2011). „Populační převládající desmosomální mutace predisponující k arytmogenní kardiomyopatii pravé komory“. Srdeční rytmus. 8 (8): 1214–21. doi:10.1016 / j.hrthm.2011.03.015. PMID 21397041.
- ^ Jain R. Atletický stav a arytmogenní dysplázie / kardiomyopatie pravé komory: Od fyziologických pozorování k patologickému vysvětlení. Hypothesis 2010, 8 (1): e2. - Více na: http://www.hypothesisjournal.com/?p=844#sthash.aB859Jm2.dpuf
- ^ Corrado D, Fontaine G, arytmogenní dysplázie / kardiomyopatie pravé komory. Potřeba mezinárodního registru. Oběh.2000; 101: e101-e106
- ^ Jardy A. „Záložník Kirk Urso, 22 let, zemřel poté, co byl z baru převezen do nemocnice“. Columbusův dispečink. Expediční tisková společnost. Citováno 21. září 2012.
- ^ Jardy A. „Koroner: Crew's Urso zemřel na již existující srdeční onemocnění“. Columbusův dispečink. Expediční tisková společnost. Citováno 21. září 2012.
- ^ „Hvězda Sevilly trpí infarktem“. BBC Sport. 2007-08-25. Citováno 2007-08-25.
- ^ Hvězda Sevilly zemře po zhroucení
- ^ "Příčina smrti". Skupina srdečních dědičných chorob. Archivovány od originál dne 18. 8. 2006. Citováno 2006-10-31.
- ^ „Šok ze smrti hvězdného hráče“. icBirmingham.co.uk. 11. září 2006. Citováno 2007-11-26.
- ^ Suzanne Crough zemřela na vzácné onemocnění srdce, říká koroner, msn.com; přístup 27. října 2015.
- ^ „James Taylor: Anglie a Nottinghamshire pálkař nucen odejít do důchodu“. BBC Sport. 2016-04-12. Citováno 2016-05-15.
- ^ Život a kariéra Jordan Boyda Hrdinové domácího týmu NHL, vyvoláno 2019-10-14
externí odkazy
| Klasifikace | |
|---|---|
| Externí zdroje |
