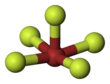
Brom-pentafluorid - Bromine pentafluoride
 | |||
| |||
| Jména | |||
|---|---|---|---|
| Název IUPAC Brom-pentafluorid | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChemSpider | |||
| Informační karta ECHA | 100.029.234 | ||
| Číslo ES |
| ||
PubChem CID | |||
| Číslo RTECS |
| ||
| UNII | |||
| UN číslo | 1745 | ||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| BrF5 | |||
| Molární hmotnost | 174,894 g.mol−1 | ||
| Vzhled | Bledě žlutá kapalina | ||
| Hustota | 2,466 g / cm3 | ||
| Bod tání | -61,30 ° C (-78,34 ° F; 211,85 K) | ||
| Bod varu | 40,25 ° C (104,45 ° F; 313,40 K) | ||
| Reaguje s vodou | |||
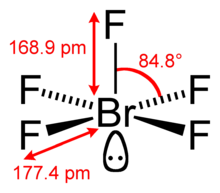
| Struktura | |||
| Čtvercový pyramidální | |||
| Nebezpečí | |||
| Hlavní nebezpečí | Prudce reaguje s vodou, silným oxidačním činidlem[1] | ||
| Bezpečnostní list | Vidět: datová stránka Externí bezpečnostní list | ||
| Piktogramy GHS |     | ||
| Signální slovo GHS | Nebezpečí | ||
| H271, H305, H314, H318, H330, H370, H371, H373 | |||
| P210, P220, P221, P260, P264, P270, P271, P280, P283, P284, P301 + 310, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P306 + 360, P307 + 311, P309 + 311, P310, P314, P320, P321, P331, P363, P370 + 378 | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | Nehořlavé | ||
| NIOSH (Limity expozice USA pro zdraví): | |||
PEL (Dovolený) | žádný[1] | ||
REL (Doporučeno) | PEL 0,1 ppm (0,7 mg / m3)[1] | ||
IDLH (Okamžité nebezpečí) | N.D.[1] | ||
| Související sloučeniny | |||
jiný anionty | Chlorid bromitý | ||
jiný kationty | Chlorpentafluorid Jod pentafluorid | ||
Příbuzný sloučeniny | Brómmonofluorid Bromtrifluorid | ||
| Stránka s doplňkovými údaji | |||
| Index lomu (n), Dielektrická konstanta (εr), atd. | |||
Termodynamické data | Fázové chování pevná látka - kapalina - plyn | ||
| UV, IR, NMR, SLEČNA | |||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Brom-pentafluorid, BrF5, je interhalogenová sloučenina a a fluorid z bróm. Je to silný fluorace činidlo.
BrF5 najde využití v kyslík izotopová analýza. Laserová ablace pevné látky křemičitany v přítomnosti uvolňování pentafluoridu bromu Ó2 pro následnou analýzu.[2] Bylo také testováno jako okysličovadlo v kapalině raketová paliva a používá se jako fluorační činidlo při zpracování uran.
Příprava
Brentpentafluorid byl poprvé připraven v roce 1931 přímou reakcí bromu s fluorem.[3] Tato reakce je vhodná pro přípravu velkého množství a provádí se při teplotách nad 150 ° C (302 ° F) s přebytkem fluoru:
- Br2 + 5 F.2 → 2 BrF5
Pro přípravu menších množství bromid draselný se používá:[3]
- KBr + 3 F2 → KF + BrF5
Tímto způsobem se získá pentafluorid bromitý téměř úplně bez trifluoridů a jiných nečistot.[3]
Reakce
Brom-pentafluorid prudce reaguje s vodou, ale bude se tvořit kyselina bromová a kyselina fluorovodíková (zvláště při moderování ředěním pomocí acetonitril ), jednoduché produkty hydrolýzy:[4]
- BrF5 + 3 H2O → HBrO3 + 5 HF
Jedná se o extrémně účinné fluorační činidlo, které dokáže přeměnit většinu sloučenin uranu na hexafluorid uranu pokojová teplota.
Nebezpečí
Brom-pentafluorid je silně žíravý pro pokožku a jeho páry dráždí oči, kůži a sliznice. Ve vlhkém vzduchu bude ve skutečnosti uvolňovat „kouř“ obsahující kyselina fluorovodíková páry přicházející z jeho reakce s vodou ve vzduchu. Expozice 100 ppm nebo více po dobu delší než jedna minuta je pro většinu experimentálních zvířat smrtelná. Chronická expozice může způsobit poškození ledvin a selhání jater.[5]
Může se spontánně vznítit nebo explodovat při kontaktu s organickými materiály nebo kovovým prachem.[5]
Reference
- ^ A b C d NIOSH Kapesní průvodce chemickými nebezpečími. "#0065". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ Clayton, R .; Mayeda, T. K. (1963). „Použití pentafluoridu bromitého při extrakci kyslíku z oxidů a silikátů pro izotopovou analýzu“. Geochimica et Cosmochimica Acta. 27 (1): 43–48. Bibcode:1963 GeCoA..27 ... 43C. doi:10.1016/0016-7037(63)90071-1.
- ^ A b C Hyde, G. A .; Boudakian, M. M. (1968). "Syntetické cesty k chlor a brom pentafluoridům". Anorganická chemie. 7 (12): 2648–2649. doi:10.1021 / ic50070a039.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemie prvků (2. vyd.). Butterworth-Heinemann. str. 834. ISBN 978-0-08-037941-8.
- ^ A b Patnaik, Pradyot (2007). Komplexní průvodce nebezpečnými vlastnostmi chemických látek (3. vyd.). Wiley-Interscience. str. 480. ISBN 0-471-71458-5.
externí odkazy
- Stránka WebBook pro BrF5
- Mezinárodní karta chemické bezpečnosti 0974
- NIOSH Kapesní průvodce chemickými nebezpečími. "#0065". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- Národní seznam znečišťujících látek - přehled fluoridů a sloučenin