Fluorid chromitý - Chromium(II) fluoride
 | |
| Jména | |
|---|---|
| Ostatní jména difluorid chromitý, fluorid chromitý, fluorid chromitý | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.030.140 |
| Číslo ES |
|
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| CrF2 | |
| Molární hmotnost | 89.9929 g · mol−1 |
| Vzhled | modrozelené duhové krystaly[1] hygroskopický, obrací se na Cr2Ó3 při zahřátí na vzduchu[1] |
| Hustota | 3,79 g / cm3[1] |
| Bod tání | 894 ° C (1641 ° F; 1167 K)[1] |
| Bod varu | > 1300 ° C (2370 ° F; 1570 K)[1] |
| 76,7 g / 100 ml | |
| Struktura | |
| monoklinický[1] | |
| Termochemie | |
Std entalpie of formace (ΔFH⦵298) | -8,645 kJ / g (pevná látka) |
| Nebezpečí | |
| Piktogramy GHS |   |
| Signální slovo GHS | Nebezpečí |
| H314, H318 | |
| P260, P264, P280, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P363, P405, P501 | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Fluorid chromitý je anorganická sloučenina se vzorcem CrF2. Existuje jako modrozelená duhová hmota. Fluorid chromitý je těžko rozpustný ve vodě, téměř nerozpustný v alkoholu a je rozpustný ve varu kyselina chlorovodíková, ale není napaden horkou destilovanou kyselina sírová nebo kyselina dusičná. Stejně jako ostatní sloučeniny chromu se oxiduje i (II) fluorid oxid chromitý ve vzduchu.[2]
Příprava a struktura
Sloučenina se připraví průchodem bezvodým fluorovodík bezvodý chlorid chromitý. Reakce bude probíhat při teplotě místnosti, ale obvykle se zahřeje na 100-200 ° C, aby se zajistilo dokončení:[3]
- CrCl2 + 2 HF → CrF2 + 2 HCl
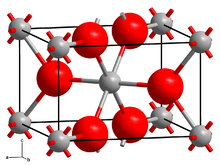
Jako mnoho difluoridů, CrF2 přijímá strukturu jako rutil s oktaedrickou molekulární geometrií o Cr (II) a trigonální geometrií na F−. Dvě ze šesti vazeb Cr-F jsou dlouhé při 2,43 Á a čtyři jsou krátké poblíž 2,00 Á.[4]
Viz také
externí odkazy
Reference
- ^ A b C d E F Perry, Dale L. (2011). Příručka anorganických sloučenin, druhé vydání. Boca Raton, Florida: CRC Press. p. 120. ISBN 978-1-43981462-8. Citováno 2014-01-10.
- ^ Merck Index, 14 ed. položka 2245
- ^ Riley, editoval Georg Brauer; přeložil Scripta Technica, Inc. Překladatel Reed F. (1963). Příručka preparativní anorganické chemie. Hlasitost 1 (2. vyd.). New York, NY: Academic Press. p. 256. ISBN 978-0121266011.CS1 maint: další text: seznam autorů (odkaz)
- ^ Jack, K. H .; Maitland, R. „Krystalové struktury a interatomová vazba chromitých a chromových fluoridů“ Proceedings of the Chemical Society, London (1957), 232. doi:10.1039 / PS9570000217
| Tento anorganické sloučenina –Příbuzný článek je a pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
