Ribose - Ribose - Wikipedia
| |||
| |||
| Jména | |||
|---|---|---|---|
| Název IUPAC (2R,3R,4S,5R) -5- (hydroxymethyl) oxolan-2,3,4-triol | |||
| Ostatní jména d-Ribose | |||
| Identifikátory | |||
3D model (JSmol ) |
| ||
| ChEMBL | |||
| ChemSpider |
| ||
| DrugBank | |||
| Číslo ES |
| ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Vlastnosti[1][2] | |||
| C5H10Ó5 | |||
| Molární hmotnost | 150.13 | ||
| Vzhled | Bílá pevná látka | ||
| Bod tání | 95 ° C (203 ° F; 368 K) | ||
| 100 g / L (25 ° C, 77 ° F) | |||
Chirální rotace ([α]D) | -21,5 ° (v2Ó) | ||
| Související sloučeniny | |||
Příbuzný aldopentózy | Arabinóza Xylóza Lyxóza | ||
Související sloučeniny | Deoxyribóza | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||

Ribose je jednoduchý cukr a uhlohydrát s molekulární vzorec C5H10Ó5 a složení lineární formy H− (C = O) - (CHOH)4-H. Přirozeně se vyskytující forma, d-ribose, je součástí ribonukleotidy z nichž RNA je postavena, a proto je tato sloučenina nezbytná pro kódování, dekódování, nařízení a výraz z geny. Má to strukturální analog, deoxyribóza, což je podobně podstatná složka DNA. l-Ribose je nepřirozený cukr, který jako první připravil Emil Fischer a Oscar Piloty v roce 1891.[3] To nebylo až do roku 1909 Phoebus Levene a Walter Jacobs poznal to d-ribose byl a přírodní produkt, enantiomer produktu Fischer a Piloty a základní součást nukleové kyseliny.[4][5][6] Fischer zvolil název „ribóza“, protože se jedná o částečné přeskupení názvu jiného cukru, arabinóza, z nichž ribóza je epimer na 2 'uhlíku; obě jména se také týkají arabská guma, ze kterého byla arabinóza poprvé izolována a ze které se připravovali l-ribose.[6][7]
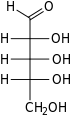
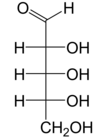
Že jo: Fischerova projekce z otevřený řetězec formy d- a l-ribose
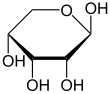
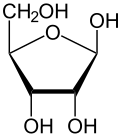
Jako většina cukrů existuje i ribóza jako směs cyklické formy v rovnováha s jeho lineární formou, a ty se snadno převádějí zejména v vodný roztok.[8] Název „ribóza“ se v biochemii a biologii používá k označení všech těchto forem, i když se v případě potřeby používají konkrétnější názvy. Ve své lineární formě lze ribózu rozpoznat jako pentóza cukr se všemi svými hydroxyl funkční skupiny na stejné straně v jeho Fischerova projekce. d-Ribóza má tyto hydroxylové skupiny na pravé straně a je spojena s systematické jméno (2R,3R,4R) -2,3,4,5-tetrahydroxypentanal,[9] zatímco l-ribóza má své hydroxylové skupiny, které se objevují na levé straně ve Fischerově projekci. Cyklizace ribózy probíhá prostřednictvím poloacetal formace kvůli útoku na aldehyd hydroxylovou skupinou C4 'za vzniku a furanóza formě nebo C5 'hydroxylovou skupinou za vzniku a pyranóza formulář. V každém případě existují dva možné geometrické výsledky, pojmenované jako α- a β- a známé jako anomery, záleží na stereochemie na hemiacetalovém atomu uhlíku („anomerní uhlík“). Při pokojové teplotě asi 76% d-ribóza je přítomna ve formách pyranózy[8]:228 (α: β = 1: 2)[10] a 24% ve formách furanózy[8]:228 (α: β = 1: 3),[10] s přítomností pouze asi 0,1% lineární formy.[11][12]
The ribonukleosidy adenosin, cytidin, guanosin, a uridin všichni jsou deriváty β-d-ribofuranóza. Metabolicky důležité druhy, které zahrnují fosforylovaný ribóza zahrnuje ADP, ATP, koenzym A,[8]:228–229 a NADH. tábor a cGMP slouží jako sekundární poslové v některých signálních drahách a jsou také deriváty ribózy. Ribóza skupina se objevuje v některých farmaceutických látkách, včetně antibiotik neomycin a paromomycin.[10]
Syntéza a zdroje
Ribóza jako její 5-fosfátový ester se typicky vyrábí z glukózy pentóza fosfátová cesta. Alespoň v některých archaeách byly identifikovány alternativní cesty.[13]
Ribózu lze syntetizovat chemicky, ale komerční produkce se spoléhá na fermentaci glukózy. Pomocí geneticky modifikovaných kmenů B. subtilis„90 g / litr ribózy lze vyrobit z 200 g glukózy. Přeměna zahrnuje intermediát glukonátu a ribulózy.[14]
Ribóza byla zjištěna v meteority.[15][16]
Struktura
Ribose je aldopentóza (monosacharid obsahující pět uhlík atomy), které ve svém otevřený řetězec forma, má aldehyd funkční skupina na jednom konci. V konvenčním schématu číslování monosacharidů jsou atomy uhlíku číslovány od C1 '(ve aldehydové skupině) do C5'. The deoxyribóza derivát nalezený v DNA se liší od ribózy tím, že má a vodík atom místo hydroxyl skupina na C2 '. Tato hydroxylová skupina vykonává funkci v Sestřih RNA.
„d-" ve jménu d-ribóza označuje stereochemie z chirální atom uhlíku nejdále od aldehydové skupiny (C4 '). v d-ribose, jako ve všech d-cukry, tento atom uhlíku má stejnou konfiguraci jako v d-glyceraldehyd.

α-d-Ribopyranóza
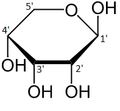
β-d-Ribopyranóza

α-d-Ribofuranóza

β-d-Ribofuranóza
Relativní množství forem ribózy v roztoku: β-d-ribopyranóza (59%), α-d-ribopyranóza (20%), β-d-ribofuranóza (13%), α-d-ribofuranóza (7%) a otevřený řetězec (0,1%).[11]
Pro zbytky ribózy v nukleosidy a nukleotid, torzní úhly pro rotaci zahrnující vazby ovlivňují konfiguraci příslušného nukleosidu a nukleotidu. The sekundární struktura nukleové kyseliny je určena rotací její 7 torzní úhly.[17] Velké množství torzních úhlů umožňuje větší flexibilitu.
U ribóz s uzavřeným prstencem není pozorována výše uvedená pozorovaná flexibilita, protože kruhový cyklus ukládá omezení počtu možných torzních úhlů ve struktuře.[17] Konformátoři uzavřených forem ribóz se liší v tom, jak jsou osamělí kyslík v molekule je umístěn odpovídající dusíkatá báze (také známý jako nukleobáze nebo jen podstavec) připevněný k ribóze. Pokud uhlík směřuje k základně, pak je ribóza označena jako endo. Pokud je uhlík obrácen od základny, pak je ribóza označena jako exo. Pokud je molekula kyslíku připojena k 2 'uhlíku ribózy s uzavřeným cyklem, pak je potvrzení exo stabilnější, protože snižuje interakce kyslíku s bází.[17] Samotný rozdíl je poměrně malý, ale při pohledu na celý řetězec RNA se mírný rozdíl rovná značnému dopadu.
- Některé konfigurace zvrásnění Ribose
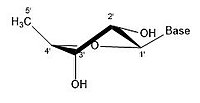
2 'endo
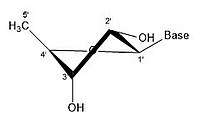
2 'endo 3' exo
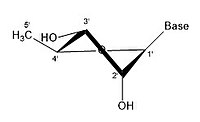
3 'endo 2' exo

3 'endo
Molekula ribózy je typicky reprezentována jako planární molekula na papíře. Navzdory tomu má obvykle nerovinnou povahu. I mezi atomy vodíku je příčinou mnoho složek na molekule ribózy sterická překážka a napětí mezi nimi. Ulehčit tomuto shlukování a napětí v kruhu, zvlnění prstence, tj. se stane nerovinným.[18] Toho svraštění je dosaženo přemístěním atomu z roviny, uvolněním napětí a poskytnutím stabilnější konfigurace.[17] Zvrásnění, jinak známé jako konformace cukrového kruhu (konkrétně ribózový cukr), lze popsat amplitudou zvrásnění i pseudorotace úhel. Úhel pseudotočení lze popsat jako rozsah „sever (N)“ nebo „jih (S)“. Zatímco oba rozsahy se nacházejí ve dvojitých šroubovicích, severní rozsah je běžně spojován s RNA a Forma DNA. Naproti tomu jižní rozsah je spojen s B tvoří DNA. Z-DNA obsahuje cukry v severní i jižní oblasti.[19] Když je přemístěn pouze jeden atom, označuje se to jako „obálkový“ zvrásnění. Když jsou dva atomy přemístěny, je to označováno jako „twist“ zvrásnění, ve vztahu k orientaci cikcaku.[20] U „endo“ zvrásnění je hlavní posun atomů na β-straně, na stejné straně jako vazba C4'-C5 'a báze. U „exo“ zvrásnění je hlavní přemístění atomů na α-tvář, na opačné straně kruhu. Hlavní formy ribózy jsou 3'-endo pucker (běžně adoptovaný RNA a A-formou DNA) a 2'-endo pucker (běžně adoptovaný B-formou DNA).[21] Tyto kroužky se vyvíjejí ze změn v úhlech kroucení kroužku; existuje nekonečná kombinace úhlů, takže existuje nekonečné množství transponovatelných puckerových konformací, z nichž každá je oddělena různorodými aktivačními energiemi.
Funkce
ATP je odvozen od ribózy; obsahuje jednu ribózu, tři fosfát skupiny a adenin základna. ATP se vytváří během buněčné dýchání z adenosindifosfát (ATP s jednou menší fosfátovou skupinou).
Signalizační cesty
Ribóza je stavebním kamenem v sekundárních signálních molekulách, jako jsou cyklický adenosinmonofosfát (cAMP), který je odvozen od ATP. Jeden konkrétní případ, ve kterém se používá cAMP, je v signální dráhy závislé na cAMP. V signálních drahách cAMP je buď stimulovaný nebo inhibiční hormonový receptor aktivován a signální molekula. Tyto receptory jsou spojeny se stimulačním nebo inhibičním regulativem G-protein. Když je aktivován stimulační G-protein, adenylyl cykláza katalyzuje ATP do cAMP pomocí Mg2+ nebo Mn2+. cAMP, sekundární posel, poté pokračuje v aktivaci protein kináza A, což je enzym který reguluje buňku metabolismus. Protein kináza A reguluje metabolické enzymy pomocí fosforylace což způsobí změnu v buňce v závislosti na původní signální molekule. Opak nastane, když je aktivován inhibiční G-protein; G-protein inhibuje adenylyl cyklázu a ATP se nepřeměňuje na cAMP.

Metabolismus
Ribóza je označována jako „molekulární měna“, protože se účastní přenosu intracelulární energie.[Citace je zapotřebí ] Například, nikotinamid adenin dinukleotid (NAD), flavin adenin dinukleotid (FAD) a nikotinamid adenin dinukleotid fosfát (NADP) všechny obsahují d-ribofuranóza skupina. Každý může být odvozený od d-ribose poté, co je převeden na d-ribóza 5-fosfát enzymem ribokináza.[22][23] NAD, FAD a NADP působí v biochemii jako akceptory elektronů redox reakce v hlavních metabolických drahách včetně glykolýza, cyklus kyseliny citronové, kvašení a elektronový transportní řetězec.

Biosyntéza nukleotidů
Nukleotidy jsou syntetizovány pomocí záchrany nebo de novo syntéza.[24] Záchrana nukleotidů používá kousky dříve vyrobených nukleotidů a znovu je syntetizuje pro budoucí použití. V de novo, aminokyseliny, oxid uhličitý, deriváty kyseliny listové a fosforibosylpyrofosfát (PRPP) se používají k syntéze nukleotidů.[24] Jak de novo, tak záchrana vyžadují PRPP, který je syntetizován z ATP a ribóza-5-fosfátu enzymem zvaným PRPP syntetáza.[24]
Modifikace
Úpravy v přírodě
Ribokináza katalyzuje konverzi d-kradnout d-ribóza-5-fosfát. Po převodu d-ribóza-5-fosfát je k dispozici pro výrobu aminokyseliny tryptofan a histidin, nebo pro použití v pentóza fosfátová cesta. Absorpce d-ribóza je v tenkém střevě 88–100% (až 200 mg / kg · h).[25]
Jedna důležitá modifikace nastává v poloze C2 'molekuly ribózy. Přidáním O-alkyl skupina, jaderný odpor RNA se zvyšuje kvůli dalším stabilizačním silám. Tyto síly se stabilizují kvůli nárůstu o intramolekulární vodíková vazba a zvýšení glykosidová vazba stabilita.[26] Výsledné zvýšení odporu vede ke zvýšení v poločas rozpadu z siRNA a potenciální terapeutický potenciál v buňkách a zvířatech.[27] The methylace ribózy na konkrétních místech souvisí s poklesem imunitní stimulace.[28]
Syntetické modifikace
Spolu s fosforylací si molekuly ribofuranózy mohou vyměňovat kyslík selen a síra produkovat podobné cukry, které se liší pouze na 4 'pozici. Těchto derivátů je více lipofilní než původní molekula. Díky zvýšené lipofilitě jsou tyto druhy vhodnější pro použití v technikách, jako je PCR, RNA aptamer post-modifikace, antisense technologie a pro fázování Rentgenová krystalografická data.[27]
Podobně jako 2 'modifikace v přírodě, syntetická modifikace ribózy zahrnuje přidání fluor v poloze 2 '. Tento fluorované ribóza působí podobně jako methylovaná ribóza, protože je schopna potlačit imunitní stimulaci v závislosti na umístění ribózy ve vlákně DNA.[26] Velký rozdíl mezi methylací a fluorací je ten, který se vyskytuje pouze prostřednictvím syntetických modifikací. Přidání fluoru vede ke zvýšení stabilizace glykosidové vazby a ke zvýšení intramolekulárních vodíkových vazeb.[26]
Lékařské použití
d-ribóza byla navržena pro použití při léčbě městnavé srdeční selhání[29] (stejně jako jiné formy srdečních chorob) a pro syndrom chronické únavy (CFS), nazývaná také myalgická encefalomyelitida (ME) v otevřené nezaslepené, nerandomizované a nepřekřížené subjektivní studii.[30]
Doplňkové d-ribóza může obejít část pentóza fosfátová cesta, cesta k výrobě energie, k výrobě d-ribóza-5-fosfát. Enzym glukóza-6-fosfát-dehydrogenáza (G-6-PDH) je často v buňkách nedostatek, ale spíše v nemocné tkáni, například v myokard buňky u pacientů se srdečním onemocněním. Nabídka d-ribose v mitochondrie přímo souvisí s produkcí ATP; snížil d-krevní zásoba snižuje množství produkovaného ATP. Studie naznačují, že doplňování d-ribóza po ischemii tkáně (např. ischemie myokardu) zvyšuje produkci ATP myokardu, a tedy mitochondriální funkci. V zásadě podávání doplňkových d-ribóza obchází enzymatický krok v pentózo-fosfátové cestě poskytnutím alternativního zdroje 5-fosfo-d-ribose 1-pyrofosfát pro výrobu ATP. Doplňkové d-ribóza zvyšuje regeneraci hladin ATP a současně snižuje poškození buněk u lidí a jiných zvířat. Jedna studie naznačuje, že použití doplňkových d-ribose snižuje instanci angina pectoris u mužů s diagnostikovanou ischemická choroba srdeční.[31] d-Ribose se používá k léčbě mnoha patologické stavy, jako je syndrom chronické únavy, fibromyalgie a dysfunkce myokardu. Používá se také ke zmírnění příznaků křečí, bolesti, ztuhlosti atd. Po cvičení a ke zlepšení sportovního výkonu[Citace je zapotřebí ].
Reference
- ^ Merck Index: Encyclopedia of Chemicals, Drugs, and Biologicals (11. vydání), Merck, 1989, ISBN 091191028X, 8205
- ^ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62. vydání). Boca Raton, FL: CRC Press. p. C-506. ISBN 0-8493-0462-8.
- ^ Fischer, Emil; Piloty, Oscar (1891). „Ueber eine neue Pentonsäure und die zweite inactive Trioxyglutarsäure“ [O nové kyselině pentonové a druhé neaktivní kyselině trioxyglutarové]. Berichte der deutschen chemischen Gesellschaft (v němčině). 24 (2): 4214–4225. doi:10.1002 / cber.189102402322.
- ^ Levene, P. A.; Jacobs, W. A. (1909). „Über Inosinsäure“ [O kyselině inosové]. Berichte der deutschen chemischen Gesellschaft (v němčině). 42 (1): 1198–1203. doi:10,1002 / cber.190904201196.
- ^ Levene, P. A.; Jacobs, W. A. (1909). „Über die Pentose in den Nucleinsäuren“ [O pentóze v nukleových kyselinách]. Berichte der deutschen chemischen Gesellschaft (v němčině). 42 (3): 3247–3251. doi:10,1002 / cber.19090420351.
- ^ A b Jeanloz, Roger W.; Fletcher, Hewitt G. (1951). "Chemie Ribose". v Hudson, Claude S.; Cantor, Sidney M. (eds.). Pokroky v chemii sacharidů. 6. Akademický tisk. str. 135–174. doi:10.1016 / S0096-5332 (08) 60066-1. ISBN 9780080562650. PMID 14894350.
- ^ Nechamkin, Howard (1958). "Některé zajímavé etymologické deriváty chemické terminologie". Přírodovědné vzdělávání. 42 (5): 463–474. Bibcode:1958SciEd..42..463N. doi:10,1002 / sce.3730420523.
- ^ A b C d Dewick, Paul M. (2013). „Kyslík jako nukleofil: hemiketaly, hemiketaly, acetaly a ketaly“. Základy organické chemie: Pro studenty farmacie, léčivé chemie a biologické chemie. John Wiley & Sons. str. 224–234. ISBN 9781118681961.
- ^ Leigh, Jeffery (červenec – srpen 2012). „Systémy nomenklatury jiné než IUPAC“. Chemistry International. Mezinárodní unie pro čistou a aplikovanou chemii. 34 (4). Citováno 15. prosince 2019.
- ^ A b C Bhutani, S. P. (2019). „Aldopentózy - cukry nukleových kyselin“. Chemie biomolekul (2. vyd.). CRC Press. str. 63–65. ISBN 9781000650907.
- ^ A b Drew, Kenneth N .; Zajíček, Jaroslav; Bondo, Gail; Bose, Bidisha; Serianni, Anthony S. (únor 1998). "13C-značené aldopentózy: detekce a kvantifikace cyklických a acyklických forem pomocí heteronukleární 1D a 2D NMR spektroskopie ". Výzkum sacharidů. 307 (3–4): 199–209. doi:10.1016 / S0008-6215 (98) 00040-8.
- ^ de Wulf, P .; Vandamme, E. J. (1997). „Mikrobiální syntéza ᴅ-ribózy: proces metabolické deregulace a fermentace“. Pokroky v aplikované mikrobiologii. 44: 167–214. doi:10.1016 / S0065-2164 (08) 70462-3. ISBN 9780120026449.
- ^ Tumbula, D. L .; Teng, Q .; Bartlett, M. G .; Whitman, W. B. (1997). „Biosyntéza ribózy a důkazy pro alternativní první krok ve společné cestě aromatických aminokyselin v Methanococcus maripaludis“. Journal of Bacteriology. 179 (19): 6010–6013. doi:10.1128 / jb.179.19.6010-6013.1997. PMC 179501. PMID 9324245.
- ^ Wulf, P. De; Vandamme, E. J. (1997). "Výroba d -ribózy fermentací". Aplikovaná mikrobiologie a biotechnologie. 48 (2): 141–148. doi:10,1007 / s002530051029. PMID 9299771. S2CID 34340369.
- ^ Steigerwald, Bill; Jones, Nancy; Furukawa, Yoshihiro (18. listopadu 2019). „První detekce cukrů v meteoritech dává stopy původu života“. NASA. Citováno 18. listopadu 2019.
- ^ Furukawa, Yoshihiro; Chikaraishi, Yoshito; Ohkouchi, Naohiko; Ogawa, Nanako O .; Glavin, Daniel P .; Dworkin, Jason P .; Abe, Chiaki; Nakamura, Tomoki (2019). „Mimozemská ribóza a jiné cukry v primitivních meteoritech“. Sborník Národní akademie věd Spojených států amerických. 116 (49): 24440–24445. Bibcode:2019PNAS..11624440F. doi:10.1073 / pnas.1907169116. PMC 6900709. PMID 31740594.
- ^ A b C d Bloomfield, Victor; Crothers, Donald; Tinoco, Ignacio (2000). Nukleové kyseliny: Struktury, vlastnosti a funkce. University Science Books. str.19 –25.
- ^ Voet, Donald; Voet, Judith (2011). Biochemie. John Wiley & Sons, Inc. str.1152, 1153. ISBN 978-0470570951.
- ^ Foloppe, Nicolas; MacKerell, Alexander D. (srpen 1998). "Konformační vlastnosti deoxyribózy a ribózových skupin nukleových kyselin: kvantová mechanická studie". The Journal of Physical Chemistry B. 102 (34): 6669–6678. doi:10.1021 / jp9818683. ISSN 1520-6106.
- ^ „Architektura nukleových kyselin“. fbio.uh.cu. Citováno 8. října 2019.
- ^ Neidle, Stephen (2008). „Stavební bloky DNA a RNA“. V Neidle, Stephen (ed.). Principy struktury nukleových kyselin. Akademický tisk. str.20 –37. doi:10.1016 / B978-012369507-9.50003-0. ISBN 9780123695079.
- ^ Bork, Peer; Sander, Chris; Valencie, Alfonso (1993). „Konvergentní vývoj podobné enzymatické funkce na různých proteinových záhybech: rodiny hexokináz, ribokináz a galaktokináz cukerných kináz“. Věda o bílkovinách. 2 (1): 31–40. doi:10.1002 / pro.5560020104. PMC 2142297. PMID 8382990.
- ^ Park, Jae; Gupta, Radhey S. (2008). „Adenosinkináza a ribokináza - rodina proteinů RK“. Buněčné a molekulární biologické vědy. 65 (18): 2875–2896. doi:10.1007 / s00018-008-8123-1. PMID 18560757. S2CID 11439854.
- ^ A b C Puigserver, Pere (2018). "Signální transdukce a metabolomika". In Hoffman, Ronald; Benz, Edward J .; Silberstein, Leslie E .; Heslop, Helen E. (eds.). Hematologie (7. vydání). Elsevier. str. 68–78. doi:10.1016 / B978-0-323-35762-3.00007-X. ISBN 9780323357623.
- ^ "Bylinné léky, doplňky A-Z index". PDRHealth.com. PDR, LLC. Archivovány od originál dne 11. října 2008.
- ^ A b C Hamlow, Lucas; On, Chenchen; Ventilátor, Lin; Wu, Ranran; Yang, Bo; Rodgers, M. T .; Berden, Giel; Oomens, J. (červen 2015). Strukturální účinky modifikací cytidinu 2'-ribózy, jak byly stanoveny Irmpd akční spektroskopií. 70. mezinárodní sympozium o molekulární spektroskopii. University of Illinois v Urbana-Champaign. Bibcode:2015isms.confEMI13H. doi:10.15278 / isms.2015.MI13.
- ^ A b Evich, Marina; Spring-Connell, Alexander M .; Germann, Markus W. (27. ledna 2017). "Dopad modifikovaných ribózových cukrů na konformaci a funkci nukleových kyselin". Heterocyklická komunikace. 23 (3): 155–165. doi:10.1515 / hc-2017-0056. ISSN 2191-0197. S2CID 91052034.
- ^ Peacock, Hayden; Fucini, Raymond V .; Jayalath, Prasanna; Ibarra-Soza, José M .; Haringsma, Henry J .; Flanagan, W. Michael; Willingham, Aarron; Beal, Peter A. (2011). "Modifikace nukleobáze a ribózy kontrolují imunostimulaci pomocí mimetické RNA MicroRNA-122". Journal of the American Chemical Society. 133 (24): 9200–9203. doi:10.1021 / ja202492e. PMC 3116021. PMID 21612237.
- ^ Omran, Heyder; McCarter, Dean; St Cyr, John; Lüderitz, Berndt (2004). „ᴅ-Ribóza pomáhá pacientům s městnavým srdečním selháním“. Experimentální a klinická kardiologie. Léto (9 (2)): 117–118. PMC 2716264. PMID 19641697.
- ^ Teitelbaum, Jacob E .; Johnson, Clarence; St Cyr, John (26. listopadu 2006). „Použití ᴅ-ribózy u syndromu chronické únavy a fibromyalgie: pilotní studie“. The Journal of Alternative and Complementary Medicine. 12 (9): 857–862. CiteSeerX 10.1.1.582.4800. doi:10.1089 / acm.2006.12.857. PMID 17109576.
- ^ "Ribose". wa.kaiserpermanente.org. Citováno 7. října 2019.