Manóza - Mannose
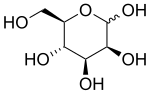 D-Mannopyranóza | |
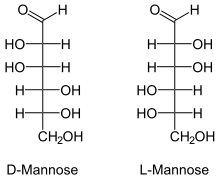 Fischerovy projekce | |
| Identifikátory | |
|---|---|
| ChEMBL | |
| ChemSpider |
|
| Informační karta ECHA | 100.007.705 |
| Pletivo | Manóza |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| Vlastnosti | |
| C6H12Ó6 | |
| Molární hmotnost | 180.156 g · mol−1 |
| -102.90·10−6 cm3/ mol | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Manóza je cukr monomer z aldohexóza řada sacharidy. Je to C-2 epimer z glukóza. Manóza je u člověka důležitá metabolismus, zejména v glykosylace jisté bílkoviny. Několik vrozené poruchy glykosylace jsou spojeny s mutacemi v enzymy podílí se na metabolismu manózy.[1]
Manóza není základní živina; může být produkován v lidském těle z glukózy nebo přeměněn na glukózu. Mannose poskytuje 2-5 kcal /G. Částečně se vylučuje do moč.
Struktura
Manóza běžně existuje jako dva různě velké prsteny pyranóza (šestičlenná) forma a furanóza (pětičlenná) forma. Každé uzavření kruhu může mít v alfa nebo beta konfiguraci anomerní pozice. Chemická látka rychle prochází izomerizace mezi těmito čtyřmi formami.
 α-D-Mannofuranóza | |
 α-D-Mannopyranóza 67% | 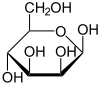 β-D-Mannopyranóza 33% |
Metabolismus

Zatímco se předpokládá, že většina manózy použité při glykosylaci pochází z glukózy, v kultivovaný hepatom buňky (rakovinné buňky z jater), většina manózy pro biosyntézu glykoproteinů pochází z extracelulární manózy, nikoli z glukózy.[2] Mnoho glykoproteinů produkovaných v játrech je vylučováno do krevního oběhu, takže manóza ve stravě je distribuována po celém těle.[3]
Manóza je přítomna v mnoha glykokonjugátech včetně Nvázaná glykosylace proteinů. C-Mannosylace je také hojná a lze ji najít v oblastech podobných kolagenu.
Trávením mnoha polysacharidů a glykoproteinů se získá manóza, která je fosforylována hexokináza za vzniku manoso-6-fosfátu. Manóza-6-fosfát se převádí na fruktóza-6-fosfát enzymem fosfomanóza izomeráza, a poté vstoupí do glykolytická cesta nebo je převeden na glukóza-6-fosfát podle glukoneogenní cesta z hepatocyty.
Manóza je dominantní monosacharid v N-vázaná glykosylace, což je a posttranslační modifikace bílkovin. Je iniciována vcelku přenos na Glc3Man9GlcNAc2 na rodící se glykoproteiny v endoplazmatickém retikulu ko-translačním způsobem, když protein vstoupil transportním systémem. Glukóza je hydrolyzovaný na plně složeném proteinu a manosové skupiny jsou hydrolyzovány ER a Golgi-rezidentními mannosidázami. Zralé lidské glykoproteiny obvykle obsahují pouze tři zbytky manózy pohřbené při postupné modifikaci pomocí GlcNAc, galaktózy a kyseliny sialové. To je důležité, protože vrozený imunitní systém u savců je zaměřen na rozpoznání exponovaných zbytků manózy. Tato aktivita je způsobena prevalencí zbytků manózy ve formě mannanů na površích kvasinek. Virus lidské imunodeficience vykazuje značné množství zbytků manózy v důsledku těsného shlukování glykanů v jeho virové špičce.[4][5] Tyto zbytky manózy jsou cílem široce neutralizujících protilátek.[6]
Biotechnologie
Rekombinantní proteiny produkované v kvasinkách mohou podléhat přidání manózy v různých vzorcích, než jaké používají buňky savců.[7] Tento rozdíl v rekombinantních proteinech od těch, které se běžně produkují v savčích organismech, může ovlivnit účinnost vakcín.
Formace
Manóza může vznikat oxidací mannitol.
Může být také vytvořen z glukózy v Lobry-de Bruyn-van Ekensteinova transformace.
Etymologie
Kořen „manózy“ i „mannitol " je manna, který bible popisuje jako jídlo dodávané Izraelitům během jejich cesty v regionu Sinaj. Několik stromů a keřů může produkovat látku zvanou manna, jako je „manna“ (Fraxinus ornus ), z jehož sekretů byl původně izolován mannitol.
Použití
Manóza (D-manóza) se používá jako doplněk výživy zabalený jako „d-manóza“, aby se zabránilo opakovaným infekcím močových cest. [8]
Konfigurace
Manóza se liší od glukózy inverzí C-2 chirální centrum. Mannose zobrazí a zvrásnění ve formě prstence řešení. Tato jednoduchá změna vede k drasticky odlišné biochemii dvou hexóz. Tato změna má stejný účinek na druhou aldohexózy, také.
Manóza PTS permeázy

Systém PEP-dependentní cukr transportující fosfotransferázu transportuje a současně fosforyluje své cukerné substráty. Manóza XYZ permeáza je členem rodiny, přičemž tato odlišná metoda je používána bakteriemi pro příjem cukru, zejména exogenních hexóz v případě manózy XYZ k uvolňování fosfátových esterů do buněčné cytoplazmy v rámci přípravy na metabolismus primárně cestou glykolýzy.[9] Transportní komplex MANXYZ se také podílí na infekci E-coli bakteriofágem lambda, přičemž podjednotky ManY a ManZ jsou dostatečné pro správnou infekci fágem lambda.[10]MANXYZ má čtyři domény ve třech polypeptidových řetězcích; ManX, ManY a ManZ. ManX podjednotka tvoří homodimer, který je lokalizován na cytoplazmatické straně membrány. ManX obsahuje dvě domény IIA a IIB spojené pantovým peptidem s každou doménou obsahující fosforylační místo a mezi oběma podjednotkami dochází k přenosu fosforylu.[11] ManX může být vázán na membránu nebo ne.[10] Podjednotky ManY a ManNZ jsou hydrofobní integrální membránové proteiny se šesti a jedním transmembránovým alfa šroubovicovým klíčem.[12] [13]Fosforylová skupina PEP se přenáší na dovážený cukr pomocí enzymu 1, histidinový proteinový fosfátový nosič a poté do podjednotek ManX, ManY a ManZ transportního komplexu ManXYZ, který fosforyluje vstupující hexózový cukr a vytváří hexos-6- fosfát.
Viz také
Reference
- ^ Freeze, H. H .; Sharma, V. (2010). „Metabolická manipulace poruch glykosylace u lidí a zvířecích modelů“. Semináře z buněčné a vývojové biologie. 21 (6): 655–662. doi:10.1016 / j.semcdb.2010.03.011. PMC 2917643. PMID 20363348.
- ^ Alton, G .; Hasilik, M .; Niehues, R .; Panneerselvam, K .; Etchison, J. R .; Fana, F .; Freeze, H. H. (1998). „Přímé využití manózy pro biosyntézu glykoproteinů savců“. Glykobiologie. 8 (3): 285–295. doi:10.1093 / glycob / 8.3.285. PMID 9451038.
- ^ Davis, J. A .; Freeze, H. H. (2001). "Studie metabolismu manózy a účinků dlouhodobého požití manózy u myši". Biochimica et Biophysica Acta (BBA) - Obecné předměty. 1528 (2–3): 116–126. doi:10.1016 / S0304-4165 (01) 00183-0. PMID 11687298.
- ^ Pritchard, Laura K .; Spencer, Daniel I.R .; Royle, Louise; Bonomelli, Camille; Seabright, Gemma E .; Behrens, Anna-Janina; Kulp, Daniel W .; Menis, Sergey; Krumm, Stefanie A. (2015-06-24). „Glykanové shlukování stabilizuje manózovou náplast HIV-1 a zachovává zranitelnost vůči široce neutralizujícím protilátkám“. Příroda komunikace. 6: 7479. Bibcode:2015NatCo ... 6.7479P. doi:10.1038 / ncomms8479. PMC 4500839. PMID 26105115.
- ^ Pritchard, Laura K .; Vasiljevic, Snezana; Ozorowski, Gabriel; Seabright, Gemma E .; Cupo, Albert; Ringe, Rajesh; Kim, Helen J .; Sanders, Rogier W .; Doores, Katie J. (2015-06-16). „Strukturální omezení určují glykosylaci trimérů obálek HIV-1“. Zprávy buněk. 11 (10): 1604–1613. doi:10.1016 / j.celrep.2015.05.017. ISSN 2211-1247. PMC 4555872. PMID 26051934.
- ^ Crispin, Max; Doores, Katie J. (2015-04-01). „Cílení na glykany odvozené od hostitele na obalené viry pro návrh vakcíny založené na protilátkách“. Aktuální názor na virologii. Virová patogeneze • Preventivní a terapeutické vakcíny. 11: 63–69. doi:10.1016 / j.coviro.2015.02.002. PMC 4827424. PMID 25747313.
- ^ Vlahopoulos, S .; Gritzapis, A. D .; Perez, S. A .; Cacoullos, N .; Papamichail, M .; Baxevanis, C. N. (2009). "Přidání manózy kvasinkami Pichia pastoris na rekombinantním proteinu HER-2 inhibuje rozpoznávání monoklonální protilátkou herceptin ". Vakcína. 27 (34): 4704–4708. doi:10.1016 / j.vakcina.2009.05.063. PMID 19520203.
- ^ Porru, D .; Parmigiani, A .; Tinelli, C .; Barletta, D .; Choussos, D .; Di Franco, C .; Rovereto, B. (2014). „Orální D-manóza u rekurentních infekcí močových cest u žen: pilotní studie“. Journal of Clinical Urology. 7 (3): 208–213. doi:10.1177/2051415813518332. S2CID 73362601.
- ^ Postma, P. W .; Lengeler, J. W .; Jacobson, G. R. (1993). "Fosfoenolpyruvát: sacharidové fosfotransferázové systémy bakterií". Mikrobiologické recenze. 57 (3): 543–594. doi:10.1128 / MMBR.57.3.543-594.1993. PMC 372926. PMID 8246840.
- ^ A b Erni, B .; Zanolari, B. (1985). „Manóza-permeáza bakteriálního fosfotransferázového systému. Genové klonování a čištění komplexu enzymu IIMan / IIIMan Escherichia coli". The Journal of Biological Chemistry. 260 (29): 15495–15503. PMID 2999119.
- ^ Erni, B .; Zanolari, B .; Graff, P .; Kocher, H. P. (1989). "Manosová permeáza Escherichia coli. Struktura domény a funkce fosforylační podjednotky". The Journal of Biological Chemistry. 264 (31): 18733–18741. PMID 2681202.
- ^ Huber, F .; Erni, B. (1996). „Membránová topologie transportéru manózy Escherichia coli K12 ". European Journal of Biochemistry / FEBS. 239 (3): 810–817. doi:10.1111 / j.1432-1033.1996.0810u.x. PMID 8774730.
- ^ Liu, Xueli; Zeng, Jianwei; Huang, Kai; Wang, Jiawei (2019-06-17). "Struktura transportéru manózy systému bakteriální fosfotransferázy". Cell Research. 29 (8): 680–682. doi:10.1038 / s41422-019-0194-z. ISSN 1748-7838. PMC 6796895. PMID 31209249.


