Aldosteron syntáza - Aldosterone synthase
Aldosteron syntáza, také zvaný steroid 18-hydroxyláza, kortikosteron 18-monooxygenáza nebo P450C18, je steroid hydroxyláza cytochrom P450 enzym podílející se na biosyntéze mineralokortikoidů aldosteron a další steroidy. Enzym katalyzuje postupné hydroxylace steroidní úhlové methylové skupiny na C18 po počáteční 11β-hydroxylaci (enzym má aktivitu steroidní 18-hydroxylázy stejně jako aktivitu steroid 11 beta-hydroxylázy). Je kódován pomocí CYP11B2 gen u lidí.
Aldosteron syntáza je protein, který je exprimován pouze v zona glomerulosa[4] z kůra nadledvin a je primárně regulován systém renin-angiotensin.[5] Je to jediný enzym schopný syntetizovat aldosteron u lidí a hraje v něm důležitou roli elektrolyt zůstatek a krevní tlak.[6]
Genetika
Aldosteron syntáza je kódována chromozom 8q 22[4] genem CYP11B2.[4] Gen obsahuje 9 exonů a rozprostírá se zhruba 7 000 párů bází DNA.[4] CYP11B2 úzce souvisí s CYP11B1. Tyto dva geny vykazují 93% homologie navzájem a jsou oba kódovány na stejném chromozomu.[7] Výzkum ukázal, že ionty vápníku se aktivují transkripční faktory na CYP11B2 prostřednictvím dobře definovaných interakcí v 5'-sousedící oblasti CYP11B2.[4]
Aldosteron syntáza je členem nadrodiny enzymů cytochromu P450.[8] Proteiny cytochromu P450 jsou monooxygenázy které katalyzují mnoho reakcí zapojených do metabolismu léčiv a syntézy cholesterol, steroidy, a další lipidy.
Funkce
Aldosteron syntáza je enzym, který má aktivitu steroidní 18-hydroxylázy i steroidní 11 beta-hydroxylázy. Aktivita 18-hydroxylázy spočívá v katalyzování postupných hydroxylací steroidní úhlové methylové skupiny na C18.
Zatímco steroid 11β-hydroxyláza (kódováno CYP11B1 gen) katalyzuje pouze hydroxylaci v poloze 11 beta (hlavně 11-deoxykortikosteron a 11-deoxykortizol), aldosteron syntáza (kódovaná CYP11B2 Gen) katalyzuje syntézu aldosteronu z deoxykortikosteronu, což je proces, který postupně vyžaduje hydroxylaci v pozicích 11 beta a 18 a oxidaci v poloze 18.[9]
Adrenokortikotropní hormon Předpokládá se, že hraje roli v regulaci aldosteron syntázy pravděpodobně stimulací syntézy 11-deoxykortikosteron což je počáteční substrát enzymatického působení v aldosteron syntáze.[10]

Metabolismus

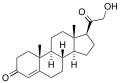
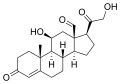
Aldosteron syntáza se převádí 11-deoxykortikosteron na kortikosteron, do 18-hydroxykortikosteron a nakonec aldosteron:
V lidském metabolismu biosyntéza aldosteronu do značné míry závisí na metabolismu cholesterol. Cholesterol se metabolizuje tzv. časnou cestou syntézy aldosteronu[11] a je hydroxylován na (20R, 22R) -dihydroxycholesterol, který je poté metabolizován jako přímý prekurzor na pregnenolon. Pregnenolon pak může následovat jednu ze dvou cest, které zahrnují metabolismus progesteron nebo testosteron a estradiol biosyntéza. Aldosteron je syntetizován sledováním metabolismu progesteron.
V potenciálním případě, kdy aldosteron syntáza není metabolicky aktivní, se tělo hromadí 11-deoxykortikosteron. Tím se zvyšuje retence solí, což vede ke zvýšení hypertenze.[12]
Substráty
Aldosteron syntáza vykazuje odlišnou katalytickou aktivitu během metabolismu jejích substrátů.[6] Zde jsou některé ze substrátů seskupených podle katalytické aktivity enzymu:
Nedostatek methyloxidázy
Nedostatek metabolicky aktivní aldosteron syntázy vede k nedostatku kortikosteron methyloxidázy typu I a II. Nedostatek je klinicky charakterizován plýtváním solí, neprospíváním a zpomalením růstu.[19] Neaktivní proteiny jsou způsobeny autozomálně recesivní dědičností defektních genů CYP11B2, ve kterých genetické mutace ničí enzymatickou aktivitu aldosteron syntázy.[19] Nedostatečná aktivita aldosteron syntázy má za následek zhoršenou biosyntézu aldosteron zatímco kortikosteron v zona glomerulosa se nadměrně produkuje u deficitu kortikosteronmethyloxidázy typu I i II. Nedostatky methyloxidázy kortikosteronu sdílejí tento účinek, avšak typ I způsobuje celkový nedostatek 18-hydroxykortikosteronu, zatímco typ II jej nadměrně produkuje.[19]
Enzymatická inhibice
Inhibice aldosteron syntázy je v současné době zkoumána jako léčba pro hypertenze, srdeční selhání, a poruchy ledvin.[20] Deaktivace enzymatické aktivity snižuje koncentrace aldosteronu v plazmě a tkáních, což klesá mineralokortikoidový receptor -závislé a nezávislé účinky na srdeční vaskulární a renální cílové orgány.[20] Ukázalo se, že inhibice rychle snižuje plazmatické a močové koncentrace aldosteronu o 70 - 80% hypokalémie korekce, mírný pokles krevního tlaku a zvýšení plazmy renin aktivita u pacientů na dietě s nízkým obsahem sodíku.[20] Probíhající lékařský výzkum se zaměřuje na syntézu inhibitorů aldosteronsyntázy druhé generace, aby se vytvořil ideálně selektivní inhibitor, protože současný orálně dodávaný LCl699 se ukázal jako nespecifický pro aldosteronsyntázu.[20]
Viz také
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000179142 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ A b C d E Bassett MH, White PC, Rainey WE (březen 2004). "Regulace exprese aldosteronsyntázy". Molekulární a buněčná endokrinologie. 217 (1–2): 67–74. doi:10.1016 / j.mce.2003.10.011. PMID 15134803. S2CID 43133280.
- ^ Peter M, Dubuis JM, Sippell WG (1999). "Poruchy nedostatku aldosteronsyntázy a steroidů 11beta-hydroxylázy". Výzkum hormonů. 51 (5): 211–22. doi:10.1159/000023374. PMID 10559665. S2CID 24182379.
- ^ A b C d E F Strushkevich N, Gilep AA, Shen L, Arrowsmith CH, Edwards AM, Usanov SA, Park HW (únor 2013). „Strukturální pohledy na specificitu substrátu aldosteronsyntázy a cílenou inhibici“. Molekulární endokrinologie. 27 (2): 315–24. doi:10.1210 / me.2012-1287. PMC 5417327. PMID 23322723.
- ^ Mornet E, Dupont J, Vitek A, White PC (prosinec 1989). "Charakterizace dvou genů kódujících lidskou steroid 11 beta-hydroxylázu (P-450 (11) beta)". The Journal of Biological Chemistry. 264 (35): 20961–7. PMID 2592361.
- ^ „CYP11B2“. Citováno 17. září 2013.
- ^ Pascoe L, Curnow KM, Slutsker L, Rösler A, White PC (červen 1992). „Mutace v lidském genu CYP11B2 (aldosteron syntáza) způsobující nedostatek kortikosteron methyloxidázy II“. Sborník Národní akademie věd Spojených států amerických. 89 (11): 4996–5000. Bibcode:1992PNAS ... 89.4996P. doi:10.1073 / pnas.89.11.4996. PMC 4921. PMID 1594605.
- ^ Brown RD, Strott CA, Liddle GW (červen 1972). „Místo stimulace biosyntézy aldosteronu angiotensinem a draslíkem“. The Journal of Clinical Investigation. 51 (6): 1413–8. doi:10,1172 / JCI106937. PMC 292278. PMID 4336939.
- ^ Williams GH (leden 2005). "Aldosteron biosyntéza, regulace a klasický mechanismus účinku". Hodnocení srdečního selhání. 10 (1): 7–13. doi:10.1007 / s10741-005-2343-3. PMID 15947886. S2CID 19588366.
- ^ "CYP11B1". Genetická domácí reference. Americká národní lékařská knihovna. Září 2013.
- ^ A b C d E F G h van Rooyen D, Gent R, Barnard L, Swart AC (duben 2018). "In vitro metabolismus 11β-hydroxyprogesteronu a 11-ketoprogesteronu na 11-ketodihydrotestosteron v zadní cestě". The Journal of Steroid Biochemistry and Molecular Biology. 178: 203–212. doi:10.1016 / j.jsbmb.2017.12.014. PMID 29277707. S2CID 3700135.
- ^ Bassett MH, White PC, Rainey WE (březen 2004). "Regulace exprese aldosteronsyntázy". Molekulární a buněčná endokrinologie. 217 (1–2): 67–74. doi:10.1016 / j.mce.2003.10.011. PMID 15134803. S2CID 43133280.
- ^ Lenders JW, Williams TA, Reincke M, Gomez-Sanchez CE (leden 2018). „DIAGNOSTIKA ENDOKRINNÍ NEMOCI: 18-oxokortizol a 18-hydroxykortizol: existuje klinická užitečnost těchto steroidů?“. Evropský žurnál endokrinologie. 178 (1): R1 – R9. doi:10.1530 / EJE-17-0563. PMC 5705277. PMID 28904009.
- ^ Freel EM, Shakerdi LA, Friel EC, Wallace AM, Davies E, Fraser R, Connell JM (září 2004). „Studie o původu cirkulujícího 18-hydroxykortizolu a 18-oxokortizolu u normálních lidských subjektů“. The Journal of Clinical Endocrinology and Metabolism. 89 (9): 4628–33. doi:10.1210 / jc.2004-0379. PMC 1283128. PMID 15356073.
- ^ Lisboa BP, Gustafsson JA (červen 1969). "Biosyntéza 18-hydroxytestosteronu v lidských fetálních játrech". European Journal of Biochemistry. 9 (3): 402–5. doi:10.1111 / j.1432-1033.1969.tb00622.x. PMID 4307594.
- ^ Nakamura Y, Yamazaki Y, Tezuka Y, Satoh F, Sasano H (listopad 2016). „Exprese CYP11B2 v adenokortikálním adenomu produkujícím aldosteron: regulační mechanismy a klinický význam“. Tohoku Journal of Experimental Medicine. 240 (3): 183–190. doi:10.1620 / tjem.240.183. PMID 27853054.
- ^ A b C Peter M, Fawaz L, Drop SL, Visser HK, Sippell WG (listopad 1997). „Dědičný defekt v biosyntéze aldosteronu: nedostatek aldosteron syntázy 1964–1997“. The Journal of Clinical Endocrinology and Metabolism. 82 (11): 3525–8. doi:10.1210 / jc.82.11.3525. PMID 9360501.
- ^ A b C d Azizi M, Amar L, Menard J (leden 2013). „Inhibice aldosteron syntázy u lidí“. Nefrologie, dialýza, transplantace. 28 (1): 36–43. doi:10.1093 / ndt / gfs388. PMID 23045428.
Další čtení
- Helmberg A (srpen 1993). "Twin geny a endokrinní onemocnění: geny CYP21 a CYP11B". Acta Endocrinologica. 129 (2): 97–108. doi:10.1530 / acta.0.1290097. PMID 8372604.
- Mírně SH, Joseph J, Ganjam VK, Weber KT (červen 1999). "Extraadrenální mineralokortikoidy a kardiovaskulární tkáň". Journal of Molecular and Cellular Cardiology. 31 (6): 1175–84. doi:10.1006 / jmcc.1999.0963. PMID 10371693.
- Stowasser M, Gunasekera TG, Gordon RD (prosinec 2001). "Rodinné odrůdy primárního aldosteronismu". Klinická a experimentální farmakologie a fyziologie. 28 (12): 1087–90. doi:10.1046 / j.1440-1681.2001.03574.x. PMID 11903322. S2CID 23091842.
- Padmanabhan N, Padmanabhan S, Connell JM (prosinec 2000). „Genetický základ kardiovaskulárních onemocnění - systém renin-angiotensin-aldosteron jako paradigma“. Journal of the Renin-Angiotensin-Aldosterone System. 1 (4): 316–24. doi:10,3317 / jraas.2000.060. PMID 11967817.
- Lifton RP, Dluhy RG, Powers M, Rich GM, Gutkin M, Fallo F a kol. (Září 1992). „Dědičná hypertenze způsobená duplikacemi chimérických genů a ektopickou expresí aldosteron syntázy“. Genetika přírody. 2 (1): 66–74. doi:10.1038 / ng0992-66. PMID 1303253. S2CID 975796.
- Mitsuuchi Y, Kawamoto T, Naiki Y, Miyahara K, Toda K, Kuribayashi I a kol. (Leden 1992). „Vrozeně defektní biosyntéza aldosteronu u lidí: účast bodových mutací genu P-450C18 (CYP11B2) u pacientů s deficitem CMO II“. Sdělení o biochemickém a biofyzikálním výzkumu. 182 (2): 974–9. doi:10.1016 / 0006-291X (92) 91827-D. PMID 1346492.
- Pascoe L, Curnow KM, Slutsker L, Connell JM, Speiser PW, New MI, White PC (září 1992). „Hyperaldosteronismus potlačující glukokortikoidy je výsledkem hybridních genů vytvořených nerovným křížením mezi CYP11B1 a CYP11B2“. Sborník Národní akademie věd Spojených států amerických. 89 (17): 8327–31. Bibcode:1992PNAS ... 89.8327P. doi:10.1073 / pnas.89.17.8327. PMC 49911. PMID 1518866.
- Pascoe L, Curnow KM, Slutsker L, Rösler A, White PC (červen 1992). „Mutace v lidském genu CYP11B2 (aldosteron syntáza) způsobující nedostatek kortikosteron methyloxidázy II“. Sborník Národní akademie věd Spojených států amerických. 89 (11): 4996–5000. Bibcode:1992PNAS ... 89.4996P. doi:10.1073 / pnas.89.11.4996. PMC 49215. PMID 1594605.
- Kawamoto T, Mitsuuchi Y, Toda K, Yokoyama Y, Miyahara K, Miura S a kol. (Únor 1992). „Role steroidu 11 beta-hydroxylázy a steroidu 18-hydroxylázy v biosyntéze glukokortikoidů a mineralokortikoidů u lidí“. Sborník Národní akademie věd Spojených států amerických. 89 (4): 1458–62. Bibcode:1992PNAS ... 89.1458K. doi:10.1073 / pnas.89.4.1458. PMC 48470. PMID 1741400.
- Curnow KM, Tusie-Luna MT, Pascoe L, Natarajan R, Gu JL, Nadler JL, White PC (říjen 1991). „Produkt genu CYP11B2 je vyžadován pro biosyntézu aldosteronu v lidské kůře nadledvin“. Molekulární endokrinologie. 5 (10): 1513–22. doi:10.1210 / oprava-5-10-1513. PMID 1775135.
- Kawainoto T, Mitsuuchi Y, Ohnishi T, Ichikawa Y, Yokoyama Y, Sumimoto H a kol. (Listopad 1990). "Klonování a exprese cDNA pro lidský cytochrom P-450aldo ve vztahu k primárnímu aldosteronismu". Sdělení o biochemickém a biofyzikálním výzkumu. 173 (1): 309–16. doi:10.1016 / S0006-291X (05) 81058-7. PMID 2256920.
- Mornet E, Dupont J, Vitek A, White PC (prosinec 1989). "Charakterizace dvou genů kódujících lidskou steroid 11 beta-hydroxylázu (P-450 (11) beta)". The Journal of Biological Chemistry. 264 (35): 20961–7. PMID 2592361.
- Martsev SP, Chashchin VL, Akhrem AA (Únor 1985). „[Rekonstrukce a studium systému multienzymů pomocí 11 beta-hydroxylázových steroidů]“. Biokhimiia. 50 (2): 243–57. PMID 3872685.
- Shizuta Y, Kawamoto T, Mitsuuchi Y, Miyahara K, Rösler A, Ulick S, Imura H (leden 1995). "Vrozené chyby biosyntézy aldosteronu u lidí". Steroidy. 60 (1): 15–21. doi:10.1016 / 0039-128X (94) 00023-6. PMID 7792802. S2CID 23433739.
- Mitsuuchi Y, Kawamoto T, Miyahara K, Ulick S, Morton DH, Naiki Y a kol. (Únor 1993). „Vrozeně defektní biosyntéza aldosteronu u lidí: inaktivace genu P-450C18 (CYP11B2) v důsledku delece nukleotidů u pacientů s deficitem CMO I“. Sdělení o biochemickém a biofyzikálním výzkumu. 190 (3): 864–9. doi:10.1006 / bbrc.1993.1128. PMID 8439335.
- Fardella CE, Rodriguez H, Montero J, Zhang G, Vignolo P, Rojas A a kol. (Prosinec 1996). "Genetická variace P450c11AS u chilských pacientů s nízkou hypertenzí reninem". The Journal of Clinical Endocrinology and Metabolism. 81 (12): 4347–51. doi:10.1210 / jc.81.12.4347. PMID 8954040.
- Nomoto S, Massa G, Mitani F, Ishimura Y, Miyahara K, Toda K a kol. (Květen 1997). „Nedostatek CMO I způsobený bodovou mutací v exonu 8 lidského genu CYP11B2 kódujícího steroid 18-hydroxylázu (P450C18)“. Sdělení o biochemickém a biofyzikálním výzkumu. 234 (2): 382–5. doi:10.1006 / bbrc.1997.6651. PMID 9177280.
- Taymans SE, Pack S, Pak E, Torpy DJ, Zhuang Z, Stratakis CA (březen 1998). „Lidský CYP11B2 (aldosteron syntáza) se mapuje na chromozom 8q24.3“. The Journal of Clinical Endocrinology and Metabolism. 83 (3): 1033–6. doi:10.1210 / jc.83.3.1033. PMID 9506770.
externí odkazy
- Aldosteron + syntáza v americké národní lékařské knihovně Lékařské předměty (Pletivo)
- Člověk CPN2 umístění genomu a CPN2 stránka s podrobnostmi o genu v UCSC Genome Browser.
- Člověk CYP11B2 umístění genomu a CYP11B2 stránka s podrobnostmi o genu v UCSC Genome Browser.
Kategorie: Cytochrom P450