Kyselina máselná - Butyric acid
| |||
 | |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC Kyselina butanová[1] | |||
| Ostatní jména | |||
| Identifikátory | |||
3D model (JSmol ) |
| ||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider | |||
| DrugBank |
| ||
| Informační karta ECHA | 100.003.212 | ||
| Číslo ES |
| ||
| |||
| KEGG |
| ||
| Pletivo | Kyselina máselná + | ||
PubChem CID | |||
| Číslo RTECS |
| ||
| UNII |
| ||
| UN číslo | 2820 | ||
Řídicí panel CompTox (EPA) |
| ||
| |||
| |||
| Vlastnosti | |||
| C 3H 7COOH | |||
| Molární hmotnost | 88.106 g · mol−1 | ||
| Vzhled | Bezbarvá kapalina | ||
| Zápach | Nepříjemné, podobné zvratkům nebo tělesnému pachu | ||
| Hustota | 1,135 g / cm3 (-43 ° C)[2] 0,9528 g / cm3 (25 ° C)[3] | ||
| Bod tání | -5,1 ° C (22,8 ° F; 268,0 K)[3] | ||
| Bod varu | 163,75 ° C (326,75 ° F; 436,90 K)[3] | ||
| Sublimuje při -35 ° C ΔsublH | |||
| Mísitelný | |||
| Rozpustnost | Mísitelný s ethanol, éter. Mírně rozpustný v CCl4 | ||
| log P | 0.79 | ||
| Tlak páry | 0,112 kPa (20 ° C) 0,74 kPa (50 ° C) 9,62 kPa (100 ° C)[4] | ||
| 5.35·10−4 L · atm / mol | |||
| Kyselost (strK.A) | 4.82 | ||
| -55.10·10−6 cm3/ mol | |||
| Tepelná vodivost | 1.46·105 W / m · K. | ||
Index lomu (nD) | 1,398 (20 ° C)[3] | ||
| Viskozita | 1,814 cP (15 ° C)[5] 1,426 cP (25 ° C) | ||
| Struktura | |||
| Monoklinický (-43 ° C)[2] | |||
| C2 / m[2] | |||
A = 8,01 Å, b = 6,82 Å, C = 10,14 Å[2] a = 90 °, β = 111,45 °, γ = 90 ° | |||
| 0,93 D (20 ° C)[5] | |||
| Termochemie | |||
Tepelná kapacita (C) | 178,6 J / mol · K.[4] | ||
Std molární entropie (S | 222,2 J / mol · K.[5] | ||
Std entalpie of formace (ΔFH⦵298) | -533,9 kJ / mol[4] | ||
Std entalpie of spalování (ΔCH⦵298) | 2183,5 kJ / mol[4] | ||
| Nebezpečí | |||
| Bezpečnostní list | Externí bezpečnostní list | ||
| Piktogramy GHS |  [6] [6] | ||
| Signální slovo GHS | Nebezpečí | ||
| H314[6] | |||
| P280, P305 + 351 + 338, P310[6] | |||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | 71 až 72 ° C (160 až 162 ° F; 344 až 345 K)[6] | ||
| 440 ° C (824 ° F; 713 K)[6] | |||
| Výbušné limity | 2.2–13.4% | ||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
LD50 (střední dávka ) | 2000 mg / kg (orálně, potkan) | ||
| Související sloučeniny | |||
Příbuzný Karboxylové kyseliny | Kyselina propionová, Kyselina pentanová | ||
Související sloučeniny | 1-Butanol Butyraldehyd Methylbutyrát | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Kyselina máselná (z Starořečtina: βούτῡρον, což znamená „máslo“), známé také pod systematickým názvem kyselina butanová, je přímý řetězec alkyl karboxylová kyselina s chemický vzorec CH3CH2CH2CO2H. Je to olejovitá, bezbarvá kapalina s nepříjemný zápach. Kyselina isomáselná (Kyselina 2-methylpropanová) je izomer. Solí a estery kyseliny máselné jsou známé jako butyráty nebo butanoáty. Kyselina se v přírodě příliš nevyskytuje, ale její estery jsou velmi rozšířené. Je to běžná průmyslová chemikálie[7] a důležitou složkou ve střevech savců.
Dějiny
Kyselina máselná byla poprvé pozorována v nečisté formě v roce 1814 francouzským chemikem Michel Eugène Chevreul. Do roku 1818 ji dostatečně očistil, aby ji charakterizoval. Chevreul však nepublikoval svůj první výzkum kyseliny máselné; místo toho uložil své nálezy v rukopisné podobě u sekretářky Akademie věd v Paříži ve Francii. Henri Braconnot, francouzský chemik, také zkoumal složení másla a publikoval svá zjištění, což vedlo ke sporům o prioritu. Již v roce 1815 Chevreul tvrdil, že našel látku odpovědnou za vůni másla.[8] V roce 1817 zveřejnil některé ze svých zjištění týkajících se vlastností kyseliny máselné a pojmenoval ji.[9] Avšak až v roce 1823 podrobně představil vlastnosti kyseliny máselné.[10] Název kyselina máselná pochází z Starořečtina: βούτῡρον, což znamená „máslo“, látka, ve které bylo poprvé nalezeno. Latinský název butyrum (nebo buturum) je podobný.
Výskyt
Triglyceridy kyseliny máselné tvoří 3–4% másla. Když máslo ztuhne, kyselina máselná se uvolní z glyceridu hydrolýza.[11] Je to jedna z podskupin mastných kyselin mastné kyseliny s krátkým řetězcem. Typická je kyselina máselná karboxylová kyselina který reaguje se zásadami a ovlivňuje mnoho kovů.[12]Nachází se v zvířecí tuk a rostlinné oleje, hovězí mléko, mateřské mléko, máslo, parmazán, tělesný zápach, zvracení, a jako produkt anaerobní kvašení (včetně v dvojtečka ).[13][14] Má to chuť něco jako máslo a nepříjemné zápach. Savci s dobrými schopnostmi detekce vůní, jako je psy, může jej detekovat v 10 části na miliardu, zatímco lidé může detekovat pouze v koncentracích nad 10 Díly na milión. v výroba potravin, používá se jako ochucovadlo.[15]
U lidí je kyselina máselná jednou ze dvou primárních endogenní agonisté člověka receptor hydroxykarboxylové kyseliny 2 (HCA2), a Gi / o-připojeno Receptor spojený s G proteinem.[16][17]
Kyselina máselná je přítomna jako taková oktylester v pastinák (Pastinaca sativa)[18] a v semeni ginkgo strom.[19]
Výroba
Průmyslový
V průmyslu vyrábí kyselinu máselnou hydroformylace z propen a Syngas, formování butyraldehyd, který je oxidovaný ke konečnému produktu.[7]
- H2 + CO + CH3CH = CH2 → CH3CH2CH2CHO → kyselina máselná
Lze jej oddělit od vodných roztoků nasycením solemi, jako je chlorid vápenatý. Vápenatá sůl, Ca (C4H7Ó2)2· H2O, je méně rozpustný v horké vodě než ve studené.
Mikrobiální biosyntéza
Butyrát se vyrábí několika fermentačními procesy prováděnými povinná anaerobní bakterie.[20] Tuto fermentační cestu objevil Louis Pasteur v roce 1861. Příklady výroby butyrátu druh bakterií:
- Clostridium butyricum
- Clostridium kluyveri
- Clostridium pasteurianum
- Faecalibacterium prausnitzii
- Fusobacterium nucleatum
- Butyrivibrio fibrisolvens
- Eubacterium limosum
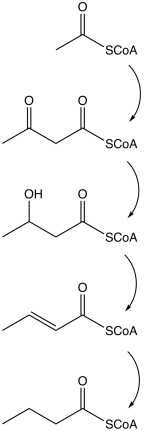
Cesta začíná na glykolytický štěpení glukóza na dva molekuly z pyruvát, jak se to děje ve většině organismů. Pyruvát je oxidovaný do acetyl koenzym A katalyzováno pyruvát: ferredoxin oxidoreduktáza. Dvě molekuly oxid uhličitý (CO.)2) a dvě molekuly elementární vodík (H2) vznikají jako odpadní produkty. Následně ATP se vyrábí v posledním kroku fermentace. Pro každou molekulu glukózy se produkují tři molekuly ATP, což je relativně vysoký výtěžek. Vyvážená rovnice pro tuto fermentaci je
- C6H12Ó6 → C.4H8Ó2 + 2 CO2 + 2 H2
Mezi další cesty k butyrátu patří redukce sukcinátu a disproporce krotonátu.
| Akce | Odpovědný enzym |
|---|---|
| Acetyl koenzym A se přeměňuje na acetoacetyl koenzym A | acetyl-CoA-acetyl transferáza |
| Acetoacetyl koenzym A se přeměňuje na p-hydroxybutyryl CoA | β-hydroxybutyryl-CoA dehydrogenáza |
| β-hydroxybutyryl CoA se převádí na krotonyl CoA | krotonáza |
| Crotonyl CoA se převádí na butyryl CoA (CH3CH2CH2C = O-CoA) | butyryl-CoA dehydrogenáza |
| A fosfát skupina nahradí CoA k vytvoření butyrylfosfát | fosfobutyryláza |
| Fosfátová skupina se připojí ADP tvořit ATP a butyrát | butyrátkináza |
Vytváří se několik druhů aceton a n-butanol v alternativní cestě, která začíná jako butyrátová fermentace. Některé z těchto druhů jsou:
- Clostridium acetobutylicum, nejvýznamnější výrobce acetonu a butanolu, používaný také v průmyslu
- Clostridium beijerinckii
- Clostridium tetanomorphum
- Clostridium aurantibutyricum
Tyto bakterie začínají fermentací butyrátu, jak je popsáno výše, ale když pH klesne pod 5, přecházejí na produkci butanolu a acetonu, aby se zabránilo dalšímu snížení pH. Pro každou molekulu acetonu se vytvoří dvě molekuly butanolu.
Ke změně dráhy dochází po tvorbě acetoacetyl CoA. Tento meziprodukt pak trvá dvěma možnými cestami:
- acetoacetyl CoA → acetoacetát → aceton
- acetoacetyl CoA → butyryl CoA → butyraldehyd → butanol
Zdroje fermentovatelných vláken
Vysoce fermentovatelné zbytky vláken, jako jsou zbytky z odolný škrob, ovesné otruby, pektin, a guar jsou transformovány pomocí bakterie tlustého střeva do mastné kyseliny s krátkým řetězcem (SCFA) včetně butyrátu, produkující více SCFA než méně fermentovatelných vláken, jako je celulózy.[14][21] Jedna studie zjistila, že rezistentní škrob trvale produkuje více butyrátu než jiné druhy vláknina.[22] Výroba SCFA z vláken v přežvýkavec zvířata, jako je skot, jsou odpovědná za obsah butyrátu v mléce a másle.[13][23]
Fruktany jsou dalším zdrojem prebiotických rozpustných dietních vláken, které lze trávit za vzniku butyrátu.[24] Často se nacházejí v rozpustných vlákninách potravin s vysokým obsahem síra, tak jako allium a křupavá zelenina. Zdroje fruktanů zahrnout pšenice (ačkoli některé kmeny pšenice, jako např špalda obsahují nižší množství),[25] žito, ječmen, cibule, česnek, Jeruzalém a zeměkoule artyčok, chřest, červená řepa, čekanka, pampeliška listy, pórek, radicchio, bílá část jarní cibulka, brokolice, růžičková kapusta, zelí, fenykl a prebiotika, jako jsou fruktooligosacharidy (FOS ), oligofruktóza, a inulin.[26][27]
Reakce
Kyselina máselná reaguje jako typická karboxylová kyselina: může se tvořit amide, ester, anhydrid, a chlorid deriváty.[28] Dopis, butyrylchlorid se běžně používá jako meziprodukt k získání ostatních.
Použití
Kyselina máselná se používá při přípravě různých esterů butyrátu. Používá se k výrobě octan butyrát celulózy (CAB), který se používá v široké škále nástrojů, barev a nátěrů a je odolnější vůči degradaci než acetát celulózy.[29] CAB se však může vystavit teplu a vlhkosti degradovat a uvolňovat kyselinu máselnou.[30]
Nízkomolekulární estery kyseliny máselné, jako např methylbutyrát, mají většinou příjemné vůně nebo chutě.[7] V důsledku toho se používají jako přísady do potravin a parfémů. Jedná se o schválenou potravinářskou příchuť v EU Databáze FLAVIS (číslo 08.005).
Díky svému silnému zápachu se také používá jako přísada do rybářských návnad.[31] Mnoho komerčně dostupných příchutí používaných v kapr (Cyprinus carpio) návnady používají jako svou esterovou bázi kyselinu máselnou; není však jasné, zda ryby přitahuje samotná kyselina máselná nebo látky do ní přidávané. Kyselina máselná však byla jednou z mála organických kyselin, které se ukázaly jako chutné pro obě lín a hořký.[32] Látka byla také použita jako a páchnoucí bomba podle Sea Shepherd Conservation Society narušit japonštinu lov velryb posádky.[33]
Farmakologie
| Inhibovaný enzym | IC50 (nM) | Vstupní poznámka |
|---|---|---|
| HDAC1 | 16,000 | |
| HDAC2 | 12,000 | |
| HDAC3 | 9,000 | |
| HDAC4 | 2,000,000 | Dolní mez |
| HDAC5 | 2,000,000 | Dolní mez |
| HDAC6 | 2,000,000 | Dolní mez |
| HDAC7 | 2,000,000 | Dolní mez |
| HDAC8 | 15,000 | |
| HDAC9 | 2,000,000 | Dolní mez |
| CA1 | 511,000 | |
| CA2 | 1,032,000 | |
| GPCR cílová | pEC50 | Vstupní poznámka |
| FFAR2 | 2.9–4.6 | Plný agonista |
| FFAR3 | 3.8–4.9 | Plný agonista |
| HCA2 | 2.8 | Agonista |
Farmakodynamika
Kyselina máselná (pKA 4.82) je plně ionizovaný na fyziologické pH, Takže to je anion je materiál, který je důležitý hlavně v biologických systémech. Je to jeden ze dvou primárních endogenní agonisté člověka receptor hydroxykarboxylové kyseliny 2 (HCA2, aka GPR109A), a Gi / o-připojeno Receptor spojený s G proteinem (GPCR),[16][17]
Jako ostatní mastné kyseliny s krátkým řetězcem (SCFA), butyrát je agonista u receptory volných mastných kyselin FFAR2 a FFAR3, které fungují jako senzory živin, které usnadňují homeostatická regulace energetické bilance; avšak ze skupiny SCFA je agonistou pouze butyrát HCA2.[36][37][38] Je to také HDAC inhibitor (konkrétně HDAC1, HDAC2, HDAC3 a HDAC8),[34][35] lék, který inhibuje funkci histon deacetyláza enzymy, čímž upřednostňuje acetylovaný stav histony v buňkách.[38] Acetylace histonu uvolňuje strukturu chromatin snížením elektrostatický přitažlivost mezi histony a DNA.[38] Obecně se má za to, že transkripční faktory nebude schopen přistupovat k oblastem, kde jsou histony úzce spojeny s DNA (tj. neacetylované, např. heterochromatin).[nutná lékařská citace ] Proto se má za to, že kyselina máselná zvyšuje transkripční aktivitu promotorů,[38] které jsou typicky umlčeny nebo downregulovány kvůli aktivitě histon-deacetylázy.
Farmakokinetika
Butyrát, který se produkuje v tlustém střevě mikrobiální fermentací vlákniny, je primárně absorbován a metabolizován kolonocyty a játry[poznámka 1] pro tvorbu ATP během energetického metabolismu; část butyrátu se však vstřebává distální tračník, který není spojen s portální žílou, což umožňuje systémová distribuce butyrátu do více orgánových systémů prostřednictvím oběhového systému.[38] Butyrát, který dosáhl systémového oběhu, může snadno překonat hematoencefalická bariéra přes monokarboxylátové transportéry (tj. určití členové Skupina transportérů SLC16A ).[39][40] Mezi další transportéry, které zprostředkovávají průchod butyrátu přes lipidové membrány, patří SLC5A8 (SMCT1), SLC27A1 (FATP1) a SLC27A4 (FATP4).[34][40]
Metabolismus
Kyselina máselná je metabolizována různými lidmi XM-ligázy (ACSM1, ACSM2B, ASCM3, ACSM4, ACSM5 a ACSM6), také známé jako butyrát-CoA ligáza.[41][42] Metabolit produkovaný touto reakcí je butyryl – CoA, a vyrábí se takto:[41]
- Adenosintrifosfát + kyselina máselná + koenzym A → adenosinmonofosfát + pyrofosfát + butyryl-CoA
Jako mastná kyselina s krátkým řetězcem butyrát je metabolizován mitochondrie jako energie (tj. adenosintrifosfát nebo ATP) prostřednictvím zdroje metabolismus mastných kyselin.[38] Zejména je důležitým zdrojem energie pro buňky lemující savce dvojtečka (kolonocyty).[24] Bez butyrátů buňky tlustého střeva procházejí autofagie (tj. vlastní trávení) a zemřít.[43]
U lidí předchůdce butyrátu tributyrin, který je přirozeně přítomen v másle, je metabolizován triacylglycerol lipáza do dibutyrin a butyrát reakcí:[44]
- Tributyrin + H2O → dibutyrin + kyselina máselná
Biochemie
Butyrát má četné účinky na energetická homeostáza a související nemoci (cukrovka a obezita ), zánět, a imunitní funkce (např. má výraz antimikrobiální a antikarcinogenní účinky) u lidí. Tyto účinky nastávají prostřednictvím jeho metabolismu vytvářením mitochondrií ATP v době metabolismus mastných kyselin nebo prostřednictvím jednoho nebo více z nich enzym modifikující histon cíle (tj histonové deacetylázy I. třídy ) a Receptor spojený s G-proteinem cíle (tj. FFAR2, FFAR3, a HCA2 ).[36][45]
Ve střevech savců
Butyrát je nezbytný pro imunitní homeostázu.[36] I když role a význam butyrátu ve střevě nejsou plně pochopeny, mnoho vědců tvrdí, že vyčerpání bakterií produkujících butyrát u pacientů s několika vaskulitickými stavy je pro patogenezi těchto poruch zásadní. Vyčerpání butyrátu ve střevě je obvykle způsobeno nepřítomností nebo vyčerpáním bakterií produkujících butyrát (BPB). Toto vyčerpání v BPB vede k mikrobiálním dysbióza. To se vyznačuje celkově nízkou biologickou rozmanitostí a vyčerpáním klíčových členů produkujících butyrát. Butyrát je základní mikrobiální metabolit, který má zásadní úlohu jako modulátor správné imunitní funkce v hostiteli. Ukázalo se, že děti bez BPB jsou náchylnější k alergickým onemocněním[46] a diabetes 1. typu.[47] Butyrát hraje klíčovou roli při udržování imunitní homeostázy jak lokálně (ve střevech), tak systémově (prostřednictvím cirkulujícího butyrátu). Bylo prokázáno, že podporuje diferenciaci regulační T buňky. Obzvláště cirkulující butyrát vyvolává generování extrathymatických regulačních T buněk. Nízké hladiny butyrátu u lidských subjektů by mohly upřednostňovat sníženou regulaci zprostředkovanou T buňkami, což by podporovalo silnou imunopatologickou odpověď T buněk.[48] Na druhé straně se uvádí, že butyrát ve střevě inhibuje lokální prozánětlivé cytokiny. Nepřítomnost nebo vyčerpání těchto BPB ve střevě by proto mohla být možným pomocníkem při příliš aktivní zánětlivé odpovědi. Butyrát ve střevě také chrání integritu intestinální epiteliální bariéry. Snížené hladiny butyrátu proto vedou k poškození nebo nefunkčnosti intestinální epiteliální bariéry.[49]
Ve výzkumné studii z roku 2013, kterou provedli Furusawa a kol., Bylo zjištěno, že butyrát odvozený od mikrobů je nezbytný pro indukci diferenciace regulačních T buněk tlustého střeva u myší. To je velmi důležité a pravděpodobně relevantní pro patogenezi a vaskulitidu spojenou s mnoha zánětlivými chorobami, protože regulační T buňky hrají ústřední roli při potlačení zánětlivých a alergických reakcí.[50] V několika výzkumných studiích bylo prokázáno, že butyrát indukuje diferenciaci regulačních T buněk in vitro a in vivo.[51] Protizánětlivá kapacita butyrátu byla rozsáhle analyzována a podporována mnoha studiemi. Bylo zjištěno, že butyrát produkovaný mikroorganismy urychluje produkci regulačních T buněk, ačkoli specifický mechanismus, kterým to dělá, není jasný.[52] V poslední době se ukázalo, že butyrát hraje zásadní a přímou roli v modulaci genové exprese cytotoxických T-buněk.[53] Butyrát má také protizánětlivý účinek na neutrofily a snižuje jejich migraci na rány. Tento účinek je zprostředkován receptorem HCA1[54]
Imunomodulace a zánět
Účinky butyrátu na imunitní systém jsou zprostředkovány inhibicí třídy I histonové deacetylázy a jeho aktivace Receptor spojený s G-proteinem cíle: HCA2 (GPR109A), FFAR2 (GPR43) a FFAR3 (GPR41).[37][55] Mezi mastné kyseliny s krátkým řetězcem butyrát je nejúčinnějším promotorem intestinálních regulačních T buněk in vitro a jediný ze skupiny, který je HCA2 ligand.[37] Ukázalo se, že je kritickým mediátorem zánětlivé reakce tlustého střeva. Má preventivní i terapeutický potenciál k potlačení zánětu zprostředkovaného ulcerózní kolitida a kolorektální karcinom.
Butyrát prokázal u lidí antimikrobiální vlastnosti, které jsou zprostředkovány antimikrobiální peptid LL-37, kterou indukuje prostřednictvím HDAC inhibice na histonu H3.[55][56][57] In vitro se zvyšuje butyrát genová exprese z FOXP3 (dále jen regulátor transkripce pro Tregs) a podporuje dvojtečku regulační T buňky (Tregs) prostřednictvím inhibice třídy I. histonové deacetylázy;[37][55] prostřednictvím těchto akcí zvyšuje výraz interleukin 10, protizánětlivý cytokin.[55][37] Butyrát také potlačuje zánět tlustého střeva inhibicí IFN-y –STAT1 signální cesty, které jsou částečně zprostředkovány inhibice histon-deacetylázy. Zatímco přechodná signalizace IFN-y je obecně spojena s normálním hostitelem imunitní odpověď chronická signalizace IFN-y je často spojena s chronickým zánětem. Bylo prokázáno, že butyrát inhibuje aktivitu HDAC1, který je vázán na promotor genu Fas v T buňkách, což vede k hyperacetylaci promotoru Fas a up-regulaci Fas receptor na povrchu T-buněk.[58]
Podobně jako u jiných HCA2 studovaní agonisté, butyrát také vyvolává výrazné protizánětlivé účinky v různých tkáních, včetně mozku, gastrointestinálního traktu, kůže a vaskulární tkáň.[59][60][61] Vazba butyrátu na FFAR3 indukuje neuropeptid Y uvolnění a podporuje funkčnost homeostáza sliznice tlustého střeva a enterického imunitního systému.[62]
Rakovina
Butyrát se ukázal jako kritický mediátor zánětlivé reakce tlustého střeva. Je zodpovědný za přibližně 70% energie z kolonocytů, což je kritický SCFA v tlustém střevě homeostáza.[63] Butyrát má preventivní i terapeutický potenciál k potlačení zánětu zprostředkovaného ulcerózní kolitida (UC) a kolorektální karcinom.[64] Produkuje různé účinky na zdravé a rakovinné buňky: toto je známé jako „butyrátový paradox“. Butyrát zejména inhibuje nádorové buňky tlustého střeva a stimuluje množení zdravých buněk epitelu tlustého střeva.[65][66]Vysvětlení, proč je butyrát zdrojem energie pro normální kolonocyty a indukuje apoptóza v rakovina tlustého střeva buňky, je Warburgův efekt v rakovinných buňkách, což vede k tomu, že butyrát není správně metabolizován. Tento jev vede k hromadění butyrátu v jádru, který působí jako a histon deacetyláza (HDAC) inhibitor.[67] Jedním z mechanismů, které jsou základem funkce butyrátu při potlačení zánětu tlustého střeva, je inhibice IFN-y /STAT1 signální dráhy. Bylo prokázáno, že butyrát inhibuje aktivitu HDAC1 který je vázán na Gen Fas promotér v T buňky, což vede k hyperacetylaci promotoru Fas a upregulaci receptoru Fas na povrchu T buněk. Navrhuje se tedy, že butyrát zvyšuje apoptóza T buněk v tlustém střevě a tím eliminuje zdroj zánětu (produkce IFN-y).[68] Butyrát inhibuje angiogeneze deaktivací Transkripční faktor Sp1 činnost a downregulování vaskulární endoteliální růstový faktor genová exprese.[69]
Stručně řečeno, výroba těkavé mastné kyseliny jako je butyrát z fermentovatelných vláken může přispívat k roli vlákniny ve stravě při rakovině tlustého střeva. Mastné kyseliny s krátkým řetězcem, které zahrnují kyselinu máselnou, se vyrábějí prospěšnými bakterie tlustého střeva (probiotika ), které se živí nebo fermentují prebiotika, což jsou rostlinné produkty, které obsahují vlákninu. Tyto mastné kyseliny s krátkým řetězcem prospívají kolonocytům zvýšením produkce energie a mohou chránit před rakovinou tlustého střeva inhibicí buněčné proliferace.[21]
Někteří vědci se naopak snažili vyloučit butyrát a považovali jej za potenciálního řidiče rakoviny.[70] Studie na myších naznačují, že řídí transformaci Nedostatek MSH2 buňky epitelu tlustého střeva.[71]
Možné ošetření obnovou butyrátu
Vzhledem k významu butyrátu jako regulátoru zánětu a přispěvatele imunitního systému by vyčerpání butyrátu mohlo být klíčovým faktorem ovlivňujícím patogenezi mnoha vaskulitický podmínky. Je proto nezbytné udržovat zdravé hladiny butyrátu ve střevě. Transplantace fekální mikrobioty (obnovit BPB a symbióza ve střevě) může být efektivní doplněním hladiny butyrátu. Při této léčbě daruje zdravý jedinec stolici k transplantaci jedinci s dysbiózou. Méně invazivní možností léčby je podávání butyrátu - jako perorálních doplňků nebo klystýrů -, který se ukázal jako velmi účinný při potlačování příznaků zánětu s minimálními nebo žádnými vedlejšími účinky. Ve studii, kde byli pacienti s ulcerózní kolitidou léčeni butyrátovými klystýry, se významně snížil zánět a krvácení úplně skončilo po zavedení butyrátu.[72]
Závislost
Kyselina máselná je HDAC inhibitor, který je selektivní pro HDAC třídy I u lidí.[34] HDAC jsou enzymy modifikující histon které mohou způsobit deacetylaci histonu a represi genové exprese. HDAC jsou důležitými regulátory synaptické formace, synaptická plasticita, a dlouhodobá paměť formace. Je známo, že HDAC třídy I se podílejí na zprostředkování vývoje závislost.[73][74][75] Kyselina máselná a další inhibitory HDAC byly použity v předklinickém výzkumu k posouzení transkripčních, nervových a behaviorálních účinků inhibice HDAC u zvířat závislých na drogách.[75][76][77]
Butyrátové soli a estery
The butyrát nebo butanoát, ion je C2H5CÓ Ó−, konjugovaná báze kyseliny máselné. Je to forma nalezená v biologických systémech v fyziologické pH. Butyrová nebo butanová sloučenina je a karboxylátová sůl nebo ester kyseliny máselné.
Příklady
Solí
Estery
- Butylbutyrát
- Butyryl-CoA
- Octan butyrát celulózy (droga)
- Estradiol benzoát butyrát
- Ethyl butyrát
- Methylbutyrát
- Pentylbutyrát
- Tributyrin
Viz také
Poznámky
- ^ Většina butyrátu, který se vstřebává krevní plazma z tlustého střeva vstupuje do oběhového systému přes portální žíla; většina butyrátu, který touto cestou vstupuje do oběhového systému, je absorbována játry.[38]
Reference
![]() Tento článek včlení text z publikace nyní v veřejná doména: Chisholm, Hugh, ed. (1911). "Kyselina máselná ". Encyklopedie Britannica (11. vydání). Cambridge University Press.
Tento článek včlení text z publikace nyní v veřejná doména: Chisholm, Hugh, ed. (1911). "Kyselina máselná ". Encyklopedie Britannica (11. vydání). Cambridge University Press.
- ^ Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 746. doi:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ A b C d Strieter FJ, Templeton DH (1962). "Krystalová struktura kyseliny máselné" (PDF). Acta Crystallographica. 15 (12): 1240–1244. doi:10.1107 / S0365110X6200328X.
- ^ A b C d Lide, David R., ed. (2009). CRC Handbook of Chemistry and Physics (90. vydání). Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ^ A b C d E Kyselina butanová v Linstrom, Peter J .; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69, Národní institut pro standardy a technologii, Gaithersburg (MD), http://webbook.nist.gov (vyvoláno 27. října 2020)
- ^ A b C "Kyselina butanová". Chemister.ru. 19. března 2007. Citováno 27. října 2020.
- ^ A b C d E Sigma-Aldrich Co., Kyselina máselná. Citováno dne 27. října 2020.
- ^ A b C Riemenschneider, Wilhelm (2002). "Karboxylové kyseliny, alifatické". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a05_235.
- ^ Chevreul (1815) „Lettre de M. Chevreul à MM. Les rédacteurs des Annales de chimie“ (Dopis pana Chevreula redaktorům Annals of Chemistry), Annales de chimie, 94 : 73–79; v poznámce pod čarou na stranách 75–76 uvádí, že našel látku, která odpovídá za vůni másla.
- ^ Chevreul (1817) „Extrait d'une lettre de M. Chevreul à MM. Les Rédacteurs du Journal de Pharmacie“ (Výňatek z dopisu pana Chevreula redakci Journal of Pharmacy), Journal de Pharmacie et des sciences accessoires, 3 : 79–81. Na str. 81, jmenoval kyselinu máselnou: „Ce principe, que j'ai appelé depuis acid butérique,…“ (Tento princip [tj. Složka], který jsem od té doby pojmenoval „kyselina máselná“,…)
- ^ E. Chevreul, Obnovuje chimiques sur les corps gras d'origine animale [Chemické výzkumy tukových látek živočišného původu] (Paříž, Francie: F.G. Levrault, 1823), stránky 115–133.
- ^ Woo, A.H .; Lindsay, R.C. (1983). "Postupná diskriminační analýza profilů volných mastných kyselin pro identifikaci zdrojů lipolytických enzymů v žluklém másle". Journal of Dairy Science. 66 (10): 2070–2075. doi:10.3168 / jds.S0022-0302 (83) 82052-9.
- ^ ICSC 1334 - Kyselina máselná. Inchem.org (23. listopadu 1998). Citováno 2020-10-27.
- ^ A b McNabney, S. M .; Henagan, T. M. (2017). „Mastné kyseliny s krátkým řetězcem v tlustém a periferním tkáni: zaměření na butyrát, rakovinu tlustého střeva, obezitu a inzulínovou rezistenci“. Živiny. 9 (12): 1348. doi:10,3390 / nu9121348. PMC 5748798. PMID 29231905.
- ^ A b Morrison, D. J .; Preston, T. (2016). „Tvorba mastných kyselin s krátkým řetězcem střevní mikroflórou a jejich dopad na lidský metabolismus“. Střevní mikroby. 7 (3): 189–200. doi:10.1080/19490976.2015.1134082. PMC 4939913. PMID 26963409.
- ^ "Kyselina máselná". Společnost Good Scents. Citováno 26. října 2020.
- ^ A b Offermanns S, Colletti SL, Lovenberg TW, Semple G, Wise A, IJzerman AP (červen 2011). „Mezinárodní unie základní a klinické farmakologie. LXXXII: Názvosloví a klasifikace receptorů hydroxykarboxylových kyselin (GPR81, GPR109A a GPR109B)“. Farmakologické recenze. 63 (2): 269–90. doi:10.1124 / pr.110.003301. PMID 21454438.
- ^ A b Offermanns S, Colletti SL, IJzerman AP, Lovenberg TW, Semple G, Wise A, Waters MG. "Receptory hydroxykarboxylové kyseliny". Průvodce farmakologií IUPHAR / BPS. Mezinárodní unie základní a klinické farmakologie. Citováno 13. července 2018.
- ^ Carroll, Mark J .; Berenbaum, květen R. (2002). "Behaviorální reakce webového červa pastináka na hostitele těkavých rostlin". Journal of Chemical Ecology. 28 (11): 2191–2201. doi:10.1023 / A: 1021093114663. PMID 12523562. S2CID 23512190.
- ^ Raven, Peter H.; Evert, Ray F .; Eichhorn, Susan E. (2005). Biologie rostlin. W. H. Freemanand Company. str.429 –431. ISBN 978-0-7167-1007-3. Citováno 11. října 2018.
- ^ Seedorf, H .; Fricke, W. F .; Veith, B .; Bruggemann, H .; Liesegang, H .; Strittmatter, A .; Miethke, M .; Buckel, W .; Hinderberger, J .; Li, F .; Hagemeier, C .; Thauer, R. K.; Gottschalk, G. (2008). „Genom z Clostridium kluyveri, přísný anaerobní s jedinečnými metabolickými funkcemi “. Sborník Národní akademie věd. 105 (6): 2128–2133. Bibcode:2008PNAS..105,2128S. doi:10.1073 / pnas.0711093105. PMC 2542871. PMID 18218779.
- ^ A b Lupton JR (únor 2004). „Produkty mikrobiální degradace ovlivňují riziko rakoviny tlustého střeva: kontroverze butyrátu“. The Journal of Nutrition. 134 (2): 479–82. doi:10.1093 / jn / 134.2.479. PMID 14747692.
- ^ Cummings JH, Macfarlane GT, Englyst HN (únor 2001). „Prebiotické trávení a fermentace“. American Journal of Clinical Nutrition. 73 (2 doplňky): 415S – 420S. doi:10.1093 / ajcn / 73.2.415s. PMID 11157351.
- ^ Grummer RR (září 1991). „Vliv krmiva na složení mléčného tuku“. Journal of Dairy Science. 74 (9): 3244–57. doi:10.3168 / jds.S0022-0302 (91) 78510-X. PMID 1779073.
- ^ A b Rivière, Audrey; Selak, Marija; Lantin, David; Leroy, Frédéric; De Vuyst, Luc (2016). „Bifidobakterie a bakterie tlustého střeva produkující butyrát: význam a strategie pro jejich stimulaci v lidském střevě“. Hranice v mikrobiologii. 7: 979. doi:10.3389 / fmicb.2016.00979. PMC 4923077. PMID 27446020.
- ^ „Často kladené otázky v oblasti stravy a IBS“. Katedra gastroenterologie, vědy o translační výživě, Monash University, Victoria, Austrálie. Citováno 24. března 2016.
- ^ Gibson, Peter R .; Shepherd, Susan J. (1. února 2010). „Na základě důkazů dietní management funkčních gastrointestinálních symptomů: přístup FODMAP“. Journal of Gastroenterology and Hepatology. 25 (2): 252–258. doi:10.1111 / j.1440-1746.2009.06149.x. ISSN 1440-1746. PMID 20136989. S2CID 20666740.
- ^ Gibson, Peter R .; Varney, Jane; Malakar, Sreepurna; Muir, Jane G. (1. května 2015). "Složky potravy a syndrom dráždivého tračníku". Gastroenterologie. 148 (6): 1158–1174.e4. doi:10.1053 / j.gastro.2015.02.005. ISSN 1528-0012. PMID 25680668.
- ^ Jenkins, P. R. (1985). "Karboxylové kyseliny a deriváty". Obecné a syntetické metody. 7. str. 96–160. doi:10.1039/9781847556196-00096. ISBN 978-0-85186-884-4.
- ^ Lokensgard, Erik (2015). Průmyslové plasty: teorie a aplikace (6. vydání). Cengage Learning.
- ^ Williams, R. Scott. „Péče o plasty: maligní plasty“. Newsletter WAAC. 24 (1). Zachování OnLine. Citováno 29. května 2017.
- ^ Mrazící návnady Archivováno 25. ledna 2010 v Wayback Machine, nutrabaits.net
- ^ Kasumyan A, Døving K (2003). "Chuťové preference u ryb". Ryby a rybolov. 4 (4): 289–347. doi:10.1046 / j.1467-2979.2003.00121.x.
- ^ Japonští velrybáři zraněni aktivisty spalujícími kyseliny Archivováno 8. června 2010 v Wayback Machine, newser.com, 10. února 2010
- ^ A b C d "Kyselina máselná". Průvodce farmakologií IUPHAR / BPS. Mezinárodní unie základní a klinické farmakologie. Citováno 13. července 2018.
- ^ A b „Kyselina butanová a butyrát sodný“. BindingDB. Vazební databáze. Citováno 27. října 2020.
- ^ A b C Kasubuchi M, Hasegawa S, Hiramatsu T, Ichimura A, Kimura I (2015). „Dietní střevní mikrobiální metabolity, mastné kyseliny s krátkým řetězcem a metabolická regulace hostitele“. Živiny. 7 (4): 2839–49. doi:10,3390 / nu7042839. PMC 4425176. PMID 25875123.
Mastné kyseliny s krátkým řetězcem (SCFA), jako je acetát, butyrát a propionát, které se produkují střevní mikrobiální fermentací vlákniny, jsou považovány za základní zdroje energie hostitele a působí jako molekuly signální transdukce prostřednictvím receptorů spojených s G-proteinem (FFAR2, FFAR3, OLFR78, GPR109A) a jako epigenetické regulátory genové exprese inhibicí histon-deacetylázy (HDAC). Nedávné důkazy naznačují, že dietní vláknina a střevní mikrobiální deriváty SCFA mají mnoho příznivých účinků na energetický metabolismus hostitele nejen zlepšením střevního prostředí, ale také přímým ovlivněním různých periferních tkání hostitele.
- ^ A b C d E Hoeppli RE, Wu D, Cook L, Levings MK (únor 2015). „Prostředí regulační biologie T buněk: cytokiny, metabolity a mikrobiom“. Přední Immunol. 6: 61. doi:10.3389 / fimmu.2015.00061. PMC 4332351. PMID 25741338.
Obrázek 1: Molekuly odvozené od mikrobů podporují diferenciaci Treg tlustého střeva. - ^ A b C d E F G Bourassa MW, Alim I, Bultman SJ, Ratan RR (červen 2016). „Butyrát, neuroepigenetika a střevní mikrobiom: Může strava s vysokým obsahem vlákniny zlepšit zdraví mozku?“. Neurosci. Lett. 625: 56–63. doi:10.1016 / j.neulet.2016.02.009. PMC 4903954. PMID 26868600.
- ^ Tsuji A (2005). „Malomolekulární přenos léčiv přes hematoencefalickou bariéru prostřednictvím transportních systémů zprostředkovaných nosičem“. NeuroRx. 2 (1): 54–62. doi:10.1602 / neurorx.2.1.54. PMC 539320. PMID 15717057.
Další studie in vivo v našich laboratořích ukázaly, že několik sloučenin včetně acetátu, propionátu, butyrátu, kyseliny benzoové, kyseliny salicylové, kyseliny nikotinové a některých β-laktamových antibiotik může být transportováno MCT na BBB.21 ... Příjem kyseliny valproové byl snížen v přítomnosti mastných kyselin se středním řetězcem, jako jsou hexanoát, oktanoát a dekanoát, ale ne propionát nebo butyrát, což naznačuje, že kyselina valproová je přijímána do mozku transportním systémem pro médium- mastné kyseliny s řetězcem, nikoli mastné kyseliny s krátkým řetězcem.
- ^ A b Vijay N, Morris ME (2014). „Role monokarboxylátových transportérů při dodávání léčiv do mozku“. Curr. Pharm. Des. 20 (10): 1487–98. doi:10.2174/13816128113199990462. PMC 4084603. PMID 23789956.
Je známo, že monokarboxylátové transportéry (MCT) zprostředkovávají transport monokarboxylátů s krátkým řetězcem, jako je laktát, pyruvát a butyrát. ... MCT1 a MCT4 byly také spojeny s transportem mastných kyselin s krátkým řetězcem, jako je acetát a mravenčan, které jsou poté metabolizovány v astrocytech [78]. ... SLC5A8 je exprimován v normální tkáni tlustého střeva a funguje jako tumor supresor v lidském tlustém střevě, přičemž k umlčení tohoto genu dochází u karcinomu tlustého střeva. Tento transportér se podílí na koncentračním vychytávání butyrátu a pyruvátu produkovaného jako produkt fermentace bakteriemi tlustého střeva.
- ^ A b "Kyselina máselná". Lidská databáze metabolomu. University of Alberta. Citováno 15. srpna 2015.
- ^ „Butanoátový metabolismus - referenční cesta“. Kyoto Encyclopedia of Genes and Genomes. Laboratoře Kanehisa. 1. listopadu 2017. Citováno 1. února 2018.
- ^ Donohoe, Dallas R .; Garge, Nikhil; Zhang, Xinxin; Slunce, Wei; O’Connell, Thomas M .; Bunger, Maureen K .; Bultman, Scott J. (4. května 2011). „Mikrobiom a butyrát regulují energetický metabolismus a autofagii v savčím tlustém střevě“. Buněčný metabolismus. 13 (5): 517–526. doi:10.1016 / j.cmet.2011.02.018. ISSN 1550-4131. PMC 3099420. PMID 21531334.
- ^ „triacylglycerol lipáza - Homo sapiens“. BRENDA. Technische Universität Braunschweig. Citováno 25. května 2015.
- ^ Tilg H, Moschen AR (září 2014). „Mikrobiota a cukrovka: vyvíjející se vztah“. Střevo. 63 (9): 1513–1521. doi:10.1136 / gutjnl-2014-306928. PMID 24833634. S2CID 22633025.
- ^ Cait, Alissa; Cardenas, Erick (prosinec 2019). „Snížený genetický potenciál pro fermentaci butyrátu ve střevním mikrobiomu kojenců, u kterých se rozvine alergická senzibilizace“. Journal of Allergy and Clinical Immunology. 144 (6): 1638-1647. E3. doi:10.1016 / j.jaci.2019.06.029. PMID 31279007.
- ^ Vatanen, T .; Franzosa, E.A.; Schwager, R .; et al. (2018). „Lidský střevní mikrobiom u pacientů s časným nástupem diabetu 1. typu ze studie TEDDY“. Příroda. 562 (7728): 589–594. Bibcode:2018Natur.562..589V. doi:10.1038 / s41586-018-0620-2. PMC 6296767. PMID 30356183.
- ^ Consolandi, Clarissa; Turroni, Silvia; Emmi, Giacomo; et al. (Duben 2015). „Pacienti s Behcetovým syndromem vykazují specifický mikrobiomový podpis“. Recenze autoimunity. 14 (4): 269–276. doi:10.1016 / j.autrev.2014.11.009. PMID 25435420.
- ^ Ye, Zi; Zhang, Ni; Wu, Chunyan; et al. (4. srpna 2018). „Metagenomická studie střevního mikrobiomu u Behcetovy choroby“. Mikrobiom. 6 (1): 135. doi:10.1186 / s40168-018-0520-6. PMC 6091101. PMID 30077182.
- ^ Cait, Alissa; Hughes, Michael R (květen 2018). „Alergický zánět plic vyvolaný mikrobiomy je zmírněn mastnými kyselinami s krátkým řetězcem“. Slizniční imunologie. 11 (3): 785–796. doi:10.1038 / mi.2017.75.
- ^ Furusawa, Yukihiro; Obata, Yuuki; Fukuda, Shinji; et al. (13. listopadu 2013). „Komensální butyrát odvozený od mikrobů indukuje diferenciaci regulačních T buněk tlustého střeva“. Příroda. 504 (7480): 446–450. Bibcode:2013Natur.504..446F. doi:10.1038 / příroda12721. PMID 24226770. S2CID 4408815.
- ^ Arpaia, Nicholas; Campbell, Clarissa; Ventilátor, Xiying; et al. (13. listopadu 2013). „Metabolity produkované komenzálními bakteriemi podporují tvorbu periferních regulačních T-buněk“. Příroda. 504 (7480): 451–455. Bibcode:2013Natur.504..451A. doi:10.1038 / příroda12726. PMC 3869884. PMID 24226773.
- ^ Luu, Maik; Weigand, Katharina; Wedi, Fatana; et al. (26. září 2018). "Regulace efektorové funkce CD8 + T buněk pomocí metabolitu butyrátu ze střevní mikroflóry". Vědecké zprávy. 8 (1): 14430. Bibcode:2018NatSR ... 814430L. doi:10.1038 / s41598-018-32860-x. PMC 6158259. PMID 30258117.
- ^ Cholan, Pradeep Manuneedhi; Han, Alvin; Woodie, Brad R .; Watchon, Maxinne; Kurz, Angela RM; Laird, Angela S .; Britton, Warwick J .; Ye, Lihua; Holmes, Zachary C .; McCann, Jessica R .; David, Lawrence A. (9. listopadu 2020). "Zachované protizánětlivé účinky a snímání butyrátu u zebrafish". Střevní mikroby. 12 (1): 1–11. doi:10.1080/19490976.2020.1824563. ISSN 1949-0976. PMC 7575005. PMID 33064972.
- ^ A b C d Wang G (2014). „Lidské antimikrobiální peptidy a proteiny“. Farmaceutika (Basilej). 7 (5): 545–94. doi:10,3390 / ph7050545. PMC 4035769. PMID 24828484.
Tabulka 3: Výběr lidských antimikrobiálních peptidů a jejich navrhovaných cílů
Tabulka 4: Některé známé faktory, které indukují expresi antimikrobiálních peptidů - ^ Yonezawa H, Osaki T, Hanawa T, Kurata S, Zaman C, Woo TD, Takahashi M, Matsubara S, Kawakami H, Ochiai K, Kamiya S (2012). "Destruktivní účinky butyrátu na buněčný obal Helicobacter pylori". J. Med. Microbiol. 61 (Pt 4): 582–9. doi:10.1099 / jmm.0.039040-0. PMID 22194341.
- ^ McGee DJ, George AE, Trainor EA, Horton KE, Hildebrandt E, Testerman TL (2011). „Cholesterol zvyšuje odolnost Helicobacter pylori vůči antibiotikům a LL-37“. Antimicrob. Agenti Chemother. 55 (6): 2897–904. doi:10.1128 / AAC.00016-11. PMC 3101455. PMID 21464244.
- ^ Zimmerman MA, Singh N, Martin PM, Thangaraju M, Ganapathy V, Waller JL, Shi H, Robertson KD, Munn DH, Liu K (2012). „Butyrát potlačuje zánět tlustého střeva prostřednictvím upregulace Fas závislé na HDAC1 a apoptózy T buněk zprostředkované Fas“. Dopoledne. J. Physiol. Gastrointest. Játra Physiol. 302 (12): G1405–15. doi:10.1152 / ajpgi.00543.2011. PMC 3378095. PMID 22517765.
- ^ Offermanns S, Schwaninger M (2015). „Nutriční nebo farmakologická aktivace HCA (2) zlepšuje neurozánět“. Trends Mol Med. 21 (4): 245–255. doi:10.1016 / j.molmed.2015.02.002. PMID 25766751.
- ^ Chai JT, Digby JE, Choudhury RP (květen 2013). „GPR109A a vaskulární zánět“. Curr Atheroscler Rep. 15 (5): 325. doi:10.1007 / s11883-013-0325-9. PMC 3631117. PMID 23526298.
- ^ Graff EC, Fang H, Wanders D, Judd RL (únor 2016). „Protizánětlivé účinky receptoru hydroxykarboxylové kyseliny 2“. Metab. Clin. Exp. 65 (2): 102–113. doi:10.1016 / j.metabol.2015.10.001. PMID 26773933.
- ^ Farzi A, Reichmann F, Holzer P (2015). „Homeostatická role neuropeptidu Y v imunitní funkci a její dopad na náladu a chování“. Acta Physiol (Oxf). 213 (3): 603–27. doi:10.1111 / apha.12445. PMC 4353849. PMID 25545642.
- ^ Zeng, Huawei; Lazarova, DL; Bordonaro, M (2014). „Mechanismy spojující dietní vlákninu, střevní mikroflóru a prevenci rakoviny tlustého střeva“. World Journal of Gastrointestinal Oncology. 6 (2): 41–51. doi:10.4251 / wjgo.v6.i2.41. PMC 3926973. PMID 24567795.
- ^ Chen, Jiezhong; Zhao, Kong-Nan; Vitetta, Luis (2019). "Účinky intestinálního mikrobiálně propracovaného butyrátu na cesty onkogenní signalizace" (pdf). Živiny. 11 (5): 1026. doi:10,3390 / nu11051026. PMC 6566851. PMID 31067776. S2CID 148568580.
- ^ Klampfer L, Huang J, Sasazuki T, Shirasawa S, Augenlicht L (srpen 2004). „Onkogenní Ras podporuje butyrátem indukovanou apoptózu prostřednictvím inhibice exprese gelsolinu“. The Journal of Biological Chemistry. 279 (35): 36680–8. doi:10,1074 / jbc.M405197200. PMID 15213223.
- ^ Vanhoutvin SA, Troost FJ, Hamer HM, Lindsey PJ, Koek GH, Jonkers DM, Kodde A, Venema K, Brummer RJ (2009). Bereswill S (ed.). „Transkripční změny vyvolané butyrátem v lidské sliznici tlustého střeva“. PLOS ONE. 4 (8): e6759. Bibcode:2009PLoSO ... 4,6759V. doi:10,1371 / journal.pone.0006759. PMC 2727000. PMID 19707587.
- ^ Encarnação, J. C .; Abrantes, A. M .; Pires, A. S .; et al. (30. července 2015). „Znovu se podívejte na vlákninu týkající se rakoviny tlustého střeva a konečníku: butyrát a jeho role v prevenci a léčbě“. Recenze rakoviny a metastáz. 34 (3): 465–478. doi:10.1007 / s10555-015-9578-9. PMID 26224132. S2CID 18573671.
- ^ Zimmerman, Mary A .; Singh, Nagendra; Martin, Pamela M .; et al. (15. června 2012). „Butyrát potlačuje zánět tlustého střeva prostřednictvím upregulace Fas závislé na HDAC1 a apoptózy T buněk zprostředkované Fas“. American Journal of Physiology. Fyziologie gastrointestinálního traktu a jater. 302 (12): G1405 – G1415. doi:10.1152 / ajpgi.00543.2011. PMC 3378095. PMID 22517765.
- ^ Prasanna Kumar, S .; Thippeswamy, G .; Sheela, M.L .; et al. (Říjen 2008). „Butyrátem indukovaná fosfatáza reguluje VEGF a angiogenezi prostřednictvím Sp1“. Archivy biochemie a biofyziky. 478 (1): 85–95. doi:10.1016 / j.abb.2008.07.004. PMID 18655767.
- ^ „Nízkosacharidová strava snižuje riziko rakoviny tlustého střeva, uvádí studie | Mediální místnost University of Toronto. media.utoronto.ca. Citováno 4. května 2016.
- ^ Belcheva, Antoaneta; Irrazabal, Thergiory; Robertson, Susan J .; Streutker, Catherine; Maughan, Heather; Rubino, Stephen; Moriyama, Eduardo H .; Copeland, Julia K .; Kumar, Sachin (17. července 2014). „Střevní mikrobiální metabolismus řídí transformaci buněk epitelu tlustého střeva s nedostatkem MSH2“. Buňka. 158 (2): 288–299. doi:10.1016 / j.cell.2014.04.051. ISSN 1097-4172. PMID 25036629.
- ^ Scheppach, W .; Sommer, H.; Kirchner, T.; et al. (1992). "Effect of butyrate enemas on the colonic mucosa in distal ulcerative colitis". Gastroenterologie. 103 (1): 51–56. doi:10.1016/0016-5085(92)91094-K. PMID 1612357.
- ^ Robison AJ, Nestler EJ (November 2011). „Transkripční a epigenetické mechanismy závislosti“. Nat. Rev. Neurosci. 12 (11): 623–637. doi:10.1038 / nrn3111. PMC 3272277. PMID 21989194.
- ^ Nestler EJ (January 2014). "Epigenetic mechanisms of drug addiction". Neuropharmacology. 76 Pt B: 259–268. doi:10.1016/j.neuropharm.2013.04.004. PMC 3766384. PMID 23643695.
- ^ A b Walker DM, Cates HM, Heller EA, Nestler EJ (February 2015). "Regulation of chromatin states by drugs of abuse". Curr. Opin. Neurobiol. 30: 112–121. doi:10.1016/j.conb.2014.11.002. PMC 4293340. PMID 25486626.
- ^ Ajonijebu DC, Abboussi O, Russell VA, Mabandla MV, Daniels WM (August 2017). "Epigenetics: a link between addiction and social environment". Cellular and Molecular Life Sciences. 74 (15): 2735–2747. doi:10.1007/s00018-017-2493-1. PMID 28255755. S2CID 40791780.
- ^ Legastelois R, Jeanblanc J, Vilpoux C, Bourguet E, Naassila M (2017). "[Epigenetic mechanisms and alcohol use disorders: a potential therapeutic target]". Biologie Aujourd'hui (francouzsky). 211 (1): 83–91. doi:10.1051/jbio/2017014. PMID 28682229.


