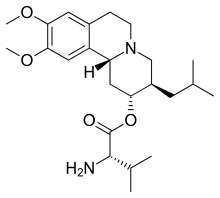
Valbenazin - Valbenazine
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Ingrezza |
| Ostatní jména | NBI-98854 |
| AHFS /Drugs.com | ingrezza |
| Trasy z správa | Pusou |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Vazba na bílkoviny | >99% |
| Metabolismus | Aktivace do hydrolýza, deaktivace pomocí CYP3A, CYP2D6 |
| Metabolity | [+] - α-Dihydrotetrabenazin (aktivní metabolit) |
| Odstranění poločas rozpadu | 15–22 hodin |
| Vylučování | 60% moči, 30% stolice |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| Informační karta ECHA | 100.236.234 |
| Chemické a fyzikální údaje | |
| Vzorec | C24H38N2Ó4 |
| Molární hmotnost | 418.578 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
Valbenazin, prodávané pod obchodním názvem Ingrezza, je lék používaný k léčbě tardivní dyskineze.[1] Působí jako vezikulární monoaminový transportér 2 (VMAT2) inhibitor.[2]
Lékařské použití
Valbenazin se používá k léčbě tardivní dyskineze u dospělých.[1] Tardivní dyskineze je neurologická porucha charakterizovaná mimovolními pohyby.[3] Klinické studie, které vedly k FDA schválení valbenazinu trvalo 6 týdnů.[1] Studie sponzorovaná průmyslovým odvětvím studovala užívání valbenzazinu po dobu až 48 týdnů, přičemž bylo shledáno, že je bezpečné a účinné pro udržení krátkodobého (6týdenního) zlepšení tardivní dyskineze.[4]
Kontraindikace
Podle informací o předepisování neexistují žádné kontraindikace pro použití valbenazinu.[1]
Valbenazin nebyl v těhotenství účinně studován a doporučuje se, aby se těhotné nebo kojící ženy užívání valbenazinu vyvarovaly.[5]
Nepříznivé účinky
Vedlejší účinky mohou zahrnovat ospalost nebo Prodloužení QT.[5] Při doporučených dávkách nebylo dosud pozorováno významné prodloužení, avšak u těch, kteří užívají inhibitory jaterních enzymů CYP2D6 nebo CYP3A4 - nebo kteří jsou slabí metabolizátoři CYP2D6 - mohou být vystaveni riziku významného prodloužení.[5]
Farmakologie
Mechanismus účinku
Je známo, že valbenazin způsobuje reverzibilní snížení dopamin uvolňování selektivní inhibicí presynaptického lidského vezikulárního monoaminového transportéru typu 2 (VMAT2). In vitro vykazuje valbenazin velkou selektivitu pro VMAT2 a malou až žádnou afinitu k VMAT1 nebo jiné monoaminové receptory.[6] Ačkoli přesná příčina tardivní dyskineze není známa, předpokládá se, že z ní může vyplývat neuroleptikum -indukovaná přecitlivělost na dopamin.[7] Selektivním snížením schopnosti VMAT2 načíst dopamin do synaptických vezikul,[8] lék snižuje celkovou hladinu dostupného dopaminu v synaptické štěrbině, v ideálním případě zmírňuje příznaky spojené s přecitlivělostí na dopamin. Význam valbenazinové selektivity inhibující VMAT2 oproti jiným monoaminovým transportérům spočívá v tom, že VMAT2 se podílí hlavně na transportu dopaminu a v mnohem menší míře i jiných monoaminů, jako je norepinefrin, serotonin, a histamin. Tato selektivita pravděpodobně sníží pravděpodobnost „off-target“ nepříznivých účinků, které mohou vyplynout z upstream inhibice těchto dalších monoaminů.[9]
Farmakokinetika
Valbenazin je a proléčivo což je ester z [+] - α-dihydrotetrabenazin (DTBZ) s aminokyselinou L-valin. Je to značně hydrolyzovaný do aktivní metabolit DTBZ. Vazba na plazmatické proteiny valbenazinu je více než 99% a DTBZ asi 64%. The biologický poločas valbenazinu a DTBZ je 15 až 22 hodin. Jaterní enzymy podílející se na inaktivaci jsou CYP3A4, CYP3A5 a CYP2D6. Lék se vylučuje, většinou ve formě neaktivních metabolitů, močí (60%) a výkaly (30%).[10]
Společnost a kultura
Obchodní aspekty
Valbenazin vyrábí společnost Neurokrinní biologické vědy, společnost se sídlem v San Diegu. Valbenazin byl prvním lékem schváleným FDA pro léčbu tardivní dyskineze dne 11. dubna 2017.[11]
Duševní vlastnictví
I když Neurocrine Biosciences v současné době nemá konečný patent na valbenazin nebo elagolix, vlastní patent na inhibitor VMAT2 [9,10-dimethoxy-3- (2-methylpropyl) -1H,2H,3H,4H,6H,7H, 11bH-pyrido- [2,1-a] isochinolin-2-yl] methanol a příbuzné sloučeniny, které zahrnují valbenazin.[12]
Jména
The Mezinárodní nechráněný název (INN) je valbenazin.[13]:114
Výzkum
Valbenazin se zkoumá k léčbě Tourettův syndrom.[14][15]
Reference
- ^ A b C d „Štítek valbenazinu“ (PDF). FDA. Dubna 2017. Citováno 16. července 2017. Aktualizace štítků viz Indexová stránka FDA pro NDA 209241
- ^ O'Brien CF, Jimenez R, Hauser RA, Factor SA, Burke J, Mandri D, Castro-Gayol JC (říjen 2015). „NBI-98854, selektivní inhibitor transportu monoaminů pro léčbu tardivní dyskineze: randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie“. Poruchy pohybu. 30 (12): 1681–7. doi:10,1002 / mds.26330. PMC 5049616. PMID 26346941.
- ^ "Tardivní dyskineze". rarediseases.info.nih.gov. 1. června 2017. Archivováno z původního dne 18. června 2017. Citováno 21. února 2018.
- ^ Janeczko L. „Dlouhodobý valbenazin se zdá bezpečný pro pacienty s tardivní dyskinezí“. www.medscape.com. Informace o zdraví agentury Reuters. Citováno 21. února 2018.
- ^ A b C „Valbenazine: Drug Information“. www.uptodate.com. Citováno 2017-07-14.
- ^ "NBI-98854 - Inhibitor VMAT2 | Tiky v léčbě dětí | Neurokrinní biologické vědy". www.neurocrine.com. Archivovány od originál dne 2015-01-30. Citováno 2016-11-13.
- ^ "tardivní dyskineze". www.priory.com. Citováno 2016-11-13.
- ^ Purves D a kol. (2018). Neurovědy (Šesté vydání). Sinauer Associates. ISBN 978-1-60535-380-7.
- ^ „NBIX: NDA pro valbenazin v Tardive Dyskinesia bude přihlášen v roce 2016…“. Citováno 2016-11-13.
- ^ Valbenazin Profesionální drogová fakta.
- ^ Úřad komisaře. „Tisková oznámení - FDA schvaluje první lék na léčbu tardivní dyskineze“. www.fda.gov. Citováno 12. dubna 2017.
- ^ USA 20160289226, Ashweek N, Harriott N, "[9,10-dimethoxy-3- (2-methylpropyl) -lh, 2h, 3h, 4h, 6h, 7h, 11bh-pyrido- [2,1-a] isochinolin-2- yl] methanol a sloučeniny, kompozice a metody k nim vztahující se “, publikované 6. října 2016, přidělené společnosti Neurocrine Biosciences, Inc.
- ^ „Mezinárodní nechráněné názvy farmaceutických látek (INN). Doporučené mezinárodní nechráněné názvy: seznam 71“ (PDF). Světová zdravotnická organizace. Citováno 18. listopadu 2016.
- ^ „Klinické studie s Tourettovým syndromem“. Neurokrinní biologické vědy. Citováno 2016-11-13.
- ^ Číslo klinického hodnocení NCT02581865 pro "Studii bezpečnosti a účinnosti NBI-98854 u dospělých s Tourettovým syndromem" na ClinicalTrials.gov
