Plicní uzlík - Lung nodule
| Plicní uzlík | |
|---|---|
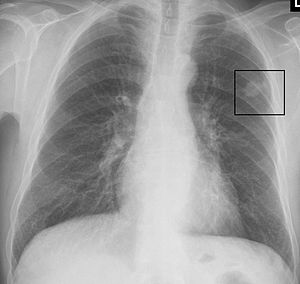 | |
| Rentgen hrudníku zobrazeno a solitární plicní uzlík (označeno černou krabičkou) v levém horním laloku. | |
| Specialita | Pulmonologie |
A plicní uzlík nebo plicní uzlík je relativně malá ohnisková hustota v plíce. A solitární plicní uzlík (SPN) nebo léze na mince,[1] je Hmotnost v plíce menší než 3 centimetry v průměru. Může existovat také více uzlů.
Jeden nebo více plicních uzlů může být náhodné zjištění nalezeno až 0,2% z rentgenové záření hrudníku[2] a kolem 1% z CT.[3]
The uzlík nejčastěji představuje a benigní nádor, jako je a granulom nebo hamartoma, ale v přibližně 20% případů představuje a zhoubný rakovina,[3] speciálně v starší dospělí a kuřáci. Naopak 10 až 20% pacientů s rakovina plic jsou diagnostikováni tímto způsobem.[3] Pokud má pacient v anamnéze kouření nebo uzlina roste, bude možná nutné vyloučit možnost rakoviny prostřednictvím dalších radiologických studií a intervencí, případně včetně chirurgická resekce. The prognóza závisí na základním stavu.
Příčiny
Ne každá kulatá skvrna na rentgenologickém snímku je solitární plicní uzlík: může být zaměňována s projekcí struktury hrudní stěna nebo kůže, například a bradavka uzdravení zlomenina žeber nebo elektrokardiografické monitorování.
Nejdůležitějším důvodem k vyloučení je jakákoli forma rakovina plic,[4] včetně vzácných forem, jako je primární plicní lymfom, karcinoidní nádor a osamělý metastáza do plic (běžná nerozpoznaná místa primárního nádoru jsou melanomy, sarkomy nebo rakovina varlat ). Mezi benigní nádory v plicích patří hamartomy a chondromy.
Nejběžnější benigní lézí mincí je a granulom (zánětlivé uzlík ), například kvůli tuberkulóza nebo a plísňové infekce, jako Kokcidioidomykóza.[5] Mezi další infekční příčiny patří a plicní absces, zápal plic (počítaje v to pneumocystis pneumonia ) nebo zřídka nocardial infekce nebo infekce červy (např dirofilariáza nebo psí dirofilárium zamoření). Plicní uzliny se mohou také objevit v poruchy imunity, jako revmatoidní artritida nebo granulomatóza s polyangiitidou nebo organizující se zápal plic.
Osamělý plicní uzlík lze považovat za arteriovenózní malformace, a hematom nebo infarkt zóna. Může to být také způsobeno bronchiální atrézie, sekvestrace, vdechnutý cizí těleso nebo pleurální deska.
Rizikové faktory
Rizikové faktory pro náhodně objevené uzliny jsou hlavně:
- Obecné rizikové faktory rakoviny plic jako je expozice kouření tabáku nebo jiný karcinogeny jako azbest a dříve diagnostikovaná rakovina, respirační infekce nebo chronická obstrukční plicní nemoc.[6]
- Velikost: větší velikost přináší vyšší riziko rakoviny[7]

- Umístění: Poloha horního laloku je rizikovým faktorem pro vznik rakoviny, zatímco poloha poblíž a trhlina nebo pohrudnice označuje benigní lymfatické uzliny,[7] zvláště pokud má trojúhelníkový tvar.[8]
- Okraj morfologie: a pikantní marže je rizikovým faktorem pro rakovinu.[7] Benigní příčiny mají tendenci mít dobře definovanou hranici, zatímco lobulované léze nebo ty s nepravidelným okrajem zasahujícím do sousední tkáně bývají maligní.[9] Zejména spikulace vysoce predikují malignitu s pozitivní prediktivní hodnotou až 90%.[8] „Znak zářezu“, který je náhlým odsazením uzliny, také zvyšuje riziko rakoviny, ale může se vyskytovat také u granulomatózních onemocnění.[8]

Kulatý dobře ohraničený pevný plicní uzlík s hladkým okrajem.[8]

Lobulovaný uzlík.[8]

Špičatý plicní uzlík.[8]

„Značka zářezu“.[8]

Trojúhelníková perifissurální uzlina může být diagnostikována jako benigní lymfatická uzlina.[8]
- Násobnost: Kde bylo zjištěno, že přítomnost až dalších 3 uzlů zvyšuje riziko rakoviny, ale klesá v případě 4 nebo více dalších, pravděpodobně proto, že naznačuje spíše předchozí granulomatózní infekci než rakovinu.[7]
- Růst míra: solidní rakoviny se obecně zdvojnásobí v objemu během 100 až 400 dnů, zatímco subsolidní rakoviny (obecně představující adenokarcinomy) se obvykle zdvojnásobí v objemu během 3 až 5 let.[7] Jedno zdvojnásobení objemu se rovná přibližně 26% zvýšení průměru.[7]
- Přítomnost emfyzém a / nebo fibróza je rizikovým faktorem pro rakovinu.[7] Pro srovnání je typické zdvojnásobení velikosti méně než 20 dní u infekcí a více než 400 dní u benigních uzlin.[10]
- Zvýšení: Pokud je zkouška provedena jako kombinovaná nekontrastní a kontrast CT osamělý uzlík s vypnutým vylepšením méně než 15 Hounsfieldovy jednotky (HU), zatímco vyšší zesílení indikuje maligní nádor (s a citlivost odhaduje na 98%).[11]
- Oblasti tuková tkáň (−40 až −120 HU) označuje a hamartoma. Pouze asi 50% hamartomů však obsahuje tuky.[8]
- Pokud existuje centrální dutina, pak tenká stěna ukazuje na benigní příčinu, zatímco silná stěna je spojena s malignitou (zejména 4 mm nebo méně oproti 16 mm nebo více).[9]

Nízký útlumový uzlík (v tomto případě tuk obsahující hamartom).[8]
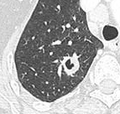
V tomto případě kavitace s relativně silnou zdí aspergilloma ).[8]

- V případě kalcifikace, vzhled podobný popcornu naznačuje hamartom, který je benigní.[2]
- V případě polopevný uzlíky, být částečně pevný má vyšší riziko rakoviny než být čistě neprůhlednost broušeného skla.
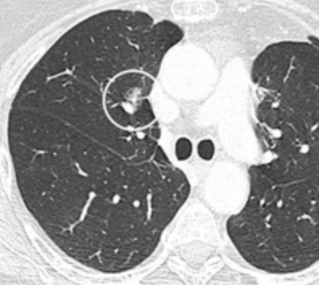
Část pevného uzlu.[8]

Opacita broušeného skla uzlík.[8]
- Pleurální zatažení je mnohem častější u rakoviny.[8] Jedná se o tah viscerální pleury směrem k uzlu.[8]
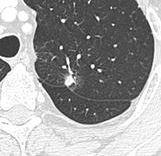
Uzlík s pleurální retrakcí.[8]
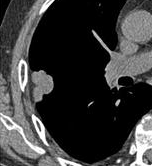
V tomto případě je pleurální retrakce považována za trojúhelníkovou tukovou složku.[8]

- Plicní uzlík přiléhající a plicní cysta je vzácný nález, přesto naznačuje rakovinu.[8]
- Bublinkové lucencie v uzlu naznačují rakovinu:[8]

- Cévní konvergence je místo, kde se cévy sbíhají do uzlíku, aniž by přiléhaly nebo se dotýkaly okraje uzlíku, a je vidět hlavně u periferních subsolidních karcinomů plic.[8] Odráží to angiogeneze.[8]
Vzduchové bronchogramy je definován jako vzor průdušek naplněných vzduchem na pozadí bezvzduchových plic a může být viděn jak u benigních, tak u maligních uzlin, ale některé jejich vzorce mohou pomoci při stratifikaci rizika.[8]
CT denzitometrie, měření absolutního útlumu na Hounsfieldova stupnice, má nízkou citlivost a specificitu a není běžně využíván, kromě toho, že pomáhá rozlišovat léze pevných částic od broušeného skla a potvrzovat viditelné mastné oblasti nebo kalcifikace.[11]
Diagnóza
A diagnostické zpracování může zahrnovat řadu skenů a biopsií.
Definice
Nodulární hustota se používá k rozlišení větších nádorů plic, menších infiltrátů nebo hmot s jinými doprovodnými vlastnostmi. Často používaná formální radiologická definice je následující: jediná léze v plicích zcela obklopená funkční plicní tkáň s průměrem menším než 3 cm a bez přidružených zápal plic, atelektáza (kolaps plic) nebo lymfadenopatie (zduření lymfatických uzlin).[12][9]
CT vyšetření
U náhodně detekovaných uzlin na CT Fleischnerova společnost pokyny jsou uvedeny v tabulce níže. U více uzlů je správa založena na nejvíce podezřelém uzlu.[7] Tyto pokyny neplatí při screeningu rakoviny plic, u pacientů s imunosupresí ani u pacientů se známou primární rakovinou.[7]
| <6 mm (<100 mm3) | 6-8 mm (100-250 mm3) | > 8 mm (> 250 mm3) | ||
|---|---|---|---|---|
| Singl uzlík | Nízké riziko | Žádné rutinní sledování | CT po 6–12 měsících, poté zvažte CT po 18–24 měsících | Zvažte CT po 3 měsících, PET-CT nebo biopsie |
| Vysoké riziko | Volitelně CT po 12 měsících | CT po 6–12 měsících, poté po 18–24 měsících | ||
| Násobek uzlíky | Nízké riziko | Žádné rutinní sledování | CT po 3–6 měsících, poté zvažte CT po 18–24 měsících | |
| Vysoké riziko | Volitelně CT po 12 měsících | CT po 3–6 měsících, poté po 18–24 měsících | ||
| Celková velikost <6 mm (<100 mm3) | Celková velikost> 6 mm (> 1003) | ||
|---|---|---|---|
| Singl uzlík | Opacita broušeného skla | Žádné rutinní sledování | CT po 6–12 měsících, aby se zjistilo, zda přetrvává, poté po 2 letech a poté další 2 roky |
| Část pevná | Žádné rutinní sledování | CT po 6–12 měsících:
| |
| Násobek uzlíky | CT po 3–6 měsících. Pokud je stabilní, zvažte CT po 2 a poté dalších 2 letech. | CT po 3–6 měsících, poté po 18–24 měsících | |
Ukázalo se, že častější CT vyšetření než to, co se doporučuje, nezlepšuje výsledky, ale zvýší radiační zátěž a zbytečná zdravotní péče lze očekávat, že u pacienta vyvolá úzkost a nejistotu.[13]
PET skenování

Pokud existuje střední riziko malignity, pokračujte v zobrazování pomocí pozitronová emisní tomografie (PET sken) je vhodný (je-li k dispozici). Lze to provést současně jako CT sken ve formě PET-CT. Asi 95% pacientů s maligním uzlem bude mít abnormální PET sken, zatímco přibližně 78% pacientů s benigním uzlem bude vypadat normálně na PET (toto je test citlivost a specifičnost ).[14] Abnormální PET sken tedy spolehlivě zachytí rakovinu, ale na PET skenu se také objeví několik dalších typů uzlíků (například zánětlivých nebo infekčních). Pokud má uzlík průměr menší než jeden centimetr, PET skenům se často vyhýbá kvůli zvýšenému riziku falešně normální Výsledek.[14][15][16] Rakovinné léze mají obvykle vysokou hladinu metabolismus na PET, což dokazuje jejich vysoká absorpce FDG (radioaktivní cukr).
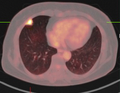
PET-CT a tuberkulóza.
Jiné zobrazování
Další potenciální formy lékařské zobrazování plicních uzlin zahrnují magnetická rezonance (MRI) nebo počítačová tomografie s emisemi jednoho fotonu (SPECT).[17]
Histopatologie
Pro dostatečně podezřelé případy biopsie, malé biopsie lze získat pomocí jehla jádra nebo bronchoskopie se běžně používají k diagnostice plicních uzlin.[18] Vedeno CT perkutánní transtorakální biopsie jehlou se také ukázaly jako velmi užitečné při diagnostice SPN.[5]
Ve vybraných případech lze uzliny také odebrat pomocí dýchacích cest pomocí bronchoskopie nebo přes hrudní stěnu pomocí aspirace tenkou jehlou (což lze provést pod vedením CT). Aspirace jehlou může načíst pouze skupiny buněk cytologie a ne tkáňový válec nebo biopsie, což vylučuje hodnocení tkáňové architektury. Teoreticky to ztěžuje diagnostiku benigních stavů, i když byly hlášeny míry vyšší než 90%.[19] Komplikace druhé techniky zahrnují krvácení do plic a únik vzduchu v pleurálním prostoru mezi plícemi a hrudní stěnou (pneumotorax ). Ne všechny tyto případy pneumotoraxu však vyžadují léčbu a hrudní trubice.[20]
Vyříznutí
Pokud zpracování naznačuje vysoké riziko rakoviny, lze provést excizi torakotomie nebo torakoskopická chirurgie s podporou videa, který může také potvrdit diagnózu pomocí mikroskopické vyšetření.
Poznámky pod čarou
- ^ "Léze mincí (plic)".
- ^ A b Ost D, Fein AM, Feinsilver SH; Fein; Feinsilver (červen 2003). "Klinická praxe. Osamělý plicní uzlík". N. Engl. J. Med. 348 (25): 2535–42. doi:10.1056 / NEJMcp012290. PMID 12815140.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ A b C Alzahouri K, Velten M, Arveux P, Woronoff-Lemsi MC, Jolly D, Guillemin F; Velten; Arveux; Woronoff-Lemsi; Rozjařený; Guillemin (2008). „Řízení SPN ve Francii. Cesty k definitivní diagnostice solitárního plicního uzlíku: multicentrická studie v 18 francouzských okresech“. Rakovina BMC. 8: 93. doi:10.1186/1471-2407-8-93. PMC 2373300. PMID 18402653.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Thiessen, N.R .; Bremner, R. (2010). „Osamělý plicní uzlík: přístup pro všeobecného chirurga“. Chirurgické kliniky Severní Ameriky. 90 (5): 1003–18. doi:10.1016 / j.suc.2010.07.002. PMID 20955880.
- ^ A b Jude, Cecilia M .; Nayak, Nita B .; Patel, Maitraya K .; Deshmukh, Monica; Batra, Poonam (2014). „Plicní kokcidioidomykóza: obrazový přehled rentgenových nálezů na hrudi a CT nálezů“. RadioGrafika. 34 (4): 912–925. doi:10,1148 / rg.344130134. PMID 25019431.
- ^ Zhan, Ping; Xie, Haiyan; Xu, Chunhua; Hao, Keke; Hou, Zhibo; Song, Yong (2013). „Strategie péče o solitární plicní uzliny“. Journal of Thoracic Disease. 5 (6): 824–829. doi:10.3978 / j.issn.2072-1439.2013.12.13. PMC 3886686. PMID 24409361.
- ^ A b C d E F G h i j k MacMahon, Heber; Naidich, David P .; Goo, Jin Mo; Lee, Kyung Soo; Leung, Ann N. C .; Mayo, John R .; Mehta, Atul C .; Ohno, Yoshiharu; Powell, Charles A .; Prokop, Mathias; Rubin, Geoffrey D .; Schaefer-Prokop, Cornelia M .; Travis, William D .; Van Schil, Paul E .; Bankier, Alexander A. (2017). „Pokyny pro správu náhodných plicních uzlin detekovaných na CT snímcích: od Fleischnerovy společnosti 2017“. Radiologie. 284 (1): 228–243. doi:10.1148 / radiol.2017161659. ISSN 0033-8419. PMID 28240562.
- ^ A b C d E F G h i j k l m n Ó str q r s t u proti w X y z Snoeckx, Annemie; Reyntiens, Pieter; Desbuquoit, Damien; Spinhoven, Maarten J .; Van Schil, Paul E .; van Meerbeeck, Jan P .; Parizel, Paul M. (2017). „Hodnocení solitárního plicního uzlíku: na velikosti záleží, ale neignorujte morfologickou sílu“. Pohledy na zobrazování. 9 (1): 73–86. doi:10.1007 / s13244-017-0581-2. ISSN 1869-4101. PMC 5825309. PMID 29143191.
- ^ A b C Winer-Muram HT (duben 2006). "Osamělý plicní uzlík". Radiologie. 239 (1): 34–49. doi:10,1148 / radiol.2391050343. PMID 16567482.
- ^ Truong, MD, Mylene T .; Ko, MD, Jane P .; Rossi, MD, Santiago E .; Rossi, MD, Ignacio; Viswanathan, MD, Chitra; Bruzzi, MBBCh, John F .; Marom, MD, Edith M .; Erasmus, MD, Jeremy J. (2014). „Aktualizace hodnocení solitárního plicního uzlu“. Radiografie. 34 (6): 1658–1679. doi:10,1148 / rg.346130092. PMID 25310422.
- ^ A b Tanay Patel (2019-02-25). "Zobrazování plicních metastáz". Medscape. Aktualizováno: 30. září 2018
- ^ Tan BB, Flaherty KR, Kazerooni EA, Iannettoni MD; Flaherty; Kazerooni; Iannettoni; Americká vysoká škola lékařů na hrudi (leden 2003). „Osamělý plicní uzlík“. Hruď. 123 (1 příplatek): 89S – 96S. doi:10,1378 / hrudník.123.1_suppl.89S. PMID 12527568. Archivovány od originál dne 12.01.2013.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Americká vysoká škola lékařů na hrudi; Americká hrudní společnost (Září 2013). „Pět věcí, které by lékaři a pacienti měli zpochybňovat“. Moudře vybírat: Iniciativa nadace ABIM. Americká vysoká škola lékařů na hrudi a Americká hrudní společnost. Citováno 6. ledna 2013., který cituje
- Smith-Bindman, R; Lipson, J; Marcus, R; Kim, KP; Mahesh, M; Gould, R; Berrington de González, A; Miglioretti, DL (14. prosince 2009). „Radiační dávka spojená s běžnými vyšetřeními počítačovou tomografií as tím spojené celoživotní riziko rakoviny“. Archiv vnitřního lékařství. 169 (22): 2078–86. doi:10.1001 / archinternmed.2009.427. PMC 4635397. PMID 20008690.
- Wiener, RS; Gould, MK; Woloshin, S; Schwartz, LM; Clark, JA (březen 2013). „Co tím myslíš, skvrna ?: Kvalitativní analýza reakcí pacientů na diskuze s jejich lékaři o plicních uzlinách“. Hruď. 143 (3): 672–7. doi:10,1378 / hrudník.12-1095. PMC 3590883. PMID 22814873.
- ^ A b Gould MK, Maclean CC, Kuschner WG, Rydzak CE, Owens DK; MacLean; Kuschner; Rydzak; Owens (únor 2001). "Přesnost pozitronové emisní tomografie pro diagnostiku plicních uzlin a hromadných lézí: metaanalýza". JAMA. 285 (7): 914–24. doi:10.1001 / jama.285.7.914. PMID 11180735.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Khan A (březen 2007). „Kritéria přiměřenosti ACR pro solitární plicní uzlík“. J Am Coll Radiol. 4 (3): 152–5. doi:10.1016 / j.jacr.2006.12.003. PMID 17412254.
- ^ Vansteenkiste JF, Stroobants SS; Stroobants (leden 2006). „PET sken u rakoviny plic: aktuální doporučení a inovace“. J Thorac Oncol. 1 (1): 71–3. doi:10.1097/01243894-200601000-00014. PMID 17409830.
- ^ Cronin P, Dwamena BA, Kelly AM, Carlos RC; Dwamena; Kelly; Carlos (2008). „Osamělé plicní uzliny: metaanalytické srovnání způsobů zobrazování v průřezu pro diagnostiku malignity“. Radiologie. 246 (3): 772–82. doi:10,1148 / radiol.2463062148. PMID 18235105.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Mukhopadhyay, S (2012). „Využití malých biopsií pro diagnostiku plicních uzlin: Dělat více s méně“. Moderní patologie. 25 Suppl 1: S43-57. doi:10.1038 / modpathol.2011.153. PMID 22214970.
- ^ Klein JS, Salomon G, Stewart EA; Salomon; Stewart (březen 1996). „Transthorakální biopsie jehlou s koaxiálně umístěnou automatickou řezací jehlou o rozměru 20: výsledky u 122 pacientů“. Radiologie. 198 (3): 715–20. doi:10.1148 / radiology.198.3.8628859. PMID 8628859.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Erasmus JJ, McAdams HP, Connolly JE; McAdams; Connolly (2000). "Osamělé plicní uzliny: Část II. Hodnocení neurčitého uzlíku". Radiografie. 20 (1): 59–66. doi:10.1148 / rentgenografie.20.1.g00ja0259. PMID 10682771.CS1 maint: více jmen: seznam autorů (odkaz)
externí odkazy
| Klasifikace | |
|---|---|
| Externí zdroje |














