Delavirdin - Delavirdine
 | |
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Rescriptor |
| AHFS /Drugs.com | Monografie |
| MedlinePlus | a600034 |
| Těhotenství kategorie |
|
| Trasy z správa | Ústní |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Biologická dostupnost | 85% |
| Vazba na bílkoviny | 98% |
| Metabolismus | Jaterní (CYP3A4 - a CYP2D6 - zprostředkovaný) |
| Odstranění poločas rozpadu | 5,8 hodiny |
| Vylučování | Renální (51%) a fekální (44%) |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| NIAID ChemDB | |
| Řídicí panel CompTox (EPA) | |
| Chemické a fyzikální údaje | |
| Vzorec | C22H28N6Ó3S |
| Molární hmotnost | 456.57 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| (ověřit) | |
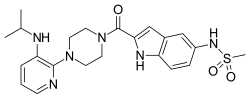
Delavirdin (DLV) (jméno značky Rescriptor) je nenukleosid inhibitor reverzní transkriptázy (NNRTI) prodávaný společností ViiV Healthcare. Používá se jako součást vysoce aktivní antiretrovirové terapie (HAART) k léčbě virus lidské imunodeficience (HIV) typu 1. Uvádí se jako mesylát. Doporučená dávka je 400 mg třikrát denně.
Ačkoli byl delavirdin schválen USA Úřad pro kontrolu potravin a léčiv v roce 1997 je jeho účinnost zejména nižší než u jiných NNRTI efavirenz a má také nepohodlný plán. Tyto faktory vedly americký DHHS k tomu, aby nedoporučoval jeho použití jako součást počáteční terapie.[1]Riziko zkřížené rezistence napříč třídou NNRTI, stejně jako její komplexní soubor lékových interakcí, činí místo delavirdinu ve druhé linii a záchranná terapie nejasný a v současné době se používá zřídka.
Interakce
Jako ritonavir, delavirdin je inhibitorem cytochrom P450 isozym CYP3A4 a interaguje s mnoha léky. Neměl by být podáván s širokou škálou léků, včetně amprenavir, fosamprenavir, simvastatin, lovastatin, rifampin, rifabutin, rifapentin, Třezalka tečkovaná, astemizol, midazolam, triazolam, námel léky a několik léků na kyselý reflux.[1]
Nepříznivé účinky
Nejběžnější nežádoucí příhoda je střední až závažná vyrážka, který se vyskytuje až u 20% pacientů.[2] Mezi další běžné nežádoucí účinky patří únava, bolest hlavy a nevolnost. Byla také hlášena jaterní toxicita.
Syntéza
Úprava režimu, která byla provedena pro ateviridin q.v. provedením reduktivní alkylace s acetonem dává 2 po odstranění chránící skupiny. Acylace tohoto aminu s imidazolidem z kyseliny 5-methylsulfonaminoindol-2-karboxylové (1) poskytuje amid, inhibitor reverzní transkriptázy, atevirdine.
externí odkazy
Reference
- ^ A b Panel DHHS. Pokyny pro použití antiretrovirových látek u dospělých a dospívajících infikovaných HIV-1 (4. května 2006). (K dispozici ke stažení z AIDSInfo Archivováno 2006-05-06 na Wayback Machine )
- ^ "Značka delavirdin mesylátových tablet RESCRIPTOR. Informace o produktu" (PDF). Archivovány od originál (PDF) dne 2006-04-15. Citováno 2006-05-18.
- ^ WO 9109849 „Romero DL, Mitchell MA, Thomas RC, Palmer JR, Tarpley WG, Aristoff PA, Smith HW,„ Diaromatic Substited Anti-AIDS Compounds “, publikováno 11. července 1991, přiděleno společnosti Upjohn Company
- ^ USA 5563142 „Palmer JR, Romero DL, Aristoff PA, Thomas RC, Smith HW,„ Diaromatické substituované sloučeniny jako činidla proti HIV-1 “, zveřejněné 8. října 1996, přidělené společnosti Upjohn Company
- ^ Romero DL, Morge RA, Genin MJ, Biles C, Busso M, Resnick L a kol. (Květen 1993). „Bis (heteroaryl) piperazin (BHAP) inhibitory reverzní transkriptázy: vztahy mezi strukturou a aktivitou nových substituovaných indolových analogů a identifikace 1 - [(5-methansulfonamido-lH-indol-2-yl) -karbonyl] -4- [3 - [(1-methylethyl) amino] -pyridinyl] piperazin monomethansulfonát (U-90152S), klinický kandidát druhé generace ". Journal of Medicinal Chemistry. 36 (10): 1505–8. doi:10.1021 / jm00062a027. PMID 7684450.

