Sachinavir - Saquinavir
 | |
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Invirase, Fortovase |
| AHFS /Drugs.com | Monografie |
| MedlinePlus | a696001 |
| Licenční údaje |
|
| Těhotenství kategorie | |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Biologická dostupnost | ~ 4% (bez ritonaviru posílení )[2] |
| Vazba na bílkoviny | 98% |
| Metabolismus | Jaterní, hlavně CYP3A4 |
| Odstranění poločas rozpadu | 9–15 hodin |
| Vylučování | výkaly (81%) a moč (3%) |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| Řídicí panel CompTox (EPA) | |
| Chemické a fyzikální údaje | |
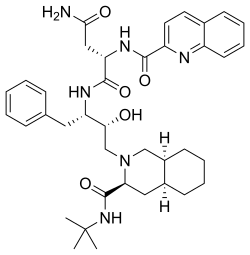
| Vzorec | C38H50N6Ó5 |
| Molární hmotnost | 670.855 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| (ověřit) | |
Sachinavir (SQV), prodávané pod obchodními názvy Invirase a Fortovase, je antiretrovirové léčivo používá se společně s jinými léky k léčbě nebo prevenci HIV / AIDS.[3] Obvykle se používá s ritonavir nebo lopinavir / ritonavir zvýšit jeho účinek.[3] Užívá se ústy.[3]
Mezi časté nežádoucí účinky patří nevolnost, zvracení, průjem a pocit únavy.[3] Mezi závažnější nežádoucí účinky patří problémy s Prodloužení QT, srdeční blok, vysoké hladiny lipidů v krvi a problémy s játry.[3] Zdá se, že je to v těhotenství bezpečné.[3] Je to v inhibitor proteázy třídy a funguje blokováním HIV proteáza.[3]
Saquinavir byl patentován v roce 1988 a poprvé prodán v roce 1995.[4][5]
Lékařské použití
Saquinavir se používá spolu s jinými léky k léčbě nebo prevenci HIV / AIDS.[3] Obvykle se používá s ritonavir nebo lopinavir / ritonavir zvýšit jeho účinek.[3]
Vedlejší efekty
Nejčastějšími nežádoucími účinky sachinaviru v obou lékových formách jsou mírné gastrointestinální příznaky, včetně průjmu, nevolnosti, řídké stolice a břišních diskomfortů. Invirase je snášen lépe než Fortovase.[nutná lékařská citace ]
Biologická dostupnost a lékové interakce
Saquinavir ve formulaci Invirase má nízkou a variabilní orální biologickou dostupnost, pokud je podáván samostatně. Formulace Fortovase ve standardní dávce dodává přibližně osmkrát účinnější léčivo než Invirase, také ve standardní dávce.[6]
Na klinice bylo zjištěno, že orální biologická dostupnost sachinaviru v obou formulacích se významně zvyšuje, když pacienti dostávají také PI ritonavir. Pro pacienty to má hlavní výhodu v tom, že mohou užívat méně sachinaviru při zachování dostatečné hladiny plazmatické hladiny sachinaviru pro účinné potlačení replikace HIV.[nutná lékařská citace ]
Mechanismus tohoto vítaného pozorování nebyl přímo znám, ale později bylo zjištěno, že ritonavir inhibuje cytochrom P450 3A4 isozym. Normálně tento enzym metabolizuje sachinavir na neaktivní formu, ale s ritonavirem, který tento enzym inhibuje, se plazmatické hladiny sachinaviru značně zvýšily. Kromě toho ritonavir také inhibuje transportéry více léků, i když v mnohem menší míře.[nutná lékařská citace ]
Na rozdíl od jiných inhibitorů proteázy se absorpce sachinaviru zdá být zlepšena o omeprazol.[7]
Mechanismus účinku
Saquinavir je inhibitor proteázy. Proteázy jsou enzymy, které štěpí proteinové molekuly na menší fragmenty. HIV proteáza je nezbytná jak pro replikaci viru v buňce, tak pro uvolňování zralých virových částic z infikované buňky. Saquinavir se váže na aktivní místo virové proteázy a brání štěpení virových polyproteinů, čímž brání zrání viru. Saquinavir inhibuje jak HIV-1, tak HIV-2 proteázy.[nutná lékařská citace ]
Dějiny

Saquinavir byl vyvinut farmaceutickou společností Roche.[9] Saquinavir byl šestý antiretrovirový přípravek a první inhibitor proteázy schválený USA Úřad pro kontrolu potravin a léčiv (FDA), vedoucí ritonavir a indinavir o několik měsíců.[10] Tato nová skupina antiretrovirotik hrála zásadní roli ve vývoji vysoce aktivní antiretrovirové terapie (HAART), která pomohla významně snížit riziko úmrtí na příčiny spojené s AIDS, jak je patrné ze snížení roční míry úmrtnosti spojené s HIV v USA, z více než 50 000 na 18 000 během dvou let.[8][11]
Roche požádala a obdržela souhlas s Invirase prostřednictvím programu „Zrychleného schvalování“ FDA - procesu určeného k urychlení uvádění léků na trh pro léčbu závažných onemocnění - rozhodnutí, které bylo kontroverzní, protože aktivisté AIDS se neshodli ohledně výhod důkladného testování oproti včasnému přístupu na nové léky.[12][je zapotřebí lepší zdroj ] Bylo znovu schváleno 7. listopadu 1997 jako Fortovase,[13] měkká gelová kapsle přeformulovaná pro zlepšení biologická dostupnost. Společnost Roche v květnu 2005 oznámila, že vzhledem ke snížené poptávce přestane být Fortovase uvedena na trh počátkem roku 2006, ve prospěch společnosti Invirase podpořené ritonavir,[14] díky schopnosti posledně uvedeného společně formulovaného léčiva inhibovat enzym, který metabolizuje léky na AIDS.[Citace je zapotřebí ]
Společnost a kultura
Náklady
Od roku 2015[Aktualizace], není k dispozici jako generické léky a je drahý.[15][16]
Formulace
Na trh byly uvedeny dvě formulace:
- tvrdá gelová tobolka mesylátu s obchodním názvem Invirase, která vyžaduje kombinaci s ritonavir ke zvýšení sachinaviru biologická dostupnost;
- tobolková formulace sachinaviru v měkkém gelu (mikroemulze,[17] perorálně podávaná formulace) s obchodním názvem Fortovase, která byla celosvětově ukončena v roce 2006.[18]
Reference
- ^ A b „Užívání sachinaviru během těhotenství“. Drugs.com. 20. března 2018. Citováno 28. ledna 2020.
- ^ „Tobolka invirase- sachinavir mesylátu INVIRASE- tableta mesylátu sachinaviru, potažená filmem“. DailyMed. 26. prosince 2019. Citováno 28. ledna 2020.
- ^ A b C d E F G h i "Saquinavir". Americká společnost farmaceutů zdravotnického systému. Archivováno z původního dne 8. září 2015. Citováno 5. září 2015.
- ^ Menší, Lisa K. (2006). Handbook of Assay Development in Drug Discovery. Hoboken: CRC Press. str. 117. ISBN 9781420015706. Archivováno z původního dne 31. března 2016.
- ^ Fischer, Jnos; Ganellin, C. Robin (2006). Analogový objev drog. John Wiley & Sons. str. 509. ISBN 9783527607495.
- ^ „Fortovase“. Drugs.com. 22. března 2019. Citováno 28. ledna 2020.
- ^ Winston A, Back D, Fletcher C a kol. (2006). „Vliv omeprazolu na farmakokinetiku sachinaviru v dávce 500 mg s ritonavirem u zdravých dobrovolníků mužů a žen“. AIDS. 20 (10): 1401–6. doi:10.1097 / 01.aids.0000233573.41597.8a. PMID 16791014. S2CID 44506039.
- ^ A b C „Dohled nad HIV - USA, 1981-2008“. Archivováno z původního dne 9. listopadu 2013. Citováno 8. listopadu 2013.
- ^ J. Hilts, Philip (8. prosince 1995). „MF.D.A. podporuje novou drogu v boji proti AIDS“. New York Times. Citováno 28. října 2020.
- ^ „Objev a vývoj antiretrovirových léků“. NIH. 26. listopadu 2018. Citováno 29. října 2020.
- ^ CDC ve svém Týdenní zpráva o nemocnosti a úmrtnosti, připisuje to „vysoce aktivní antiretrovirové terapii“, bez zmínky o kterémkoli z těchto léků, viz předchozí citace. Je zapotřebí další citace, aby se dosáhlo tohoto přesného spojení mezi touto kapkou a zavedením inhibitorů proteázy.
- ^ "Drogy! Drogy! Drogy! Přehled schválených léků proti HIV". Tělo. Archivováno z původního dne 9. listopadu 2013. Citováno 20. února 2013.
- ^ „Balíček pro schválení léků: Fortovase / Saquinavir NDA 20828“. NÁS. Úřad pro kontrolu potravin a léčiv (FDA). 24. prosince 1999. Citováno 28. ledna 2020.
- ^ Stažení Fortovase (PDF) Archivováno 2006-05-14 na Wayback Machine
- ^ Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. str. 72. ISBN 9781284057560.
- ^ „Obecná dostupnost služby Invirase“. Drugs.com. Citováno 9. července 2020.
- ^ Gibaud S, Attivi D (srpen 2012). "Mikroemulze pro orální podání a jejich terapeutické aplikace" (PDF). Znalecký posudek na dodávku drog. 9 (8): 937–51. doi:10.1517/17425247.2012.694865. PMID 22663249. S2CID 28468973.
- ^ News-Medical.Net. 18. května 2005 Roche ukončí prodej a distribuci přípravku Fortovase (saquinavir) Archivováno 2015-02-22 na Wayback Machine
externí odkazy
- "Saquinavir". Informační portál o drogách. Americká národní lékařská knihovna.
- Saquinavir se váže na bílkoviny v PDB
