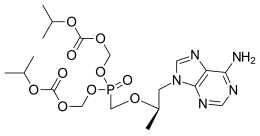
Tenofovir disoproxil - Tenofovir disoproxil
 | |
| Klinické údaje | |
|---|---|
| Výslovnost | /ˌtəˈnoʊFəproti.rˌdɪsəˈprɑːks.l/ |
| Obchodní názvy | Viread, další |
| Ostatní jména | Tenofovir-disoproxil-fumarát, Bis (POC) PMPA |
| AHFS /Drugs.com | Monografie |
| MedlinePlus | a602018 |
| Licenční údaje | |
| Těhotenství kategorie |
|
| Trasy z správa | Pusou (tablety ) |
| ATC kód | |
| Právní status | |
| Právní status | |
| Farmakokinetické data | |
| Biologická dostupnost | 25% |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ChEBI | |
| ChEMBL | |
| NIAID ChemDB | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.129.993 |
| Chemické a fyzikální údaje | |
| Vzorec | C19H30N5Ó10P |
| Molární hmotnost | 519.448 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
 | |
| Klinické údaje | |
|---|---|
| Ostatní jména | 9- (2-fosfonyl-methoxypropyly) adenin (PMPA) |
| MedlinePlus | a602018 |
| Trasy z správa | Ústní |
| ATC kód |
|
| Farmakokinetické data | |
| Vazba na bílkoviny | < 1% |
| Odstranění poločas rozpadu | 17 hodin |
| Vylučování | Ledviny |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.129.993 |
| Chemické a fyzikální údaje | |
| Vzorec | C9H14N5Ó4P |
| Molární hmotnost | 287.216 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| (ověřit) | |
Tenofovir disoproxil, prodávané pod obchodním názvem Viread mimo jiné je to lék používaný k léčbě chronických onemocnění žloutenka typu B a předcházet a léčit HIV / AIDS.[1] Obecně se doporučuje používat s jinými antiretrovirotiky.[1] Může být použit k prevenci HIV / AIDS u osob s vysokým rizikem před expozicí a po poranění jehlou nebo jiné potenciální expozice.[1] Prodává se samostatně i společně emtricitabin / tenofovir a efavirenz / emtricitabin / tenofovir.[1] Neléčí HIV / AIDS ani hepatitidu B.[1][2] Je k dispozici ústy jako tableta nebo prášek.[1]
Mezi časté nežádoucí účinky patří nevolnost, vyrážka, průjem, bolest hlavy, bolest, deprese a slabost.[1] Mezi závažné nežádoucí účinky patří vysoký laktát v krvi a zvětšená játra.[1] Neexistují žádné absolutní kontraindikace.[1] Často se doporučuje během těhotenství a zdá se být v bezpečí.[1] Je to nukleotidový inhibitor reverzní transkriptázy a funguje tak, že snižuje schopnost virů replikovat se.[1]
Tenofovir byl patentován v roce 1996 a schválen pro použití ve Spojených státech v roce 2001.[3] Je na Seznam základních léčivých přípravků Světové zdravotnické organizace.[4] Je k dispozici jako generické léky od roku 2017.[5]
Lékařské použití
Tenofovir-disoproxil se používá k léčbě infekce HIV-1 a léčbě chronické hepatitidy B. U infekce HIV-1 je tenofovir indikován v kombinaci s jinými antiretrovirovými látkami u osob ve věku 2 let a starších. U pacientů s chronickou hepatitidou B je tenofovir indikován u pacientů ve věku 12 let a starších.[6]
Snížení rizika HIV
Tenofovir lze použít k prevenci HIV u lidí, kteří jsou vystaveni vysokému riziku infekce pohlavním přenosem nebo injekčním užíváním drog. A Cochrane recenze zkoumali použití tenofoviru k prevenci HIV před expozicí a zjistili, že samotný tenofovir i tenofovir / emtricitabin kombinace u vysoce rizikových pacientů snížila riziko nákazy HIV.[7] Spojené státy. Centra pro kontrolu a prevenci nemocí (CDC) rovněž provedla studii ve spolupráci s Thajské ministerstvo veřejného zdraví zjistit účinnost poskytování denních dávek tenofoviru osobám, které nelegálně injekčně užívají drogy preventivní opatření. Výsledky odhalily 48,9% snížený výskyt viru u skupiny subjektů, které dostaly lék, ve srovnání s kontrolní skupinou, která dostávala placebo.[8]
Nepříznivé účinky
Tenofovir-disoproxil je obecně dobře snášen s nízkou mírou přerušení léčby u populace s HIV a chronickou hepatitidou B.[9] Neexistují žádné kontraindikace pro použití tohoto léku.[6] Nejčastěji hlášenými nežádoucími účinky způsobenými užíváním tenofovir-disoproxilu byly závratě, nevolnost a průjem.[9] Mezi další nepříznivé účinky patří deprese, poruchy spánku, bolesti hlavy, svědění, vyrážka a horečka. Varování USA box varuje před možným nástupem laktátová acidóza nebo poškození jater v důsledku použití tenofovir-disoproxilu.[10]
Dlouhodobé užívání tenofovir-disoproxilu je spojeno s nefrotoxicita a úbytek kostní hmoty. Prezentace nefrotoxicity se může objevit jako Fanconiho syndrom, akutní poškození ledvin nebo pokles rychlost glomerulární filtrace (GFR).[11] Přerušení léčby tenofovir-disoproxilem může potenciálně vést k obrácení poškození ledvin. Nefrotoxicita může být způsobena akumulací tenofovir-disoproxilu v proximálních tubulech, což vede ke zvýšeným sérovým koncentracím.[9]
Interakce
Tenofovir interaguje s didanosin a inhibitory HIV-1 proteázy. Tenofovir zvyšuje koncentrace didanosinu a může mít za následek nežádoucí účinky, jako je pankreatitida a neuropatie. Tenofovir také interaguje s inhibitory proteázy HIV-1, jako je atazanavir snížením koncentrací atazanaviru a zvýšením koncentrací tenofoviru.[6] Jelikož se tenofovir vylučuje ledvinami, mohou také problémy způsobovat léky, které zhoršují funkci ledvin.[12]
Farmakologie
Mechanismus účinku
Tenofovir disoproxil je a nukleotidový analogový inhibitor reverzní transkriptázy (NtRTI).[13] Selektivně inhibuje virové reverzní transkriptáza, klíčový enzym v retrovirech, jako je virus lidské imunodeficience (HIV), zatímco vykazuje omezenou inhibici lidských enzymů, jako jsou DNA polymerázy α, β a mitochondriální DNA polymeráza y.[6][13] In vivo se tenofovir-disoproxil-fumarát převádí na tenofovir, acyklický analog deoxyadenosin-5'-monofosfátu (d-AMP). Tenofovir postrádá hydroxylovou skupinu v poloze odpovídající 3 'uhlíku d-AMP, což brání tvorbě 5 'až 3' fosfodiester vazba nezbytná pro prodloužení řetězce DNA.[13] Jakmile je tenofovir začleněn do rostoucího řetězce DNA, způsobuje předčasné ukončení transkripce DNA a brání virové replikaci.[13]
Farmakokinetika
Tenofovir disoproxil je a proléčivo který se rychle vstřebává ze střeva a štěpí se, aby uvolnil tenofovir.[6] Uvnitř buněk je tenofovir fosforylovaný k tenofovir-difosfátu (který je analogický s a trifosfát, protože samotný tenofovir již jeden má fosfonát zbytek), aktivní sloučenina, která inhibuje reverzní transkriptázu prostřednictvím ukončení řetězce.[12][13]
U osob nalačno biologická dostupnost je 25% a nejvyšší krevní plazma koncentrací je dosaženo po jedné hodině.[13] Pokud se užívá s mastným jídlem, nejvyšší plazmatické koncentrace se dosáhne po dvou hodinách a plocha pod křivkou se zvyšuje o 40%.[13] Je to inhibitor cytochrom P450 1A2.[14]
Tenofovir se vylučuje hlavně ledvinami, oběma glomerulární filtrace a tím tubulární sekrece pomocí transportních proteinů OAT1, OAT3 a ABCC4.[12]
Dějiny
Tenofovir byl původně syntetizován Antonín Holý na Ústavu organické chemie a biochemie UK Akademie věd České republiky v Praha. Patent[15] podaný Holým v roce 1984 nezmiňuje potenciální použití sloučeniny k léčbě infekce HIV, které bylo objeveno teprve o rok dříve.
V roce 1985 popsali De Clercq a Holý aktivitu PMPA proti HIV v buněčné kultuře.[16] Krátce nato spolupráce s biotechnologickou společností Gilead Sciences vedlo ke zkoumání potenciálu PMPA jako léčby pacientů infikovaných HIV. V roce 1997 vědci z Gileadu a Kalifornské univerzity v San Francisku prokázali, že tenofovir vykazuje u lidí anti-HIV účinky, pokud jsou podávány subkutánní injekcí.[17]
Počáteční forma tenofoviru použitá v těchto studiích měla omezený potenciál pro široké použití, protože špatně pronikl do buněk a nebyl absorbován při podání ústy. Gilead vyvinul prolékovou verzi tenofoviru, tenofovir-disoproxilu. Tato verze tenofoviru se často označuje jednoduše jako „tenofovir“. V této verzi léku jsou maskovány dva negativní náboje skupiny kyseliny tenofovir-fosfonové, což zvyšuje orální absorpci.
Tenofovir-disoproxil byl v USA schválen v roce 2001 pro léčbu HIV a v roce 2008 pro léčbu chronický žloutenka typu B.[18][19]
Lékové formy
Lze užívat tenofovir-disoproxil pusou a prodává se mimo jiné pod značkou Viread.[20] Tenofovir disoproxil je a pro-droga forma tenofovir-fosfonátu, který se uvolňuje intracelulárně a přeměňuje se na tenofovir-difosfát.[21] Je uváděn na trh společností Gilead Sciences (jako fumarát, zkráceně TDF).[22]
Tenofovir-disoproxil je také dostupný v pilulkách, které kombinují řadu antivirotik do jedné dávky. Známé kombinace zahrnují Atripla (tenofovir-disoproxil / emtricitabin / efavirenz), Complera (tenofovir-disoproxil / emtricitabin / rilpivirin), Stribild (tenofovir-disoproxil / emtricitabin / elvitegravir / kobicistat) a Truvada (tenofovir-disoproxil / emtricitabin).[20]
Společnost Gilead vytvořila druhou proléčivou formu aktivního léčiva, tenofovir-difosfát, tzv tenofovir alafenamid. Od tenofovir-disoproxilu se liší svou aktivací v lymfoidní buňky. To umožňuje akumulaci aktivních metabolitů v těchto buňkách, což vede k nižší systémové expozici a potenciální toxicitě.[9]
Chemie
Tenofovir má teplotu tání 279 ° C (534 ° F).[23] Tenofovir-disoproxil-fumarát je bílý až téměř bílý krystalický prášek, který je rozpustný v methanolu, málo rozpustný ve vodě (13,4 mg / ml[24]), a velmi málo rozpustný v dichlormethan.[25]
Detekce v tělních tekutinách
Tenofovir lze měřit v plazmě kapalinovou chromatografií. Takové testování je užitečné pro monitorování terapie a prevenci akumulace a toxicity léku u lidí s problémy s ledvinami nebo játry.[26][27][28]
Reference
- ^ A b C d E F G h i j k "Tenofovir-disoproxil-fumarát". Americká společnost farmaceutů zdravotnického systému. Archivováno z původního dne 30. listopadu 2016. Citováno 29. listopadu 2016.
- ^ Martin P, Lau DT, Nguyen MH, Janssen HL, Dieterich DT, Peters MG, Jacobson IM (listopad 2015). „Algoritmus léčby při léčbě infekce virem chronické hepatitidy B ve Spojených státech: aktualizace z roku 2015“. Klinická gastroenterologie a hepatologie. 13 (12): 2071–87.e16. doi:10.1016 / j.cgh.2015.07.007. PMID 26188135.
- ^ Fischer, Janos; Ganellin, C. Robin (2006). Analogový objev drog. John Wiley & Sons. str. 505. ISBN 9783527607495. Archivováno z původního dne 2017-09-08.
- ^ Světová zdravotnická organizace (2019). Seznam základních léků Světové zdravotnické organizace: 21. seznam 2019. Ženeva: Světová zdravotnická organizace. hdl:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Licence: CC BY-NC-SA 3.0 IGO.
- ^ „Teva oznamuje exkluzivní spuštění generické verze Viread ve Spojených státech“. www.tevapharm.com.
- ^ A b C d E Gilead Sciences, Inc. Informace o předepisování. Archivováno 07.02.2013 na Wayback Machine Revidováno: listopad 2012.
- ^ Okwundu CI, Uthman OA, Okoromah CA (červenec 2012). „Antiretrovirová preexpoziční profylaxe (PrEP) pro prevenci HIV u vysoce rizikových jedinců“. Cochrane Database of Systematic Reviews. 7 (7): CD007189. doi:10.1002 / 14651858.CD007189.pub3. PMID 22786505.
- ^ Emma Bourke (14. června 2013). „Preventivní droga může snížit přenos HIV mezi injekčními uživateli drog“. Konverzace Austrálie. Konverzační mediální skupina. Archivováno z původního dne 1. listopadu 2013. Citováno 17. června 2013.
- ^ A b C d Ustianowski A, Arends JE (červen 2015). „Tenofovir: Co jsme se naučili po 7,5 milionu osobních let používání. Infekční nemoci a terapie. 4 (2): 145–57. doi:10.1007 / s40121-015-0070-1. PMC 4471058. PMID 26032649.
- ^ "Tenofovir: MedlinePlus Drug Information". medlineplus.gov. Archivováno od originálu 10. 11. 2016. Citováno 2016-11-09.
- ^ Morlat P, Vivot A, Vandenhende MA, Dauchy FA, Asselineau J, Déti E, Gerard Y, Lazaro E, Duffau P, Neau D, Bonnet F, Chêne G (2013-06-12). „Role tradičních rizikových faktorů a antiretrovirových léků ve výskytu chronického onemocnění ledvin, kohorta ANRS CO3 Aquitaine, Francie, 2004–2012“. PLOS ONE. 8 (6): e66223. Bibcode:2013PLoSO ... 866223M. doi:10.1371 / journal.pone.0066223. PMC 3680439. PMID 23776637.
- ^ A b C Haberfeld, H, ed. (2015). Kodex Rakousko (v němčině). Vídeň: Österreichischer Apothekerverlag.
- ^ A b C d E F G Drugbank: Tenofovir Archivováno 08.09.2015 na Wayback Machine
- ^ Pubchem. "Tenofovir disoproxil". pubchem.ncbi.nlm.nih.gov. Citováno 2018-04-17.
- ^ „Patent US4808716 - 9- (fosfonylmethoxyalkyl) adeniny, způsob přípravy a ... - Google Patents“. Archivováno z původního dne 2014-05-09.
- ^ USA 4724233 A, De Clercq, Erik; Antonin Holy & Ivan Rosenberg, „Terapeutická aplikace fosfonylmethoxyalkyladeninů“
- ^ Deeks SG, Barditch-Crovo P, Lietman PS, Hwang F, Cundy KC, Rooney JF, Hellmann NS, Safrin S, Kahn JO (září 1998). „Bezpečnost, farmakokinetika a antiretrovirová aktivita intravenózního 9- [2- (R) - (fosfonomethoxy) propyl] adeninu, nové terapie proti viru lidské imunodeficience (HIV), u dospělých infikovaných HIV.“. Antimikrobiální látky a chemoterapie. 42 (9): 2380–4. doi:10.1128 / aac.42.9.2380. PMC 105837. PMID 9736567.
- ^ Schvalovací dopis FDA (týkající se léčby hepatitidy B) Archivováno 2009-02-25 na Wayback Machine
- ^ FDA čistí Viread na hepatitidu B. Archivováno 08.09.2017 na Wayback Machine
- ^ A b „Drugs @ FDA: FDA Approved Drug Products“. www.accessdata.fda.gov. Archivováno od originálu 10. 11. 2016. Citováno 2016-11-09.
- ^ Mouton JP, Cohen K, Maartens G (listopad 2016). „Klíčové problémy s toxicitou u antiretrovirové terapeutické léčby první linie doporučené WHO“. Odborný přehled klinické farmakologie. 9 (11): 1493–1503. doi:10.1080/17512433.2016.1221760. PMID 27498720. S2CID 205930751.
- ^ Emau P, Jiang Y, Agy MB, Tian B, Bekele G, Tsai CC (listopad 2006). „Postexpoziční profylaxe pro SIV revisited: zvířecí model pro prevenci HIV“. Výzkum a terapie AIDS. 3: 29. doi:10.1186/1742-6405-3-29. PMC 1687192. PMID 17132170.
- ^ Dinnendahl, V; Fricke, U, eds. (2011). Arzneistoff-profil (v němčině). 9 (25 ed.). Eschborn, Německo: Govi Pharmazeutischer Verlag. ISBN 978-3-7741-9846-3.
- ^ „AIDSinfo databáze léků: Tenofovir disoproxil fumarát“. Národní institut zdraví. Archivováno z původního dne 28. dubna 2017. Citováno 4. srpna 2016.
- ^ „Tenofovir-disoproxil-fumarát“ (PDF). Světová zdravotnická organizace. Červen 2010. Archivováno (PDF) od originálu 2016-08-08.
- ^ Delahunty T, Bushman L, Robbins B, Fletcher CV (červenec 2009). „Simultánní stanovení tenofoviru a emtricitabinu v plazmě pomocí LC / MS / MS a izotopově značených interních standardů“. Chromatografický deník B. 877 (20–21): 1907–14. doi:10.1016 / j.jchromb.2009.05.029. PMC 2714254. PMID 19493710.
- ^ Kearney BP, Yale K, Shah J, Zhong L, Flaherty JF (2006). „Farmakokinetika a doporučení pro dávkování tenofovir-disoproxil-fumarátu u pacientů s poškozením jater nebo ledvin“. Klinická farmakokinetika. 45 (11): 1115–24. doi:10.2165/00003088-200645110-00005. PMID 17048975. S2CID 6322957.
- ^ R. Baselt, Dispozice toxických drog a chemických látek u člověka, 8. vydání, Biomedical Publications, Foster City, Kalifornie, 2008, s. 1490–1492.
externí odkazy
- "Tenofovir disoproxil". Informační portál o drogách. Americká národní lékařská knihovna.
- „Tenofovir-disoproxil-fumarát“. Informační portál o drogách. Americká národní lékařská knihovna.
