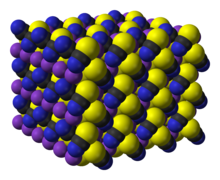
Thiokyanát draselný - Potassium thiocyanate
 | |
| Jména | |
|---|---|
| Ostatní jména Sulfokyanát draselný Isothiokyanát draselný Thiokyanid draselný Rodanid draselný | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.005.792 |
PubChem CID | |
| Číslo RTECS |
|
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| KSCN | |
| Molární hmotnost | 97,181 g mol−1 |
| Vzhled | Bezbarvý rozmělněný krystaly |
| Zápach | Bez zápachu |
| Hustota | 1,886 g / cm3 |
| Bod tání | 173,2 ° C (343,8 ° F; 446,3 K) |
| Bod varu | 500 ° C (932 ° F; 773 K) (rozkládá se) |
| 177 g / 100 ml (0 ° C) 217 g / 100 ml (20 ° C) | |
| Rozpustnost | aceton: 21,0 g / 100 ml ethanol: rozpustný |
| −48.0·10−6 cm3/ mol | |
| Nebezpečí | |
| Bezpečnostní list | ICSC 1088 |
Klasifikace EU (DSD) (zastaralý) | Toxický (T) |
| R-věty (zastaralý) | R20 / 21/22 R32 R52 / 53 |
| S-věty (zastaralý) | (S2) S13 S61 |
| NFPA 704 (ohnivý diamant) | |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
LD50 (střední dávka ) | 854 mg / kg (orálně, potkan)[1] |
| Související sloučeniny | |
jiný anionty | Kyanát draselný Kyanid draselný |
jiný kationty | Thiokyanát sodný Thiokyanát amonný |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Thiokyanát draselný je chemická sloučenina s molekulárním vzorcem KSCN. Je to důležitá sůl thiokyanát anion, jeden z pseudohalogenidy. Sloučenina má nízkou teplotu tání ve srovnání s většinou ostatních anorganických solí.
Použití v chemické syntéze
Vodný KSCN reaguje téměř kvantitativně s Pb (č3)2 dát Pb (SCN)2, který byl použit k převodu acylchloridy na isothiokyanáty.[2]
KSCN převádí ethylenkarbonát na ethylensulfid.[3] Za tímto účelem se KSCN nejprve roztaví ve vakuu, aby se odstranila voda. V související reakci konvertuje KSCN cyklohexenoxid na odpovídající episulfid.[4]
- C6H10O + KSCN → C.6H10S + KOCN
KSCN je také výchozím produktem pro syntézu karbonylsulfid.
Jiná použití
Zředěný vodný KSCN se občas používá pro středně realistické krevní efekty ve filmu a divadle. Může být natřen na povrch nebo ponechán jako bezbarvý roztok. Při kontaktu s chlorid železitý roztok (nebo jiné roztoky obsahující Fe3+ ), produkt reakce je roztok s krvavě červenou barvou, v důsledku tvorby thiokyanatoiron komplexní ion. Tato chemikálie se tedy často používá k vytvoření efektu „stigmat“. Jelikož jsou obě řešení bezbarvá, lze je umístit samostatně na každou ruku. Když dojde ke kontaktu rukou, roztoky reagují a účinek vypadá pozoruhodně stigmata.[Citace je zapotřebí ]
Podobně se tato reakce používá jako a test pro Fe3+ v laboratoř.
Reference
- ^ Chambers, Michaele. „ChemIDplus - 333-20-0 - ZNNZYHKDIALBAK-UHFFFAOYSA-M - thiokyanát draselný [NF] - Hledání podobných struktur, synonyma, vzorce, odkazy na zdroje a další chemické informace“. chem.sis.nlm.nih.gov. Citováno 19. dubna 2018.
- ^ Smith, P. A. S .; Kan, R. O. (1973). „2a-thiohomoftalimid“. Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 5, str. 1051
- ^ Searles, S .; Lutz, E. F .; Hays, H. R .; Mortensen, H. E. (1973). "Ethylensulfid". Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 5, str. 562
- ^ van Tamelen, E. E. (1963). „Cyklohexensulfid“. Organické syntézy.; Kolektivní objem, 4, str. 232

