Stříbrný - Silver
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| stříbrný | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Vzhled | lesklý bílý kov | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standardní atomová hmotnost Ar, std(Ag) | 107.8682(2)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stříbro v periodická tabulka | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Protonové číslo (Z) | 47 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina | skupina 11 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Doba | období 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | d-blok | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategorie prvku | Přechodný kov | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurace elektronů | [Kr ] 4d10 5 s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrony na skořápku | 2, 8, 18, 18, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyzikální vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fáze naSTP | pevný | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bod tání | 1234.93 K. (961,78 ° C, 1763,2 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bod varu | 2435 K (2162 ° C, 3924 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hustota (ur.t.) | 10,49 g / cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| když kapalina (přit.t.) | 9 320 g / cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplo fúze | 11.28 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Odpařovací teplo | 254 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární tepelná kapacita | 25,350 J / (mol · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Tlak páry
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační stavy | −2, −1, +1, +2, +3 (anamfoterní kysličník) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativita | Paulingova stupnice: 1,93 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr | empirická: 144odpoledne | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 145 ± 17 hodin | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsův poloměr | 172 hodin | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Další vlastnosti | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Přirozený výskyt | prvotní | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalická struktura | obličejově centrovaný kubický (FCC) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku tenká tyč | 2680 m / s (přir.t.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplotní roztažnost | 18,9 µm / (m · K) (při 25 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 429 W / (m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná difuzivita | 174 mm2/ s (při 300 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrický odpor | 15,87 nΩ · m (při 20 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetické objednávání | diamagnetický[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetická susceptibilita | −19.5·10−6 cm3/ mol (296 K)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Youngův modul | 83 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tažný modul | 30 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hromadný modul | 100 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Poissonův poměr | 0.37 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohsova tvrdost | 2.5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vickersova tvrdost | 251 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brinellova tvrdost | 206–250 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Číslo CAS | 7440-22-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dějiny | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objev | před 5 000 př | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hlavní izotopy stříbra | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
stříbrný je chemický prvek s symbol Ag (z latinský argentum, odvozené z Protoindoevropský hǵerǵ: "lesklý" nebo "bílý") a protonové číslo 47. Měkký, bílý, lesklý přechodový kov, vykazuje nejvyšší elektrická vodivost, tepelná vodivost, a odrazivost ze všech kov.[Citace je zapotřebí ] Kov se nachází v zemské kůře v čisté, volné elementární formě („nativní stříbro“), jako slitina s zlato a další kovy a minerály jako např argentit a chlorgyrit. Většina stříbra se vyrábí jako vedlejší produkt měď, zlato, Vést, a zinek rafinace.
Stříbro je již dlouho oceňováno jako a drahé kovy. Stříbrný kov se používá v mnoha zlaté mince, někdy vedle zlata:[4] i když je hojnější než zlato, je mnohem méně hojné jako a nativní metal.[5] Jeho čistota se obvykle měří na a promile základ; 94% čistá slitina je popsána jako „0,940 jemná“. Jako jeden ze sedmi kovy starověku, stříbro hrálo trvalou roli ve většině lidských kultur.
Jiné než v měna a jako investice střední (mince a pruty ), stříbro se používá v solární panely, filtrace vody, šperky, ozdoby, vysoce hodnotné nádobí a náčiní (odtud výraz „stříbro "), v elektrické kontakty a vodiče, ve specializovaných zrcadlech, lakování oken, v katalýza chemických reakcí, jako barvivo v vitráže a ve specializovaných cukrovinkách. Jeho sloučeniny se používají v fotografický a rentgen film. Zředěné roztoky dusičnan stříbrný a další sloučeniny stříbra se používají jako dezinfekční prostředky a mikrobiocidy (oligodynamický účinek ), přidáno k obvazy a obvazy na rány, katétry, a další lékařské nástroje.
Vlastnosti

Stříbro je podobné ve svých fyzikálních a chemických vlastnostech svým dvěma vertikálním sousedům v skupina 11 z periodická tabulka, měď a zlato. Jeho 47 elektronů je uspořádáno v konfigurace [Kr] 4d105 s1, podobně jako měď ([Ar] 3d104 s1) a zlato ([Xe] 4f145 d106 s1); skupina 11 je jednou z mála skupin v d-blok který má zcela konzistentní sadu elektronových konfigurací.[7] Tato výrazná elektronová konfigurace s jediným elektronem v nejvyšším obsazeném subškrtu nad naplněnou d subshell odpovídá mnoha singulárním vlastnostem kovového stříbra.[8]
Stříbro je extrémně měkké, tvárný a tvárný přechodový kov, i když je o něco méně tvárný než zlato. Stříbro krystalizuje v a obličejově centrovaný kubický mříž s hromadným koordinačním číslem 12, kde je delokalizován pouze jediný elektron 5 s, podobně jako u mědi a zlata.[9] Na rozdíl od kovů s neúplnými d-skořápkami chybí kovové vazby ve stříbře a kovalentní charakter a jsou relativně slabé. Toto pozorování vysvětluje minimum tvrdost a vysoká tažnost monokrystaly stříbra.[10]
Stříbro má brilantně bílý kovový lesk, který může trvat vysoko polština,[11] a který je tak charakteristický, že se název samotného kovu stal a název barvy.[8] Na rozdíl od mědi a zlata je energie potřebná k excitaci elektronu z naplněného pásma d do pásma vodivosti sp ve stříbře dostatečně velká (kolem 385 kJ / mol), takže již neodpovídá absorpci ve viditelné oblasti spektra, ale spíše v ultrafialový; proto stříbro není barevný kov.[8] Chráněné stříbro má lepší optické vlastnosti odrazivost než hliník na všech vlnových délkách delších než ~ 450 nm.[12] Při vlnových délkách kratších než 450 nm je odrazivost stříbra horší než odrazivost hliníku a klesá k nule poblíž 310 nm.[13]
Velmi vysoká elektrická a tepelná vodivost je společná pro prvky ve skupině 11, protože jejich jediný elektron je volný a neinteraguje s naplněnou d subshell, protože takové interakce (které se vyskytují v předchozích přechodových kovech) snižují mobilitu elektronů.[14] The elektrická vodivost stříbra je největší ze všech kovů, dokonce větší než měď, ale pro tuto vlastnost se široce nepoužívá kvůli vyšším nákladům. Výjimka je v vysokofrekvenční inženýrství, zejména v VHF a vyšší frekvence, kde postříbření zlepšuje elektrickou vodivost, protože ty proudy mají tendenci proudit na povrchu vodičů spíše než vnitřkem. V době druhá světová válka ve Spojených státech, 13540 tun stříbra bylo použito pro elektromagnety v kalutrony pro obohacení uran, hlavně kvůli válečnému nedostatku mědi.[15][16][17] Čisté stříbro má nejvyšší tepelná vodivost jakéhokoli kovu, i když vodivost uhlík (v diamant allotrope ) a supertekuté helium-4 jsou ještě vyšší.[7] Stříbro má také nejnižší kontaktní odpor z jakéhokoli kovu.[7]
Stříbro se snadno formuje slitiny s mědí a zlatem, stejně jako zinek. Slitiny zinku a stříbra s nízkou koncentrací zinku lze považovat za kubické pevné roztoky zinku ve stříbře zaměřené na obličej, protože struktura stříbra je do značné míry nezměněna, zatímco koncentrace elektronů stoupá, když se přidává více zinku. Zvyšování koncentrace elektronů dále vede k centrovaný na tělo (koncentrace elektronů 1,5), složitý kubický (1,615) a šestihranný uzavřený fáze (1,75).[9]
Izotopy
Přirozeně se vyskytující stříbro se skládá ze dvou stabilních izotopy, 107Ag a 109Ag, s 107Ag je o něco hojnější (51 839% přirozená hojnost ). Toto téměř stejné množství je v periodické tabulce vzácné. The atomová hmotnost je 107,8682 (2) u;[18][19] tato hodnota je velmi důležitá z důvodu důležitosti sloučenin stříbra, zejména halogenidů, v gravimetrická analýza.[18] Oba izotopy stříbra jsou vyráběny ve hvězdách prostřednictvím s-proces (pomalý záchyt neutronů), stejně jako v supernovách přes r-proces (rychlé zachycení neutronů).[20]
Dvacet osm radioizotopy byly charakterizovány, nejstabilnější bytost 105Ag s a poločas rozpadu 41,29 dne, 111Ag s poločasem rozpadu 7,45 dnů a 112Ag s poločasem 3,13 hodiny. Stříbro má mnoho jaderné izomery, nejstabilnější bytost 108 mAg (t1/2 = 418 let), 110 mAg (t1/2 = 249,79 dnů) a 106 mAg (t1/2 = 8,28 dne). Všechny zbývající radioaktivní izotopy mají poločasy kratší než hodinu a většina z nich má poločasy kratší než tři minuty.[21]
Izotopy stříbra se pohybují v relativní atomová hmotnost od 92 950 u (93Ag) na 129,950 u (130Ag);[22] primární režim rozpadu před nejhojnějším stabilním izotopem, 107Ag, je elektronový záchyt a primární režim po je rozpad beta. Primární produkty rozpadu před 107Ag jsou palladium (prvek 46) izotopy a primární produkty poté jsou kadmium (prvek 48) izotopy.[21]
Palladium izotop 107Pd se rozpadá emisí beta na 107Ag s poločasem rozpadu 6,5 milionu let. Železné meteority jsou jedinými objekty s dostatečně vysokým poměrem palladia ke stříbru, aby poskytly měřitelné variace 107Ag hojnost. Radiogenní 107Ag byl poprvé objeven v Santa Clara meteorit v roce 1978.[23] Objevitelé navrhují koalescenci a diferenciaci malých železných jader planety mohlo dojít 10 milionů let po a nukleosyntetický událost. 107Pd–107Ag korelace pozorované v tělech, které byly od roku 2004 zjevně roztaveny navýšení z Sluneční Soustava musí odrážet přítomnost nestabilních nuklidů v rané sluneční soustavě.[24]
Chemie
| Oxidace Stát | Koordinace číslo | Stereochemie | Zástupce sloučenina |
|---|---|---|---|
| 0 (d10s1) | 3 | Rovinný | Ag (CO)3 |
| 1 (d10) | 2 | Lineární | [Ag (CN)2]− |
| 3 | Trigonální rovinná | AgI (PEt2Ar)2 | |
| 4 | Čtyřboká | [Ag (průjmy)2]+ | |
| 6 | Osmistěn | AgF, AgCl, AgBr | |
| 2 (d9) | 4 | Čtvercový rovinný | [Ag (py)4]2+ |
| 3 (d8) | 4 | Čtvercový rovinný | [AgF4]− |
| 6 | Osmistěn | [AgF6]3− |
Stříbro je poměrně nereaktivní kov. Je to proto, že jeho naplněná 4d skořápka není příliš účinná při stínění elektrostatických sil přitahování z jádra k nejvzdálenějšímu elektronu 5 s, a proto je stříbro blízko spodní části elektrochemická řada (E0(Ag+/ Ag) = +0,799 V).[8] Ve skupině 11 má stříbro nejnižší první ionizační energii (ukazuje nestabilitu orbitálu 5 s), ale má vyšší druhou a třetí ionizační energii než měď a zlato (vykazuje stabilitu 4d orbitalů), takže chemie stříbra je převážně v oxidačním stavu +1, což odráží stále omezenější rozsah oxidačních stavů podél přechodové řady, jak se d-orbitaly plní a stabilizují.[26] Na rozdíl od mědi, pro kterou je větší hydratační energie Cu2+ ve srovnání s Cu+ je důvodem, proč je první stabilnější ve vodném roztoku a pevných látkách, přestože chybí stabilně naplněná d-subshell druhého, se stříbrem je tento účinek zaplaven jeho větší druhou ionizační energií. Ag+ je stabilní druh ve vodném roztoku a pevných látkách s Ag2+ je mnohem méně stabilní, protože oxiduje vodu.[26]
Většina sloučenin stříbra má významné kovalentní charakter díky malé velikosti a vysoké první ionizační energii (730,8 kJ / mol) stříbra.[8] Navíc, stříbro je Pauling elektronegativita 1,93 je vyšší než u Vést (1,87) a jeho elektronová afinita 125,6 kJ / mol je mnohem vyšší než u vodík (72,8 kJ / mol) a ne o moc méně než u kyslík (141,0 kJ / mol).[27] Díky své plné d-skořápce vykazuje stříbro v hlavním oxidačním stavu +1 relativně málo vlastností přechodných kovů vlastních ze skupin 4 až 10, které tvoří poměrně nestabilní organokovové sloučeniny, tvořící lineární komplexy vykazující velmi nízkou hodnotu koordinační čísla jako 2, a tvoří amfoterní oxid[28] stejně jako Zintl fáze jako post-přechodové kovy.[29] Na rozdíl od předchozích přechodných kovů je oxidační stav +1 stříbra stabilní i v nepřítomnosti n-akceptorové ligandy.[26]
Stříbro nereaguje se vzduchem, dokonce ani při rudém žáru, a proto o něm uvažoval alchymisté jako ušlechtilý kov spolu se zlatem. Jeho reaktivita je střední mezi reaktivitou mědi (která se tvoří oxid měďnatý při zahřátí na vzduchu na červené teplo) a zlato. Stejně jako měď reaguje i stříbro síra a jeho sloučeniny; v jejich přítomnosti stříbro na vzduchu zakalí a vytvoří černou sulfid stříbrný (měď tvoří zelenou síran místo toho, zatímco zlato nereaguje). Na rozdíl od mědi nebude stříbro reagovat s halogeny, s výjimkou fluor plyn, se kterým tvoří difluorid. Zatímco stříbro není napadeno neoxidujícími kyselinami, kov se snadno rozpouští v horkém koncentrovaném stavu kyselina sírová, stejně jako zředěné nebo koncentrované kyselina dusičná. V přítomnosti vzduchu, zejména v přítomnosti peroxid vodíku stříbro se snadno rozpouští ve vodných roztocích kyanid.[25]
Tři hlavní formy zhoršení historických stříbrných artefaktů jsou poskvrnění, vznik chlorid stříbrný v důsledku dlouhodobého ponoření do slané vody, stejně jako reakce s dusičnan ionty nebo kyslík. Čerstvý chlorid stříbrný je světle žlutý a po vystavení světlu nafialovělý; mírně vyčnívá z povrchu artefaktu nebo mince. Srážení mědi ve starověkém stříbře lze použít k datování artefaktů, protože měď je téměř vždy součástí slitin stříbra.[30]
Stříbrný kov je napaden silnými oxidačními činidly, jako jsou manganistan draselný (KMnO
4) a dichroman draselný (K.
2Cr
2Ó
7) a za přítomnosti bromid draselný (KBr). Tyto sloučeniny se používají ve fotografii k bělidlo stříbrné obrázky a převádí je na bromid stříbrný, který lze opravit pomocí thiosíran nebo přestavěn na zesílit původní obrázek. Stříbrné formy kyanid komplexy (kyanid stříbrný ), které jsou rozpustné ve vodě v přítomnosti přebytku kyanidových iontů. Roztoky kyanidu stříbrného se používají v galvanické pokovování stříbra.[31]
Běžný oxidační stavy stříbra jsou (v pořadí obvyklosti): +1 (nejstabilnější stav; například dusičnan stříbrný, AgNO3); +2 (vysoce oxidující; například fluorid stříbrný, AgF2); a dokonce velmi zřídka +3 (extrémně oxidující; například tetrafluoroargentát draselný (III), KAgF4).[32] Stav +1 je zdaleka nejběžnější, následovaný snadno redukovatelným stavem +2. Stav +3 vyžaduje k dosažení velmi silných oxidačních činidel, jako jsou fluor nebo peroxodisíran, a některé sloučeniny stříbra (III) reagují s atmosférickou vlhkostí a napadají sklo.[33] Ve skutečnosti se fluorid stříbrný obvykle získává reakcí stříbra nebo monofluoridu stříbra s nejsilnějším známým oxidačním činidlem, krypton difluorid.[34]
Sloučeniny
Oxidy a chalkogenidy

Stříbro a zlato mají poměrně nízkou hodnotu chemické afinity u kyslíku nižší než měď, a proto se očekává, že oxidy stříbra jsou tepelně docela nestabilní. Rozpustné soli stříbra (I) se vysráží tmavě hnědé oxid stříbrný, Ag2O, po přidání zásady. (Hydroxid AgOH existuje pouze v roztoku; jinak se spontánně rozkládá na oxid.) Oxid stříbrný se velmi snadno redukuje na kovové stříbro a rozkládá se na stříbro a kyslík nad 160 ° C.[35] Tato a další sloučeniny stříbra (I) mohou být oxidovány silným oxidačním činidlem peroxodisíran na černý AgO, smíšený oxid stříbrný (I, III) vzorce AgJáAgIIIÓ2. Některé další smíšené oxidy se stříbrem v neintegrovaných oxidačních stavech, jmenovitě Ag2Ó3 a Ag3Ó4jsou také známé, stejně jako Ag3O, který se chová jako kovový vodič.[35]
Sulfid stříbrný, Ag2S, je velmi snadno vytvořen z jeho základních prvků a je příčinou černé barvy na některých starých stříbrných předmětech. Může být také vytvořen z reakce sirovodík se stříbrným kovem nebo vodným Ag+ ionty. Mnoho nestechiometrických selenidy a teluridy jsou známy; zejména AgTe~3 je nízkoteplotní supravodič.[35]
Halogenidy

Jediný známý dihalogenid stříbra je difluorid, AgF2, které lze získat z prvků za tepla. K syntéze se často používá silné, ale tepelně stabilní a tedy bezpečné fluorační činidlo, fluorid stříbrný (II) uhlovodíky.[36]
V ostrém kontrastu s tím jsou známy všechny čtyři halogenidy stříbra. The fluorid, chlorid, a bromid mají strukturu chloridu sodného, ale jodid má tři známé stabilní formy při různých teplotách; že při pokojové teplotě je kubický směs zinku struktura. Všechny je lze získat přímou reakcí jejich příslušných prvků.[36] Jak halogenová skupina sestupuje, halogenid stříbrný získává stále více kovalentní charakter, rozpustnost klesá a barva se mění z bílého chloridu na žlutý jodid jako energie potřebná pro přenos náboje ligand-kov (X−Ag+ → XAg) klesá.[36] Fluorid je anomální, protože fluoridový iont je tak malý, že má značné množství solvatace energie, a proto je vysoce rozpustný ve vodě a tvoří di- a tetrahydráty.[36] Další tři halogenidy stříbra jsou vysoce nerozpustné ve vodných roztocích a velmi běžně se používají v gravimetrii analytické metody.[18] Všichni čtyři jsou fotocitlivý (ačkoli monofluorid je tak pouze na ultrafialový světlo), zejména bromid a jodid, které se fotodeformují na stříbrný kov, a proto se používaly v tradiční fotografii.[36] Jedná se o reakci:[37]
- X− + hν → X + e− (excitace halogenidového iontu, který se vzdá svého extra elektronu do vodivého pásma)
- Ag+ + e− → Ag (osvobození iontu stříbra, který získá elektron, aby se stal atomem stříbra)
Proces není reverzibilní, protože uvolněný atom stříbra se obvykle nachází na a vada krystalu nebo místo nečistot, takže energie elektronu je snížena natolik, že je „uvězněna“.[37]
Ostatní anorganické sloučeniny

Bílý dusičnan stříbrný, AgNO3, je univerzální předchůdce mnoha dalších sloučenin stříbra, zejména halogenidů, a je mnohem méně citlivý na světlo. Kdysi se to volalo měsíční žíravina protože se volalo stříbro luna starými alchymisty, kteří věřili, že stříbro je spojováno s Měsícem.[38] Často se používá pro gravimetrickou analýzu využívající nerozpustnost těžších halogenidů stříbra, pro které je běžným předchůdcem.[18] Dusičnan stříbrný se v mnoha ohledech používá organická syntéza, např. pro deprotekce a oxidace. Ag+ váže alkeny reverzibilně a k separaci směsí alkenů se selektivně vstřebává dusičnan stříbrný. Výsledný adukt lze rozložit amoniak k uvolnění volného alkenu.[39]
Žlutá uhličitan stříbrný, Ag2CO3 lze snadno připravit reakcí vodných roztoků uhličitan sodný s nedostatkem dusičnanu stříbrného.[40] Jeho hlavní použití je pro výrobu stříbrného prášku pro použití v mikroelektronice. Snižuje se pomocí formaldehyd, produkující stříbro bez alkalických kovů:[41]
- Ag2CO3 + CH2O → 2 Ag + 2 CO2 + H2
Uhličitan stříbrný se také používá jako a činidlo v organické syntéze, jako je Koenigs-Knorrova reakce. V Oxidace fetizonu, uhličitan stříbrný na celit působí jako oxidační činidlo tvořit laktony z dioly. Používá se také k převodu alkyl bromidy do alkoholy.[40]
Stříbro fulminát, AgCNO, výkonný, dotykový explozivní použito v perkusní čepice, se vyrábí reakcí kovového stříbra s kyselinou dusičnou v přítomnosti ethanol. Další nebezpečně výbušné sloučeniny stříbra jsou azid stříbrný, AgN3, vytvořený reakcí dusičnan stříbrný s azid sodný,[42] a acetylid stříbrný, Ag2C2, vznikl při reakci stříbra s acetylén plyn dovnitř amoniak řešení.[26] Ve své nejcharakterističtější reakci se azid stříbrný výbušně rozkládá a uvolňuje plynný dusík: vzhledem k fotocitlivosti solí stříbra může být toto chování vyvoláno zářením světla na jeho krystaly.[26]
- 2 AgN
3 (s) → 3 N
2 (g) + 2 Ag (s)
Koordinační sloučeniny
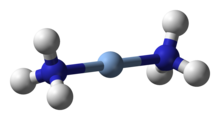
Komplexy stříbra bývají podobné komplexům jeho lehčí homologní mědi. Komplexy stříbra (III) bývají vzácné a velmi snadno se redukují na stabilnější stavy nižší oxidace, i když jsou o něco stabilnější než komplexy mědi (III). Například čtvercový rovinný periodát [Ag (IO5ACH)2]5− a řekněte [Ag {TeO4(ACH)2}2]5− komplexy lze připravit oxidací stříbra (I) zásadou peroxodisíran. Žlutý diamagnetický [AgF4]− je mnohem méně stabilní, kouří ve vlhkém vzduchu a reaguje se sklem.[33]
Komplexy stříbra (II) jsou běžnější. Stejně jako valenční izoelektronické měďnaté komplexy jsou obvykle čtvercové planární a paramagnetické, což je zvýšeno větším štěpením pole pro 4d elektrony než pro 3d elektrony. Vodný Ag2+, vyrobený oxidací Ag+ ozonem, je velmi silným oxidačním činidlem, a to i v kyselých roztocích: je stabilizovaný v kyselina fosforečná kvůli složité tvorbě. Oxidace peroxodisíranu je obecně nezbytná, aby se získaly stabilnější komplexy s heterocyklickými aminy, například [Ag (py)4]2+ a [Ag (bipy)2]2+: jsou stabilní za předpokladu, že protiion nemůže snížit stříbro zpět do +1 oxidačního stavu. [AgF4]2− je také známý ve své fialové barnaté soli, stejně jako některé komplexy stříbra (II) s N- nebo Ó-donorové ligandy, jako jsou pyridinkarboxyláty.[43]
Zdaleka nejdůležitější oxidační stav pro stříbro v komplexech je +1. Ag+ kation je diamagnetický, stejně jako jeho homology Cu+ a Au+, protože všechny tři mají uzavřenou elektronovou konfiguraci bez nepárových elektronů: její komplexy jsou bezbarvé za předpokladu, že ligandy nejsou příliš snadno polarizované, jako například I−. Ag+ tvoří soli s většinou aniontů, ale zdráhá se koordinovat s kyslíkem, a proto je většina těchto solí nerozpustná ve vodě: výjimkou jsou dusičnany, chloristany a fluoridy. Tetracoordinate čtyřboký vodný iont [Ag (H2Ó)4]+ je známa, ale charakteristická geometrie pro Ag+ kation je 2-souřadnicový lineární. Například chlorid stříbrný se snadno rozpouští v přebytku vodného amoniaku za vzniku [Ag (NH3)2]+; soli stříbra jsou rozpuštěny ve fotografii v důsledku tvorby komplexu thiosíranu [Ag (S2Ó3)2]3−; a kyanid těžba stříbrných (a zlatých) děl vznikem komplexu [Ag (CN)2]−. Kyanid stříbrný tvoří lineární polymer {Ag – C≡N → Ag – C≡N →}; stříbrný thiokyanát má podobnou strukturu, ale místo toho vytváří cikcak kvůli sp3-hybridizováno atom síry. Chelatující ligandy nejsou schopni tvořit lineární komplexy a komplexy stříbra (I) s nimi mají tendenci tvořit polymery; existuje několik výjimek, například téměř čtyřboká difosfin a průjm komplexy [Ag (L – L)2]+.[44]
Organokovový
Za standardních podmínek stříbro nevytváří jednoduché karbonyly, kvůli slabosti vazby Ag – C. Několik je známo při velmi nízkých teplotách kolem 6–15 K, například zelený, planární paramagnetický Ag (CO)3, který dimerizuje na 25–30 K, pravděpodobně vytvořením vazeb Ag – Ag. Dále, karbonyl stříbra [Ag (CO)] [B (OTeF5)4] je známo. Polymerní AgLX komplexy s alkeny a alkyny jsou známé, ale jejich vazby jsou termodynamicky slabší než dokonce vazby Platina komplexy (i když se vytvářejí snadněji než komplexy analogických komplexů zlata): jsou také docela nesymetrické a ukazují slabé π vazba ve skupině 11. Ag – C σ vazby mohou být také tvořeny stříbrem (I), jako je měď (I) a zlato (I), ale jednoduché alkyly a aryly stříbra (I) jsou ještě méně stabilní než ty, které mají měď (I) (které mají tendenci explodovat pod okolní podmínky). Například špatná tepelná stabilita se odráží v relativních teplotách rozkladu AgMe (-50 ° C) a CuMe (-15 ° C), jakož i teplotách PhAg (74 ° C) a PhCu (100 ° C).[45]
Vazba C – Ag je stabilizována perfluoralkyl ligandy, například v AgCF (CF3)2.[46] Alkenylsilverové sloučeniny jsou také stabilnější než jejich protějšky s alkylsilverem.[47] Stříbrný-NHC komplexy se snadno připravují a běžně se používají k přípravě dalších NHC komplexů vytěsňováním labilních ligandů. Například reakce komplexu bis (NHC) stříbro (I) s bis (acetonitril) palladium dichlorid nebo chlorido (dimethylsulfid) zlato (I):[48]
Intermetalické

Stříbrné formy slitiny s většinou ostatních prvků v periodické tabulce. Prvky ze skupin 1–3, s výjimkou vodík, lithium, a berylium, jsou velmi dobře mísitelné se stříbrem v kondenzované fázi a tvoří intermetalické sloučeniny; ti ze skupin 4–9 jsou jen špatně mísitelní; prvky ve skupinách 10–14 (kromě bór a uhlík ) mají velmi složité fázové diagramy Ag – M a tvoří komerčně nejdůležitější slitiny; a zbývající prvky v periodické tabulce nemají konzistenci ve svých fázových diagramech Ag – M. Zdaleka nejdůležitější jsou takové slitiny s mědí: většina stříbra používaného pro ražení mincí a šperků je ve skutečnosti slitina stříbra a mědi a eutektická směs se používá ve vakuu tvrdé pájení. Tyto dva kovy jsou zcela mísitelné jako kapaliny, ale ne jako pevné látky; jejich význam v průmyslu vychází ze skutečnosti, že jejich vlastnosti mají tendenci být vhodné v širokém rozmezí variací v koncentraci stříbra a mědi, ačkoli nejužitečnější slitiny mají tendenci být bohatší na stříbro než eutektická směs (71,9% stříbra a 28,1% mědi 60,1% stříbra a 28,1% mědi podle atomu).[49]
Většina ostatních binárních slitin je málo použitelná: například slitiny stříbra a zlata jsou příliš měkké a stříbrné -kadmium slitiny příliš toxické. Ternární slitiny mají mnohem větší význam: zubní amalgámy jsou to obvykle slitiny stříbro – cín – rtuť, slitiny stříbro – měď – zlato jsou v klenotnictví velmi důležité (obvykle na straně bohaté na zlato) a mají širokou škálu tvrdostí a barev, slitiny stříbro – měď – zinek jsou užitečné jako nízko- tavení slitin pro tvrdé pájení a stříbro – kadmium–indium (zahrnující tři sousední prvky v periodické tabulce) je užitečné v jaderné reaktory kvůli jeho vysokému zachycení tepelných neutronů průřez, dobré vedení tepla, mechanická stabilita a odolnost proti korozi v horké vodě.[49]
Etymologie
Slovo „stříbro“ se objevuje v Stará angličtina v různých hláskováních, jako např seolfor a siolfor. to je příbuzný s Stará vysoká němčina silabar; gotický silubr; nebo Stará norština silfr, vše nakonec pochází z Proto-germánský * silubra. The Balto-slovanský slova pro stříbro jsou spíše podobná germánským (např. ruština серебро [serebró], polština srebro, Litevský sidãbras), stejně jako Keltiberský formulář silabur. Mohou mít společný indoevropský původ, i když jejich morfologie spíše naznačuje neindoevropský Wanderwort.[50][51] Někteří vědci proto navrhli a Paleo-hispánský původ, ukazující na Baskičtina formulář zilharr jako důkaz.[52]
Chemický symbol Ag pochází z latinský slovo pro „stříbro“, argentum (porovnej Starořečtina ἄργυρος, árgyros), z Protoindoevropský kořen *h₂erǵ- (dříve rekonstruovaný jako * arǵ-), což znamená „bílý“ nebo „zářící“. Toto bylo obvyklé protoindoevropské slovo pro kov, jehož reflexy chybí v germánštině a balto-slovanštině.[51]
Dějiny

Silver byl jedním ze sedmi kovy starověku které byly známé prehistorickým lidem a jejichž objev se tak ztratil v historii.[53] Zejména tři kovy skupiny 11, měď, stříbro a zlato, se vyskytují v elementární forma v přírodě a byly pravděpodobně používány jako první primitivní formy peníze na rozdíl od jednoduchého směnného obchodu.[54] Na rozdíl od mědi však stříbro nevedlo k růstu hutnictví kvůli jeho nízké strukturální pevnosti a byl častěji používán ornamentálně nebo jako peníze.[55] Vzhledem k tomu, že stříbro je reaktivnější než zlato, byly zásoby nativního stříbra mnohem omezenější než zásoby zlata.[54] Například stříbro bylo v Egyptě dražší než zlato až do 15. století před naším letopočtem:[56] předpokládá se, že Egypťané oddělili zlato od stříbra zahřátím kovů solí a následným redukcí chlorid stříbrný vyrobené na kov.[57]
Situace se změnila objevem cupellation, technika, která umožňovala získat stříbrný kov z jeho rud. Zatímco struska hromady nalezené v Malá Asie a na ostrovech Egejské moře naznačují, že se stříbro oddělovalo od Vést již v 4. tisíciletí před naším letopočtem,[7] a jedním z prvních středisek těžby stříbra v Evropě bylo Sardinie na začátku Chalcolithic období,[58] tyto techniky se široce rozšířily až později, kdy se rozšířily po celém regionu i mimo něj.[56] Počátky výroby stříbra v roce 2006 Indie, Čína, a Japonsko byly téměř jistě stejně staré, ale kvůli svému vysokému věku nejsou dobře zdokumentovány.[57]

Když Féničané nejprve přišel k tomu, co je nyní Španělsko, získali tolik stříbra, že to všechno na své lodě nevejde, a ve výsledku místo stříbra použili olovo ke zvážení svých kotev.[56] V době řecké a římské civilizace byly stříbrné mince základem ekonomiky:[54] Řekové už těžili stříbro galenit v 7. století před naším letopočtem,[56] a vzestup Athény bylo částečně umožněno blízkými stříbrnými doly v Laurium, z nichž vytěžili asi 30 tun ročně od roku 600 do roku 300 před naším letopočtem.[59] Stabilita Římská měna spoléhal do značné míry na dodávky stříbrných prutů, převážně ze Španělska, které Římští horníci vyrobeno v měřítku, které před rokem nemělo obdoby objev Nového světa. Dosažení špičkové produkce 200 tun ročně obíhalo odhadované zásoby stříbra 10 000 tun Římská ekonomika v polovině druhého století našeho letopočtu pětkrát až desetkrát větší než kombinované množství stříbra, které má k dispozici středověká Evropa a Abbasid Caliphate kolem 800 nl[60][61] Ve stejném časovém období zaznamenali Římané také těžbu stříbra ve střední a severní Evropě. Tato výroba se téměř úplně zastavila s pádem Římské říše, aby se obnovila až v době Karel Veliký: do té doby již byly vytěženy desítky tisíc tun stříbra.[57]
Střední Evropa se během roku 2006 stala centrem produkce stříbra Středověk, protože středomořská ložiska využívaná starými civilizacemi byla vyčerpána. V roce byly otevřeny stříbrné doly Čechy, Sasko, Krušné hory, Alsasko, Lahn kraj, Siegerland, Slezsko, Maďarsko, Norsko, Steiermark, Salzburg a jižní Černý les. Většina z těchto rud byla docela bohatá na stříbro a bylo možné je jednoduše ručně oddělit od zbývající skály a poté roztavit; vyskytly se také některé vklady nativního stříbra. Mnoho z těchto dolů bylo brzy vyčerpáno, ale několik z nich zůstalo aktivní až do Průmyslová revoluce, předtím se světová produkce stříbra pohybovala kolem skromných 50 tun ročně.[57] V Americe vysokoteplotní olovo cupellation technologie byla vyvinuta civilizacemi před Inky již v letech 60–120 nl; Během této doby se nadále těžila ložiska stříbra v Indii, Číně, Japonsku a předkolumbovské Americe.[57][62]
S objevením Ameriky a drancováním stříbra španělskými dobyvateli se Střední a Jižní Amerika stala dominantními producenty stříbra až do začátku 18. století, zejména Peru, Bolívie, Chile, a Argentina:[57] poslední z těchto zemí se později pojmenovala podle kovu, který tvořil tolik minerálního bohatství.[59] Obchod se stříbrem ustoupil globální síti směny. Jak řekl jeden historik, stříbro „obletělo svět a rozběhlo svět“.[63] Velká část tohoto stříbra skončila v rukou Číňanů. Portugalský obchodník v roce 1621 poznamenal, že stříbro „putuje po celém světě ... předtím, než se vrhlo do Číny, kde zůstává jako ve svém přirozeném středu“.[64] Hodně z toho přesto šlo do Španělska, což španělským vládcům umožnilo sledovat vojenské a politické ambice v Evropě i v Americe. „Doly Nového světa,“ uzavřelo několik historiků, „podporovaly španělskou říši.“[65]
V 19. století se primární produkce stříbra přesunula zejména do Severní Ameriky Kanada, Mexiko, a Nevada v Spojené státy: určitá druhotná výroba z rud olova a zinku probíhala také v Evropě a ložiska v Sibiř a Ruský Dálný východ stejně jako v Austrálie byly těženy.[57] Polsko se objevil jako významný producent v 70. letech po objevu ložisek mědi bohatých na stříbro, než se centrum výroby v následujícím desetiletí vrátilo do Ameriky. Dnes jsou Peru a Mexiko stále mezi primárními producenty stříbra, ale distribuce produkce stříbra po celém světě je poměrně vyvážená a zhruba pětina nabídky stříbra pochází z recyklace místo nové produkce.[57]

Proto-Elamite klečící býk, který držel chrlenou nádobu; 3100–2900 př.nl; 16,3 x 6,3 x 10,8 cm; Metropolitní muzeum umění (New York City)

Staroegyptský figurka z Horus jako bůh sokola s egyptskou korunou; asi 500 před naším letopočtem; stříbro a elektrum; výška: 26,9 cm; Staatliche Sammlung für Ägyptische Kunst (Mnichov, Německo)

Starořečtina tetradrachm; 315–308 př. průměr: 2,7 cm; Metropolitní muzeum umění

Starogrécká pozlacená mísa; 2. – 1. Století před naším letopočtem; výška: 7,6 cm, rozměr: 14,8 cm; Metropolitní muzeum umění

římský talíř; 1. – 2. Století nl; výška: 0,1 cm, průměr: 12,7 cm; Metropolitní muzeum umění

Římská busta z Serapis; 2. století; 15,6 x 9,5 cm; Metropolitní muzeum umění

Ušní umyvadlo se scénami z příběhu Diany a Actaeona; 1613; délka: 50 cm, výška: 6 cm, šířka: 40 cm; Rijksmuseum (Amsterdam, Holandsko )

francouzština Rokoko mísa; 1749; výška: 26,3 cm, šířka: 39 cm, hloubka: 24 cm; Metropolitní muzeum umění

Francouzská rokoková káva; 1757; výška: 29,5 cm; Metropolitní muzeum umění

francouzština Neoklasicistní konev; 1784–1785; výška: 32,9 cm; Metropolitní muzeum umění

Neo-rokoko konvice na kávu; 1845; celkově: 32 x 23,8 x 15,4 cm; Cleveland Museum of Art (Cleveland, Ohio, USA)

francouzština secese dezertní lžíce; kolem roku 1890; Cooper Hewitt, Smithsonian Design Museum (New York City)

Secese jardinière; kolem 1905–1910; výška: 22 cm, šířka: 47 cm, hloubka: 22,5 cm; Cooper Hewitt, Smithsonian Design Museum

Ruční zrcátko; 1906; výška: 20,7 cm, hmotnost: 88 g; Rijksmuseum (Amsterdam, Holandsko )
Symbolická role

Silver hraje určitou roli v mytologii a našel různé využití jako metafora a ve folklóru. Řecký básník Hesiod je Práce a dny (řádky 109–201) uvádí různé věky člověka pojmenoval podle kovů, jako je zlato, stříbro, bronz a železo, aby vysvětlil po sobě jdoucí věky lidstva.[66] Ovid je Proměny obsahuje další převyprávění příběhu, obsahující ilustraci metaforického použití stříbra znamenat druhého nejlepšího v sérii, lepší než bronz, ale horší než zlato:
Ale když je to dobré Saturn, banish'd shora,
Byl jel do pekla, svět byl pod Jove.
Hle, úspěšná doba stříbrného věku,
Vynikající mosaz, ale ještě lepší než zlato.— Ovid, Proměny, Book I, trans. John Dryden
Ve folklóru se často myslelo, že stříbro má mystické síly: například a kulka odlitá ze stříbra je v takovém folklóru často považována za jedinou zbraň, která je účinná proti vlkodlak, čarodějnice, nebo jiný příšery.[67][68][69] Z toho je idiom a stříbrná kulka rozvinutý do obrazného odkazu na jakékoli jednoduché řešení s velmi vysokou účinností nebo téměř zázračnými výsledky, jak je široce diskutováno softwarové inženýrství papír Žádná stříbrná kulka.[70] Mezi další pravomoci připisované stříbře patří detekce jedu a usnadnění průchodu do bájná říše víl.[69]
Výroba stříbra také inspirovala obrazný jazyk. Jasné odkazy na kupelaci se vyskytují v celém Starý zákon z bible, například v Jeremiáš Napomenutí Judy: „Měchy jsou spáleny, olovo je pohlceno ohněm; zakladatel se marně rozplývá; bezbožní nejsou vytrženi. Zatracené stříbro je lidé budou nazývat, protože je Pán zavrhl.“ (Jeremjáš 6: 19–20) Jeremjáš si byl také vědom plechového stříbra, což ilustruje tvárnost a tažnost kovu: „Stříbro roztažené do desek je přineseno z Taršíše a zlato z Uphazu, práce dělníka a rukou zakladatele: jejich oděvy jsou modrá a fialová: všechny jsou dílem mazaných mužů. “ (Jeremjáš 10: 9)[56]
Stříbro má také negativnější kulturní významy: idiom třicet kusů stříbra, odkazující na odměnu za zradu, odkazuje na úplatek Jidáš Iškariotský je řečeno v Nový zákon vzít od židovských vůdců v Jeruzalém otočit Ježíš z Nazaretu k vojákům velekněze Kaifáše.[71] Z etického hlediska také stříbro symbolizuje chamtivost a degradaci vědomí; to je negativní aspekt, zvrácení jeho hodnoty.[72]
Výskyt a výroba
Množství stříbra v zemské kůře je 0,08Díly na milión, téměř přesně stejné jako u rtuť. Většinou se vyskytuje v sulfid zejména rudy akantit a argentit, Ag2Vklady S. Argentite někdy také obsahují rodák stříbro, když se vyskytují v redukčním prostředí, a při kontaktu se slanou vodou se přemění na chlorgyrit (počítaje v to roh stříbro ), AgCl, který převládá v Chile a Nový Jížní Wales.[73] Většina ostatních minerálů stříbra je stříbro pnictides nebo chalkogenidy; jsou to obecně lesklé polovodiče. Většina skutečných ložisek stříbra, na rozdíl od stříbrných ložisek jiných kovů, pocházela z Terciární období vulkanismus.[74]
Hlavním zdrojem stříbra jsou rudy mědi, mědi a niklu, olova a olova a zinku získané z Peru, Bolívie, Mexiko, Čína, Austrálie, Chile, Polsko a Srbsko.[7] Peru, Bolívie a Mexiko těží stříbro od roku 1546 a stále jsou významnými světovými producenty. Nejlepší doly produkující stříbro jsou Cannington (Austrálie), Fresnillo (Mexiko), San Cristóbal (Bolívie), Antamina (Peru), Rudna (Polsko) a Penasquito (Mexiko).[75] Nejlepší krátkodobé projekty rozvoje dolů do roku 2015 jsou Pascua Lama (Chile), Navidad (Argentina), Ja Municipio (Mexiko), Malku Khota (Bolívie),[76] a Hackett River (Kanada).[75] v Střední Asie, Tádžikistán je známo, že má jedny z největších ložisek stříbra na světě.[77]
Stříbro se obvykle vyskytuje v přírodě v kombinaci s jinými kovy nebo v minerálech, které obsahují sloučeniny stříbra, obvykle ve formě sulfidy jako galenit (sulfid olovnatý) nebo cerussit (uhličitan olovnatý). Takže primární produkce stříbra vyžaduje tavení a poté cupellation stříbrných olovnatých rud, historicky důležitý proces.[78] Olovo se taví při 327 ° C, oxid olovnatý při 888 ° C a stříbro se taví při 960 ° C. K oddělení stříbra se slitina znovu taví při vysoké teplotě 960 ° C až 1 000 ° C v oxidačním prostředí. Olovo oxiduje na oxid olovnatý, pak známý jako litarge, který zachycuje kyslík z ostatních přítomných kovů. Kapalný oxid olovnatý je odstraněn nebo absorbován kapilární akce do obložení krbu.[79][80][81]
- Ag(s) + 2Pb(s) + Ó
2(g) → 2PbO(absorbováno) + Ag (l)
Dnes je stříbrný kov primárně vyráběn místo toho jako sekundární vedlejší produkt elektrolytický rafinace mědi, olova a zinku a aplikací Parkesův proces na olověném slitku z rudy, který obsahuje také stříbro.[82] V takových procesech stříbro sleduje dotyčný neželezný kov prostřednictvím jeho koncentrace a tavení a je později vyčištěno. Například při výrobě mědi je čištěná měď elektrolyticky usazené na katodě, zatímco méně reaktivní drahé kovy, jako je stříbro a zlato, se shromažďují pod anodou jako takzvaný „anodový sliz“. Ten se potom oddělí a čistí od obecných kovů působením zředěného horkým vzduchem sírová kyselinou a zahříváním pomocí toku vápna nebo oxidu křemičitého, než se stříbro vyčistí na více než 99,9% čistotu elektrolýzou dusičnan řešení.[73]
Jemné stříbro komerční kvality má čistotu nejméně 99,9% a čistoty vyšší než 99,999%. V roce 2014 bylo Mexiko největším producentem stříbra (5 000 tun nebo 18,7% z celkové světové hodnoty 26 800 t), následovaná Čínou (4 060 t) a Peru (3 780 t).[82]
V mořském prostředí
Koncentrace stříbra je nízká mořská voda (pmol / l). Úrovně se liší podle hloubky a mezi vodními útvary. Koncentrace rozpuštěného stříbra se pohybují od 0,3 pmol / lv pobřežních povrchových vodách do 22,8 pmol / lv pelagických hlubinách.[83] Analýza přítomnosti a dynamiky stříbra v mořském prostředí je obtížná kvůli těmto zvláště nízkým koncentracím a složitým interakcím v životním prostředí.[84] Ačkoli jde o vzácný stopový kov, jeho koncentrace jsou značně ovlivněny fluviálními, aeolickými, atmosférickými a nadpřirozenými vstupy, jakož i antropogenními vstupy prostřednictvím vypouštění, likvidace odpadu a emisí průmyslových společností.[85][86] Other internal processes such as decomposition of organic matter may be a source of dissolved silver in deeper waters, which feeds into some surface waters through upwelling and vertical mixing.[86]
In the Atlantic and Pacific, silver concentrations are minimal at the surface but rise in deeper waters.[87] Silver is taken up by plankton in the photic zone, remobilized with depth, and enriched in deep waters. Silver is transported from the Atlantic to the other oceanic water masses.[85] In North Pacific waters, silver is remobilized at a slower rate and increasingly enriched compared to deep Atlantic waters. Silver has increasing concentrations that follow the major oceanic conveyor belt that cycles water and nutrients from the North Atlantic to the South Atlantic to the North Pacific.[88]
There is not an extensive amount of data focused on how marine life is affected by silver despite the likely deleterious effects it could have on organisms through bioakumulace, association with particulate matters, and sorpce.[83] Not until about 1984 did scientists begin to understand the chemical characteristics of silver and the potential toxicity. Ve skutečnosti, rtuť is the only other trace metal that surpasses the toxic effects of silver; however, the full extent of silver toxicity is not expected in oceanic conditions because of its ability to transfer into nonreactive biological compounds.[89]
In one study, the presence of excess ionic silver and silver nanoparticles caused bioaccumulation effects on zebrafish organs and altered the chemical pathways within their gills.[90] In addition, very early experimental studies demonstrated how the toxic effects of silver fluctuate with salinity and other parameters, as well as between life stages and different species such as finfish, molluscs, and crustaceans.[91] Another study found raised concentrations of silver in the muscles and liver of dolphins and whales, indicating pollution of this metal within recent decades. Silver is not an easy metal for an organism to eliminate and elevated concentrations can cause death.[92]
Monetary use

The earliest known coins were minted in the kingdom of Lýdie v Malá Asie kolem roku 600 př. n.l.[93] The coins of Lydia were made of elektrum, which is a naturally occurring slitina of gold and silver, that was available within the territory of Lydia.[93] Od té doby, stříbrné standardy, in which the standard economic zúčtovací jednotka is a fixed weight of silver, have been widespread throughout the world until the 20th century. Pozoruhodný stříbrné mince through the centuries include the Řecká drachma,[94] Říman denár,[95] the Islamic dirham,[96] the karshapana from ancient India and rupie od doby Mughalská říše (grouped with copper and gold coins to create a trimetallic standard),[97] a Španělský dolar.[98][99]
The ratio between the amount of silver used for coinage and that used for other purposes has fluctuated greatly over time; for example, in wartime, more silver tends to have been used for coinage to finance the war.[100]
Today, silver bullion has the ISO 4217 currency code XAG, one of only four drahé kovy to have one (the others being palladium, Platina, and gold).[101] Silver coins are produced from cast rods or ingots, rolled to the correct thickness, heat-treated, and then used to cut mezery z. These blanks are then milled and minted in a coining press; modern coining presses can produce 8000 silver coins per hour.[100]
Cena
Silver prices are normally quoted in trojských uncí. One troy ounce is equal to 31.1034768 grams. The London silver fix is published every working day at noon London time.[102] This price is determined by several major international banks and is used by London bullion market members for trading that day. Prices are most commonly shown as the americký dolar (USD), the Libra šterlinků (GBP), and the Euro (EUR).
Aplikace
Jewellery and silverware


The major use of silver besides coinage throughout most of history was in the manufacture of šperky and other general-use items, and this continues to be a major use today. Mezi příklady patří table silver for cutlery, for which silver is highly suited due to its antibacterial properties. Západní koncertní flétny are usually plated with or made out of mincovní stříbro;[104] in fact, most silverware is only silver-plated rather than made out of pure silver; the silver is normally put in place by galvanické pokovování. Silver-plated glass (as opposed to metal) is used for mirrors, vacuum flasks, and Christmas tree decorations.[105]
Because pure silver is very soft, most silver used for these purposes is alloyed with copper, with finenesses of 925/1000, 835/1000, and 800/1000 being common. One drawback is the easy tarnishing of silver in the presence of sirovodík a jeho deriváty. Including precious metals such as palladium, platinum, and gold gives resistance to tarnishing but is quite costly; obecné kovy jako zinek, kadmium, křemík, a germanium do not totally prevent corrosion and tend to affect the lustre and colour of the alloy. Electrolytically refined pure silver plating is effective at increasing resistance to tarnishing. The usual solutions for restoring the lustre of tarnished silver are dipping baths that reduce the silver sulfide surface to metallic silver, and cleaning off the layer of tarnish with a paste; the latter approach also has the welcome side effect of polishing the silver concurrently.[104] A simple chemical approach to removal of the sulfide tarnish is to bring silver items into contact with aluminium foil whilst immersed in water containing a conducting salt, such as sodium chloride.[Citace je zapotřebí ]
Lék
In medicine, silver is incorporated into wound dressings and used as an antibiotic coating in medical devices. Wound dressings containing sulfadiazin stříbrný nebo silver nanomaterials are used to treat external infections. Silver is also used in some medical applications, such as močové katétry (where tentative evidence indicates it reduces catheter-related infekce močového ústrojí ) a dovnitř endotracheal breathing tubes (where evidence suggests it reduces ventilator-associated zápal plic ).[106][107] Stříbro ion je bioaktivní and in sufficient koncentrace readily kills bakterie in vitro. Silver ions interfere with enzymes in the bacteria that transport nutrients, form structures, and synthesise cell walls; these ions also bond with the bacteria's genetic material. Silver and silver nanoparticles are used as an antimicrobial in a variety of industrial, healthcare, and domestic application: for example, infusing clothing with nanosilver particles thus allows them to stay odourless for longer.[108][109] Bacteria can, however, develop resistance to the antimicrobial action of silver.[110] Silver compounds are taken up by the body like rtuť compounds, but lack the toxicity of the latter. Silver and its alloys are used in cranial surgery to replace bone, and silver–tin–mercury amalgams are used in dentistry.[105] Fluorid diaminu stříbrného, the fluoride salt of a koordinační komplex with the formula [Ag(NH3)2]F, is a topical medicament (drug) used to treat and prevent zubní kaz (cavities) and relieve dentinal hypersensitivity.[111]
Elektronika
Silver is very important in electronics for conductors and electrodes on account of its high electrical conductivity even when tarnished. Bulk silver and silver foils were used to make vacuum tubes, and continue to be used today in the manufacture of semiconductor devices, circuits, and their components. For example, silver is used in high quality connectors for RF, VHF, and higher frequencies, particularly in tuned circuits such as cavity filters where conductors cannot be scaled by more than 6%. Tištěné obvody a RFID antennas are made with silver paints,[7][112] Powdered silver and its alloys are used in paste preparations for conductor layers and electrodes, ceramic capacitors, and other ceramic components.[113]
Brazing alloys
Silver-containing tvrdé pájení alloys are used for brazing metallic materials, mostly kobalt, nikl, and copper-based alloys, tool steels, and precious metals. The basic components are silver and copper, with other elements selected according to the specific application desired: examples include zinc, tin, cadmium, palladium, mangan, a fosfor. Silver provides increased workability and corrosion resistance during usage.[114]
Chemical equipment
Silver is useful in the manufacture of chemical equipment on account of its low chemical reactivity, high thermal conductivity, and being easily workable. stříbrný kelímky (alloyed with 0.15% nickel to avoid recrystallisation of the metal at red heat) are used for carrying out alkaline fusion. Copper and silver are also used when doing chemistry with fluor. Equipment made to work at high temperatures is often silver-plated. Silver and its alloys with gold are used as wire or ring seals for oxygen compressors and vacuum equipment.[115]
Katalýza
Silver metal is a good catalyst for oxidace reactions; in fact it is somewhat too good for most purposes, as finely divided silver tends to result in complete oxidation of organic substances to oxid uhličitý and water, and hence coarser-grained silver tends to be used instead. For instance, 15% silver supported on α-Al2Ó3 or silicates is a catalyst for the oxidation of ethylen na ethylenoxid at 230–270 °C. Dehydrogenation of methanolu na formaldehyd is conducted at 600–720 °C over silver gauze or crystals as the catalyst, as is dehydrogenation of isopropanol na aceton. In the gas phase, glykol výnosy glyoxal a ethanol výnosy acetaldehyd, while organic aminy are dehydrated to nitrily.[115]
Fotografování
The photosensitivity of the silver halides allowed for their use in traditional photography, although digital photography, which does not use silver, is now dominant. The photosensitive emulsion used in black-and-white photography is a suspension of silver halide crystals in gelatin, possibly mixed in with some noble metal compounds for improved photosensitivity, developing, and tuning. Colour photography requires the addition of special dye components and sensitisers, so that the initial black-and-white silver image couples with a different dye component. The original silver images are bleached off and the silver is then recovered and recycled. Silver nitrate is the starting material in all cases.[116]
The use of silver nitrate and silver halides in photography has rapidly declined with the advent of digital technology. From the peak global demand for photographic silver in 1999 (267,000,000 trojských uncí or 8304.6 metrických tun ) the market contracted almost 70% by 2013.[117]
Nanočástice
Nanosilver particles, between 10 and 100 nanometres in size, are used in many applications. They are used in conductive inks for printed electronics, and have a much lower melting point than larger silver particles of micrometre size. They are also used medicinally in antibacterials and antifungals in much the same way as larger silver particles.[109] Navíc podle European Union Observatory for Nanomaterials (EUON), silver nanoparticles are used both in pigments, as well as cosmetics.[118][119]
Různé

Pure silver metal is used as a food colouring. Má to E174 designation and is approved in the Evropská unie.[120] Traditional Pakistani and Indian dishes sometimes include decorative silver foil known as vark,[121] and in various other cultures, silver dražé are used to decorate cakes, cookies, and other dessert items.[122]
Photochromic lenses include silver halides, so that ultraviolet light in natural daylight liberates metallic silver, darkening the lenses. The silver halides are reformed in lower light intensities. Colourless silver chloride films are used in radiation detectors. Zeolit sieves incorporating Ag+ ions are used to desalinate seawater during rescues, using silver ions to precipitate chloride as silver chloride. Silver is also used for its antibacterial properties for water sanitisation, but the application of this is limited by limits on silver consumption. Koloidní stříbro is similarly used to disinfect closed swimming pools; while it has the advantage of not giving off a smell like chlornan treatments do, colloidal silver is not effective enough for more contaminated open swimming pools. Malý jodid stříbrný crystals are used in cloud setí to cause rain.[109]
Opatření
| Nebezpečí | |
|---|---|
| Piktogramy GHS |  |
| Signální slovo GHS | Varování |
| H410 | |
| P273, P391, P501[123] | |
| NFPA 704 (ohnivý diamant) | |
Silver compounds have low toxicity compared to those of most other těžké kovy, as they are poorly absorbed by the human body when digested, and that which does get absorbed is rapidly converted to insoluble silver compounds or complexed by metalothionein. However, silver fluoride and silver nitrate are caustic and can cause tissue damage, resulting in gastroenteritida, průjem, falling krevní tlak, cramps, paralysis, and zástava dechu. Animals repeatedly dosed with silver salts have been observed to experience anémie, slowed growth, necrosis of the liver, and fatty degeneration of the liver and kidneys; rats implanted with silver foil or injected with koloidní stříbro have been observed to develop localised tumours. Parenterálně admistered colloidal silver causes acute silver poisoning.[124] Some waterborne species are particularly sensitive to silver salts and those of the other precious metals; in most situations, however, silver does not pose serious environmental hazards.[124]
In large doses, silver and compounds containing it can be absorbed into the oběhový systém and become deposited in various body tissues, leading to argyria, which results in a blue-grayish pigmentation of the skin, eyes, and sliznice. Argyria is rare, and so far as is known, does not otherwise harm a person's health, though it is disfiguring and usually permanent. Mild forms of argyria are sometimes mistaken for cyanóza.[124][7]
Metallic silver, like copper, is an antibacterial agent, which was known to the ancients and first scientifically investigated and named the oligodynamic effect podle Carl Nägeli. Silver ions damage the metabolism of bacteria even at such low concentrations as 0.01–0.1 milligrams per litre; metallic silver has a similar effect due to the formation of silver oxide. This effect is lost in the presence of síra due to the extreme insolubility of silver sulfide.[124]
Some silver compounds are very explosive, such as the nitrogen compounds silver azide, silver amide, and silver fulminate, as well as acetylid stříbrný, silver oxalate, and silver(II) oxide. They can explode on heating, force, drying, illumination, or sometimes spontaneously. To avoid the formation of such compounds, ammonia and acetylén should be kept away from silver equipment. Salts of silver with strongly oxidising acids such as silver chlorate and silver nitrate can explode on contact with materials that can be readily oxidised, such as organic compounds, sulfur and soot.[124]
Viz také
- Stříbrná mince
- Stříbrná medaile
- Zdarma stříbro
- Seznam zemí podle produkce stříbra
- List of silver compounds
- Stříbro jako investice
- Silverpoint výkres
Reference
- ^ Meija, Juris; et al. (2016). „Atomic weights of the elements 2013 (IUPAC Technical Report)“. Čistá a aplikovaná chemie. 88 (3): 265–91. doi:10.1515 / pac-2015-0305.
- ^ Lide, D. R., ed. (2005). "Magnetic susceptibility of the elements and inorganic compounds". CRC Handbook of Chemistry and Physics (PDF) (86. vydání). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. pp. E110. ISBN 0-8493-0464-4.
- ^ "Bullion vs. Numismatic Coins: Difference between Bullion and Numismatic Coins". www.providentmetals.com. Citováno 17. prosince 2017.
- ^ "'World has 5 times more gold than silver' | Nejnovější zprávy a aktualizace na Daily News & Analysis “. dna. 3. března 2009. Citováno 17. prosince 2017.
- ^ Masuda, Hideki (2016). „Kombinovaná přenosová elektronová mikroskopie - pozorování procesu formování na místě a měření fyzikálních vlastností kovových drátů s jednou atomovou velikostí na místě“. V Janeček, Miloš; Kral, Robert (eds.). Moderní elektronová mikroskopie ve fyzikálních a biologických vědách. InTech. doi:10.5772/62288. ISBN 978-953-51-2252-4.
- ^ A b C d E F G Hammond, C. R. (2004). The Elements, in Handbook of Chemistry and Physics (81. vydání). CRC tisk. ISBN 978-0-8493-0485-9.
- ^ A b C d E Greenwood a Earnshaw, str. 1177
- ^ A b Greenwood a Earnshaw, str. 1178
- ^ George L. Trigg; Edmund H. Immergut (1992). Encyclopedia of applied physics. 4: Combustion to Diamagnetism. VCH Publishers. pp. 267–72. ISBN 978-3-527-28126-8. Citováno 2. května 2011.
- ^ Alex Austin (2007). The Craft of Silversmithing: Techniques, Projects, Inspiration. Sterling Publishing Company, Inc. str. 43. ISBN 978-1-60059-131-0.
- ^ Edwards, H.W.; Petersen, R.P. (1936). "Reflectivity of evaporated silver films". Fyzický přehled. 50 (9): 871. Bibcode:1936PhRv...50..871E. doi:10.1103/PhysRev.50.871.
- ^ "Silver vs. Aluminum". Observatoř Gemini. Citováno 1. srpna 2014.
- ^ Russell AM & Lee KL 2005, Strukturně-vlastnické vztahy v neželezných kovech, Wiley-Interscience, New York, ISBN 0-471-64952-X. str. 302.
- ^ Nichols, Kenneth D. (1987). The Road to Trinity. Morrow, NY: Morrow. str. 42. ISBN 978-0-688-06910-0.
- ^ Young, Howard (11 September 2002). "Eastman at Oak Ridge During World War II". Archivovány od originál dne 8. února 2012.
- ^ Oman, H. (1992). "Not invented here? Check your history". Aerospace and Electronic Systems Magazine. 7 (1): 51–53. doi:10.1109/62.127132. S2CID 22674885.
- ^ A b C d "Atomic Weights of the Elements 2007 (IUPAC)". Archivovány od originál dne 6. září 2017. Citováno 11. listopadu 2009.
- ^ "Atomic Weights and Isotopic Compositions for All Elements (NIST)". Citováno 11. listopadu 2009.
- ^ Cameron, A.G.W. (1973). „Hojnost prvků ve sluneční soustavě“ (PDF). Recenze vesmírných věd. 15 (1): 121–46. Bibcode:1973SSRv ... 15..121C. doi:10.1007 / BF00172440. S2CID 120201972.
- ^ A b Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "PakUBASE hodnocení jaderných a rozpadových vlastností ", Jaderná fyzika A, 729: 3–128, Bibcode:2003NuPhA.729 ... 3A, doi:10.1016 / j.nuclphysa.2003.11.001
- ^ "Atomic Weights and Isotopic Compositions for Silver (NIST)". Citováno 11. listopadu 2009.
- ^ Kelly, William R .; Wasserburg, G. J. (1978). „Důkazy o existenci 107Pd in the early solar system" (PDF). Dopisy o geofyzikálním výzkumu. 5 (12): 1079–82. Bibcode:1978GeoRL ... 5,1079 tis. doi:10.1029 / GL005i012p01079.
- ^ Russell, Sara S.; Gounelle, Matthieu; Hutchison, Robert (2001). "Origin of Short-Lived Radionuclides". Filozofické transakce královské společnosti A. 359 (1787): 1991–2004. Bibcode:2001RSPTA.359.1991R. doi:10.1098/rsta.2001.0893. JSTOR 3066270. S2CID 120355895.
- ^ A b Greenwood a Earnshaw, str. 1179
- ^ A b C d E Greenwood a Earnshaw, str. 1180
- ^ Greenwood a Earnshaw, str. 1176
- ^ Lidin RA 1996, Příručka o anorganických látkách, Begell House, New York, ISBN 1-56700-065-7. str. 5
- ^ Goodwin F, Guruswamy S, Kainer KU, Kammer C, Knabl W, Koethe A, Leichtfreid G, Schlamp G, Stickler R & Warlimont H 2005, „Noble kovy a slitiny ušlechtilých kovů“, v Springer Handbook of Condensed Matter and Materials Data, W Martienssen & H Warlimont (eds), Springer, Berlín, str. 329–406, ISBN 3-540-44376-2. str. 341
- ^ "Silver Artifacts" v Corrosion – Artifacts. NACE Resource Center
- ^ Bjelkhagen, Hans I. (1995). Silver-halide recording materials: for holography and their processing. Springer. str.156 –66. ISBN 978-3-540-58619-7.
- ^ Riedel, Sebastian; Kaupp, Martin (2009). "The highest oxidation states of the transition metal elements". Recenze koordinační chemie. 253 (5–6): 606–24. doi:10.1016/j.ccr.2008.07.014.
- ^ A b Greenwood a Earnshaw, str. 1188
- ^ Greenwood a Earnshaw, str. 903
- ^ A b C Greenwood and Earnshaw, pp. 1181–82
- ^ A b C d E Greenwood and Earnshaw, pp. 1183–85
- ^ A b Greenwood and Earnshaw, pp. 1185–87
- ^ „Definice lunární žíraviny“. dictionary.die.net. Archived from the original on 31 January 2012.CS1 maint: BOT: stav původní adresy URL neznámý (odkaz)
- ^ Cope, A. C .; Bach, R. D. (1973). "trans-cyklookten". Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 5, str. 315
- ^ A b McCloskey C.M.; Coleman, G.H. (1955). "β-d-Glucose-2,3,4,6-Tetraacetate". Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 3, str. 434
- ^ Andreas Brumby et al. "Silver, Silver Compounds, and Silver Alloys" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2008. doi:10.1002/14356007.a24_107.pub2
- ^ Meyer, Rudolf; Köhler, Josef & Homburg, Axel (2007). Výbušniny. Wiley–VCH. str.284. ISBN 978-3-527-31656-4.
- ^ Greenwood a Earnshaw, str. 1189
- ^ Greenwood and Earnshaw, pp. 1195–96
- ^ Greenwood and Earnshaw, pp. 1199–200
- ^ Miller, W.T.; Burnard, R.J. (1968). "Perfluoroalkylsilver compounds". J. Am. Chem. Soc. 90 (26): 7367–68. doi:10.1021 / ja01028a047.
- ^ Holliday, A .; Pendlebury, R.E. (1967). "Sloučeniny vinyllead I. Štěpení vinylových skupin z tetravinylleadu". J. Organomet. Chem. 7 (2): 281–84. doi:10.1016 / S0022-328X (00) 91078-7.
- ^ Wang, Harrison M.J .; Lin, Ivan J. B. (1998). „Snadná syntéza komplexů karbenu se stříbrem (I). Užitečná činidla pro přenos karbenu“. Organometallics. 17 (5): 972–75. doi:10.1021 / om9709704.
- ^ A b Ullmann, str. 54–61
- ^ Kroonen, Guus (2013). Etymologický slovník proto-germánský. Brill. str. 436. ISBN 978-90-04-18340-7.
- ^ A b Mallory, James P.; Adams, Douglas Q. (2006). Oxfordský úvod do protoindoevropského a protoindoevropského světa. Oxford University Press. 241–242. ISBN 978-0-19-928791-8.
- ^ Boutkan, Dirk; Kossmann, Maarten (2001). „O etymologii“ stříbra"". TEĎ. Evoluce jazyků v severozápadní Evropě. 38 (1): 3–15. doi:10.1075 / nowele.38.01bou. ISSN 0108-8416.
- ^ Týdny, str. 4
- ^ A b C Greenwood a Earnshaw, str. 1173–74
- ^ Readon, Arthur C. (2011). Metalurgie pro nekovové. ASM International. str. 73–84. ISBN 978-1-61503-821-3.
- ^ A b C d E Týdny, str. 14–19
- ^ A b C d E F G h Ullmann, s. 16–19
- ^ Maria Grazia Melis. „Stříbro na neolitické a eneolitické Sardinii, v H. Meller / R. Risch / E. Pernicka (ed.), Metalle der Macht - Frühes Gold und Silber. 6. Mitteldeutscher Archäologentag vom 17. bis 19. Oktober 2013 in Halle (Saale ), Tagungen des Landesmuseums für ". Citovat deník vyžaduje
| deník =(Pomoc) - ^ A b Emsley, John (2011). Stavební kameny přírody: průvodce AZ prvky. Oxford University Press. 492–98. ISBN 978-0-19-960563-7.
- ^ Patterson, C.C. (1972). „Zásoby a ztráty stříbra ve starověku a středověku“. The Economic History Review. 25 (2): 205235 (216, tabulka 2, 228, tabulka 6). doi:10.1111 / j.1468-0289.1972.tb02173.x.
- ^ de Callataÿ, François (2005). „Řecko-římská ekonomika v dlouhodobém horizontu: olovo, měď a vraky lodí“. Journal of Roman Archaeology. 18: 361–72 [365ff]. doi:10.1017 / s104775940000742x.
- ^ Carol A. Schultze; Charles Stanish; David A. Scott; Thilo Rehren; Scott Kuehner; James K. Feathers (2009). „Přímý důkaz o 1900 letech původní produkce stříbra v povodí jezera Titicaca v jižním Peru“. Sborník Národní akademie věd Spojených států amerických. 106 (41): 17280–83. Bibcode:2009PNAS..10617280S. doi:10.1073 / pnas.0907733106. PMC 2754926. PMID 19805127.
- ^ Frank, Andre Gunder (1998). ReOrient: Globální ekonomika v asijském věku. Berkeley: University of California Press. str.131.
- ^ von Glahn, Richard (1996). „Mýtus a realita měnové krize v sedmnáctém století v Číně“. Journal of Economic History. 2: 132.
- ^ Flynn, Dennis O .; Giraldez, Arturo (1995). „Born with“ Silver Spoon"". Journal of World History. 2: 210.
- ^ Joseph Eddy Fontenrose: Práce, spravedlnost a Hesiodových pět věků. V: Klasická filologie. V. 69, Nr. 1, 1974, s. 1–16.
- ^ Jackson, Robert (1995). Čarodějnictví a okultismus. Devizes, publikování kvintetu. str. 25. ISBN 978-1-85348-888-7.
- ^ Стойкова, Стефана. „Дельо хайдутин“. Българска народна поезия и проза в седем тома (v bulharštině). Т. III. Хайдушки и исторически песни. Název: ЕИ „LiterNet“. ISBN 978-954-304-232-6.
- ^ A b St. Clair, Kassia (2016). The Secret Lives of Color. Londýn: John Murray. str. 49. ISBN 9781473630819. OCLC 936144129.
- ^ Brooks, Frederick. P., Jr. (1987). „No Silver Bullet - Essence and Accident in Software Engineering“ (PDF). Počítač. 20 (4): 10–19. CiteSeerX 10.1.1.117.315. doi:10.1109 / MC.1987.1663532. S2CID 372277.
- ^ Matouš 26:15
- ^ Chevalier, Jean; Gheerbrant, Alain (2009). Dicționar de Simboluri. Mituri, Svěrák, Obiceiuri, Gesturi, Forme, Figuri, Culori, Numere [Slovník symbolů. Mýty, sny, návyky, gesta, tvary, postavy, barvy, čísla] (v rumunštině). Polirom. 105. ISBN 978-973-46-1286-4.
- ^ A b Greenwood a Earnshaw, str. 1174–67
- ^ Ullmann, s. 21–22
- ^ A b CPM Group (2011). CPM Silver Yearbook. New York: Euromoney Books. str. 68. ISBN 978-0-9826741-4-7.
- ^ „Předběžné ekonomické posouzení, technická zpráva 43-101“ (PDF). South American Silver Corp. Archivovány od originál (PDF) dne 19. ledna 2012.
- ^ „Proč jsou Kyrgyzstán a Tádžikistán tak rozděleny v zahraniční těžbě?“. EurasiaNet.org. 7. srpna 2013. Citováno 19. srpna 2013.
- ^ Kassianidou, V. 2003. Včasná těžba stříbra ze složitých polymetalických rud, Craddock, P.T. a Lang, J (eds) Mining and Metal production through the Ages. London, British Museum Press: 198–206
- ^ Craddock, P.T. (1995). Počáteční těžba a výroba kovů. Edinburgh: Edinburgh University Press. str. 223
- ^ Bayley, J., Crossley, D. a Ponting, M. (eds). 2008. „Kovy a zpracování kovů. Rámec výzkumu pro archeometalurgii“. Společnost pro historickou metalurgii 6.
- ^ Pernicka, E., Rehren, Th., Schmitt-Strecker, S. 1998. Pozdní produkce stříbra Uruk cupellation v Habuba Kabira, Sýrie v Metallurgica Antiqua: na počest Hanse-Gerta Bachmanna a Roberta Maddina od Bachmanna, HG, Maddina, Robert, Rehren, Thilo, Hauptmann, Andreas, Muhly, James David, Deutsches Bergbau-Museum: 123–34.
- ^ A b Hilliard, Henry E. "Stříbrný". USGS.
- ^ A b Barriada, Jose L .; Tappin, Alan D .; Evans, E. Hywel; Achterberg, Eric P. (2007). "Měření rozpuštěného stříbra v mořské vodě". Trac Trends in Analytical Chemistry. 26 (8): 809–817. doi:10.1016 / j.trac.2007.06.004. ISSN 0165-9936.
- ^ Fischer, Lisa; Smith, Geoffrey; Hann, Stephan; Bruland, Kenneth W. (2018). „Ultra-stopová analýza stříbra a platiny v mořské vodě pomocí ICP-SFMS po off-line separaci matrice a předkoncentraci“. Marine Chemistry. 199: 44–52. doi:10.1016 / j.marchem.2018.01.006. ISSN 0304-4203.
- ^ A b Ndung’u, K .; Thomas, M. A.; Flegal, A.R. (2001). "Stříbro v západním rovníku a jižním Atlantickém oceánu". Deep Sea Research Část II: Aktuální studie v oceánografii. 48 (13): 2933–2945. doi:10.1016 / S0967-0645 (01) 00025-X. ISSN 0967-0645.
- ^ A b Zhang, Yan; Amakawa, Hiroši; Nozaki, Yoshiyuki (2001). „Oceánské profily rozpuštěného stříbra: přesná měření v povodích západního severního Pacifiku, Ochotského moře a Japonského moře“. Marine Chemistry. 75 (1–2): 151–163. doi:10.1016 / S0304-4203 (01) 00035-4. ISSN 0304-4203.
- ^ Flegal, A.R .; Sañudo-Wilhelmy, S.A .; Scelfo, G.M. (1995). „Stříbro ve východním Atlantiku“. Marine Chemistry. 49 (4): 315–320. doi:10.1016 / 0304-4203 (95) 00021-I. ISSN 0304-4203.
- ^ Ranville, Mara A .; Flegal, A. Russell (2005). „Stříbro v severním Tichém oceánu“. Geochemie, geofyzika, geosystémy. 6 (3): n / a – n / a. doi:10.1029 / 2004GC000770. ISSN 1525-2027.
- ^ Ratte, Hans Toni (1999). „Bioakumulace a toxicita sloučenin stříbra: přehled“. Toxikologie prostředí a chemie. 18 (1): 89–108. doi:10.1002 / atd. 5620180112. ISSN 0730-7268.
- ^ Lacave, José María; Vicario-Parés, Unai; Bilbao, Eider; Gilliland, Douglas; Mura, Francesco; Dini, Luciana; Cajaraville, Miren P .; Orbea, Amaia (2018). „Expozice dospělých zebrafish vodou nanočásticím stříbra a iontovému stříbru vede k rozdílné akumulaci stříbra a účinkům na buněčné a molekulární úrovni“. Věda o celkovém prostředí. 642: 1209–1220. doi:10.1016 / j.scitotenv.2018.06.128. ISSN 0048-9697.
- ^ Calabrese, A., Thurberg, F.P., Gould, E. (1977). Účinky kadmia, rtuti a stříbra na mořská zvířata. Marine Fisheries Review, 39 (4): 5-11. https://fliphtml5.com/hzci/lbsc/basic
- ^ Chen, Meng-Hsien; Zhuang, Ming-Feng; Chou, Lien-Siang; Liu, Jean-Yi; Shih, Chieh-Chih; Chen, Chiee-Young (2017). „Tkáňové koncentrace čtyř tchajwanských zubatých kytovců, které ukazují na znečištění stříbrem a kadmiem v západním Tichém oceánu“. Bulletin o znečištění moří. 124 (2): 993–1000. doi:10.1016 / j.marpolbul.2017.03.028. ISSN 0025-326X.
- ^ A b „Počátky ražení mincí“. britishmuseum.org. Citováno 21. září 2015.
- ^ "Tetradrachm". Merriam-Webster. Citováno 20. ledna 2008.
- ^ Crawford, Michael H. (1974). Římská republikánská ražba, Cambridge University Press, 2 svazky. ISBN 0-521-07492-4
- ^ Oxfordský anglický slovník, 1. vydání, s.v. 'dirhem'
- ^ etymonline.com (20. září 2008). "Etymologie rupie". Citováno 20. září 2008.
- ^ Ray Woodcock (1. května 2009). Globalizace od Genesis po Ženevu: Soutok lidstva. Trafford Publishing. 104–05. ISBN 978-1-4251-8853-5. Citováno 13. srpna 2013.
- ^ Thomas J. Osborne (2012). Pacific Eldorado: Historie Velké Kalifornie. John Wiley & Sons. str. 31. ISBN 978-1-118-29217-4. Citováno 13. srpna 2013.
- ^ A b Ullmann, str. 63–65
- ^ "Seznam kódů aktuální měny a fondů - měna ISO". SNV. Citováno 29. března 2020.
- ^ "Cena LBMA stříbra". LBMA. Citováno 29. března 2020.
- ^ Marcin Latka. "Stříbrný sarkofág svatého Stanislava". artinpl. Citováno 3. srpna 2019.
- ^ A b Ullmann, str. 65–67
- ^ A b Ullmann, str. 67–71
- ^ Beattie, M .; Taylor, J. (2011). „Slitina stříbra vs. nepotažené močové katétry: Systematický přehled literatury“. Journal of Clinical Nursing. 20 (15–16): 2098–108. doi:10.1111 / j.1365-2702.2010.03561.x. PMID 21418360.
- ^ Bouadma, L .; Wolff, M .; Lucet, J.C. (srpen 2012). „Pneumonie spojená s ventilátorem a její prevence“. Aktuální názor na infekční nemoci. 25 (4): 395–404. doi:10.1097 / QCO.0b013e328355a835. PMID 22744316. S2CID 41051853.
- ^ Maillard, Jean-Yves; Hartemann, Philippe (2012). „Stříbro jako antimikrobiální látka: fakta a mezery ve znalostech“. Kritické recenze v mikrobiologii. 39 (4): 373–83. doi:10.3109 / 1040841X.2012.713323. PMID 22928774. S2CID 27527124.
- ^ A b C Ullmann, str. 83–84
- ^ Panáček, Aleš; Kvítek, Libor; Smékalová, Monika; Večeřová, Renata; Kolář, Milan; Röderová, Magdalena; Dyčka, Filip; Šebela, Marek; Prucek, Robert; Tomanec, Ondřej; Zbořil, Radek (leden 2018). "Bakteriální rezistence na nanočástice stříbra a jak ji překonat". Přírodní nanotechnologie. 13 (1): 65–71. Bibcode:2018NatNa..13 ... 65P. doi:10.1038 / s41565-017-0013-r. PMID 29203912. S2CID 26783560.
- ^ Rosenblatt, A .; Stamford, T.C.M .; Niederman, R. (2009). „Fluorid diaminový stříbrný: zubní kaz“ - kulička fluoridu stříbrného"". Journal of Dental Research. 88 (2): 116–25. doi:10.1177/0022034508329406. PMID 19278981. S2CID 30730306.
- ^ Nikitin, Pavel V .; Lam, Sander & Rao, K.V.S. (2005). „Nízkonákladové stříbrné inkoustové RFID antény“ (PDF). 2005 Mezinárodní sympozium IEEE Antennas and Propagation Society. 2B. str. 353. doi:10.1109 / APS.2005.1552015. ISBN 978-0-7803-8883-3. S2CID 695256. Archivovány od originálu dne 21. března 2016.CS1 maint: BOT: stav původní adresy URL neznámý (odkaz)
- ^ Ullmann, s. 71–78
- ^ Ullmann, str. 78–81
- ^ A b Ullmann, str. 81–82
- ^ Ullmann, str. 82
- ^ „Velký zdroj poptávky po stříbrných prutech zmizel“. BullionVault. Citováno 20. července 2014.
- ^ „Středisko pro sledování pigmentů nanomateriálů v Evropské unii“.
- ^ „Observatoř Evropské unie pro katalog nanomateriálů obsahující přísady nano kosmetiky“.
- ^ Martínez-Abad, A .; Ocio, M.J .; Lagarón, J.M .; Sánchez, G. (2013). „Hodnocení polylaktidových filmů naplněných stříbrem pro inaktivaci salmonel a kočičích kalicivirů in vitro a na čerstvé krájené zelenině“. International Journal of Food Microbiology. 162 (1): 89–94. doi:10.1016 / j.ijfoodmicro.2012.12.024. PMID 23376782.
- ^ Sarvate, Sarita (4. dubna 2005). "Stříbrný povlak". Indie proudy. Archivovány od originálu dne 14. února 2009. Citováno 5. července 2009.CS1 maint: BOT: stav původní adresy URL neznámý (odkaz)
- ^ Meisler, Andy (18. prosince 2005). „Bouře na košíku s čajem“. Los Angeles Times.
- ^ „MSDS - 373249“.
- ^ A b C d E Ullmann, str. 88–91
Zdroje použité výše
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemie prvků (2. vyd.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- Týdny, Mary Elvira; Leichester, Henry M. (1968). Objev prvků. Easton, PA: Journal of Chemical Education. ISBN 978-0-7661-3872-8. LCCN 68-15217.
- Andreas Brumby, Peter Braumann, Klaus Zimmermann, Francis Van Den Broeck, Thierry Vandevelde, Dan Goia, Hermann Renner, Günther Schlamp, Klaus Zimmermann, Wolfgang Weise, Peter Tews, Klaus Dermann, Alfons Knödler, Karl-Heinz Schröder, Bernd Kempf, Hans Martin Lüschow, Cartrin Peter, Rainer Schiele. "Stříbro, sloučeniny stříbra a slitiny stříbra". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a24_107.pub2.CS1 maint: používá parametr autoři (odkaz)
Další čtení
- William L. Silber, The Story of Silver: How the White Metal Shaped America America and the Modern World. Princeton, NJ: Princeton University Press, 2019.
externí odkazy
- stříbrný na Periodická tabulka videí (University of Nottingham)
- Society of American Silversmiths
- Stříbrný institut Web stříbrného průmyslu
- Sbírka stříbrných předmětů Vzorky stříbra
- Doprava, osud a účinky stříbra na životní prostředí
- CDC - Kapesní průvodce chemickými riziky NIOSH - stříbro
- Obrázek ve sbírce Element od Heinricha Pnioka


















