Oxid rhodičitý - Rhodium(IV) oxide
 | |
| Identifikátory | |
|---|---|
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.032.021 |
| Číslo ES |
|
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| RhO2 | |
| Molární hmotnost | 134,904 g / mol |
| Vzhled | černá krystalická pevná látka |
| Hustota | 7,2 g / cm3 |
| Bod tání | 1 050 ° C (1 920 ° F; 1 320 K) (rozkládá se) |
| Rozpustnost | nerozpustný v Lučavka královská |
| Struktura | |
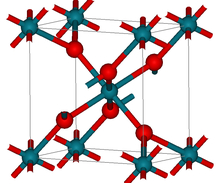
| čtyřúhelníkový (rutil ) | |
| Nebezpečí | |
Klasifikace EU (DSD) (zastaralý) | nezapsáno |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Oxid rhodičitý (nebo oxid rhodičitý) je chemická sloučenina se vzorcem RhÓ2.
Chemické vlastnosti
RhO2 je vysoce nerozpustný i za horka Lučavka královská.[1]
Struktura
RhO2 má čtyřúhelníkový rutil struktura.[2]
Fyzikální vlastnosti
RhO2 má kovový měrný odpor s hodnotami <10−4 Ohm · cm. Transformuje se ve vzduchu na Rh2Ó3 při 850 ° C a poté na kov a kyslík při 1050 ° C.[2]
Viz také
Reference
- ^ O. Muller a R. Roy (1968). „Tvorba a stabilita oxidů platiny a rhodia při vysokých tlacích kyslíku a strukturách Pt3Ó4, β-PtO2 a RhO2". Journal of the Less Common Metals. 16 (2): 129–146. doi:10.1016/0022-5088(68)90070-2.
- ^ A b R. D. Shannon (1968). „Syntéza a vlastnosti dvou nových členů rodiny rutilů RhO2 a PtO2". Polovodičová komunikace. 6 (3): 139–143. doi:10.1016/0038-1098(68)90019-7.
| Tento anorganické sloučenina –Vztahující se článek je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
