Beta-karbolin - Beta-Carboline
tento článek potřebuje další citace pro ověření. (Prosinec 2007) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC 9H-β-karbolin | |
Ostatní jména
| |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.005.418 |
| Pletivo | norharman |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C11H8N2 | |
| Molární hmotnost | 168,20 g / mol |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
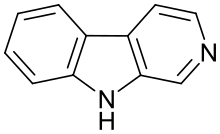
β-Carboline (9H-pyrido [3,4-b]indol ), také známý jako norharmane, je dusík heterocyklus. Je to také prototyp třídy indol alkaloid sloučeniny známé jako β-karboliny.[1]
Farmakologie
β-karbolin alkaloidy jsou rozšířené v rostliny a zvířata a často působí jako GABAA inverzní agonisté. Jako součásti liany Banisteriopsis caapi, β-karboliny harmine, harmalin, a tetrahydroharmin hrají klíčovou roli ve farmakologii domorodých obyvatel psychedelická droga ayahuasca zabráněním rozpadu dimethyltryptamin reverzibilní inhibicí ve střevě monoaminooxidáza, čímž je po perorálním podání psychoaktivní. Některé β-karboliny, zejména tryptolin a pinoline, se mohou přirozeně tvořit v lidském těle. Ten je pravděpodobně zapleten spolu s melatonin v roli epifýza při regulaci cyklus spánku-bdění.[Citace je zapotřebí ] β-karbolin je a GABAA místo benzodiazepinů inverzní agonista a proto může mít křeče, anxiogenní a efekty zvyšující paměť.[2] 3-hydroxymethyl-beta-karbolin blokuje účinek flurazepamu na podporu spánku u hlodavců a sám o sobě může snížit spánek v závislosti na dávce.[3] 9-methyl-β-karboliny Zdá se, že vyvolávají Poškození DNA když je vystaven ultrafialové světlo.[4]
Struktura
β-Karbolin patří do skupiny indolové alkaloidy a skládá se z pyridin prsten, který je spojen s indol kostra.[5] Struktura β-karbolinu je podobná jako u tryptamin, s ethylamin řetěz znovu připojen k indol zazvonit přes extra uhlík atom, za vzniku struktury se třemi kruhy. Předpokládá se, že biosyntéza β-karbolinů následuje tuto cestu z analogických tryptaminů.[6] Různé úrovně nasycení jsou možné ve třetím kruhu, který je zde uveden v strukturní vzorec vybarvením volitelně dvojných vazeb červenou a modrou:

Příklady β-karbolinů
Některé z důležitějších β-karbolinů jsou uvedeny v tabulce níže. Jejich struktury mohou obsahovat výše uvedené vazby označené červenou nebo modrou.
| Krátké jméno | Red Bond | Blue Bond | R1 | R6 | R7 | R9 | Struktura |
|---|---|---|---|---|---|---|---|
| β-karbolin | × | × | H | H | H | H |  |
| Tryptolin | H | H | H | H | 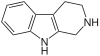 | ||
| Pinoline | H | OCH3 | H | H |  | ||
| Harmane | × | × | CH3 | H | H | H |  |
| Harmine | × | × | CH3 | H | OCH3 | H |  |
| Harmalin | × | CH3 | H | OCH3 | H |  | |
| Tetrahydroharmin | CH3 | H | OCH3 | H |  | ||
| 9-methyl-β-karbolin | × | × | H | H | H | CH3 | 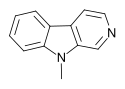 |
Výskyt v přírodě
Tato sekce případně obsahuje nevhodné nebo nesprávně interpretované citace to ne ověřit text. (Prosinec 2007) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |

Je známo, že osm rostlinných rodin exprimuje 64 různých druhů β-karbolinových alkaloidů. Suchou hmotností semena Peganum harmala (Syrian Rue) obsahují mezi 0,16%[7] a 5,9%[8] β-karbolinové alkaloidy.
V důsledku přítomnosti β-karbolinů v pokožka z štíři, jejich kůže je známa fluoreskují při vystavení určitým vlnovým délkám ultrafialový světlo jako světlo produkované a černé světlo.[9]
Skupina derivátů β-karbolinu, nazývaná eudistominy byly extrahovány z ascidians (námořní pláštěnci z rodiny Ascidiacea ), jako Ritterella sigillinoides,[10] Lissoclinum křehký [11] nebo Pseudodistoma aureum.[12] Nostokarbolin byl izolován od sladké vody sinice.
Je známo, že deriváty β-karbolinu indukují produkci sekundární metabolit v různých druzích půdy „Streptomyces“.[13][14] Tyto molekuly, definované jako biomediátor, je známo, že zvyšují expresi sekundární metabolit biosyntetické geny vazbou na velký regulátor vázání ATP rodiny LuxR.
Viz také
Reference
- ^ „Složky β-karbolinových alkaloidů z Thermoactinomyces SP. Kmen izolovaný z ostrova Livingston, Antarktida“. doi:10.5504 / BBEQ.2012.0021. Citovat deník vyžaduje
| deník =(Pomoc) - ^ Venault P, Chapouthier G (2007). „Od behaviorální farmakologie beta-karbolinů po záchvaty, úzkost a paměť“. ScientificWorldJournal. 7: 204–23. doi:10.1100 / tsw.2007.48. PMC 5901106. PMID 17334612.
- ^ Mendelson, W .; Cain, M; Cook, J .; Paul, S .; Skolnick, P (1983-01-28). „Antagonista benzodiazepinových receptorů snižuje spánek a zvrací hypnotické účinky flurazepamu.“ Věda. 219 (4583): 414–416. Bibcode:1983Sci ... 219..414M. doi:10.1126 / science.6294835. ISSN 0036-8075. PMID 6294835. S2CID 43038332.
- ^ Vignoni M, Rasse-Suriani FA, Butzbach K, Erra-Balsells R, Epe B, Cabrerizo FM (2013). "Mechanismy poškození DNA fotoexcitovanými 9-methyl-β-karboliny". Org Biomol Chem. 11 (32): 5300–9. doi:10.1039 / c3ob40344k. PMID 23842892.
- ^ Encyklopedie psychoaktivních rostlin: etnofarmakologie a její aplikace. Ratsch, Christian. Park Street Press c. 2005
- ^ Baiget, Jessica; Llona-Minguez, Sabin; Lang, Stuart; MacKay, Simon P; Suckling, Colin J; Sutcliffe, Oliver B (2011). „Oxid manganičitý zprostředkovaný syntézou methyl-9H-pyrido [3,4-b] indol-1-karboxylátu v jedné nádobě: Stručná syntéza alangiobussininu“. Beilstein Journal of Organic Chemistry. 7: 1407–11. doi:10,3762 / bjoc.7.164. PMC 3201054. PMID 22043251.
- ^ Hemmateenejad B, Abbaspour A, Maghami H, Miri R, Panjehshahin MR (srpen 2006). „Částečná multivariační spektrální kalibrační metoda založená na nejmenších čtvercích pro současné stanovení derivátů beta-karbolinu v extraktech semen Peganum harmala“. Anální Chim Acta. 575 (2): 290–9. doi:10.1016 / j.aca.2006.05.093. PMID 17723604.
- ^ Herraiz T, González D, Ancín-Azpilicueta C, Arán VJ, Guillén H (2010). „Alkaloidy beta-karbolinu v Peganum harmala a inhibice lidské monoaminooxidázy (MAO)“. Food Chem. Toxicol. 48 (3): 839–43. doi:10.1016 / j.fct.2009.12.019. hdl:10261/77694. PMID 20036304.
- ^ Stachel SJ, Stockwell SA, van Vranken DL (srpen 1999). „Fluorescence štírů a kataraktogeneze“. Chem. Biol. 6 (8): 531–9. doi:10.1016 / S1074-5521 (99) 80085-4. PMID 10421760.
- ^ Lake RJ, Blunt JW, Munro MH (1989). „Eudistominy z novozélandského ascidianu Ritterella sigillinoides". Aust. J. Chem. 42 (7): 1201–1206. doi:10.1071 / CH9891201.
- ^ Badre A, Boulanger A, Abou-Mansour E, Banaigs B, Combaut G, Francisco C (duben 1994). „Eudistomin U a isoeudistomin U, nové alkaloidy z karibského ascidianu Lissoclinum křehký". J. Nat. Prod. 57 (4): 528–533. doi:10.1021 / np50106a016. PMID 8021654.
- ^ Davis RA, Carroll AR, Quinn RJ (červen 1998). „Eudistomin V, nový β-karbolin od australského ascidiána Pseudodistoma aureum". J. Nat. Prod. 61 (7): 959–960. doi:10.1021 / np9800452. PMID 9677285.
- ^ Panthee, S; Takahashi, S; Hayashi, T; Shimizu, T; Osada, H (9. dubna 2019). „Biomediátory β-karbolinu indukují produkci reveromycinu u Streptomyces sp. SN-593“. Vědecké zprávy. 9 (1): 5802. doi:10.1038 / s41598-019-42268-w. PMID 30967594.
- ^ Panthee, S; Kito, N; Hayashi, T; Shimizu, T; Ishikawa, J; Hamamoto, H; Osada, H; Takahashi, S (23. června 2020). „Chemické signály β-karbolinu indukují produkci reveromycinu prostřednictvím regulátoru rodiny LuxR u Streptomyces sp. SN-593“. Vědecké zprávy. 10 (1): 10230. doi:10.1038 / s41598-020-66974-r. PMID 32576869.
externí odkazy
- Beta-karboliny v americké národní lékařské knihovně Lékařské předměty (Pletivo)
- TiHKAL # 44
- TiHKAL obecně
- Beta-karboliny v kávě
- Farzin D, Mansouri N (červenec 2006). „Antidepresivní účinek harmanu a dalších beta-karbolinů v testu nuceného plavání myší“. Eur Neuropsychopharmacol. 16 (5): 324–8. doi:10.1016 / j.euroneuro.2005.08.005. PMID 16183262.
