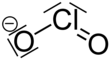
Chloritan sodný - Sodium chlorite
| |||
| |||
 | |||
| Jména | |||
|---|---|---|---|
| Název IUPAC Chloritan sodný | |||
| Ostatní jména Kyselina chlorovodíková, sodná sůl Textone | |||
| Identifikátory | |||
| |||
3D model (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| Informační karta ECHA | 100.028.942 | ||
| Číslo ES |
| ||
| KEGG | |||
PubChem CID | |||
| Číslo RTECS |
| ||
| UNII | |||
| UN číslo | 1496 | ||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| NaClO2 | |||
| Molární hmotnost | 90,442 g / mol (bezvodý) 144,487 g / mol (trihydrát) | ||
| Vzhled | bílá pevná látka | ||
| Zápach | bez zápachu | ||
| Hustota | 2,468 g / cm3, pevný | ||
| Bod tání | bezvodý se rozkládá při 180–200 ° C trihydrát se rozkládá při 38 ° C | ||
| 75,8 g / 100 ml (25 ° C) 122 g / 100 ml (60 ° C) | |||
| Rozpustnost | málo rozpustný v methanolu, ethanol | ||
| Kyselost (strK.A) | 10-11 | ||
| Struktura | |||
| monoklinický | |||
| Termochemie | |||
Std entalpie of formace (ΔFH⦵298) | -307,0 kJ / mol | ||
| Farmakologie | |||
| D03AX11 (SZO) | |||
| Nebezpečí | |||
| Bezpečnostní list | BL | ||
| Piktogramy GHS |     | ||
| Signální slovo GHS | Nebezpečí | ||
| H272, H301, H310, H330, H314, H318, H400 | |||
| P210, P220, P221, P260, P262, P264, P270, P271, P273, P280, P284, P301 + 330 + 331, P303 + 361 + 353, P305 + 351 + 338, P310, P361, P363, P370 + 378, P391, P403 + 233, P405, P501 | |||
| Požití nebezpečí | Kategorie 3 | ||
| Inhalace nebezpečí | Kategorie 2 | ||
| Oko nebezpečí | Kategorie 1 | ||
| Kůže nebezpečí | Kategorie 1B | ||
| NFPA 704 (ohnivý diamant) | |||
| Bod vzplanutí | Nehořlavé | ||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
LD50 (střední dávka ) | 350 mg / kg (potkan, orálně) | ||
| Související sloučeniny | |||
jiný anionty | Chlorid sodný Chlornan sodný Chlorečnan sodný Chloristan sodný | ||
jiný kationty | Chloritan draselný Chloritan barnatý | ||
Související sloučeniny | Chlordioxid Kyselina chlorovodíková | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Chloritan sodný (NaClO2) je chemická sloučenina používaná při výrobě papíru a jako dezinfekční prostředek.
Použití
Hlavní aplikací chloritanu sodného je tvorba chlordioxid pro bělení a odstraňování textilu, buničiny a papíru. Používá se také k dezinfekci komunálních úpraven vody po přeměně na oxid chloričitý.[1]:2 Výhodou této aplikace ve srovnání s běžněji používaným chlorem je to trihalomethany (jako chloroform ) nejsou vyráběny z organických kontaminantů.[1]:25,33 Chlordioxid vyrobený z chloritanu sodného je schválen FDA za určitých podmínek pro dezinfekci vody používané k mytí ovoce, zeleniny a drůbeže.[2][úplná citace nutná ]
Chloritan sodný, NaClO2, někdy v kombinaci s chlorid zinečnatý, také nachází uplatnění jako součást terapeutických výplachů, ústních vod,[3][4] zubní pasty a gely, ústní spreje jako konzervační látky v očních kapkách,[5] a v čisticím roztoku kontaktních čoček pod obchodním názvem Purite.
Používá se také k sanitaci vzduchovodů a systémů HVAC / R a prostorů pro zadržování zvířat (stěny, podlahy a další povrchy).
Chemické činidlo
v organická syntéza, chloritan sodný se často používá jako činidlo v Pinnickova oxidace pro oxidaci aldehydy na karboxylové kyseliny. Reakce se obvykle provádí v fosforečnan sodný pufrovaný roztok v přítomnosti zachycovače chloru (obvykle 2-methyl-2-buten ).[6]
V roce 2005 byl chloritan sodný použit jako oxidační činidlo k přeměně alkylfuranů na odpovídající 4-oxo-2-alkenoové kyseliny v jednoduché syntéze.[7]
Okyselený chloritan sodný
Míchání roztoku chloritanu sodného se slabým potravinářským kyselým roztokem (obvykle kyselina citronová ), oba stabilní, produkuje krátkodobý okyselený chloritan sodný (ASC), který má silné dekontaminační vlastnosti. Po smíchání hlavní účinné látky kyselina chloritá se vyrábí v rovnováze s chloritanovým aniontem. Podíl se mění podle pH, teploty a dalších faktorů, pohybuje se v rozmezí přibližně 5–35% kyselina chloritá s 65–95% chloritan; kyselější roztoky mají za následek vyšší podíl kyseliny chlorité. Kyselina chlorovodíková se rozpadá na chlordioxid který se zase rozpadá na chloritanový anion a nakonec chloridový anion. ASC se používá k sanitaci tvrdých povrchů, které přicházejí do styku s potravinami, a jako promývací nebo oplachovací prostředek pro různé druhy potravin, včetně červeného masa, drůbeže, mořských plodů, ovoce a zeleniny. Vzhledem k tomu, že oxo-chlorové sloučeniny jsou při správné přípravě nestabilní, neměly by při vhodném zacházení na potravinách zůstat žádné měřitelné zbytky.[8][9] ASC se také používá jako dudlík pro kontrolu mastitida u mléčného skotu.[10]
Použití ve veřejných krizích
The Výzkumné, vývojové a technické centrum americké armády Natick Soldier vyrobil přenosnou metodu generování oxidu chloričitého bez potřeby energie, známou jako ClO2, plyn, popsal jako jeden z nejlepších biocidy k dispozici pro potírání kontaminantů, které sahají od neškodných mikrobů a potravinových patogenů po kategorii A. Bioteror agenti. V týdnech po Útoky z 11. září když antrax byl zaslán v dopisech veřejným činitelům, byly použity týmy nebezpečných materiálů ClO2 dekontaminovat kancelářskou budovu Hart Senate a poštovní zařízení Brentwood.[11]
Při řešení pandemie COVID-19 Americká agentura na ochranu životního prostředí zveřejnil seznam mnoha dezinfekční prostředky které splňují jeho kritéria pro použití v environmentálních opatřeních proti původci koronavirus.[12][13] Některé jsou založeny na chloritanu sodném, který je aktivován chlordioxid, ačkoli se u každého produktu používají odlišné formulace. Mnoho dalších produktů na seznamu EPA obsahuje chlornan sodný, který je podobný názvu, ale neměl by být zaměňován s chloritanem sodným, protože mají velmi odlišné způsoby chemického působení.
Bezpečnost
Chloritan sodný, jako mnoho jiných oxidační činidla, by měly být chráněny před neúmyslnou kontaminací organickými materiály, aby se zabránilo tvorbě výbušné směsi. Chemická látka je stabilní v čisté formě a při prudkém nárazu nevybuchne, pokud nejsou přítomny organické kontaminanty, například na mastném kladivu, které narazí na chemikálii na kovadlině.[14] Rovněž se snadno zapálí třením, pokud je kombinováno s a redukční činidlo jako práškový cukr, síra nebo červený fosfor.
Toxicita
Chloritan sodný je silný oxidant a lze tedy očekávat, že způsobí klinické příznaky podobný dobře známému chlorečnan sodný: methemoglobinemie, hemolýza, selhání ledvin.[15] Dávka 10-15 gramů chlorečnan sodný může být smrtelná.[16] Methemoglobémie byla prokázána u potkanů a koček,[17] a nedávné studie EMEA potvrdili, že klinická symptomatologie je velmi podobná té, kterou způsobuje chlorečnan sodný u potkanů, myší, králíků a zelené opice.[18]
V lékařské literatuře je pouze jeden případ člověka chloritan otrava.[19] Zdá se, že potvrzuje, že toxicita je rovný chlorečnan sodný. Z analogie s chlorečnanem sodným lze očekávat, že způsobí i malá množství asi 1 gramu nevolnost, zvracení a dokonce život ohrožující hemolýza v glukóza-6-fosfátdehydrogenáza osoby s nedostatkem.
EPA stanovila maximální hladinu kontaminujících látek 1 miligram chloritanu na litr (1 mg / l) v pitné vodě.[20]
Prodejci „Zázračný minerální roztok ”, Směs chloritanu sodného a kyseliny citrónové také známá jako„ MMS “, která je propagována jako a léčit vše byli odsouzeni, pokutováni nebo jinak disciplinováni ve více jurisdikcích po celém světě. Produkty MMS byly různě označovány jako hadí olej a kompletní šarlatánství. Spojené státy. Úřad pro kontrolu potravin a léčiv vydal několik varování před konzumací MMS.[21][22][23][24][25][26][27][28][29]
Výroba
Volná kyselina, kyselina chloritá, HClO2, je stabilní pouze při nízkých koncentracích. Protože jej nelze koncentrovat, nejedná se o komerční produkt. Odpovídající sodná sůl, chloritan sodný, NaClO2 je dostatečně stabilní a levná, aby byla komerčně dostupná. Odpovídající soli těžkých kovů (Ag+, Hg+, Tl+, Pb2+a také Cu2+ a NH4+) se výbušninou rozkládají.
Chloritan sodný pochází z nepřímo chlorečnan sodný NaClO3. Nejprve se chlorečnan sodný sníží na chlordioxid, typicky v silně kyselém roztoku za použití redukčních činidel, jako je siřičitan sodný, oxid siřičitý nebo kyselina chlorovodíková. Tento meziprodukt se poté absorbuje do vodného roztoku hydroxid sodný kde jej jiné redukční činidlo převádí na chloritan sodný. Dokonce peroxid vodíku Může být použito jako redukční činidlo, přičemž jako vedlejší produkt vzniká plynný kyslík, nikoli jiné anorganické soli nebo materiály, které by mohly kontaminovat požadovaný produkt.[30]
Obecné odkazy
- „Chemistry of the Elements“, N.N. Greenwood a A. Earnshaw, Pergamon Press, 1984.
- „Kirk-Othmer Concise Encyclopedia of Chemistry“, Martin Grayson, redaktor, John Wiley & Sons, Inc., 1985
Reference
- ^ A b Pokyny EPA, kapitola 4: Chlordioxid (PDF), Agentura na ochranu životního prostředí USA, archivováno (PDF) od originálu 11. 10. 2008, vyvoláno 2012-02-27
- ^ „Chlordioxid“ (PDF). Archivováno (PDF) z původního dne 2012-03-30. Citováno 2011-11-02.
- ^ Cohen, Joyce (2008-05-13). „Nové ústní vody mohou pomoci vyrazit dech“. USA dnes. Archivováno od původního dne 2012-06-26.
- ^ „SmartMouth 2 Step Mouth Rinse“. dentist.net. Archivováno z původního dne 29. října 2010. Citováno 26. dubna 2018.
- ^ Mrkejte slzy
- ^ Bal BS, Childers WE, Pinnick HW (1981). „Oxidace α, β-nenasycených aldehydů“. Čtyřstěn (abstraktní). 37 (11): 2091–2096. doi:10.1016 / S0040-4020 (01) 97963-3.
- ^ Annangudi SP, Sun M, Salomon RG (2005). „Efektivní syntéza 4-oxo-2-alkenových kyselin z 2-alkylfuranů“. Synlett (abstraktní). 9 (9): 1468–1470. doi:10,1055 / s-2005-869833.
- ^ Manipulace / zpracování s okyseleným chloritanem sodným (PDF), Služba zemědělského marketingu (USDA), 21. července 2008, archivováno od originálu 8. dubna 2013, vyvoláno 9. prosince 2012
- ^ Rao, Madduri V (2007), Okyselený chloritan sodný (ACS), chemické a technické hodnocení (PDF), Organizace pro výživu a zemědělství OSN, archivováno (PDF) od originálu 3. prosince 2012, vyvoláno 9. prosince 2012
- ^ Hillerton, J. E.; Cooper, J .; Morelli, J. (2007). „Předcházení mastitidě skotu dezinfekčním prostředkem na struky po mléku s obsahem okyseleného chloritanu sodného“. Journal of Dairy Science. 90 (3): 1201–1208. doi:10.3168 / jds.S0022-0302 (07) 71607-7. PMID 17297095.
- ^ Natick hraje klíčovou roli v boji proti šíření eboly Archivováno 2015-06-24 na Wayback Machine Citováno: 23/01/2016
- ^ US EPA, OCSPP (2020-03-13). "Seznam N: Dezinfekční prostředky pro použití proti SARS-CoV-2". US EPA. Citováno 2020-03-28.
- ^ „Jak víme, že dezinfekční prostředky by měly zabít koronavirus COVID-19“. Chemické a technické novinky. Citováno 2020-03-31.
- ^ Taylor, M. C. (1940). "Vlastnosti a reakce chlorečnanu sodného". Průmyslová a inženýrská chemie. 32 (7): 899–903. doi:10.1021 / ie50367a007.
- ^ Goldfrank's Toxicologic Emergencies, McGraw-Hill Professional; 8. vydání (28. března 2006), ISBN 978-0-07-143763-9
- ^ "Chloráty". PoisonCentre.be (francouzsky). Archivovány od originál dne 2012-12-11. Citováno 2012-12-11.
- ^ Klinická toxikologie komerčních produktů. Robert E. Gosselin, Roger P. Smith, Harold C. Hodge, Jeannet Braddock. Uitgever: Williams & Wilkins; 5. vydání (září 1984) ISBN 978-0-683-03632-9
- ^ „Chloritan sodný - souhrnná zpráva“ (PDF). Evropská agentura pro hodnocení léčivých přípravků - Jednotka pro hodnocení veterinárních léčiv. Archivovány od originál (PDF) dne 10.7.2007. Citováno 2007-07-10.
- ^ Lin, JL; Lim, PS (1993). "Akutní otrava chloritanem sodným spojená se selháním ledvin". Ren Fail. 15: 645–8. doi:10.3109/08860229309069417. PMID 8290712.
- ^ „ATSDR: ToxFAQs pro chlordioxid a chloritan“. Archivováno z původního dne 2012-07-02.
- ^ „Prodejce„ Miracle Mineral Solution “usvědčen z marketingu toxické chemikálie jako zázračného léku“. Ministerstvo spravedlnosti Spojených států. Archivováno od originálu 11. května 2016. Citováno 11. května 2016.
- ^ „Zajištění dobrovolného dodržování předpisů - Kerri Rivera“ (PDF). NBC Chicago. Archivováno (PDF) z původního dne 4. dubna 2016. Citováno 24. září 2016.
- ^ Australská komise pro hospodářskou soutěž a ochranu spotřebitele v. Leanne Rita Vassallo a Aaron David Smith (FCA 954 20. srpna 2009). Text
- ^ Pulkkinen, Levi (3. srpna 2009). „Sexy příběhy, falešné léky vedou k akci ze strany státu AG“. SeattlePI.com. zaměstnanci seattlepi.com. OCLC 3734418. Archivováno od originálu 2. listopadu 2013. Citováno 12. února 2012.
- ^ „Washingtonský generální prokurátor se vrací k vrácení peněz spotřebitelům závislým na australských šarlatánských webových stránkách“ (Tisková zpráva). Washingtonský státní úřad generálního prokurátora. 8. března 2010. Archivováno od originálu 7. prosince 2011. Citováno 12. února 2012.
- ^ „Australanští podvodníci po bodnutí po 1,2 milionu dolarů“. ITnews for Australian Business. Haymarket Media. 26. srpna 2009. Archivováno z původního dne 20. září 2011. Citováno 12. února 2012.
- ^ „Žena řekla, aby přestala prodávat zázračný lék proti rakovině'". ABC News. Austrálie. 23.dubna 2009. Archivováno z původního dne 14. června 2013. Citováno 12. února 2012.
- ^ „Neregistrovaný poskytovatel zdravotní péče nařídil zastavit klamání pacientů s rakovinou“ (Tisková zpráva). Ministr cestovního ruchu a poctivého obchodování, ctihodný Peter Lawlor. 23.dubna 2009. Archivováno z původního dne 3. dubna 2011. Citováno 12. února 2012.
- ^ Mole, Beth (2019-08-14). „Lidé stále pijí bělidlo - a zvracejí a chrlí své vnitřnosti“. Ars Technica. Citováno 2019-08-15.
- ^ Qian, Yu; Chen, Yun; Jiang, Yanbin; Zhang, Lijuan (2007). "Čistý výrobní proces chloritanu sodného z chlorečnanu sodného". Journal of Cleaner Production. 15 (10): 920–926. doi:10.1016 / j.jclepro.2004.07.008.