Heparin - Heparin
 | |
 | |
| Klinické údaje | |
|---|---|
| Výslovnost | /ˈhɛp.rɪn/ HEP-ər-in |
| AHFS /Drugs.com | Monografie |
| Těhotenství kategorie |
|
| Trasy z správa | IV, SQ |
| ATC kód | |
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Biologická dostupnost | Nevyzpytatelný |
| Metabolismus | Játra |
| Odstranění poločas rozpadu | 1,5 hodiny |
| Vylučování | Moč[2] |
| Identifikátory | |
| Číslo CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.029.698 |
| Chemické a fyzikální údaje | |
| Vzorec | C12H19NÓ20S3 |
| Molární hmotnost | 12 000–15 000 g / mol |
| |
| | |
Heparin, také známý jako nefrakcionovaný heparin (UFH), je lék a přirozeně se vyskytující glykosaminoglykan.[3][4] Jako lék se používá jako antikoagulant (ředidlo krve).[3] Konkrétně se také používá při léčbě infarkty a nestabilní angina pectoris.[3] Je to dáno injekce do žíly nebo pod kůží.[3] Jiná použití zahrnují uvnitř zkumavky a ledvinové dialýzy.[4][5]
Mezi časté nežádoucí účinky patří krvácení, bolest v místě vpichu a nízké krevní destičky.[3] Mezi závažné nežádoucí účinky patří heparinem indukovaná trombocytopenie.[3] Větší péče je nutná u pacientů s špatná funkce ledvin.[3] Heparin se zdá být relativně bezpečný pro použití během těhotenství a kojení.[6] Heparin je produkován bazofily a žírné buňky celkově savci.[7]
Objev heparinu byl oznámen v roce 1916.[8] Je na Seznam základních léčivých přípravků Světové zdravotnické organizace.[9] A frakcionovaný verze heparinu, známá jako nízkomolekulární heparin, je také k dispozici.[10]
Lékařské použití
Heparin působí jako antikoagulant, zabraňuje tvorbě sraženin a rozšiřování stávajících sraženin v krvi. I když samotný heparin nerozkládá sraženiny, které se již vytvořily (na rozdíl od aktivátor tkáňového plazminogenu ), umožňuje tělu přirozenost lýza sraženiny mechanismy, které normálně fungují k rozpadu sraženin, které se vytvořily. Heparin se obecně používá k antikoagulaci za následujících podmínek:
- Akutní koronární syndrom, např. NSTEMI
- Fibrilace síní
- Hluboká žilní trombóza a plicní embolie
- Kardiopulmonální bypass pro operace srdce
- ECMO obvod pro mimotělní podpora života
- Hemofiltrace
- Trvání centrální nebo periferní žíly katétry
Heparin a jeho nízkomolekulární deriváty (např. enoxaparin, dalteparin, tinzaparin ) jsou účinné při prevenci hlubokých žilních trombóz a plicních embolií u rizikových osob,[11][12] ale žádné důkazy nenaznačují, že jeden z nich je v prevenci úmrtnosti účinnější než druhý.[13]
Nepříznivé účinky
Vážným vedlejším účinkem heparinu je heparinem indukovaná trombocytopenie (HIT), způsobené imunologickou reakcí, která vyvolává krevní destičky terč imunologické odpovědi, vedoucí k degradaci krevních destiček, která způsobuje trombocytopenii. Tento stav se obvykle přeruší po ukončení léčby a obecně se mu lze vyhnout použitím syntetických heparinů. Benigní forma trombocytopenie je také spojena s časným užíváním heparinu, které odezní bez zastavení podávání heparinu.
Jsou známy dva nehemoragické vedlejší účinky léčby heparinem. První je zvýšení séra aminotransferáza hladiny, které byly hlášeny až u 80% pacientů užívajících heparin. Tato abnormalita není spojena s dysfunkcí jater a zmizí po vysazení léku. Další komplikace je hyperkalemie, který se vyskytuje u 5 až 10% pacientů užívajících heparin a je výsledkem potlačení aldosteronu vyvolaného heparinem. Hyperkalemie se může objevit během několika dní po zahájení léčby heparinem. Vzácněji vedlejší účinky alopecie a osteoporóza může nastat při chronickém užívání.
Stejně jako u mnoha léků může být předávkování heparinem smrtelné. V září 2006 se heparinu dostalo celosvětové publicity, když tři předčasně narozené děti zemřely poté, co byly omylem předávkovány heparinem v nemocnici v Indianapolis.[14]
Kontraindikace
Tato sekce potřebuje další citace pro ověření. (Dubna 2017) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
Heparin je kontraindikován u osob s rizikem krvácení (zejména u lidí s nekontrolovaným krevním tlakem, onemocněním jater a cévní mozkovou příhodou), závažným onemocněním jater nebo těžkou hypertenzí.[15]
Protijed na heparin
Protamin sulfát byl podáván k vyrovnání antikoagulačního účinku heparinu (1 mg na 100 jednotek heparinu, který byl podán za poslední čtyři hodiny).[16] Může být použit u těch, kteří předávkují heparinem, nebo ke zvrácení účinku heparinu, když již není potřeba.[17]
Fyziologická funkce
Normální role heparinu v těle je nejasná. Heparin je obvykle uložen v sekrečních granulích žírné buňky a uvolněna pouze do vaskulatura v místech poranění tkáně. Bylo navrženo, že namísto antikoagulace je hlavním účelem heparinu obrana na takových místech před napadením bakteriemi a jinými cizími materiály.[18] Kromě toho je pozorován u mnoha široce odlišných druhů, včetně některých bezobratlých, kteří nemají podobný systém srážení krve. Je to vysoce sulfatovaný glykosaminoglykan. Má nejvyšší zápor hustota náboje ze všech známých biologická molekula.[19]
Evoluční ochrana
Kromě hovězí a vepřové tkáně, ze které se běžně extrahuje heparin farmaceutické kvality, byl také extrahován a charakterizován z:
Biologická aktivita heparinu u druhů 6–11 je nejasná a dále podporuje myšlenku, že hlavní fyziologickou rolí heparinu není antikoagulace. Tyto druhy nemají žádný systém srážení krve podobný systému přítomnému u druhů uvedených v seznamu 1–5. Výše uvedený seznam také ukazuje, jak vysoký je heparin evolučně konzervované, přičemž molekuly podobné struktury jsou produkovány širokou škálou organismů patřících k mnoha různým phyla.[Citace je zapotřebí ]
Farmakologie
v Příroda, heparin je a polymer různé velikosti řetězu. Nefrakcionovaný heparin (UFH) jako léčivo je heparin, který dosud nebyl frakcionovaný izolovat frakci molekul s nízkou molekulární váha. V porovnání, nízkomolekulární heparin (LMWH) prošla kvůli své výrobě frakcionací farmakodynamika předvídatelnější. Často lze použít buď UFH nebo LMWH; v některých situacích je vhodnější jedno nebo druhé.[33]
Mechanismus účinku
Heparin se váže na inhibitor enzymu antitrombin III (AT), způsobující konformační změnu, která má za následek jeho aktivaci zvýšením flexibility jeho smyčky reaktivního místa.[34] Aktivovaný AT se poté deaktivuje trombin, faktor Xa a další proteázy. Rychlost inaktivace těchto proteáz pomocí AT se může zvýšit až 1000krát v důsledku vazby heparinu.[35] Heparin se váže na AT prostřednictvím specifické sekvence sulfatace pentasacharidem obsažené v heparinovém polymeru:
- GlcNAc / NS (6S) -GlcA-GlcNS (3S, 6S) -IdoA (2S) -GlcNS (6S)
Konformační změna AT na vazbě na heparin zprostředkovává jeho inhibici faktoru Xa. Pro inhibici trombinu se však trombin musí také vázat na heparinový polymer v místě proximálně od pentasacharidu. Vysoce negativní hustota náboje heparinu přispívá k jeho velmi silné elektrostatický interakce s trombin.[19] Vznik a ternární komplex mezi AT, trombinem a heparinem vede k inaktivaci trombinu. Z tohoto důvodu je aktivita heparinu proti trombinu závislá na velikosti, přičemž ternární komplex vyžaduje pro efektivní tvorbu alespoň 18 sacharidových jednotek.[36] Naproti tomu aktivita antifaktoru Xa prostřednictvím AT vyžaduje pouze vazebné místo pro pentasacharid.
Tento rozdíl ve velikosti vedl k vývoji nízkomolekulární hepariny (LMWHs) a fondaparinux jako antikoagulancia. Fondaparinux se zaměřuje spíše na aktivitu proti faktoru Xa než na inhibici aktivity trombinu, s cílem usnadnit jemnější regulaci koagulace a zlepšit terapeutický index. Jedná se o syntetický pentasacharid, jehož chemická struktura je téměř identická s pentasacharidovou sekvencí vázající AT, kterou lze nalézt v polymerním heparinu a heparan sulfát.
U LMWH a fondaparinuxu riziko osteoporóza a heparinem indukovaná trombocytopenie (HIT) je snížen. Monitorování aktivovaný parciální tromboplastinový čas není také nutný a neodráží antikoagulační účinek, protože APTT je necitlivý na změny faktoru Xa.
Danaparoid směs heparansulfátu, dermatan sulfát, a chondroitin sulfát lze použít jako antikoagulant u pacientů, u kterých se vyvinula HIT. Protože danaparoid neobsahuje heparin nebo fragmenty heparinu, je zkřížená reaktivita danaparoidu s protilátkami indukovanými heparinem uváděna jako méně než 10%.[37]
Účinky heparinu se měří v laboratoři částečným časem tromboplastinu (aPTT ), jedno z opatření v době, kdy trvá krevní plazma srážet. Částečný čas tromboplastinu by neměl být zaměňován s protrombinový čas nebo PT, který měří čas srážení krve jinou cestou koagulační kaskáda.
Správa

Podává se heparin parenterálně protože není absorbován ze střeva kvůli vysokému zápornému náboji a velké velikosti. Může být aplikován intravenózně nebo subkutánně (pod kůži); intramuskulární injekce (do svalu) se vyhýbají kvůli možnosti formování hematomy. Kvůli své krátké biologii poločas rozpadu asi jednu hodinu musí být heparin podáván často nebo kontinuálně infuze. Nefrakcionovaný heparin má poločas asi jednu až dvě hodiny po infuzi,[38] zatímco LMWH má poločas rozpadu čtyři až pět hodin.[39] Použití LMWH umožnilo dávkování jednou denně, což nevyžaduje kontinuální infuzi léčiva. Pokud je nutná dlouhodobá antikoagulace, heparin se často používá pouze k zahájení antikoagulační léčby až do perorálního antikoagulancia, např. warfarin se projeví.
The Americká vysoká škola lékařů na hrudi publikuje klinické pokyny na dávkování heparinu.[40]
Přirozená degradace nebo odstranění
Nefrakcionovaný heparin má poločas asi jednu až dvě hodiny po infuzi,[38] zatímco nízkomolekulární heparin Poločas rozpadu je asi čtyřikrát delší. Nižší dávky heparinu mají mnohem kratší poločas než ty větší. Vazba heparinu na makrofág buňky jsou internalizovány a depolymerovány makrofágy. Rovněž se rychle váže na endoteliální buňky, což vylučuje vazbu na antitrombin, která vede k antikoagulačnímu účinku. U vyšších dávek heparinu bude vazba endoteliálních buněk nasycena, takže vylučování heparinu z krevního řečiště ledvinami bude pomalejší proces.[41]
Chemie
Struktura heparinu

Nativní heparin je polymer s a molekulární váha v rozmezí od 3 do 30 kDa, ačkoli průměrná molekulová hmotnost většiny komerčních heparinových přípravků je v rozmezí 12 až 15 kDa.[42] Heparin je členem glykosaminoglykan rodina sacharidy (což zahrnuje úzce související molekulu heparan sulfát ) a sestává z variabilně sulfatovaného opakování disacharid jednotka.[43]Níže jsou uvedeny hlavní disacharidové jednotky, které se vyskytují v heparinu. Nejběžnější disacharidová jednotka se skládá z 2-O-sulfatované kyselina iduronová a 6-0-sulfátovaný, N-sulfátovaný glukosamin, IdoA (2S) -GlcNS (6S). Například to tvoří 85% heparinů z hovězího plic a asi 75% z heparinu ze střevní sliznice prasat.[44]
Níže nejsou uvedeny vzácné disacharidy obsahující 3-O-sulfatovaný glukosamin (GlcNS (3S, 6S)) nebo volnou aminovou skupinu (GlcNH3+). Za fyziologických podmínek ester a amide sulfátové skupiny jsou deprotonovány a přitahují kladně nabité protiionty za vzniku heparinové soli. Heparin se obvykle podává v této formě jako antikoagulant.

GlcA-GlcNAc 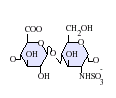
GlcA-GlcNS 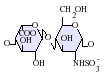
IdoA-GlcNS 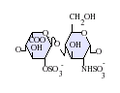
IdoA (2S) -GlcNS 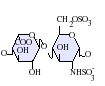
IdoA-GlcNS (6S) 
IdoA (2S) -GlcNS (6S)
GlcA = β-D-kyselina glukuronová, IdoA = α-L-kyselina iduronová, IdoA (2S) = 2Ó-sulfo-α-L-iduronová kyselina, GlcNAc = 2-deoxy-2-acetamido-α-D-glukopyranosyl, GlcNS = 2-deoxy-2-sulfamido-α-D-glukopyranosyl, GlcNS (6S) = 2-deoxy-2-sulfamido-α-D-glukopyranosyl-6-Ó-síran
Jedna jednotka heparinu („Howell jednotka ") je množství přibližně ekvivalentní 0,002 mg čistého heparinu, což je množství potřebné k udržení 1 ml tekutin kočičí krve po dobu 24 hodin při 0 ° C.[45]
Trojrozměrná struktura
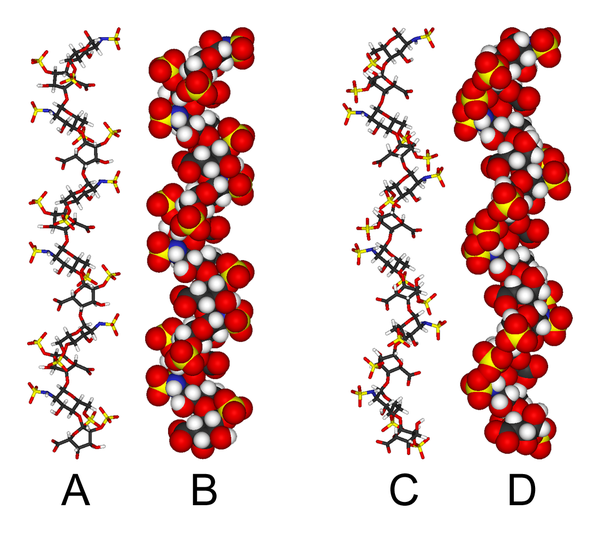
Trojrozměrná struktura heparinu je komplikovaná, protože kyselina iduronová mohou být přítomny v jedné ze dvou nízkoenergetických konformací, když jsou interně umístěny v oligosacharidu. Konformační rovnováha je ovlivněna stavem sulfatace sousedních glukosaminových cukrů.[46] Nicméně struktura roztoku heparinu dodekasacharidu složeného pouze ze šesti opakovacích jednotek GlcNS (6S) -IdoA (2S) byla stanovena pomocí kombinace technik NMR spektroskopie a molekulárního modelování.[47] Byly zkonstruovány dva modely, z nichž jeden byl v IdoA (2S) 2S0 konformace (A a B níže) a jeden, ve kterém jsou v 1C4 konformace (C a D níže). Žádný důkaz však nenaznačuje, že ke změnám mezi těmito konformacemi dochází ve vzájemné shodě. Tyto modely odpovídají kódu banky proteinových dat 1HPN.[48]
Na obrázku výše:
- A = 1HPN (všechny zbytky IdoA (2S) v 2S0 konformace) Prohlížeč Jmol
- B = poloměr van der Waals model vyplňování prostoru A
- C = 1 HPN (všechny zbytky IdoA (2S) v 1C4 konformace) Prohlížeč Jmol
- D = van der Waalsův model vyplňování poloměru prostoru C
V těchto modelech přijímá heparin helikální konformaci, jejíž rotace umisťuje shluky sulfátových skupin v pravidelných intervalech asi 17angstromy (1.7 nm ) na obou stranách spirálové osy.
Depolymerizační techniky
Převážná většina analýz prováděných na struktuře a funkci heparinu a heparansulfátu (HS) je základem buď chemických nebo enzymatických depolymerizačních technik nebo jejich kombinací.
Enzymatická
Enzymy tradičně používané k trávení heparinu nebo HS jsou přirozeně produkovány půdní bakterií Pedobacter heparinus (dříve pojmenovaný Flavobacterium heparinum).[49] Tato bakterie je schopna používat buď heparin nebo HS jako svůj jediný zdroj uhlíku a dusíku. K tomu produkuje řadu enzymů, jako je lyázy, glukuronidázy, sulfoesterázy, a sulfamidázy.[50] Lyázy se používají hlavně ve studiích heparin / HS. Bakterie produkuje tři lyázy, heparinázy I (ES 4.2.2.7 ), II (č EC číslo přiděleno) a III (ES 4.2.2.8 ) a každý má odlišné substrátové specificity, jak je podrobně popsáno níže.[51][52]
| Enzym heparinázy | Specifičnost podkladu |
| Heparináza I | GlcNS (± 6S) -IdoA (2S) |
| Heparináza II | GlcNS / Ac (± 6S) -IdoA (± 2S) GlcNS / Ac (± 6S) -GlcA |
| Heparináza III | GlcNS / Ac (± 6S) -GlcA / IdoA (s preferencí pro GlcA) |

Lyázy štěpí heparin / HS a eliminace beta mechanismus. Tato akce generuje nenasycenou dvojnou vazbu mezi C4 a C5 uronátového zbytku.[53][54] Nenasycený uronát C4-C5 se nazývá ΔUA nebo UA. Je to citlivé UV záření chromofor (maximální absorpce při 232 nm) a umožňuje sledovat rychlost enzymového štěpení a také poskytuje vhodný způsob detekce fragmentů produkovaných enzymovým štěpením.
Chemikálie
Kyselina dusitá lze použít k chemické depolymerizaci heparinu / HS. Kyselina dusitá může být použita při pH 1,5 nebo při vyšším pH 4. Za obou podmínek působí kyselina dusitá deaminativní štěpení řetězce.[55]

Při „vysokém“ (4) i „nízkém“ (1,5) pH dochází k deaminativnímu štěpení mezi GlcNS-GlcA a GlcNS-IdoA, i když pomalejší rychlostí při vyšším pH. Deaminační reakce, a tedy štěpení řetězce, je bez ohledu na O-sulfataci nesenou kteroukoli monosacharidovou jednotkou.
Při nízkém pH vede deaminativní štěpení k uvolňování anorganického SO4a konverze GlcNS na anhydromanóza (muž). Ošetření kyselinou dusitou s nízkým pH je vynikající metodou pro rozlišení N-sulfatovaných polysacharidů, jako je heparin a HS, od jiných než N-sulfatovaných polysacharidů, jako je chondroitin sulfát a dermatan sulfát, chondroitinsulfát a dermatansulfát nejsou citlivé na štěpení kyselinou dusitou.
Detekce v tělních tekutinách
Současné klinické laboratorní testy pro heparin se spoléhají spíše na nepřímé měření účinku léčiva než na přímé měření jeho chemické přítomnosti. Tyto zahrnují aktivovaný parciální tromboplastinový čas (APTT) a antifaktorová aktivita Xa. Vybraným vzorkem je obvykle čerstvá, nehemolyzovaná plazma z krve, která byla antikoagulována citrátem, fluoridem nebo oxalátem.[56][57]
Dějiny
Heparin objevil Jay McLean a William Henry Howell v roce 1916, ačkoli do klinických studií vstoupil až v roce 1935.[58] Původně byl izolován od psa játra buňky, proto jeho název (hepar nebo „ήπαρ“ je řečtina pro „játra“; hepar + -v ).
McLean byl studentem druhého ročníku lékařské fakulty Univerzita Johna Hopkinse, a pracoval pod vedením Howella při vyšetřování prokoagulačních přípravků, když izoloval v tucích rozpustný fosfatidový antikoagulant v jaterní tkáni.[59] V roce 1918 Howell vytvořil termín „heparin“ pro tento typ antikoagulancia rozpustného v tucích. Na počátku 20. let izoloval Howell ve vodě rozpustný produkt polysacharid antikoagulant, který také nazval „heparin“, i když se lišil od dříve objevených fosfatidových přípravků.[60][61] McLeanova práce jako chirurga pravděpodobně změnila zaměření skupiny Howell na hledání antikoagulancií, což nakonec vedlo k objevu polysacharidů.
Ve třicátých letech minulého století několik vědců zkoumalo heparin. Erik Jorpes na Karolinska Institutet publikoval svůj výzkum struktury heparinu v roce 1935,[62] což umožnilo švédské společnosti Vitrum AB uvést na trh první produkt s heparinem pro intravenózní použití v roce 1936. V letech 1933 a 1936 Connaught Medical Research Laboratories, poté součást University of Toronto, zdokonalila techniku výroby bezpečného netoxického heparinu, který by mohl být podáván pacientům, ve fyziologickém roztoku. První lidské pokusy s heparinem začaly v květnu 1935 a do roku 1937 bylo jasné, že Connaughtův heparin je bezpečný, snadno dostupný a účinný jako krevní antikoagulant. Před rokem 1933 byl heparin dostupný v malém množství, byl extrémně drahý a toxický a v důsledku toho neměl žádnou lékařskou hodnotu.[63]
Další funkce
- Zkumavky, Vacutainers, a kapilární trubky, které používají lithium sůl heparinu (lithium heparin) jako antikoagulant jsou obvykle označeny zelenými nálepkami a zelenými vrcholy. Heparin má výhodu oproti EDTA neovlivnění úrovní většiny ionty. Hladiny ionizovaného vápníku však mohou být sníženy, pokud je koncentrace heparinu ve vzorku krve příliš vysoká.[64] Heparin může s některými interferovat imunotesty, nicméně. Protože se obvykle používá lithium heparin, nelze z těchto zkumavek získat hladinu lithia u člověka; za tímto účelem obsahují královské modré (a tmavě zelené) vacutainery obsahující sodík používá se heparin.
- Okysličovače krve potažené heparinem jsou k dispozici pro použití v přístrojích srdce-plíce. Mimo jiné se předpokládá, že se tyto specializované oxygenátory celkově zlepšují biokompatibilita a hostitelská homeostáza poskytnutím charakteristik podobných charakteristikám nativního endotelu.
- DNA vazebná místa na RNA polymeráza může být obsazen heparinem, což brání polymeráze ve vazbě na promotorovou DNA. Tato vlastnost je využívána v řadě molekulárně biologických testů.
- Běžné diagnostické postupy vyžadují PCR amplifikace pacientovy DNA, která se snadno extrahuje z bílých krvinek ošetřených heparinem. To představuje potenciální problém, protože heparin může být extrahován spolu s DNA a bylo zjištěno, že interferuje s PCR reakcí při tak nízkých úrovních jako 0,002 U v 50 μL reakční směsi.[65]
- Heparin byl použit jako a chromatografie pryskyřice, působící jako oba afinitní ligand a iontoměnič.[66][67][68] Jeho polyaniontová struktura může napodobovat nukleové kyseliny, jako je DNA a RNA, což je užitečné pro čištění proteinů vázajících nukleové kyseliny, včetně DNA a RNA polymerázy a transkripční faktory.[69] Specifická afinita heparinu k VSV-G,[70] A virová obálka glykoprotein často zvyklý pseudotyp retrovir a lentiviral vektory pro genová terapie, umožňuje jeho použití pro následné čištění virových vektorů.[71][72]
Společnost a kultura
Kontaminace připomíná
Vzhledem k živočišnému zdroji farmaceutického heparinu je počet potenciálních nečistot ve srovnání s plně syntetickým terapeutickým činidlem relativně vysoký. Mezi možné biologické kontaminanty patří viry, bakteriální endotoxiny, látky přenosné spongiformní encefalopatie (TSE), lipidy, proteiny a DNA. Během přípravy heparinu farmaceutické kvality ze zvířecích tkání mohou být zavedeny nečistoty, jako jsou rozpouštědla, těžké kovy a cizí kationty. Metody používané k minimalizaci výskytu a identifikaci a / nebo eliminaci těchto kontaminujících látek jsou však dobře zavedené a jsou uvedeny v pokynech a lékopisech. Hlavní výzvou v analýze nečistot heparinu je detekce a identifikace strukturně souvisejících nečistot. Nejčastější nečistotou v heparinu je dermatansulfát (DS), známý také jako chondroitin sulfát B. Základním kamenem DS je disacharid složený z 1,3-vázaného N-acetyl galaktosaminu (GalN) a zbytku kyseliny uronové prostřednictvím 1,4 vazeb za vzniku polymeru. DS se skládá ze tří možných stavebních bloků kyseliny uronové (GlcA, IdoA nebo IdoA2S) a čtyř možných hexosaminů (GalNAc, Gal-NAc4S, GalNAc6S nebo GalNAc4S6S). Přítomnost kyseliny iduronové v DS ji odlišuje od chrondroitin sulfátu A a C a přirovnává ji k heparinu a HS. DS má celkově nižší hustotu záporného náboje ve srovnání s heparinem. Běžný přírodní kontaminant, DS je v heparinovém API přítomen na úrovních 1–7%, ale nemá prokázanou biologickou aktivitu, která ovlivňuje antikoagulační účinek heparinu.[73]
V prosinci 2007 se US Food and Drug Administration (FDA) připomněla zásilku heparinu kvůli růstu bakterií (Serratia marcescens ) v několika neotevřených injekčních stříkačkách tohoto produktu. S. marcescens může vést k život ohrožujícím zraněním a / nebo smrti.[74]
Odvolání z roku 2008 z důvodu falšování drog z Číny
V březnu 2008 major připomíná heparinu bylo oznámeno FDA kvůli kontaminaci surové zásoby heparinu dovážené z Číny.[75][76] Podle FDA zabil falšovaný heparin ve Spojených státech téměř 80 lidí.[77] Cizoložník byl identifikován jako „nadměrně sulfátovaný“ derivát chondroitin sulfát, populární doplněk odvozený od měkkýšů, který se často používá artritida, jehož cílem bylo nahradit skutečný heparin v testech účinnosti.[78]
Podle New York Times: „Problémy s heparinem hlášené agentuře zahrnují potíže s dýcháním, nevolnost, zvracení, nadměrné pocení a rychle klesající krevní tlak, které v některých případech vedly k životu nebezpečnému šoku“.
Použití při vraždách
V roce 2006 Petr Zelenka, zdravotní sestra v Česká republika, záměrně podával pacientům velké dávky, zabil 7 a pokusil se zabít 10 dalších.[79]
Problémy s předávkováním
V roce 2007 zdravotní sestra v Cedars-Sinai Medical Center omylem dal 12denní dvojčata herce Dennis Quaid dávka heparinu, která byla 1 000násobek doporučené dávky pro kojence.[80] Předávkování údajně vzniklo proto, že označení a design verze pro dospělé a kojence byly podobné. Rodina Quaidů následně žalovala výrobce, Baxter Healthcare Corp.,[81][82] a usadil se v nemocnici za 750 000 $.[83] Před Quaidovou nehodou bylo předávkováno šest novorozenců v metodistické nemocnici v Indianapolis v Indianě. Tři děti po chybě zemřely.[84]
V červenci 2008 se narodila další dvojčata v nemocnici Christus Spohn Hospital South v Corpus Christi, Texas, zemřel po náhodném podání předávkování drogou. Předávkování bylo způsobeno chybou míchání v nemocniční lékárně a nemělo vztah k obalu nebo označení produktu.[85] Od července 2008[Aktualizace], byla vyšetřována přesná příčina smrti dvojčat.[86][87]
V březnu 2010 byla dvouletému pacientovi po transplantaci z Texasu podána smrtelná dávka heparinu v lékařském centru University of Nebraska. Přesné okolnosti její smrti jsou stále předmětem vyšetřování.[88]
Výroba
Vychází se z heparinu farmaceutické kvality slizniční tkáně poražen masná zvířata jako např prasečí (prasečí) střeva nebo hovězí (dobytek) plíce.[89] Pokroky v syntéze heparinu byly učiněny v letech 2003 a 2008.[90] V roce 2011 byl popsán chemoenzymatický proces syntézy nízkomolekulárních heparinů z jednoduchých disacharidů.[91]
Výzkum
Jak je podrobně uvedeno v tabulce níže, potenciál je velký pro vývoj struktur podobných heparinu léky k léčbě široké škály nemoci, kromě jejich současného použití jako antikoagulancia.[92][93]
| Stavy nemoci citlivé na heparin | Heparinův účinek v experimentálních modelech | Klinický stav |
| Syndrom získané immunití nedostatečnisti | Snižuje schopnost virus lidské imunodeficience typy 1 a 2 k adsorpci na kultivované buňky T4.[94] | – |
| Syndrom respirační tísně dospělých | Snižuje aktivaci a akumulaci buněk v dýchacích cestách, neutralizuje mediátory a cytotoxické buněčné produkty a zlepšuje funkci plic na zvířecích modelech | Řízeno klinické testy |
| Alergická encefalomyelitida | Efektivní v zvířecí modely | – |
| Alergická rýma | Účinky jako u syndromu respirační tísně dospělých, ačkoli nebyl testován žádný konkrétní model nosu | Řízené klinické hodnocení |
| Artritida | Inhibuje akumulaci buněk, kolagen ničení a angiogeneze | Neoficiální zpráva |
| Astma | Co se týče syndromu respirační tísně dospělých, ukázalo se však také, že zlepšuje funkci plic v experimentálních modelech | Kontrolované klinické studie |
| Rakovina | Inhibuje nádor růst, metastáza a angiogeneze a zvyšuje dobu přežití na zvířecích modelech | Několik neoficiálních zpráv |
| Reakce přecitlivělosti opožděného typu | Efektivní na zvířecích modelech | – |
| Zánětlivé onemocnění střev | Inhibuje obecně přenos zánětlivých buněk, nebyl testován žádný konkrétní model | Kontrolované klinické studie |
| Intersticiální cystitida | Efektivní v humánním experimentálním modelu intersticiální cystitidy | Související molekula se nyní používá klinicky |
| Odmítnutí transplantace | Prodlužuje aloštěp přežití na zvířecích modelech | – |
- - označuje, že nejsou k dispozici žádné informace
V důsledku účinku heparinu na tak širokou škálu chorobných stavů je skutečně ve vývoji řada léčiv, jejichž molekulární struktury jsou identické nebo podobné těm, které se nacházejí v částech polymerního řetězce heparinu.[92]
| Molekula léčiva | Účinek nového léku ve srovnání s heparinem | Biologické aktivity |
| Heparin tetrasacharid | Nonantikoagulant, neimunogenní, perorálně aktivní | Antialergický |
| Pentosan polysulfát | Rostlina odvozená, málo antikoagulační aktivita, protizánětlivá, orálně aktivní | Protizánětlivé, antiadhezivní, antimetastatické |
| Fosfomannopentanóza sulfát | Silný inhibitor z heparanáza aktivita | Antimetastatický, antiangiogenní, protizánětlivý |
| Selektivně chemicky O-desulfátovaný heparin | Nemá antikoagulační aktivitu | Protizánětlivé, antialergické, antiadhezivní |
Reference
- ^ Injekce sodné soli heparinu Archivováno 05.09.2013 na Wayback Machine
- ^ heparin. In: Lexi-Drugs Online [databáze na internetu]. Hudson (OH): Lexi-Comp, Inc .; 2007 [citováno 2/10/12]. Dostupný z: http://online.lexi.com Archivováno 2012-02-15 na Wayback Machine. pro zobrazení je vyžadováno předplatné.
- ^ A b C d E F G „Heparin sodný“. Americká společnost farmaceutů zdravotnického systému. Archivováno z původního dne 27. ledna 2016. Citováno 1. ledna 2016.
- ^ A b „Injekce Heparin (sliznice) BP - Souhrn údajů o přípravku (SPC) - (eMC)“. www.medicines.org.uk. Září 2016. Archivováno z původního dne 20. prosince 2016. Citováno 15. prosince 2016.
- ^ McClatchey, Kenneth D. (2002). Klinická laboratorní medicína. Lippincott Williams & Wilkins. str. 662. ISBN 9780683307511. Archivováno od originálu 10. 9. 2017.
- ^ „Varování ohledně těhotenství a kojení heparinu“. Druhy.com. Archivováno z původního dne 27. ledna 2016. Citováno 15. ledna 2016.
- ^ Guyton, A. C .; Hall, J. E. (2006). Učebnice lékařské fyziologie. Elsevier Saunders. str. 464. ISBN 978-0-7216-0240-0.
- ^ Li, Jie Jack; Corey, E. J. (2013). Objevování drog: praktiky, procesy a perspektivy. John Wiley & Sons. str. 189. ISBN 9781118354469. Archivováno od originálu 10. 9. 2017.
- ^ Světová zdravotnická organizace (2019). Seznam základních léků Světové zdravotnické organizace: 21. seznam 2019. Ženeva: Světová zdravotnická organizace. hdl:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Licence: CC BY-NC-SA 3.0 IGO.
- ^ Rietschel, Robert L .; Fowler, Joseph F .; Fisher, Alexander A. (2008). Fisherova kontaktní dermatitida. PMPH-USA. str. 142. ISBN 9781550093780. Archivováno od originálu 10. 9. 2017.
- ^ Agnelli G; Piovella F; Buoncristiani P; et al. (1998). „Enoxaparin plus kompresní punčochy ve srovnání se samotnými kompresními punčochami v prevenci žilní tromboembolie po elektivní neurochirurgii“. N Engl J Med. 339 (2): 80–85. doi:10.1056 / NEJM199807093390204. PMID 9654538.
- ^ Bergqvist D; Agnelli G; Cohen AT; et al. (2002). "Trvání profylaxe proti venózní tromboembolii s enoxaparinem po chirurgickém zákroku na rakovinu". N Engl J Med. 346 (13): 975–980. doi:10.1056 / NEJMoa012385. PMID 11919306.
- ^ Handoll HH, Farrar MJ, McBirnie J, Tytherleigh-Strong G, Milne AA, Gillespie WJ (2002). „Heparin, nízkomolekulární heparin a fyzikální metody prevence hluboké žilní trombózy a plicní embolie po operaci zlomenin kyčle“. Cochrane Database Syst Rev (4): CD000305. doi:10.1002 / 14651858.CD000305. PMC 7043307. PMID 12519540.
- ^ Kusmer, Ken (20. září 2006). "Dítě z 3. ind. Preemie zemře na předávkování". Fox News. Associated Press. Archivovány od originál dne 18. 10. 2007. Citováno 2007-01-08.
- ^ Příručka australských léčivých přípravků 2019 (online). Adelaide: Australian Medicines Handbook Pty Ltd; 2019 leden. Dostupné z: https://amhonline.amh.net.au/
- ^ Interní lékařstvíJay H. Stein, str. 635
- ^ "Protamin sulfát". Americká společnost farmaceutů zdravotnického systému. Archivováno z původního dne 6. listopadu 2016. Citováno 8. prosince 2016.
- ^ Nader, H.B .; Chavante, S.F .; Dos-Santos, E.A.; Oliveira, F.W .; De-Paiva, J.F .; Jerônimo, S.M.B .; Medeiros, G.F .; De-Abreu, L.R.D .; et al. (1999). „Heparan sulfáty a hepariny: podobné sloučeniny plnící stejnou funkci u obratlovců a bezobratlých?“. Braz. J. Med. Biol. Res. 32 (5): 529–538. doi:10.1590 / S0100-879X1999000500005. PMID 10412563.
- ^ A b Cox, M .; Nelson D. (2004). Lehninger, Principy biochemie. Freemane. str.254. ISBN 978-0-7167-4339-2.
- ^ Warda M .; Mao W .; et al. (2003). "Turecké střevo jako komerční zdroj heparinu? Srovnávací strukturální studie střevních ptačích a savčích glykosaminoglykanů". Comp. Biochem. Physiol. B Biochem. Mol. Biol. 134 (1): 189–197. doi:10.1016 / S1096-4959 (02) 00250-6. PMID 12524047.
- ^ Ototani N, Kikuchi M, Yosizawa Z (1981). "Srovnávací studie struktur vysoce aktivních a relativně neaktivních forem velrybího heparinu". J. Biochem. 90 (1): 241–6. doi:10.1093 / oxfordjournals.jbchem.a133456. PMID 7287679.
- ^ Warda M; Gouda EM .; et al. (2003). "Izolace a charakterizace surového heparinu ze dromedárního střeva: hodnocení nového zdroje farmaceutického heparinu". Comp. Biochem. Physiol. C Toxicol. Pharmacol. 136 (4): 357–365. doi:10.1016 / j.cca.2003.10.009. PMID 15012907.
- ^ Bland CE; Ginsburg H .; et al. (1982). "Myší heparin proteoglykan. Syntéza monovrstvy fibroblastů žírných buněk během proliferace žírných buněk závislých na lymfocytech". J. Biol. Chem. 257 (15): 8661–8666. PMID 6807978.
- ^ Linhardt RJ; Ampofo SA .; et al. (1992). "Izolace a charakterizace lidského heparinu". Biochemie. 31 (49): 12441–12445. doi:10.1021 / bi00164a020. PMID 1463730.
- ^ Hovingh P, Linker A (1982). "Neobvyklý heparan sulfát izolovaný z humrů (Homarus americanus)". J. Biol. Chem. 257 (16): 9840–9844. PMID 6213614.
- ^ Hovingh P, Linker A (1993). „Glykosaminoglykany v Anodonta californiensis„sladkovodní slávka“. Biol. Býk. 185 (2): 263–276. doi:10.2307/1542006. JSTOR 1542006. PMID 27768418. Archivovány od originál dne 2007-09-27. Citováno 2007-03-22.
- ^ Pejler G; Danielsson A .; et al. (1987). "Struktura a antitrombin-vazebné vlastnosti heparinu izolovaného z škeblí Anomalocardia brasiliana a Tivela mactroides". J. Biol. Chem. 262 (24): 11413–11421. PMID 3624220.
- ^ Dietrich CP; Paiva JF .; et al. (1999). „Strukturální rysy a antikoagulační aktivity nového přírodního nízkomolekulárního heparinu z krevety Penaeus brasiliensis“. Biochim. Biophys. Acta. 1428 (2–3): 273–283. doi:10.1016 / S0304-4165 (99) 00087-2. PMID 10434045.
- ^ A b Medeiros GF; Mendes; A.; et al. (2000). „Distribuce sulfatovaných glykosaminoglykanů v živočišné říši: rozšířený výskyt sloučenin podobných heparinu u bezobratlých“. Biochim. Biophys. Acta. 1475 (3): 287–294. doi:10.1016 / S0304-4165 (00) 00079-9. PMID 10913828.
- ^ Flengsrud, Ragnar; Larsen, Mette Lie; Ødegaard, Ole Rasmus (2010). "Čištění, charakterizace a studie in vivo lososového heparinu". Výzkum trombózy. 126 (6): e409 – e417. doi:10.1016 / j.thromres.2010.07.004. ISSN 0049-3848. PMID 20937523.
- ^ Flengsrud R (2016). „Disacharidová analýza chondroitinu a heparinu z chovaného lososa obecného“. Glycoconjugate Journal. 33 (2): 121–123. doi:10.1007 / s10719-016-9652-8. hdl:11250/2388232. PMID 26993287. S2CID 671954.
- ^ Zhang, Fuming; Zhang, Zhenqing; Thistle, Robert; McKeen, Lindsey; Hosoyama, Saori; Toida, Toshihiko; Linhardt, Robert J .; Page-McCaw, Patrick (2008). "Strukturální charakterizace glykosaminoglykanů zebrafish v různých věkových kategoriích". Glycoconjugate Journal. 26 (2): 211–218. doi:10.1007 / s10719-008-9177-x. ISSN 0282-0080. PMC 2643322. PMID 18777207.
- ^ Hetzel, GR; et al. (2005), „The heparins: all the nephrologist should know“, Transplantace vytáčení Nephrol, 20 (10): 2036–2042, doi:10.1093 / ndt / gfi004, PMID 16030035.
- ^ Chuang YJ; Swanson R .; et al. (2001). „Heparin zvyšuje specificitu antitrombinu pro trombin a faktor Xa nezávisle na sekvenci reaktivní středové smyčky. Důkaz exositového determinantu specificity faktoru Xa v antitrombinu aktivovaném heparinem“. J. Biol. Chem. 276 (18): 14961–14971. doi:10,1074 / jbc.M011550200. PMID 11278930.
- ^ Bjork I, Lindahl U .; Lindahl (1982). "Mechanismus antikoagulačního působení heparinu". Mol. Buňka. Biochem. 48 (3): 161–182. doi:10.1007 / BF00421226. PMID 6757715. S2CID 29785682.
- ^ Herbert, Jean-Marc; Petitou, Maurice; Hérault, Jean-Pascal; Bernat, André; et al. (1999). "Syntéza trombinu inhibující heparinová mimetika bez vedlejších účinků". Příroda. 398 (6726): 417–422. Bibcode:1999 Natur.398..417P. doi:10.1038/18877. ISSN 0028-0836. PMID 10201371. S2CID 4339441.
- ^ Shalansky, Karen. DANAPAROID (Orgaran) pro trombocytopenii vyvolanou heparinem. Archivováno 2007-09-28 na Wayback Machine Vancouver Hospital & Health Sciences Center, únor 1998 Newsletter Drug & Therapeutics. Citováno dne 8. ledna 2007.
- ^ A b Eikelboom JW, Hankey GJ; Hankey (2002). „Nízkomolekulární hepariny a heparinoidy“. Medical Journal of Australia. 177 (7): 379–383. doi:10.5694 / j.1326-5377.2002.tb04807.x. PMID 12358583. S2CID 25553190. Archivováno z původního dne 2011-09-09.
- ^ Weitz JI (2004). „Nová antikoagulancia pro léčbu žilní tromboembolie“. Oběh. 110 (9 Suppl 1): I19–26. doi:10.1161 / 01.CIR.0000140901.04538.ae. PMID 15339877.
- ^ Hirsh, Jacku; Raschke, Robert (září 2004). „Heparin a nízkomolekulární heparin: Sedmá konference ACCP o antitrombotické a trombolytické terapii“. Hruď. 126 (3): 188S - 203S. doi:10,1378 / hrudník.126.3_suppl.188S. PMID 15383472.
- ^ Weitz DS, Weitz JI; Weitz (2010). „Aktualizace o heparinu: co potřebujeme vědět?“. Journal of trombózy a trombolýzy. 29 (2): 199–207. doi:10.1007 / s11239-009-0411-6. PMID 19882363. S2CID 33367673.
- ^ Francis CW, Kaplan KL (2006). "Kapitola 21. Principy antitrombotické terapie". In Lichtman MA, Beutler E, Kipps TJ, et al. (eds.). Williamsova hematologie (7. vydání). ISBN 978-0-07-143591-8. Archivovány od originál dne 07.07.2011.
- ^ Bentolila, A .; et al. (2000). „Syntéza a biologická aktivita polymerů na bázi aminokyselin podobná heparinu“. Polymery pro pokročilé technologie. 11 (8–12): 377–387. doi:10.1002 / 1099-1581 (200008/12) 11: 8/12 <377 :: AID-PAT985> 3.0.CO; 2-D.
- ^ Gatti, G .; Casu, B .; Hamer, G. K .; Perlin, A. S. (1979). "Studie o konformaci heparinu pomocí1H a13C NMR spektroskopie". Makromolekuly. 12 (5): 1001–1007. Bibcode:1979 MaMol..12.1001G. doi:10.1021 / ma60071a044. ISSN 0024-9297.
- ^ „Online lékařský slovník“. Centrum pro vzdělávání proti rakovině. 2000. Archivovány od originál dne 2007-08-13. Citováno 2008-07-11.
- ^ Ferro D, Provasoli A a kol. (1990). "Populace populací zbytků kyseliny L-iduronové v glykosaminoglykanových sekvencích". Sacharidy. Res. 195 (2): 157–167. doi:10.1016 / 0008-6215 (90) 84164-P. PMID 2331699.
- ^ Mulloy B, Forster MJ, Jones C, Davies DB (1. ledna 1993). „Studie N.M.R. a molekulárního modelování konformace roztoku heparinu“. Biochem. J. 293 (Pt 3): 849–858. doi:10.1042 / bj2930849. PMC 1134446. PMID 8352752.
- ^ B. Mulloy, M. J. Forster. „Studie N.M.R. a molekulárního modelování konformace roztoku heparinu“.
- ^ Shaya D; Tocilj A .; et al. (2006). „Krystalová struktura heparinázy II z Pedobacter heparinus a její komplex s disacharidovým produktem“. J. Biol. Chem. 281 (22): 15525–15535. doi:10,1074 / jbc.M512055200. PMID 16565082.
- ^ Galliher PM; Cooney CL .; et al. (1981). „Produkce heparinázy Flavobacterium heparinum“. Appl. Environ. Microbiol. 41 (2): 360–365. doi:10.1128 / AEM.41.2.360-365.1981. PMC 243699. PMID 7235692.
- ^ Linhardt RJ; Turnbull JE .; et al. (1990). "Zkoumání substrátové specificity heparinu a heparan sulfát lyáz". Biochemie. 29 (10): 2611–2617. doi:10.1021 / bi00462a026. PMID 2334685.
- ^ Desai UR; Wang HM .; Linhardt RJ. (1993). "Studie specificity na heparin lyázách z Flavobacterium heparinum". Biochemie. 32 (32): 8140–8145. doi:10.1021 / bi00083a012. PMID 8347612.
- ^ Linker A, Hovingh P .; Hovingh (1972). "Izolace a charakterizace oligosacharidů získaných z heparinu působením heparinázy". Biochemie. 11 (4): 563–568. doi:10.1021 / bi00754a013. PMID 5062409.
- ^ Linhardt RJ; Rice KG .; et al. (1988). "Mapování a kvantifikace hlavních oligosacharidových složek heparinu". Biochem. J. 254 (3): 781–787. doi:10.1042 / bj2540781. PMC 1135151. PMID 3196292.
- ^ Shively JE, Conrad HE .; Conrad (1976). "Tvorba anhydrosacharů při chemické depolymerizaci heparinu". Biochemie. 15 (18): 3932–3942. doi:10.1021 / bi00663a005. PMID 9127.
- ^ Hansen R, Koster A, Kukucka M, Mertzlufft F, Kuppe H (2000). „Rychlý test koagulace plné krve založený na anti-Xa aktivitě pro sledování nefrakcionovaného heparinu během kardiopulmonálního bypassu: pilotní vyšetřování“. Anesth. Analg. 91 (3): 533–538. doi:10.1213/00000539-200009000-00006. PMID 10960371. S2CID 44678237.
- ^ R. Baselt, Dispozice toxických drog a chemických látek u člověka, 8. vydání, Biomedical Publications, Foster City, CA, 2008, s. 728–729.
- ^ „Heparin používaný jako antikoagulant“. AnimalResearch.info. Archivováno z původního dne 2013-10-23.
- ^ MCLEAN, J. (1. ledna 1959). „Objev heparinu“. Oběh. 19 (1): 75–78. doi:10.1161 / 01.CIR.19.1.75. PMID 13619023.
- ^ Howell, W H. (1922). „Heparin, antikoagulant“. Dopoledne. J. Physiol. 63: 434–435.
- ^ Mueller RL, Scheidt S (1994). „Historie léků na trombotická onemocnění. Objev, vývoj a směry pro budoucnost“. Oběh. 89 (1): 432–449. doi:10.1161 / 01.cir.89.1.432. PMID 8281678.
- ^ Jorpes E (srpen 1935). "Chemie heparinu". The Biochemical Journal. 29 (8): 1817–1830. doi:10.1042 / bj0291817. PMC 1266692. PMID 16745848.
- ^ Rutty, CJ. „Miracle Blood Lubricant: Connaught and the Story of Heparin, 1928–1937“. Služby v oblasti výzkumu kulturního dědictví. Archivovány od originál 23. srpna 2007. Citováno 2007-05-21.
- ^ Higgins, C. (říjen 2007). „Použití heparinu při přípravě vzorků pro analýzu krevních plynů“ (PDF). Lékařský laboratorní pozorovatel. 39 (10): 16–8, 20, kvíz 22-3. PMID 18018679. Archivovány od originál (PDF) dne 10. 9. 2016. Citováno 2016-04-18.
- ^ Yokota M, Tatsumi N, Nathalang O, Yamada T, Tsuda I (1999). "Effects of heparin on polymerase chain reaction for blood white cells". J. Clin. Laboratoř. Anální. 13 (3): 133–40. doi:10.1002/(SICI)1098-2825(1999)13:3<133::AID-JCLA8>3.0.CO;2-0. PMC 6807949. PMID 10323479.
- ^ Xiong S, Zhang L, He QY (2008). "Fractionation of proteins by heparin chromatography". 2D PAGE: Sample Preparation and Fractionation. Methods Mol Biol. Metody v molekulární biologii ™. 424. str.213–21. doi:10.1007/978-1-60327-064-9_18. ISBN 978-1-58829-722-8. PMID 18369865.
- ^ "Affinity Chromatography". Sigma-Aldrich. Archivováno od originálu 2016-05-07.
- ^ "HiTrap Heparin HP". GE Healthcare Life Sciences. Archivováno od originálu na 2017-08-01.
- ^ "Performing a Separation of DNA binding proteins with GE Healthcare Products Based on Heparin". Sigma-Aldrich. Citováno 2019-04-16.
- ^ Guibinga GH, Miyanohara A, Esko JD, Friedmann T (May 2002). "Cell surface heparin sulfate is a receptor for attachment of envelope protein-free retrovirus-like particles and VSV-G pseudotyped MLV-derived retrovirus vectors to target cells". Mol Ther. 1 (5): 538–546. doi:10.1006/mthe.2002.0578. PMID 11991744.
- ^ Segura MM, Kamen A, Garnier A (2008). "Purification of retrovirus particles using heparin affinity chromatography". Gene Therapy Protocols. Methods Mol Biol. 434. s. 1–11. doi:10.1007/978-1-60327-248-3_1. ISBN 978-1-60327-247-6. PMID 18470635.
- ^ Segura MM, Kamen A, trudel P, Garnier A (20 May 2005). "A novel purification strategy for tetrovirus gene therapy vectors using heparin affinity chromatography". Biotechnol Bioeng. 4 (90): 391–404. doi:10.1002/bit.20301. PMID 15812800.
- ^ Beni S, Limtiaco JF, Larive CK (September 2011). "Analysis and characterization of heparin impurities". Analytická a bioanalytická chemie. 399 (2): 527–539. doi:10.1007/s00216-010-4121-x. PMC 3015169. PMID 20814668.
- ^ AM2 PAT, Inc. Issues Nationwide Recall of Pre-Filled Heparin Lock Flush Solution USP (5 mL in 12 mL Syringes) Archivováno 2007-12-23 na Wayback Machine, Am2pat, Inc. Press release, December 20, 2007[ověření se nezdařilo ]
- ^ CBS News, Podezření na ředění krve Archivováno 2012-10-23 na Wayback Machine
- ^ Informační stránka FDA Archivováno 2012-04-15 na Wayback Machine s informacemi a odkazy na vyšetřování FDA.
- ^ Darby, Nigel (18 September 2018). "The Past And Future Of Managing Raw Material And Process Risks In Biomanufacturing". Drug Discovery Online. VertMarkets. A Supply Chain Under Scrutiny. Citováno 1. listopadu 2018.
- ^ Zawisza, Julie (29 March 2008). "FDA Media Briefing on Heparin" (PDF). US Food and Drug Administration. Archivováno (PDF) z původního dne 6. března 2010. Citováno 2008-04-23.
- ^ Sestra spáchala vraždy, aby „otestovala“ lékaře Archivováno 2009-09-24 na Wayback Machine, Radio Praha, May 12, 2006
- ^ Ornstein, Charles; Gorman, Anna. (21. listopadu 2007) Los Angeles Times Report: Dennis Quaid's twins get accidental overdose. Archivováno 7. Března 2008 v Wayback Machine
- ^ Dennis Quaid and wife sue drug maker Archivováno 2010-06-28 na Wayback Machine, USA Today, December 4, 2007
- ^ Dennis Quaid files suit over drug mishap Archivováno 2008-07-04 na Wayback Machine, Los Angeles Times, December 5, 2007
- ^ Quaid Awarded $750,000 Over Hospital Negligence Archivováno 2009-04-15 na Wayback Machine, SFGate.com, December 16, 2008
- ^ WTHR story Archivováno 29. 06. 2011 na Wayback Machine about Methodist Hospital overdose
- ^ Statement by Dr. Richard Davis, Chief Medical Officer, CHRISTUS Spohn Health System[trvalý mrtvý odkaz ], 10. července 2008
- ^ At a Glance Heparin Overdose at Hospital Archivováno 2008-10-25 na Wayback Machine, Dallas Morning News, July 11. 2008
- ^ "Officials Investigate Infants' Heparin OD at Texas Hospital Archivováno 2008-07-11 na Wayback Machine." ABC News. July 11, 2008. Retrieved on July 24, 2008.
- ^ "Heparin Overdose Kills Toddler At Hospital, Staff Investigated Archivováno 2012-03-20 na Wayback Machine." "KETV Omaha." March 31, 2010.
- ^ Linhardt RJ, Gunay NS.; Gunay (1999). "Production and Chemical Processing of Low Molecular Weight Heparins". Sem. Tromb. Lem. 3: 5–16. PMID 10549711.
- ^ Bhattacharya, Ananyo (August 2008). "Flask synthesis promises untainted heparin". Chemický svět. Royal Society of Chemistry. Archivováno z původního dne 21. října 2012. Citováno 6. února 2011.
- ^ Xu, Y .; Masuko, S .; Takieddin, M .; Xu, H .; Liu, R .; Jing, J .; Mousa, S. A .; Linhardt, R. J .; Liu, J. (2011). „Chemoenzymatická syntéza homogenních heparinů s ultra nízkou molekulovou hmotností“. Věda. 334 (6055): 498–501. Bibcode:2011Sci ... 334..498X. doi:10.1126 / science.1207478. PMC 3425363. PMID 22034431.
- ^ A b Lever R.; Page C.P. (2002). "Novel drug opportunities for heparin". Recenze přírody Objev drog. 1 (2): 140–148. doi:10.1038/nrd724. PMID 12120095. S2CID 7334825.
- ^ Coombe D.R.; Kett W.C. (2005). "Heparan sulfate-protein interactions: therapeutic potential through structure-function insights". Buňka. Mol. Life Sci. 62 (4): 410–424. doi:10.1007/s00018-004-4293-7. PMID 15719168. S2CID 6380429.
- ^ Baba M, Pauwels R, Balzarini J, Arnout J, Desmyter J, De Clercq E (1988). "Mechanism of inhibitory effect of dextran sulfate and heparin on replication of human immunodeficiency virus in vitro". Proc. Natl. Acad. Sci. USA. 85 (16): 6132–6. Bibcode:1988PNAS...85.6132B. doi:10.1073/pnas.85.16.6132. PMC 281919. PMID 2457906.
Další čtení
- Marcum JA (January 2000). "The origin of the dispute over the discovery of heparin". Journal of the History of Medicine and Allied Sciences. 55 (1): 37–66. doi:10.1093/jhmas/55.1.37. PMID 10734720. S2CID 30050513.
- Mulloy B, Hogwood J, Gray E, Lever R, Page CP (January 2016). "Pharmacology of Heparin and Related Drugs". Farmakologické recenze. 68 (1): 76–141. doi:10.1124/pr.115.011247. PMID 26672027.
externí odkazy
- History of heparin
- "Heparin". Informační portál o drogách. Americká národní lékařská knihovna.