Apixaban - Apixaban
 | |
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Eliquis, další |
| Ostatní jména | BMS-562247-01 |
| AHFS /Drugs.com | Monografie |
| MedlinePlus | a613032 |
| Licenční údaje | |
| Těhotenství kategorie | |
| Trasy z správa | Pusou |
| ATC kód | |
| Právní status | |
| Právní status | |
| Farmakokinetické data | |
| Biologická dostupnost | ~50% |
| Vazba na bílkoviny | ~87% |
| Metabolismus | CYP3A4, CYP3A5, CYP1A2 a další |
| Odstranění poločas rozpadu | 9–14 h |
| Vylučování | Žluč (75%), ledviny (25%) |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.167.332 |
| Chemické a fyzikální údaje | |
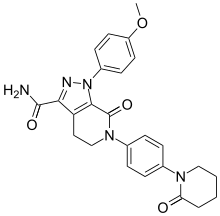
| Vzorec | C25H25N5Ó4 |
| Molární hmotnost | 459.506 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| (ověřit) | |
Apixaban, prodávané pod značkou Eliquis mimo jiné je antikoagulant léky používané k léčbě a prevenci krevní sraženiny a zabránit mrtvice u lidí s nonvalvular fibrilace síní.[2][3][4] Konkrétně se používá k prevenci tvorby krevních sraženin boky nebo náhrada kolena a u pacientů s anamnézou předchozích sraženin.[2][4] Používá se jako alternativa k warfarin a nevyžaduje monitorování pomocí krevních testů.[2] Je to přijato pusou.[2]
Mezi časté nežádoucí účinky patří krvácející a nevolnost.[2][3] Mezi další nežádoucí účinky patří krvácení kolem páteře a alergické reakce.[2] Použití se nedoporučuje během těhotenství nebo kojení.[3][1] Použití se zdá být relativně bezpečné u pacientů s mírným problémy s ledvinami.[3] Ve srovnání s warfarinem má méně interakce s jinými léky.[5] Je to přímý inhibitor faktoru Xa.[2]
Apixaban byl schválen pro lékařské použití v Evropské unii v květnu 2011 a ve Spojených státech v prosinci 2012.[6][7][2] V roce 2017 se jednalo o 93. nejčastěji předepisovanou léčbu ve Spojených státech s více než osmi miliony receptů.[8][9] V prosinci 2019 byly ve Spojených státech schváleny generické verze.[4]
Lékařské použití
Apixaban je indikován pro následující:[10]
- Chcete-li snížit riziko mrtvice a embolie u lidí s nonvalvular fibrilace síní.
- Hluboká žilní trombóza Prevence (DVT). DVT mohou vést k plicní embolie (PE) u pacientů s chirurgickým zákrokem na náhradu kolene nebo kyčle.
- Léčba jak DVT, tak PE.
- Snížení rizika opakování DVT a PE po počáteční terapii.
V EU je apixaban indikován k prevenci žilních tromboembolických příhod (VTE) u dospělých, kteří podstoupili elektivní náhradu kyčelního nebo kolenního kloubu, k prevenci cévní mozkové příhody a systémové embolie u dospělých s nevalvulární fibrilací síní (NVAF) s jedním nebo více více rizikových faktorů, k léčbě hluboké žilní trombózy (DVT) a plicní embolie (PE) u dospělých a k prevenci rekurentní DVT a PE u dospělých.[6]
Fibrilace síní
Apixaban doporučuje Národní institut pro zdraví a klinickou dokonalost k prevenci cévní mozkové příhody a systémové embolie u lidí s nevalvulární fibrilací síní a s alespoň jedním z následujících rizikových faktorů: předchozí cévní mozková příhoda nebo přechodný ischemický záchvat, věk 75 let nebo starší, diabetes mellitus nebo symptomatické srdeční selhání.[11]
Apixaban a další antikoagulancia (dabigatran, edoxaban a rivaroxaban ) se zdají být stejně účinné jako warfarin při prevenci nehemoragické cévní mozkové příhody u lidí s fibrilací síní a jsou spojeny s nižším rizikem intrakraniálního krvácení.[12][13]
Přestože apixaban mohou používat lidé s výrazně sníženou funkcí ledvin a pacienti na hemodialýze, nebyl u těchto skupin studován.[2] Lze použít celou dávku apixabanu (5 mg [bid]), pokud neplatí alespoň dvě z následujících charakteristik: věk pacienta je 80 let nebo starší, tělesná hmotnost je 60 kg nebo méně a kreatinin v séru je 1,5 mg / dL nebo vyšší , v takovém případě je indikováno snížení dávky na 2,5 mg dvakrát denně.[14]
Vedlejší efekty
Krvácející
Apixaban může zvýšit riziko krvácení, které může být závažné a potenciálně smrtelné. Současné užívání s jinými léky, které ovlivňují srážení krve může toto riziko dále zvýšit. To zahrnuje léky, jako jsou jiná antikoagulancia, heparin, aspirin, antiagregační léky, selektivní inhibitory zpětného vychytávání serotoninu, inhibitory zpětného vychytávání serotoninu a norepinefrinu, a nesteroidní protizánětlivé léky (NSAID).[10][15][16][17]
Andexanet alfa je Úřad pro kontrolu potravin a léčiv (FDA) schváleno protijed pro apixaban u lidí s nekontrolovanými a život ohrožujícími krvácivými příhodami.[18][19]
Páteřní punkce
Po spinální anestézii nebo punkci jsou lidé, kteří jsou léčeni antitrombotiky, vystaveni vyššímu riziku vzniku a hematom, který může způsobit dlouhodobé nebo trvalé ochrnutí. Riziko toho může být zvýšeno použitím epidurální nebo intratekální katétry po chirurgickém zákroku nebo při současném užívání léčivých látek, které ovlivňují hemostáza.[10]
Mechanismus účinku
Apixaban je vysoce selektivní, orálně biologicky dostupný a reverzibilní přímý inhibitor volného a sraženého faktor Xa. Faktor Xa katalyzuje přeměnu protrombinu na trombin, konečný enzym v koagulační kaskádě, který je zodpovědný za fibrin tvorba sraženin.[20] Apixaban nemá přímý účinek na agregace krevních destiček, ale inhibicí faktoru Xa nepřímo snižuje tvorbu sraženin vyvolanou trombinem.[10]
Dějiny
Apixaban byl schválen pro lékařské použití v Evropské unii v květnu 2011.[6]
A nová aplikace léku (NDA) ke schválení apixabanu byl předložen do USA Úřad pro kontrolu potravin a léčiv (FDA) Bristol-Myers Squibb (BMS) a Pfizer společně po ukončení klinického hodnocení ARISTOTLE v roce 2011.[21][7] Apixaban byl schválen pro prevenci cévní mozkové příhody u lidí s fibrilací síní 28. prosince 2012.[7][22] Dne 13. března 2014 bylo schváleno pro další indikaci prevence hluboká žilní trombóza a plicní embolie u lidí, kteří nedávno podstoupili náhradu kolene nebo kyčle.[23][24] 21. srpna 2014 schválila FDA apixaban pro další indikaci léčby opakující se hluboké žilní trombózy a plicní embolie.[23][25] Během svého vývoje byla droga známá jako BMS-562247-01.[26] Do konce roku 2019 činil prodej produktu společností BMS třicet procent jejich čtvrtletních výnosů.[27] V prosinci 2019 schválila americká FDA generickou verzi, kterou společně vyrobila Mylan a Mikro laboratoře.[27]
Reference
- ^ A b C „Užívání Apixabanu (Eliquis) během těhotenství“. Drugs.com. 21. června 2019. Citováno 13. srpna 2020.
- ^ A b C d E F G h i „Monografie Apixaban pro profesionály“. Drugs.com. Americká společnost farmaceutů zdravotnického systému. Citováno 27. března 2019.
- ^ A b C d Britské národní složení: BNF 76 (76 ed.). Pharmaceutical Press. 2018. s. 124–125. ISBN 9780857113382.
- ^ A b C „FDA schvaluje první generika Eliquis“. NÁS. Úřad pro kontrolu potravin a léčiv (FDA). 23. prosince 2019. Archivováno z původního dne 23. prosince 2019. Citováno 23. prosince 2019.
 Tento článek včlení text z tohoto zdroje, který je v veřejná doména.
Tento článek včlení text z tohoto zdroje, který je v veřejná doména. - ^ Kiser, Kathryn (2017). Perorální antikoagulační léčba: případy a klinická korelace. Springer. p. 11. ISBN 9783319546438.
- ^ A b C „Eliquis EPAR“. Evropská agentura pro léčivé přípravky. Citováno 22. dubna 2020. Text byl zkopírován z tohoto zdroje, kterým je © Evropská agentura pro léčivé přípravky. Reprodukce je povolena za předpokladu, že je uveden zdroj.
- ^ A b C „Balíček pro schválení léků: Eliquis (apixaban) NDA # 202155“. NÁS. Úřad pro kontrolu potravin a léčiv (FDA). 13. února 2013. Citováno 23. prosince 2019.
- ^ „Top 300 roku 2020“. ClinCalc. Citováno 11. dubna 2020.
- ^ „Apixaban - statistika užívání drog“. ClinCalc. Citováno 11. dubna 2020.
- ^ A b C d „Tabletu Eliquis- apixaban, potahované 30denní startovací balení Eliquis- souprava apixaban“. DailyMed. 26. listopadu 2019. Citováno 22. dubna 2020.
- ^ „Apixaban k prevenci cévní mozkové příhody a systémové embolie u lidí s nevalvulární fibrilací síní“ (PDF). National Institute for Health and Care Excellence. Leden 2013. Citováno 26. února 2016.
- ^ Gómez-Outes, A; Terleira-Fernández, AI; Calvo-Rojas, G; Suárez-Gea, ML; Vargas-Castrillón, E (2013). „Dabigatran, rivaroxaban nebo apixaban versus warfarin u pacientů s nevalvulární fibrilací síní: Systematický přehled a metaanalýza podskupin“. Trombóza. 2013: 640723. doi:10.1155/2013/640723. PMC 3885278. PMID 24455237.
- ^ Lowenstern, Angela; Al-Khatib, Sana M .; Sharan, Lauren; Chatterjee, Ranee; Allen LaPointe, Nancy M .; Shah, Bimal; Borre, Ethan D .; Raitz, Giselle; Sbohem, Adame; Yapa, Roshini; Davis, J. Kelly (4. prosince 2018). „Intervence pro prevenci tromboembolických příhod u pacientů s fibrilací síní: systematický přehled“. Annals of Internal Medicine. 169 (11): 774–787. doi:10,7326 / M18-1523. ISSN 0003-4819. PMC 6825839. PMID 30383133.
- ^ Informace o předpisu však uznávají, že „studie klinické účinnosti a bezpečnosti s přípravkem Eliquis nezaznamenávaly pacienty s terminálním onemocněním ledvin (ESRD) na dialýze“.
- ^ „Fibrilace síní a nová perorální antikoagulační léčiva“. NÁS. Úřad pro kontrolu potravin a léčiv (FDA). 2. prosince 2015. Citováno 22. dubna 2020.
- ^ „Fibrilace síní, perorální antikoagulační léky a jejich reverzní látky“. US Food and Drug Administration. 2. prosince 2015. Citováno 22. dubna 2020.
- ^ „Při použití přímých perorálních antikoagulancií po studii financované EMA není nutná žádná změna“. Evropská agentura pro léčivé přípravky (EMA). 27. března 2020. Citováno 22. dubna 2020.
- ^ "Injekce andexxa- andexanet alfa, prášek, lyofilizovaný, pro roztok". DailyMed. 8. ledna 2019. Citováno 23. prosince 2019.
- ^ „Andexxa (koagulační faktor Xa (rekombinantní), inaktivovaný-zhzo)“. NÁS. Úřad pro kontrolu potravin a léčiv (FDA). 31. prosince 2018. Citováno 22. dubna 2020.
- ^ Frost C, Wang J, Nepál S a kol. (Únor 2013). „Apixaban, perorální, přímý inhibitor faktoru Xa: bezpečnost jedné dávky, farmakokinetika, farmakodynamika a účinek potravy u zdravých subjektů“. Br J Clin Pharmacol. 75 (2): 476–87. doi:10.1111 / j.1365-2125.2012.04369.x. PMC 3558798. PMID 22759198.
- ^ Granger, Christopher (15. září 2011). "Apixaban versus warfarin u pacientů s fibrilací síní". New England Journal of Medicine. 365 (11): 981–992. doi:10.1056 / NEJMoa1107039. PMID 21870978.
- ^ Cada, Dennis J .; Levien, Terri L .; Baker, Danial E. (29. května 2013). "Apixaban". Nemocniční lékárna. 48 (6): 494–511. doi:10,1310 / hpj4806-494. ISSN 0018-5787. PMC 3839491. PMID 24421512.
- ^ A b "Léky schválené FDA: Eliquis (apixaban)". NÁS. Úřad pro kontrolu potravin a léčiv (FDA). Citováno 23. prosince 2019.
- ^ Neale, Todd (14. března 2014). „FDA podporuje Apixaban pro prevenci DVT“. MedPage Today. Citováno 17. září 2015.
- ^ „Americký FDA schvaluje Eliquis (apixaban) pro léčbu hluboké žilní trombózy (DVT) a plicní embolie (PE) a pro snížení rizika opakované DVT a PE po počáteční terapii“ (Tisková zpráva). Pfizer. 21. srpna 2014. Citováno 26. února 2016.
- ^ "Apixaban". pubchem.ncbi.nlm.nih.gov. Citováno 3. ledna 2020.
- ^ A b „PRVNÍ: Mylan, Micro Labs dostanou uznání USFDA za generickou verzi ředidla pro krev Eliquis“. Obchodní lékařské dialogy. Nové Dillí, Indie: Minerva Medical Treatment. 24. prosince 2019. Citováno 24. prosince 2019.
externí odkazy
- "Apixaban". Informační portál o drogách. Americká národní lékařská knihovna.
