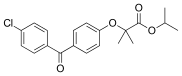
Fenofibrát - Fenofibrate
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Fenoglide, Lipofen, další |
| AHFS /Drugs.com | Monografie |
| MedlinePlus | a601052 |
| Licenční údaje |
|
| Těhotenství kategorie |
|
| Trasy z správa | Pusou |
| ATC kód | |
| Právní status | |
| Právní status | |
| Farmakokinetické data | |
| Vazba na bílkoviny | 99% |
| Metabolismus | glukuronidace |
| Odstranění poločas rozpadu | 20 h |
| Vylučování | moč (60%), výkaly (25%) |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Informační karta ECHA | 100.051.234 |
| Chemické a fyzikální údaje | |
| Vzorec | C20H21ClÓ4 |
| Molární hmotnost | 360.83 g · mol−1 |
| 3D model (JSmol ) | |
| Bod tání | 80 až 81 ° C (176 až 178 ° F) |
| |
| |
| (ověřit) | |
Fenofibrát, prodávané pod značkou Tricor mimo jiné je lék na fibrát třída používaná k léčbě abnormální hladiny lipidů v krvi.[2] Je to méně výhodné statin léky, protože se nezdá, že by snižovaly riziko srdeční choroba nebo smrt.[2][3] Jeho použití se doporučuje společně se změnami stravy.[2] Užívá se ústy.[2]
Mezi časté nežádoucí účinky patří problémy s játry, dýchací potíže, bolesti břicha, svalové problémy a nevolnost.[2] Mezi závažné nežádoucí účinky patří toxická epidermální nekrolýza, rhabdomyolýza, žlučové kameny, krevní sraženiny a pankreatitida.[2] Použití v těhotenství a kojení se nedoporučuje.[3][4] Funguje řadou mechanismů.[2]
To bylo patentováno v roce 1969 a vstoupilo do lékařského použití v roce 1975.[5] Je k dispozici jako generické léky.[3] V roce 2017 se jednalo o 70. nejčastěji předepisovanou léčbu ve Spojených státech s více než jedenácti miliony receptů.[6][7]
Lékařské použití
Fenofibrát se používá hlavně pro primární použití hypercholesterolemie nebo smíšené dyslipidemie. Zdá se, že fenofibrát snižuje riziko kardiovaskulární onemocnění a možná diabetická retinopatie u těch s diabetes mellitus,[8][9] a nejprve indikováno pro snížení progrese diabetické retinopatie u pacientů s diabetem typu 2 a stávající diabetickou retinopatií v Austrálii.[10] Rovněž se jeví jako užitečné při snižování amputace dolních končetin u stejné skupiny lidí.[11] Fenofibrát má také použití mimo označení jako další terapie vysoké hladiny kyseliny močové v krvi u lidí, kteří mají dna.[12]
Používá se navíc k strava snížit zvýšené lipoprotein s nízkou hustotou cholesterol (LDL), celkem cholesterol, triglyceridy (TG) a apolipoprotein B (apo B) a ke zvýšení lipoprotein s vysokou hustotou cholesterolu (HDL) u dospělých s primární hypercholesterolemií nebo smíšenou dyslipidemií.[13]
- Těžká hypertriglyceridemie typ IV nebo V
Používá se jako doplněk stravy k léčbě dospělých s těžkou hypertriglyceridemií. Zlepšení kontroly glykemie u diabetiků vykazujících chylomikronemii nalačno obvykle sníží potřebu farmakologických intervencí.[13]
Statiny zůstávají první linií pro léčbu cholesterolu v krvi. Pokyny AHA z roku 2013 nenalezly důkazy o rutinním užívání dalších léků.[14]
V roce 2016 FDA dále podala „Zrušení schválení indikací souvisejících se společným podáváním se statiny v aplikacích pro tablety s prodlouženým uvolňováním niacinu a tobolkami s opožděným uvolňováním kyseliny fenofibrové“ s tím, že „agentura dospěla k závěru, že souhrn vědeckých důkazů již není podporuje závěr, že snížení hladiny triglyceridů vyvolané léčivem a / nebo zvýšení hladin HDL cholesterolu u pacientů léčených statiny má za následek snížení rizika kardiovaskulárních příhod. tablety a tobolky kyseliny fenofibrové DR pro společné podávání se statiny již nepřevažují nad riziky a schválení pro tuto indikaci by mělo být zrušeno. “[15]
Kontraindikace
Fenofibrát je kontraindikován u:[13]
- Pacienti s těžkou poškození ledvin, včetně pacientů na dialýze (2,7násobné zvýšení expozice a zvýšená akumulace během chronického dávkování u pacientů s odhadem rychlost glomerulární filtrace <30 ml / min)
- Pacienti s aktivním onemocněním jater, včetně pacientů s primární biliární cirhóza a nevysvětlitelné trvalé jaterní funkční test abnormality
- Pacienti s již existujícími žlučník choroba
- Kojící matky
- Pacienti se známými přecitlivělost na fenofibrát nebo kyselinu fenofibrovou
Nepříznivé účinky
Nejběžnější nežádoucí účinky (> 3% pacientů se současně podávanými statiny) jsou[16]
- Bolest hlavy
- Bolesti zad
- Nasofaryngitida
- Nevolnost
- Myalgie
- Bolesti kloubů nebo artralgie
- Průjem
- Infekce horních cest dýchacích
- Kameny (Ledvinové kameny )
Opatření
Pokud se fenofibrát a statin podávají jako kombinovaná léčba, doporučuje se podávat fenofibrát ráno a statin v noci, aby se maximální dávky nepřekrývaly.[17]
Muskuloskeletální
- Myopatie a rhabdomyolýza; zvýšené riziko při současném podávání se statinem, zejména u starších pacientů a pacientů s cukrovka, selhání ledvin, hypotyreóza[16]
Hepatotoxicita
- Může zvýšit sérum transaminázy; jaterní testy by měly být pravidelně sledovány[16]
Nefrotoxicita
- Může zvýšit sérum kreatinin úrovně; renální funkce by měly být pravidelně sledovány u pacientů s chronické onemocnění ledvin[16]
Žlučové
- Může zvýšit vylučování cholesterolu do žluči, což vede k riziku cholelitiáza; pokud existuje podezření, jsou indikovány studie žlučníku. Viz část „Interakce“ níže Sekvestrant žlučových kyselin[16]
Srážení / krvácení
- Při souběžné léčbě perorálními antikoagulancii Coumadin buďte opatrní (např. warfarin ). Upravte dávkování přípravku Coumadin tak, aby byl protrombinový čas / INR udržován na požadované úrovni, aby se zabránilo komplikacím krvácení.[16]
Předávkovat
„Neexistuje žádná specifická léčba předávkování tobolkami se zpožděným uvolňováním kyselinou fenofibrovou. Je indikována obecná podpůrná péče, včetně monitorování Známky života a pozorování klinického stavu. “Navíc hemodialýza by nemělo být považováno za možnost předávkování, protože fenofibrát se silně váže na plazmatické proteiny a nedialyzuje dobře.[16]
Interakce
Tyto lékové interakce s fenofibrátem jsou považovány za hlavní a mohou vyžadovat úpravy léčby:
- Sekvestranty žlučových kyselin (např. cholestyramin, colestipol ): Pokud se to vezme dohromady, pryskyřice žlučových kyselin se mohou vázat na fenofibrát, což vede ke snížení absorpce fenofibrátu. Aby se maximalizovala absorpce, musí pacienti oddělit podávání nejméně 1 hodinu před nebo 4 hodiny až 6 hodin po užití sekvestrantu žlučových kyselin.[16][18]
- Imunosupresiva (např. cyklosporin nebo takrolimus ): Při současném užívání imunosupresiv a fenofibrátu existuje zvýšené riziko renální dysfunkce. Při současném podávání dalších léků, které snižují funkci ledvin, postupujte opatrně.[19]
- Antagonisté vitaminu K (např. warfarin ): Jak již bylo zmíněno, fenofibrát interaguje s kumadinovými antikoagulancii, aby se zvýšilo riziko krvácení. Může být nezbytná úprava dávkování antagonisty vitaminu K.[16]
- Statiny: Kombinace statiny a fenofibrát může zvýšit riziko rhabdomyolýzy nebo myopatie.[20]
Mechanismus účinku
„Stručně řečeno, zvýšený katabolismus částic bohatých na triglyceridy a snížená sekrece VLDL jsou základem hypotriglyceridemického účinku fibrátů, zatímco jejich účinek na metabolismus HDL je spojen se změnami v HDL. apolipoprotein výraz."[21]
Fenofibrát je derivát kyseliny fibrové, a proléčivo obsahující kyselinu fenofibrovou navázanou na isopropylester. Aktivací snižuje hladinu lipidů receptor aktivovaný proliferátorem peroxisomu alfa (PPARα). PPARα se aktivuje lipoproteinová lipáza a snižuje apoprotein CIII, což zvyšuje lipolýzu a eliminaci částic bohatých na triglyceridy z plazmy.[21]
PPARa také zvyšuje apoproteiny AI a AII, snižuje apoprotein B obsahující VLDL a LDL a zvyšuje apoprotein AI a AII obsahující HDL.
Formulace
Fenofibrát je k dispozici v několika formulace a prodává se pod několika značkami, včetně Tricor od AbbVie, Lipofen od Kowa Pharmaceuticals America Inc, Lofibra od Teva, Lipanthyl, Lipidil, Lipantil micro a Supralip od Abbott Laboratories, Fenocor-67 od Ordain Health Care, Fibractiv 105/35 od Cogentrix Pharma (Indie), Fenogal od SMB Laboratories, Antara od Oscient Pharmaceuticals, Tricheck od Zydus (CND), Atorva TG od Zydus Medica, Golip od GolgiUSA a Stanlip od Ranbaxy (Indie). Různé formulace se mohou lišit, pokud jde o farmakokinetické vlastnosti biologická dostupnost; některé musí být užívány s jídlem, zatímco jiné mohou být užívány bez ohledu na jídlo.[22]
Aktivní forma fenofibrátu, kyselina fenofibrová, je k dispozici také ve Spojených státech a prodává se jako Trilipix. Kyselinu fenofibrovou lze užívat bez ohledu na načasování jídla.[16][23]
Kontroverze
Ve Spojených státech byl Tricor přeformulován v roce 2005. Toto přeformulování je kontroverzní, protože je považováno za pokus potlačit konkurenci generických ekvivalentů drogy,[24] a je předmětem antimonopolní zákon soudní spor od výrobce generických léků Teva.[24] Lofibra, která je také k dispozici ve Spojených státech, je dostupná v 54 a 160 mg tabletách a 67, 134 a 200; mg mikronizovaný kapsle.[25] Generické ekvivalenty tobolek Lofibra jsou v současné době k dispozici ve všech třech silách ve Spojených státech. V Evropě je k dispozici buď potahovaná tableta nebo kapsle; rozsah síly zahrnuje 67, 145, 160 a 200 mg. Rozdíly mezi silnými stránkami jsou výsledkem změněných biologická dostupnost (frakce absorbovaná tělem) v důsledku velikosti částic. Například 200 mg může být nahrazeno 160 mg mikronizovaného fenofibrátu. Síla 145 mg je nová síla, která se objevila v letech 2005-2006 a která také nahrazuje 200 nebo 160 mg, protože fenofibrát je nanonizovaný (tj. Velikost částic je pod 400 nm).
Dějiny
Fenofibrát byl poprvé syntetizován v roce 1974 jako derivát klofibrát, a krátce nato byl uveden na francouzský trh. Původně byl známý jako procetofen a později byl přejmenován na fenofibrát Světová zdravotnická organizace Mezinárodní nechráněný název pokyny.[26]
Fenofibrát byl vyvinut společností Groupe Fournier SA z Francie, kterou v roce 2005 získala společnost Solvay Pharmaceuticals, obchodní jednotka belgické společnosti Solvay S.A.. V roce 2009 společnost Solvay získala společnost Abbott Laboratories (nyní AbbVie v USA a Mylan v Evropě, Kanadě, Austrálii, na Novém Zélandu a v Japonsku).
Výzkum
COVID-19
V červenci 2020 vědci z Izraele a USA navrhli, že fenofibrát může významně zpomalit replikaci viru SARS-CoV-2 v plicních buňkách.[27] Tato hypotéza čeká na testování v klinických studiích.
Reference
- ^ „Fenofibrát 267mg tobolky - souhrn údajů o přípravku (SmPC)“. (emc). 12. února 2020. Citováno 13. dubna 2020.
- ^ A b C d E F G „Monografie o kyselině fenofibrové / fenofibrátu pro profesionály“. Drugs.com. Americká společnost farmaceutů zdravotnického systému. Citováno 3. března 2019.
- ^ A b C Britské národní složení: BNF 76 (76 ed.). Pharmaceutical Press. 2018. str. 198. ISBN 9780857113382.
- ^ „Varování týkající se těhotenství a kojení fenofibrátem“. Drugs.com. Citováno 3. března 2019.
- ^ Fischer, Jnos; Ganellin, C. Robin (2006). Analogový objev drog. John Wiley & Sons. str. 474. ISBN 9783527607495.
- ^ „Top 300 roku 2020“. ClinCalc. Citováno 11. dubna 2020.
- ^ „Fenofibrát - statistika užívání drog“. ClinCalc. Citováno 11. dubna 2020.
- ^ Wong TY, Simó R, Mitchell P (červenec 2012). „Fenofibrát - potenciální systémová léčba diabetické retinopatie?“. Jsem J. Ophthalmol. 154 (1): 6–12. doi:10.1016 / j.ajo.2012.03.013. PMID 22709833.
- ^ Fazio S (2009). "Více klinických lekcí ze studie FIELD". Cardiovasc Drugs Ther. 23 (3): 235–41. doi:10.1007 / s10557-008-6160-5. PMID 19160032. S2CID 7987660.
- ^ „Australská veřejná hodnotící zpráva o fenofibrátu“. TGA. TGA. Citováno 27. června 2015.
- ^ Steiner G (2009). „Jak můžeme zlepšit řízení vaskulárního rizika u cukrovky typu 2: postřehy z oblasti FIELD“. Cardiovasc Drugs Ther. 23 (5): 403–8. doi:10.1007 / s10557-009-6190-7. PMID 19757004. S2CID 12747599.
- ^ Khanna D, Fitzgerald JD, Khanna PP, Bae S, Singh MK, Neogi T, Pillinger MH, Merill J, Lee S, Prakash S, Kaldas M, Gogia M, Perez-Ruiz F, Taylor W, Lioté F, Choi H, Singh JA, Dalbeth N, Kaplan S, Niyyar V, Jones D, Yarows SA, Roessler B, Kerr G, King C, Levy G, Furst DE, Edwards NL, Mandell B, Schumacher HR, Robbins M, Wenger N, Terkeltaub R (2012). „Pokyny American College of Rheumatology pro léčbu dny. Část 1: systematické nefarmakologické a farmakologické terapeutické přístupy k hyperurikemii“. Arthritis Care Res (Hoboken). 64 (10): 1431–46. doi:10,1002 / akr.21772. PMC 3683400. PMID 23024028.
- ^ A b C Příloha: Abbot Laboratories (říjen 2010)
- ^ Stone NJ, Robinson JG, Lichtenstein AH, Bairey Merz CN, Blum CB, Eckel RH, Goldberg AC, Gordon D, Levy D, Lloyd-Jones DM, McBride P, Schwartz JS, Shero ST, Smith SC, Watson K, Wilson PW , Eddleman KM, Jarrett NM, LaBresh K, Nevo L, Wnek J, Anderson JL, Halperin JL, Albert NM, Bozkurt B, Brindis RG, Curtis LH, DeMets D, Hochman JS, Kovacs RJ, Ohman EM, Pressler SJ, Sellke FW, Shen WK, Smith SC, Tomaselli GF (2014). „Pokyny ACC / AHA z roku 2013 k léčbě cholesterolu v krvi ke snížení aterosklerotického kardiovaskulárního rizika u dospělých: zpráva pracovní skupiny American College of Cardiology / American Heart Association o praktických pokynech“. Oběh. 129 (25 Suppl 2): S1–45. doi:10.1161 / 01.cir.0000437738.63853.7a. PMID 24222016.
- ^ https://s3.amazonaws.com/public-inspection.federalregister.gov/2016-08887.pdf
- ^ A b C d E F G h i j Informace o předepisování štítku FDA na bázi kyseliny fenofibrové„Informace o štítku FDA“ (PDF). FDA.
- ^ Wierzbicki AS, Mikhailidis DP, Wray R, Schacter M, Cramb R, Simpson WG, Byrne CB (2003). „Kombinace statin-fibrát: léčba hyperlipidemie: přehled“. Curr Med Res Opin. 19 (3): 155–68. doi:10.1185/030079903125001668. PMID 12814127. S2CID 35948128.
- ^ Informace o produktu: TriCor (TM), fenofibrát. Abbott Laboratories, North Chicago, IL, 1998.
- ^ Informace o produktu: Sandimmune (R) perorální kapsle, perorální roztok, intravenózní injekce, cyklosporinové perorální kapsle, perorální roztok, intravenózní injekce. Novartis Pharmaceuticals Corporation, East Hanover, NJ, 2010.
- ^ Informace o produktu: TRICOR® tablety pro perorální podání, tablety fenofibrát pro perorální podání. Abbott Laboratories, North Chicago, IL, 2007.
- ^ A b Staels B, Dallongeville J, Auwerx J, Schoonjans K, Leitersdorf E, Fruchart JC (1998). "Mechanismus působení fibrátů na metabolismus lipidů a lipoproteinů". Oběh. 98 (19): 2088–93. CiteSeerX 10.1.1.1004.321. doi:10.1161 / 01.cir.98.19.2088. PMID 9808609.
- ^ Ling H, Luoma JT, Hilleman D (2013). „Přehled aktuálně dostupných formulací fenofibrátu a kyseliny fenofibrové“. Kardiologický výzkum. 4 (2): 47–55. doi:10,4021 / cr270w. PMC 5358213. PMID 28352420.
- ^ Alagona P (2010). „Kyselina fenofibrová: nový fibrát schválený pro použití v kombinaci se statinem k léčbě smíšené dyslipidémie“. Cévní zdraví a řízení rizik. 6: 351–62. doi:10,2147 / vhrm.s6714. PMC 2879297. PMID 20531954.
- ^ A b Žádost společnosti Abbott o zamítnutí protimonopolního zákona ohledně společnosti Tricor byla zamítnuta. FDANews, Denní bulletin o drogách, (1. června 2006) [1]
- ^ Web produktů TEVA Pharmartsau6i8mkst7oceutical Lofibra
- ^ Lalloyer F, Staels B (2010). „Fibráty, glitazony a receptory aktivované proliferátorem peroxisomu“. Arterioskler. Tromb. Vasc. Biol. 30 (5): 894–9. doi:10.1161 / ATVBAHA.108.179689. PMC 2997800. PMID 20393155.
- ^ „Hebrejský vědec z U.: Droga mohla vymýtit COVID-19 z plic za několik dní“. The Jerusalem Post. Citováno 2020-07-14.
externí odkazy
- "Fenofibrát". Informační portál o drogách. Americká národní lékařská knihovna.
