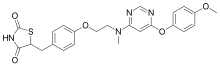
Lobeglitazon - Lobeglitazone
 | |
| Klinické údaje | |
|---|---|
| Obchodní názvy | Duvie |
| Ostatní jména | CKD-501 |
| Trasy z správa | Ústní |
| ATC kód |
|
| Právní status | |
| Právní status |
|
| Farmakokinetické data | |
| Vazba na bílkoviny | >99%[1] |
| Metabolismus | játra (CYP2C9, 2C19 a 1A2)[1] |
| Odstranění poločas rozpadu | 7,8–9,8 hodin[2] |
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| Řídicí panel CompTox (EPA) | |
| Chemické a fyzikální údaje | |
| Vzorec | C24H24N4Ó5S |
| Molární hmotnost | 480.54 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
Lobeglitazon (jméno výrobku Duvie, Chong Kun Dang ) je antidiabetikum v thiazolidindion třída drog. Jako agonista pro oba PPARα a PPARy, funguje jako inzulín senzibilizátor vazbou na PPAR receptory v tukových buňkách a zvyšují tak reakci buněk na inzulín.[3]
Lékařské použití
Lobeglitazon se používá k regulaci hladiny glukózy v krvi u pacientů s diabetes mellitus 2. typu. Může být použit samostatně nebo v kombinaci s metforminem.[4]
Lobeglitazon byl schválen ministerstvem pro bezpečnost potravin a léčiv (Korea) v roce 2013 a postmarketingový dohled probíhá do roku 2019.[4][5][potřebuje aktualizaci ]
Farmakokinetika
Absolutní biologická dostupnost lobeglitazonu je u potkanů asi 95%.[1] U člověka je střední clearance v ustáleném stavu (CLss/ F) byla 1,13 l / h napříč v rozmezí dávek 1 až 4 mg. V rozmezí dávek byl průměrný poločas 10,3 h.[2] Vylučování močí bylo zanedbatelné množství při eliminaci lobeglitazonu u potkanů a lidí.[1][2]
Vazba léčiva na plazmatické bílkoviny je více než 99%.[1][6] Průměrný poměr koncentrace v krvi a plazmě byl 0,636. Nenavázaná frakce lobeglitazonu v mikrozomálním inkubačním médiu byla 0,479.[6]
Lobeglitazon byl primárně distribuován do jater s poměrem koncentrace tkáně k plazmě 5,59 a méně do srdce, plic a tuku. Poměry koncentrace tkáně k plazmě se pohybovaly od přibližně 0,25 do 4,0 pro hlavní tkáně u potkanů.[1]
Mezi šesti hlavními transportéry membrán doporučenými Úřadem pro kontrolu potravin a léčiv Spojených států lobeglitazon interaguje s OATP1B1, OAT3 a MDR1.[1] In vitro byl lobeglitazon substrátem hlodavce OATP1B2.[6] Lobeglitazon interagoval s CYP1A2, 2C9 a 2C19.[1]
Distribuce lobeglitazonu do jater byla u potkanů inhibována atorvastatinem.[6]
Reference
- ^ A b C d E F G h Lee JH, Noh CK, Yim CS, Jeong YS, Ahn SH, Lee W, Kim DD, Chung SJ (2015). „Kinetika absorpce, distribuce, metabolismu a vylučování lobeglitazonu, nového aktivátoru gama aktivovaného peroxidovým proliferátorem u potkanů“. Journal of Pharmaceutical Sciences. 104 (9): 3049–3059. doi:10,1002 / jps.24378. PMID 25648999.
- ^ A b C Kim JW, Kim JR, Yi S, Shin KH, Shin HS, Yoon SH, Cho JY, Kim DH, Shin SG, Jang IJ, Yu KS (2011). „Tolerance a farmakokinetika lobeglitazonu (CKD-501), agonisty receptoru γ aktivovaného proliferátorem peroxisomu: jednorázová a vícenásobná, dvojitě zaslepená, randomizovaná kontrolní studie u zdravých mužských korejských subjektů.“ Klinická terapie. 33 (11): 1819–1830. doi:10.1016 / j.clinthera.2011.09.023. PMID 22047812.
- ^ Lee JH, Woo YA, Hwang IC, Kim CY, Kim DD, Shim CK, Chung SJ (2009). „Kvantifikace CKD-501, lobeglitazonu, v plazmě potkanů metodou kapalinové chromatografie / tandemové hmotnostní spektrometrie a její aplikace na farmakokinetické studie“. Journal of Pharmaceutical and Biomedical Analysis. 50 (5): 872–877. doi:10.1016 / j.jpba.2009.06.003. PMID 19577404.
- ^ A b „Informace o povolení MFDS pro Duvie Tablet 0,5mg“. Ministerstvo pro bezpečnost potravin a léčiv. Archivovány od originál (Zveřejnění informací) dne 3. března 2016. Citováno 23. října 2014.
- ^ „국내 개발 20 번째 신약 '듀비 에 정' 허가 (20. nový lék vyvinutý v Koreji„ Duvie Tablet “byl schválen)“. Tisková zpráva Chong Kun Dang. 4. července 2013. Archivovány od originál dne 23. září 2015. Citováno 23. října 2014.
- ^ A b C d Yim CS, Jeong YS, Lee SY, Pyeon W, Ryu HM, Lee JH, Lee KR, Maeng HJ, Chung SJ (2017). „Specifická inhibice distribuce loobeglitazonu do jater atorvastatinem u potkanů: důkazy interakce zprostředkované rOATP1B2 v transportu jater“. Metabolismus a dispozice léků. 45 (3): 246–259. doi:10.1124 / dmd.116.074120. PMID 28069721.
