Muraglitazar - Muraglitazar - Wikipedia
 | |
| Klinické údaje | |
|---|---|
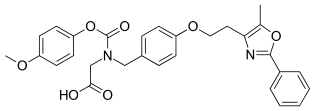
| Ostatní jména | 2 - [(4-methoxyfenoxy) karbonyl - [[4- [2- (5-methyl-2-fenyl-1,3-oxazol-4-yl) ethoxy] fenyl] methyl] amino] octová kyselina |
| ATC kód |
|
| Právní status | |
| Právní status |
|
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| Řídicí panel CompTox (EPA) | |
| Chemické a fyzikální údaje | |
| Vzorec | C29H28N2Ó7 |
| Molární hmotnost | 516.550 g · mol−1 |
| 3D model (JSmol ) | |
| |
| |
| | |
Muraglitazar (navrhované obchodní jméno Pargluva) je dvojí agonista receptoru aktivovaného proliferátorem peroxisomu s afinitou k PPARα a PPARy.[1]
Droga byla dokončena klinické studie fáze III,[2] nicméně v květnu 2006 Bristol-Myers Squibb oznámila, že ukončila další vývoj.[3]
Údaje o muraglitazaru jsou vzhledem k nedávnému zavedení tohoto přípravku poměrně řídké. Jedna dvojitě zaslepená randomizovaná klinická studie[2] porovnání muraglitazaru a pioglitazon zjistil, že účinky prvního z nich byly příznivé, pokud jde o HDL-C zvýšení, snížení celkem cholesterol, apolipoprotein B, triglyceridy a větší snížení HbA1c (str <0,0001 pro všechna srovnání). Skupina muraglitazarů však měla vyšší úmrtnost ze všech příčin, vyšší výskyt otok a srdeční selhání a větší přírůstek hmotnosti ve srovnání se skupinou s pioglitazonem. A metaanalýza klinických studií fáze II a III s muraglitazarem odhalilo, že to bylo spojeno s vyšším výskytem infarkt myokardu, mrtvice, přechodné ischemické ataky a městnavé srdeční selhání (CHF) ve srovnání s placebem nebo pioglitazonem.[4]
Tím, že upozornil na nepříznivé události zveřejněné prostřednictvím procesu poradního výboru FDA, Dr. Nissen narazil na mechanismus řízení FDA zvenčí. Tento mechanismus se uskutečnil s rosiglitazonem (Avandia) a vedl k tomu, že FDA vyžadovala prokázání srdeční bezpečnosti pro nové léky k léčbě diabetu 2. typu. Tento proces popisuje Dr. Robert Misbin v INSULIN-History od FDA Insider, publikovaného 1. června 2020 na Amazonu.
Reference
- ^ Waites CR, Dominick MA, Sanderson TP, Schilling BE (listopad 2007). „Neklinické hodnocení bezpečnosti muraglitazaru, nového agonisty PPARalfa / gama“ (PDF). Toxikologické vědy. 100 (1): 248–58. doi:10.1093 / toxsci / kfm193. PMID 17675651.
- ^ A b Kendall DM, Rubin CJ, Mohideen P, Ledeine JM, Belder R, Gross J a kol. (Květen 2006). „Zlepšení kontroly glykemie, triglyceridů a hladin HDL cholesterolu pomocí muraglitazaru, aktivátoru receptoru aktivovaného duálním (alfa / gama) proliferátorem peroxisomu, u pacientů s diabetem typu 2 nedostatečně kontrolovaných monoterapií metforminem: dvojitě zaslepený, randomizovaný srovnávací studie " (PDF). Péče o cukrovku. 29 (5): 1016–23. doi:10.2337 / diacare.2951016. PMID 16644631.
- ^ „Bristol-Myers Squibb oznamuje ukončení výroby přípravku Muraglitazar, vyšetřovací orální léčby diabetu 2. typu“. PR Newswire od společnosti Bristol-Myers Squibb. 18. května 2006. Citováno 9. listopadu 2016.
- ^ Nissen SE, Wolski K, Topol EJ (listopad 2005). „Účinek muraglitazaru na smrt a závažné nežádoucí kardiovaskulární příhody u pacientů s diabetes mellitus 2. typu“. JAMA. 294 (20): 2581–6. doi:10.1001 / jama.294.20.joc50147. PMID 16239637.
| Tento lék článek týkající se gastrointestinální systém je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
