Toxická epidermální nekrolýza - Toxic epidermal necrolysis - Wikipedia
| Toxická epidermální nekrolýza | |
|---|---|
| Ostatní jména | Lyellův syndrom, Lyellův syndrom[1] |
 | |
| Charakteristická ztráta kůže toxickou epidermální nekrolýzou | |
| Specialita | Dermatologie |
| Příznaky | Horečka, kožní puchýře, olupování kůže, bolestivá kůže, červené oči[2] |
| Komplikace | Dehydratace, sepse, zápal plic, selhání více orgánů.[2] |
| Obvyklý nástup | Věk> 40[3] |
| Rizikové faktory | HIV / AIDS, systémový lupus erythematodes, genetika[2] |
| Diagnostická metoda | > 30% postižené kůže, kožní biopsie[3] |
| Diferenciální diagnostika | Plané neštovice, stafylokoková epidermolýza, syndrom stafylokokové opařené kůže, autoimunitní bulózní onemocnění[3] |
| Léčba | Hospitalizace, zastavení příčiny, léky proti bolesti[3] |
| Prognóza | Úmrtnost 20–50%[2][3] |
| Frekvence | 1–2 na milion ročně (společně se SJS)[2] |
Toxická epidermální nekrolýza (DESET) je druh závažné kožní reakce.[2] Dohromady s Stevens-Johnsonův syndrom (SJS) tvoří spektrum nemocí, přičemž TEN je závažnější.[2] Mezi časné příznaky patří horečka a příznaky podobné chřipce.[2] O několik dní později pokožka začne puchýřit a olupovat se a vytvářet bolestivé syrové oblasti.[2] Sliznice, jako jsou ústa, jsou také obvykle zapojeny.[2] Mezi komplikace patří dehydratace, sepse, zápal plic, a selhání více orgánů.[2]
Nejběžnější příčinou jsou určité léky, jako je lamotrigin, karbamazepin, alopurinol, sulfonamidová antibiotika, a nevirapin.[2] Mezi další příčiny patří infekce jako Mycoplasma pneumoniae a cytomegalovirus nebo příčina může zůstat neznámá.[3][4] Mezi rizikové faktory patří HIV / AIDS a systémový lupus erythematodes.[2] Diagnóza je založena na a kožní biopsie a postižení více než 30% kůže.[3] TEN je typ závažné kožní nežádoucí účinky (SCARs) společně s SJS, SJS / TEN a léková reakce s eozinofilií a systémovými příznaky.[5] Říká se tomu SJS, když je postiženo méně než 10% kůže a střední forma s 10 až 30% postižením.[3] Erythema multiforme (EM) se obecně považuje za samostatnou podmínku.[6]
Léčba obvykle probíhá v nemocnice jako v a vypalovací jednotka nebo jednotka intenzivní péče.[3][7] Snahy zahrnují zastavení příčiny, léky proti bolesti, a antihistaminika.[3][4] Antibiotika, intravenózní imunoglobuliny, a kortikosteroidy lze také použít.[3][4] Léčba obvykle nemění průběh základního onemocnění.[3] Spolu se SJS postihuje 1 až 2 osoby na milion ročně.[2] Je častější u žen než u mužů.[3] Typický nástup je ve věku nad 40 let.[3] Kůže obvykle dorůstá během dvou až tří týdnů; zotavení však může trvat měsíce a většina z nich má chronické problémy.[3][4]
Příznaky a symptomy
Prodrome
TEN nakonec vede k rozsáhlému postižení kůže s zarudnutí, nekróza a oddělení horní (epidermální) vrstvy kůže a sliznice. Než se tyto závažné nálezy vyvinou, mají lidé často chřipku prodrom s kašlem, rýmou, horečkou, snížená chuť k jídlu a nevolnost. Historie expozice léčivu existuje v průměru 14 dní (v rozmezí 1–4 týdnů) před nástupem příznaků, ale může dojít až k 48 hodinám, pokud se jedná o reexpozici.[8]
Nálezy na kůži
Počáteční nálezy na kůži zahrnují červenofialové, tmavé, ploché skvrny známé jako makuly které začínají na kufru a odtud se rozprostírají. Tyto kožní léze se pak transformují na velké puchýře. Postižená kůže pak může být nekrotická nebo se prohýbat z těla a odlupovat se ve velkých řádcích.[7]
Toxická epidermální nekrolýza na nohou

Vznikající puchýře ve 4. den instance TEN

Zadní část pacienta s TEN v den 10, na vrcholu stavu
Slizniční nálezy
Téměř všichni lidé s TEN mají také orální, oční a genitální postižení. Na kterémkoli se mohou objevit bolestivé krusty a eroze slizniční povrch.[9] Ústa jsou puchýřková a erodovaná, což ztěžuje stravování a někdy vyžaduje krmení nasogastrická trubice nosem nebo a žaludeční sonda přímo do žaludku. Oči mohou otokovat, krustit a ulcerovat, což může vést k oslepnutí. Nejběžnější problém s očima je vážný zánět spojivek.[10]
Komplikace
Ti, kteří přežijí akutní fázi TEN, často trpí dlouhodobými komplikacemi ovlivňujícími kůži a oči. Kožní projevy mohou zahrnovat jizvení, erupce melanocytární névy, vulvovaginální stenóza, a dyspareunie. Epitel průdušnice, průdušek nebo gastrointestinálního traktu může být zapojen do SJS a TEN.[11] Oční příznaky jsou nejčastější komplikací u TEN, kterou zažívá 20–79% pacientů s TEN, a to iu těch, u kterých se okamžitě nevyskytují oční projevy. Ty mohou zahrnovat suché oči, fotofobie, symblepharon, zjizvení rohovky nebo xeróza subkonjunktivální fibróza, trichiasis, snížená zraková ostrost a slepota.[12]
Způsobit
Bylo hlášeno, že lékové reakce způsobují 80–95% případů TEN.[6]
Drogy nejčastěji zapojené do TEN jsou:
- antibiotika
- nesteroidní protizánětlivé léky
- alopurinol
- antimetabolity (methotrexát )
- antiretrovirové léky (nevirapin)
- kortikosteroidy
- anxiolytika (chlormezanon )
- antikonvulziva (fenobarbital, fenytoin, karbamazepin, lamotrigin, a kyselina valproová ).[13][11]
Bylo také hlášeno, že TEN je důsledkem infekce Mycoplasma pneumoniae nebo virus dengue. Kontrastní látky používané při zobrazovacích studiích a také transplantace z kostní dřeň nebo orgány byly také spojeny s vývojem TEN.[13][6]
HIV
HIV pozitivní jedinci mají 1000násobné riziko rozvoje SJS / TEN ve srovnání s běžnou populací. Důvod tohoto zvýšeného rizika není jasný.[7]
Genetika
Některé genetické faktory jsou spojeny se zvýšeným rizikem TEN. Například jisté Typy HLA jako HLA-B * 1502,[14] HLA-A * 3101,[15]HLA-B * 5801,[16] a HLA ‐ B * 57: 01[17] Bylo prokázáno, že jsou spojeny s vývojem TEN, když jsou vystaveny konkrétním lékům.
Patogeneze
Úloha imunitního systému v přesné patogenezi TEN zůstává nejasná. Ukazuje se, že určitý typ imunitní buňky (cytotoxické CD8 + T buňky ) je primárně zodpovědný za smrt keratinocytů a následné oddělení kůže. Keratinocyty jsou buňky nalezené níže v epidermis a specializují se na udržování pohromadě okolních buněk kůže. Předpokládá se, že imunitní buňky CD8 + se stanou hyperaktivní stimulací z drog nebo metabolitů léků. CD8 + T buňky pak zprostředkovávají smrt keratinocytových buněk uvolňováním řady molekul, včetně perforinu, granzymu B a granulysinu. V patogenezi TEN se také podílejí další látky, včetně faktoru alfa nekrózy nádorů a ligandu fas.[6]
Diagnóza
Diagnóza TEN je založena na klinických i histologických nálezech. Časná TEN může připomínat nespecifické reakce na léky, proto by lékaři měli udržovat vysoký index podezření na TEN. Přítomnost orální, oční a / nebo genitální mukozitidy je diagnosticky užitečná, protože tyto nálezy jsou přítomny téměř u všech pacientů s TEN. The Nikolského znamení (oddělení papilární dermis od bazální vrstvy při mírném bočním tlaku) a Asboe-Hansen znamení (laterální rozšíření bullaů tlakem) jsou také užitečné diagnostické příznaky zjištěné u pacientů s TEN.[7]
Vzhledem k významné morbiditě a mortalitě na TEN, stejně jako ke zlepšení výsledků rychlé léčby, existuje významný zájem o objev biomarkerů v séru pro včasnou diagnostiku TEN. Sérový granulysin a sérový protein s vysokou mobilitou v séru B1 (HMGB1) patří mezi několik zkoumaných markerů, které se v raných výzkumech ukázaly jako slibné.[7]
Histologie
Definitivní diagnóza TEN často vyžaduje potvrzení biopsie. Histologicky časná TEN vykazuje rozptýlené nekrotické keratinocyty. U pokročilejších TEN je vizualizována epidermální nekróza plné tloušťky s subepidermálním rozdělením a nedostatečným zánětlivým infiltrátem v papilární dermis. Epidermální nekróza nalezená v histologii je pro TEN citlivým, ale nespecifickým nálezem.[7]

Konfluentní epidermální nekróza, nízká mag
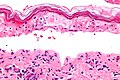
Konfliktní epidermální nekróza, vysoká mag
Diferenciální diagnostika
- Syndrom stafylokokové opařené kůže
- Droga vyvolaná lineární imunoglobulin A dermatóza
- Akutní reakce štěpu proti hostiteli
- Akutní generalizovaná exantematózní pustulóza
- Erytrodermie
- Drogová reakce s eozinofilií a systémovými příznaky aka DRESS
- Zobecněná morbilliformní erupce[18]
Léčba
Primární léčbou TEN je vysazení příčinného faktoru (faktorů), obvykle problematického léku, včasné doporučení a léčba u vypalovací jednotky nebo jednotky intenzivní péče, podpůrný management a nutriční podpora.[7]
Současná literatura přesvědčivě nepodporuje použití žádné adjuvantní systémové terapie. Počáteční zájem o Intravenózní imunoglobulin (IVIG) pochází z výzkumu, který ukazuje, že IVIG může in vitro inhibovat apoptózu keratinocytů zprostředkovanou Fas-FasL.[19] Výzkumné studie bohužel odhalují protichůdnou podporu pro použití IVIG při léčbě TEN.[20] Schopnost vyvodit obecnější závěry z dosavadního výzkumu byla omezena nedostatkem kontrolovaných studií a nekonzistencí v designu studie, pokud jde o závažnost onemocnění, dávku IVIG a načasování podávání IVIG.[7]K posouzení skutečného přínosu IVIG v TEN jsou zapotřebí větší a vysoce kvalitní zkoušky.
V TEN byla vyzkoušena řada dalších adjuvantní léčby, včetně kortikosteroidy, cyklosporin, cyklofosfamid, plazmaferéza, pentoxifyllin, acetylcystein, ulinastatin, infliximab, a faktory stimulující kolonie granulocytů (pokud je TEN přidružen-leukopenie existuje). Existují smíšené důkazy o použití kortikosteroidů a nedostatečné důkazy pro ostatní terapie.[7] Metaanalýza z roku 2002 dospěla k závěru, že neexistují spolehlivé důkazy o léčbě TEN.[21] Thalidomid neprokázaly žádný přínos a byly spojeny se zvýšenou úmrtností ve srovnání s placebem.[21]
Prognóza
Úmrtnost na toxickou epidermální nekrolýzu je 25–30%.[7] Lidé s SJS nebo TEN způsobenými léčbou mají lepší prognózu, čím dříve je kauzální léčba vysazena.[11] Ztráta kůže zanechává pacienty náchylnými k infekcím houby a bakterie a může mít za následek sepse, hlavní příčina úmrtí na tuto nemoc.[13] Smrt je způsobena buď infekce nebo dýchací obtíže což je buď kvůli zápal plic nebo poškození obložení dýchacích cest. Při stanovení prognózy jednotlivých případů může hrát roli mikroskopická analýza tkáně (zejména stupeň dermálního mononukleárního zánětu a obecně stupeň zánětu).[22]
Skóre závažnosti
„Skóre závažnosti nemoci u toxické epidermální nekrolýzy“ (SCORTEN) je skórovací systém vyvinutý k hodnocení závažnosti TEN a předpovědi úmrtnosti u pacientů s akutní TEN.[23]
Za každý z následujících faktorů je uveden jeden bod:[12]
- věk> 40 let
- srdeční frekvence> 120 tepů za minutu
- nesoucí diagnózu rakoviny
- separace pokožky na více než deseti procentech povrch těla (BSA) 1. den.
- Dusík v močovině v krvi> 28 mg / dL
- Glukóza> 252 mg / dl (14 mmol / l)
- Bikarbonát <20 mEq / l
Skóre
- 0–1: 3,2% úmrtnost
- 2: 12,2% úmrtnost
- 3: 35,3% úmrtnost
- 4: 58,3% úmrtnost
- ≥ 5: 90% úmrtnost
Tento bodovací systém je nejcennější, když se používá první a třetí den hospitalizace, a může podceňovat úmrtnost pacientů s respiračními příznaky.[12]
Reference
- ^ Rapini, Ronald P .; Bolognia, Jean L .; Jorizzo, Joseph L. (2007). Dermatologie: dvoudílná sada. St. Louis: Mosby. ISBN 978-1-4160-2999-1.
- ^ A b C d E F G h i j k l m n „Stevens-Johnsonův syndrom / toxická epidermální nekrolýza“. Genetická domácí reference. Červenec 2015. Archivováno z původního dne 27. dubna 2017. Citováno 26. dubna 2017.
- ^ A b C d E F G h i j k l m n Ó „Orphanet: Toxická epidermální nekrolýza“. Orphanet. Listopadu 2008. Archivováno z původního dne 27. dubna 2017. Citováno 26. dubna 2017.
- ^ A b C d "Stevens-Johnsonův syndrom". ZAHRADA. Archivováno z původního dne 28. srpna 2016. Citováno 26. srpna 2016.
- ^ Adler NR, Aung AK, Ergen EN, Trubiano J, Goh MS, Phillips EJ (2017). „Nedávný pokrok v chápání závažných kožních nežádoucích účinků“. British Journal of Dermatology. 177 (5): 1234–1247. doi:10.1111 / bjd.15423. PMC 5582023. PMID 28256714.
- ^ A b C d Schwartz, RA; McDonough, PH; Lee, BW (srpen 2013). „Toxická epidermální nekrolýza: Část I. Úvod, historie, klasifikace, klinické příznaky, systémové projevy, etiologie a imunopatogeneze“. Journal of the American Academy of Dermatology. 69 (2): 173.e1–13, kvíz 185–6. doi:10.1016 / j.jaad.2013.05.003. PMID 23866878.
- ^ A b C d E F G h i j Schwartz, RA; McDonough, PH; Lee, BW (srpen 2013). „Toxická epidermální nekrolýza: část II. Prognóza, následky, diagnostika, diferenciální diagnostika, prevence a léčba“. Journal of the American Academy of Dermatology. 69 (2): 187.e1–16, kvíz 203–4. doi:10.1016 / j.jaad.2013.05.002. PMID 23866879.
- ^ Jordan, MH; Lewis, MS; Jeng, JG; Rees, JM (1991). „Léčba toxické epidermální nekrolýzy spalovacími jednotkami: jiný trh nebo jiná hrozba?“. The Journal of Burn Care & Rehabilitation. 12 (6): 579–81. doi:10.1097/00004630-199111000-00015. PMID 1779014.
- ^ Roujeau, JC; Stern, RS (10. listopadu 1994). „Závažné nežádoucí kožní reakce na léky“. The New England Journal of Medicine. 331 (19): 1272–85. doi:10.1056 / nejm199411103311906. PMID 7794310.
- ^ Morales, ME; Purdue, GF; Verity, SM; Arnoldo, BD; Blomquist, PH (říjen 2010). „Oční projevy Stevens-Johnsonova syndromu a toxické epidermální nekrolýzy a vztah k SCORTENU“. American Journal of Ophthalmology. 150 (4): 505–510.e1. doi:10.1016 / j.ajo.2010.04.026. PMID 20619392.
- ^ A b C Maverakis, Emanual; Wang, Elizabeth A .; Shinkai, Kanade; Mahasirimongkol, Surakameth; Margolis, David J .; Avigan, Mark; Chung, Wen-Hung; Goldman, Jennifer; Granát, Lois La (01.06.2017). „Stevens-Johnsonův syndrom a pokyny pro standardní podávání zpráv a hodnocení toxické epidermální nekrolýzy: Výsledky pracovní skupiny National Institutes of Health“ (PDF). JAMA Dermatologie. 153 (6): 587–592. doi:10.1001 / jamadermatol.2017.0160. ISSN 2168-6068. PMID 28296986.
- ^ A b C DeMers, G; Meurer, WJ; Shih, R; Rosenbaum, S; Vilke, GM (prosinec 2012). "Tkáňový aktivátor plazminogenu a mrtvice: přehled literatury pro klinického lékaře". The Journal of Emergency Medicine. 43 (6): 1149–54. doi:10.1016 / j.jemermed.2012.05.005. PMID 22818644.
- ^ A b C Garra, GP (2007). "Toxická epidermální nekrolýza Archivováno 2007-12-27 na Wayback Machine ". Emedicine.com. Citováno dne 13. prosince 2007.
- ^ Hung, SI; Chung, WH; Jee, SH; Chen, WC; Chang, YT; Lee, WR; Hu, SL; Wu, MT; Chen, GS; Wong, TW; Hsiao, PF; Chen, WH; Shih, HY; Fang, WH; Wei, CY; Lou, YH; Huang, YL; Lin, JJ; Chen, YT (duben 2006). „Genetická citlivost na kožní nežádoucí reakce vyvolané karbamazepinem“. Farmakogenetika a genomika. 16 (4): 297–306. doi:10.1097 / 01.fpc.0000199500.46842.4a. PMID 16538176.
- ^ McCormack, M; Alfirevic, A; Měšťan, S; Farrell, JJ; Kasperavičiūtė, D; Carrington, M; Parapety, GJ; Marson, T; Jia, X; de Bakker, PI; Chinthapalli, K; Molokhia, M; Johnson, MR; O'Connor, GD; Chaila, E; Alhusaini, S; Shianna, KV; Radtke, RA; Heinzen, EL; Walley, N; Pandolfo, M; Pichler, W; Park, BK; Depondt, C; Sisodiya, SM; Goldstein, DB; Deloukas, P; Delanty, N; Cavalleri, GL; Pirmohamed, M (24. března 2011). „HLA-A * 3101 a hypersenzitivní reakce vyvolané karbamazepinem u Evropanů“. The New England Journal of Medicine. 364 (12): 1134–43. doi:10.1056 / nejmoa1013297. PMC 3113609. PMID 21428769.
- ^ Tohkin, M; Kaniwa, N; Saito, Y; Sugiyama, E; Kurose, K; Nishikawa, J; Hasegawa, R; Aihara, M; Matsunaga, K; Abe, M; Furuya, H; Takahashi, Y; Ikeda, H; Muramatsu, M; Ueta, M; Sotozono, C; Kinoshita, S; Ikezawa, Z; Japan Pharmacogenomics Data Science, Consortium (únor 2013). „Celogenomová asociační studie hlavních determinantů Stevens-Johnsonova syndromu souvisejícího s alopurinolem a toxické epidermální nekrolýzy u japonských pacientů“. The Pharmacogenomics Journal. 13 (1): 60–9. doi:10.1038 / tpj.2011.41. PMID 21912425.
- ^ Alfirevic, Ana; Pirmohamed, Munir; Marinovic, Branka; Harcourt-Smith, Linda; Jorgensen, Andrea L; Cooper, Tess E (17. července 2019). „Genetické testování pro prevenci závažné kožní vyrážky vyvolané drogami“. Cochrane Database of Systematic Reviews. 7: CD010891. doi:10.1002 / 14651858.CD010891.pub2. PMC 6636675. PMID 31314143.
- ^ Schwartz, RA; McDonough, PH; Lee, BW (srpen 2013). „Toxická epidermální nekrolýza: část II. Prognóza, následky, diagnostika, diferenciální diagnostika, prevence a léčba“. Journal of the American Academy of Dermatology. 69 (2): 187.e1–16, kvíz 203–4. doi:10.1016 / j.jaad.2013.05.002. PMID 23866879.
- ^ Zajicek, R; Pintar, D; Broz, L; Suca, H; Königova, R (květen 2012). „Toxická epidermální nekrolýza a Stevens-Johnsonův syndrom v pražském vypalovacím centru 1998-2008“. Časopis Evropské akademie dermatologie a venerologie: JEADV. 26 (5): 639–43. doi:10.1111 / j.1468-3083.2011.04143.x. PMID 21668825.
- ^ Rajaratnam R, Mann C, Balasubramaniam P, et al. (Prosinec 2010). „Toxická epidermální nekrolýza: retrospektivní analýza 21 po sobě jdoucích případů léčených v terciárním centru“. Clin. Exp. Dermatol. 35 (8): 853–62. doi:10.1111 / j.1365-2230.2010.03826.x. PMID 20456393.
- ^ A b Majumdar, Samit; Mockenhaupt, Maja; Roujeau, Jean-Claude; Townshend, Askari P (2002-10-21). „Intervence pro toxickou epidermální nekrolýzu“. Cochrane Database of Systematic Reviews (4): CD001435. doi:10.1002 / 14651858.CD001435. ISSN 1465-1858. PMID 12519556.
- ^ Quinn AM; Brown, K; Bonish, BK; Curry, J; Gordon, KB; Sinacore, J; Gamelli, R; Nickoloff, BJ; et al. (2005). „Odhalení histologických kritérií s prognostickým významem při toxické epidermální nekrolýze“. Arch Dermatol. 141 (6): 683–7. doi:10.1001 / archderm.141.6.683. PMID 15967913.
- ^ Schwartz, RA; McDonough, PH; Lee, BW (srpen 2013). „Toxická epidermální nekrolýza: část II. Prognóza, následky, diagnostika, diferenciální diagnostika, prevence a léčba“. Journal of the American Academy of Dermatology. 69 (2): 187.e1–16, kvíz 203–4. doi:10.1016 / j.jaad.2013.05.002. PMID 23866879.
externí odkazy
| Klasifikace | |
|---|---|
| Externí zdroje |





