Kostní morfogenetický protein 4 - Bone morphogenetic protein 4
Kostní morfogenetický protein 4 je protein že u lidí je kódováno BMP4 gen.[4][5] BMP4 se nachází na chromozomu 14q22-q23
BMP4 je členem kostní morfogenetický protein rodina, která je součástí transformující růstový faktor-beta nadčeleď. The nadčeleď zahrnuje velké rodiny růstových a diferenciačních faktorů. BMP4 je evolučně vysoce konzervativní. BMP4 se nachází v časném embryonálním vývoji ve ventrální okrajové zóně a v oku, srdeční krvi a ušní vačku.[6]
Objev
Kostní morfogenetické proteiny byly původně identifikovány podle schopnosti demineralizovat kost extrakt vyvolat endochondrální osteogeneze in vivo v extraskeletálním místě.
Funkce
BMP4 je a polypeptid patřící k TGF-p nadrodina proteinů. Stejně jako ostatní kostní morfogenetické proteiny, se podílí na vývoji kostí a chrupavek, konkrétně na vývoji zubů a končetin a opravě zlomenin. Tento konkrétní člen rodiny hraje důležitou roli při nástupu tvorby endochondrální kosti u lidí. Ukázalo se, že se podílí na vývoji svalů, kostí mineralizace, a ureterální pupen rozvoj.[Citace je zapotřebí ]
V člověku embryonální vývoj, BMP4 je kritická signální molekula potřebná pro rané období diferenciace embrya a stanovení osy hřbetní a břišní. BMP4 je vylučován z hřbetní části notochord, a jedná ve shodě s zvukový ježek (uvolněno z ventrální části notochordu) k vytvoření hřbetní-ventrální osy pro diferenciaci pozdějších struktur.[Citace je zapotřebí ]
BMP4 stimuluje diferenciaci nadložní ektodermální tkáně.[Citace je zapotřebí ]
Je známo, že kostní morfogenetické proteiny stimulují tvorbu kostí u dospělých zvířat. To je považováno za vyvolávající osteoblastický oddanost a diferenciace kmenových buněk, jako je mezenchymální kmenové buňky.[Citace je zapotřebí ]Je známo, že BMP hrají velkou roli v embryonálním vývoji. V embryu BMP4 pomáhá vytvořit formaci osy hřbetní a ventrální xenopus indukcí ventrální mezodermy. U myší dochází k narušení inaktivace BMP4 mezoderm od tváření.[Citace je zapotřebí ] Rovněž stanoví dorzálně-ventrální vzorování vyvíjející se neurální trubice pomocí BMP7 a vyvolávání hřbetních znaků.[Citace je zapotřebí ]
BMP4 také omezuje rozsah, v jakém dochází k neurální diferenciaci u embryí xenopus indukcí epidermis. Mohou pomáhat při vyvolávání bočních charakteristik somitů. Somité jsou nutní pro vývoj věcí, jako jsou svaly končetin.[Citace je zapotřebí ] BMP4 pomáhá při vzorování vyvíjející se hlavy, i když indukuje apoptózu neurální lišta buňky; to se děje v zadním mozku.[7]
U dospělých je BMP4 důležitý pro neurogenezi (tj. Generování nových neuronů), ke které dochází po celý život ve dvou neurogenních výklencích mozku, zubatý gyrus z hipokampus a subventrikulární zóna (SVZ) přiléhající k postranním komorám. V těchto výklencích jsou nepřetržitě generovány nové neurony z kmenových buněk. Ve skutečnosti se ukázalo, že u zubatého gyru udržuje BMP4 nervové kmenové buňky v klidovém stavu, čímž brání vyčerpání zásoby kmenových buněk.[8] V SVZ K zahájení neurogeneze z dospělých nervových kmenových buněk a potlačení alternativního osudu oligodendrogliogeneze je nutná signalizace zprostředkovaná BMP prostřednictvím Smad4.[9] Navíc bylo prokázáno, že v SVZ má BMP4 prodifferenční účinek, protože zachraňuje defekt terminální diferenciace v neurosférách SVZ, kde gen Tis21 /BTG2 - vyžadováno pro diferenciaci terminálu - bylo odstraněno.[10] Tis21 je pozitivním regulátorem exprese BMP4 v SVZ.[10]
BMP4 je důležité pro kost a chrupavka metabolismus. Signalizace BMP4 byla nalezena při tvorbě časných mezodermů a zárodečných buněk. Regulace končetinových pupenů a vývoj plic, jater, zubů a buněk mezenchymu obličeje jsou další důležité funkce připisované signalizaci BMP4.[11] Tvorba číslic je ovlivněna BMP4 spolu s dalšími signály BMP. Interdigitální mezenchym vykazuje BMP4, který zabraňuje apoptóze regionu.[12] Tvorba zubu závisí na expresi BMP4, která indukuje Msx 1 a 2. Tyto transkripční faktory způsobují, že se tvořící zub stává a řezákem.
BMP4 také hraje důležitou roli v tukové tkáni: je to nezbytné pro bílý adipogeneze a propaguje adipocyt diferenciace.[13] Navíc je také důležité pro hnědý tuk, kde indukuje UCP1 související s netřesením termogeneze.[13]
Sekrece BMP4 pomáhá způsobit diferenciaci ureterálního pupenu do močovodu.[14]
BMP4 antagonizuje organizátorovou tkáň a je exprimován v časném vývoji v tkáni ektodermu a mezodermu. Po gastrulaci je transkripce BMP4 omezena na ventrolaterální okrajovou zónu kvůli inhibici z dorzalizující strany vyvíjejícího se embrya. BMP4 pomáhá při ventralizaci mezodermu, který vede po formaci osy dorzálně-ventrální. v Xenopus Bylo zjištěno, že BMP4 pomáhá při tvorbě krve a krevních ostrovů.[15]
BMP4, původně vyjádřený v epidermis, se nachází ve střešní desce během formování neurální trubice. Gradient signalizace BMP se nachází v protikladu k a Sonic ježek, Psst, přechod. Tato exprese BMP4 charakterizuje hřbetní neurony.[16]
BMP4, ve spojení s FGF2, podporují diferenciaci kmenových buněk na mezodermální linie. Po diferenciaci buňky ošetřené BMP4 a FGF2 obecně produkují vyšší množství osteogenní a chondorgenní diferenciace než neošetřené kmenové buňky.[17] Také ve spojení s FGF2 může produkovat progenitorové buňky štítné žlázy z pluripotentních kmenových buněk u myší a lidí.[18]
Bylo prokázáno, že BMP4 indukuje expresi genové rodiny Msx, o které se předpokládá, že je součástí tvorby chrupavky z somitický mezoderm.[19]
BMP4, a parakrinní růstový faktor, byl nalezen u potkanů vaječníky. BMP4, ve spojení s BMP7, regulovat brzy ovariální folikul vývoj a přechod folikulů od primordia k primárnímu. Kromě toho bylo prokázáno, že inhibice BMP4 protilátkami snižuje celkovou velikost vaječníků. Tyto výsledky naznačují, že BMP4 může pomoci při přežití a prevenci apoptózy v oocyty.[11]
U ptáků bylo prokázáno, že BMP4 ovlivňuje velikost zobáku Darwinovy pěnkavy. Nízké množství BMP4 koreluje s nízkou hloubkou a šířkou zobáku. Naopak vysoký výraz BMP4 vytváří vysoké hloubky a šířky zobáku. Genetická regulace BMP4 poskytuje základ pro přirozený výběr ptačích zobáků.[20]
Struktura bílkovin
Získávání aktivního karboxy-terminál peptid se 116 zbytky, je lidský bmp4 zpočátku syntetizován jako čtyřicetiprocentní zbytkový preproprotein, který je štěpen posttranslačně. BMP4 má sedm zbytků, které jsou konzervované a glykosylované.[21] Monomery jsou drženy disulfidovými můstky a 3 páry cysteinových aminokyselin. Tato konformace se nazývá „cystinový uzel“. BMP4 může tvořit homodimery nebo heterodimery s podobnými BMPS. Jedním z příkladů je BMP7. Tato schopnost tvořit homodimery nebo heterodimery dává schopnost mít větší osteoinduktivní aktivitu než jen samotný bmp4.[22] Dosud není známo mnoho o tom, jak BMPS interaguje s extracelulární matricí. O cestách, které pak degradují BMP4, se toho ví málo.
Inhibice
Inhibice signálu BMP4 (o chordin, člun ze dřeva nebo follistatin ) způsobí, že se ektoderm diferencuje na neurální deska. Pokud tyto buňky také přijímají signály z FGF, budou rozlišovat do míchy; v nepřítomnosti FGF se buňky stávají mozkovou tkání.
Zatímco nadměrná exprese BMP4 exprese může vést k ventralizaci, inhibice s dominantním negativem může mít za následek úplnou dorsalizaci embrya nebo tvorbu dvou os.[23]
Je důležité si uvědomit, že myši, u kterých byl BMP4 inaktivován, obvykle uhynuly během gastrulace. Předpokládá se, že inaktivace lidského BMP4 by pravděpodobně měla stejný účinek. Mutace, které jsou u lidí jemné, však mohou mít jemné účinky také fenotypicky.[Citace je zapotřebí ]
Izoformy
Bylo popsáno alternativní sestřih v 5 'nepřekládané oblasti tohoto genu a jsou popsány tři varianty, všechny kódující identický protein.[24]
Molekulární mechanismy
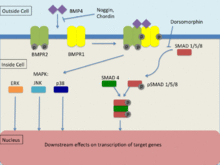
BMP4 se jako člen rodiny transformujícího růstového faktoru β (TGF-β) váže na 2 různé typy receptorů serin-threoninkinázy známé jako BMPR1 a BMPR2.[25] K přenosu signálu prostřednictvím těchto receptorů dochází prostřednictvím Smadu a mapy kináza cesty k uskutečnění transkripce jeho cílových genů. Aby došlo k přenosu signálu, musí být funkční oba receptory. BMP je schopen vázat se na BMPR2 bez BMPR1, afinita se však významně zvyšuje v přítomnosti obou receptorů. BMPR1 je transfosforylován prostřednictvím BMPR2, který indukuje downstream signalizaci v buňce a ovlivňuje transkripci.[25]
Smad signalizační cesta
Receptory rodiny TGF-p nejčastěji používají Smad signální cesta k přenosu signálů.[25] Receptory typu 2 jsou zodpovědné za aktivaci typu 1 receptory kde jejich funkce zahrnuje fosforylaci R-Smadů (Smad-1, Smad-5, Smad-8). Po fosforylaci vznikne R-SMAD komplex ve spojení se společným partnerem Smad (co-Smad) nastává tam, kde migruje do jádra. Tato signalizace cesta je regulován inhibitorem malé molekuly známým jako dorsomorphin, který zabraňuje následným účinkům R-smad.[25]
Signální dráhy mapové kinázy (MAPK)
Mitogen aktivované proteinové kinázy (MAPK) procházejí fosforylací prostřednictvím signální kaskády, kde MAPKKK fosforyluje a aktivuje MAPKK a MAPKK fosforyluje a aktivuje MAPK který pak indukuje intracelulární odpověď.[26] Aktivace MAPKKK probíhá prostřednictvím interakce hlavně GTPáz nebo jiné skupiny proteinových kináz. Receptory TGF-p indukují MAPK signální dráhy ERK, JNK a p38.[26] BMP4 je také známo, že aktivuje signalizační dráhy ERK, JNK a p38 MAPK, zatímco bylo zjištěno, že působí nezávisle na signálních drahách Smad, jsou většinou aktivní ve spojení se Smad.[27] Aktivace drah ERK a JNK působí na fosforylaci Smadu, a proto reguluje jeho aktivaci. Kromě toho mohou být cesty MAPK schopné přímo ovlivňovat transkripční faktory interagující se Smad prostřednictvím substrátu JNK nebo p38, který indukuje konvergenci dvou signálních drah. Je uvedeno, že tato konvergence spočívá hlavně v kooperativním chování, existují však důkazy, které naznačují, že se mohou občas vzájemně působit. Rovnováha, která existuje mezi přímou aktivací těchto signálních drah, má navíc významný účinek na buněčné odpovědi indukované TGF-β.[27]
Klinický význam
Zvýšení exprese BMP4 bylo spojeno s řadou kostních onemocnění, včetně dědičné poruchy Fibrodysplasia Ossificans Progressiva.[28]
Ze sekvenčních studií kandidátních genů zapojených do rozštěpení existují silné důkazy, že mutace v genu pro morfogenetický protein 4 (BMP4) v kostech mohou být spojeny s patogenezí rozštěp rtu a patra.[29]
Vývoj očí
Oči jsou nezbytné zejména pro organismy pozemní obratlovci, pozorovat kořist a překážky; to je rozhodující pro jejich přežití. Tvorba očí začíná jako optické váčky a čočka odvozená z neuroectoderm. Je známo, že kostní morfogenní proteiny stimulují tvorbu očních čoček. Během časného vývoje očí dochází k tvorbě optický váček je nezbytný u myší a BMP4 exprimovaný silně v optickém váčku a slabě v okolí mezenchymu a povrchový ektoderm. Tento koncentrační gradient BMP4 v optickém váčku je kritický pro indukci čočky. Výzkumník Dr. Furuta a Dr. Hogan zjistili, že pokud by provedli laserovou mutaci na embryích myší a způsobili BMP4 homozygotní nula mutace, toto embryo nebude vyvíjet čočku. Také dělali in situ hybridizace BMP4 gen zobrazující zelenou barvu a Sox2 gen v červené barvě, o kterém si mysleli, že se také podílí na tvorbě čočky. Poté, co provedli tyto dvě hybridizace in situ v embryích myší, zjistili, že v optice se nacházejí jak zelené, tak červené barvy váček embryí myší. To naznačovalo, že BMP4 a Sox2 jsou vyjádřeny na správném místě ve správný čas optického váčku a dokazují, že mají některé základní funkce pro indukci čočky. Dále provedli následný experiment injekcí BMP4 do BMP4 homozygotní mutantní embrya zachránila formaci čočky (12). To naznačovalo, že BMP4 je pro tvorbu čoček rozhodně nutný. Vědci však také zjistili, že některé z mutovaných myší nelze zachránit. Později zjistili, že těmto mutantům chybí Msx 2 který je aktivován BMP4. Mechanismus, který předpovídali, byl ten, že BMP4 bude aktivní Msx 2 v optickém váčku a kombinace koncentrace BMP4 a Msx2 společně aktivní Sox2 a Sox2 je nezbytná pro diferenciaci čočky.[30]
Injekce Nogginu do buněk optických vláken u myší významně snižuje proteiny BMP4 v buňkách. To naznačuje, že Noggin je dostatečný k inhibici produkce BMP4. Navíc další inhibitorový protein Bylo zjištěno, že Alk6 blokuje BMP4 v aktivaci Msx2, která zastavuje diferenciaci čoček.[31] O mechanismu inhibice BMP4 a následné regulaci Sox2 však stále existuje mnoho neznámého. V budoucnu se vědci snaží najít úplnější cestu vývoje celého oka a doufají, že jednoho dne najdou způsob, jak vyléčit některá geneticky způsobená oční onemocnění.
Ztráta vlasů
Ztráta vlasů nebo známá jako alopecie je způsobeno změnou vlasový kořínek morfologie a cyklování vlasových folikulů neobvyklým způsobem.[32] Cykly vlasových folikulů jsou cykly růstu, nebo anagen, regrese nebo katagen a odpočinek nebo telogen.[33] U savců vývoj srsti řídí vzájemné epiteliální a mezynchymální interakce. Geny jako BMP4 a BMP2 jsou aktivní v prekurzorech vlasové šachty. Konkrétně BMP4 se nachází v dermální papilla. BMP4 je součástí signalizační sítě, která řídí vývoj vlasů. Je nezbytný pro indukci biochemických drah a signalizaci pro regulaci diferenciace vlasové šachty v anagenním vlasovém folikulu. Děje se to kontrolou výrazu transkripční faktory které regulují diferenciaci vlasů. Stále však není jasné, kde BMP působí v genetické síti. Signalizace bmp4 může potenciálně řídit expresi terminálních diferenciačních molekul, jako jsou keratiny. Ukázalo se, že i další regulátory řídí vývoj vlasových folikulů. HOXC13 a FOXN1 jsou považovány za důležité regulátory, protože experimenty se ztrátou funkce ukazují zhoršenou diferenciaci vlasové šachty, která nezasahuje do tvorby vlasového folikulu.[34]
Když je BMP4 exprimován ektopicky, u transgenních myší vlasový folikul vnější kořenový obal (ORS) je inhibována proliferace buněčné matrice. BMP4 také aktivuje vlasy keratin genová exprese s poznámkou, že BMP4 je důležitý při diferenciaci vlasové šachty. Člun ze dřeva, známý inhibitor BMP4, se nachází v buňkách matrice vlasové cibulky. Dalšími důležitými faktory, které je třeba při vývoji vlasů vzít v úvahu, je vyjádření Shh (zvukový ježek ), BMP7, BMP2, WNT, a β-katenin protože jsou vyžadovány v rané fázi morfogeneze.[35]
Jiné geny, které mohou inhibovat nebo interagovat s BMP4, jsou noggin, follistatin, skřítek, což je vše vyjádřeno ve vyvíjejících se vlasových folikulech.[36] U myší, u kterých chybí noggin, je méně vlasových folikulů než u normální myši a vývoj folikul je potlačen. U kuřecích embryí se ukazuje, že ektopicky exprimovaný noggin produkuje zvětšené folikuly a signalizace BMP4 ukazuje potlačovaný osud plakidu v okolních buňkách.[22] Během experimentů in vivo bylo také prokázáno, že Noggin indukuje růst vlasů v postnatální kůži.[37]
BMP4 je důležitou součástí biologických cest, které zahrnovaly regulaci diferenciace vlasové šachty v anagenním vlasovém folikulu. Nejsilnější hladiny exprimovaného BMP4 se nacházejí v dřeň, buňky vlasové šachty, distální vlasová matice a potenciální prekurzory pokožka. Dvě hlavní metody, které BMP4 inhibují expresi vlasů, spočívají v omezení exprese růstového faktoru ve vlasové matrici a antagonismu mezi signalizací růstu a diferenciace.[35]
Cesty, které regulují tvorbu vlasových folikulů a růst vlasů, jsou klíčové při vývoji terapeutických metod pro podmínky vypadávání vlasů. Mezi takové podmínky patří vývoj nových folikulů, změna tvaru charakteristik existujících folikulů a změna růstu vlasů ve stávajících vlasových folikulech. Kromě toho může BMP4 a cesta, kterou funguje, poskytnout terapeutické cíle pro prevenci vypadávání vlasů.[33]
Reference
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000021835 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ van den Wijngaard A, Weghuis DO, Boersma CJ, van Zoelen EJ, Geurts van Kessel A, Olijve W (listopad 1995). „Jemné mapování genu morfogenetického proteinu 4 lidské kosti (BMP4) na chromozom 14q22-q23 hybridizací in situ“. Genomika. 27 (3): 559–60. doi:10.1006 / geno.1995.1096. hdl:2066/22049. PMID 7558046.
- ^ Oida S, Iimura T, Maruoka Y, Takeda K, Sasaki S (listopad 1995). "Klonování a sekvence kostního morfogenetického proteinu 4 (BMP-4) z lidské placentární cDNA knihovny". DNA sekv. 5 (5): 273–5. doi:10.3109/10425179509030980. PMID 7579580.
- ^ Knöchel S, Dillinger K, Köster M, Knöchel W (listopad 2001). "Struktura a exprese genů BMP-2 a BMP-4 pro Xenopus tropicalis". Mech. Dev. 109 (1): 79–82. doi:10.1016 / S0925-4773 (01) 00506-8. PMID 11677055. S2CID 792305.
- ^ Graham et al., 1994
- ^ Mira H, Andreu Z, Suh H, Lie DC, Jessberger S, Consiglio A, San Emeterio J, Hortigüela R, Marqués-Torrejón MA, Nakashima K, Colak D, Götz M, Fariñas I, Gage FH (2010). „Signalizace pomocí BMPR-IA reguluje klid a dlouhodobou aktivitu nervových kmenových buněk v dospělém hipokampu“. Buňková kmenová buňka. 7 (1): 78–89. doi:10.1016 / j.stem.2010.04.016. PMID 20621052.
- ^ Colak D, Mori T, Brill MS, Pfeifer A, Falk S, Deng C, Monteiro R, Mummery C, Sommer L, Götz M (2008). „Neurogeneze dospělých vyžaduje signalizaci kostního morfogenního proteinu zprostředkovaného Smad4 v kmenových buňkách“. The Journal of Neuroscience. 28 (2): 434–446. doi:10.1523 / JNEUROSCI.4374-07.2008. PMC 6670509. PMID 18184786.
- ^ A b Farioli-Vecchioli S, Ceccarelli M, Saraulli D, Micheli L, Cannas S, D'Alessandro F, Scardigli R, Leonardi L, Cinà I, Costanzi M, Mattera A, Cestari V, Tirone F (2014). „Tis21 je vyžadován pro neurogenezi dospělých v subventrikulární zóně a pro čichové chování regulující cykliny, BMP4, Hes1 / 5 a Ids“. Neurosci přední buňky. 8: 98. doi:10.3389 / fncel.2014.00098. PMC 3977348. PMID 24744701.
- ^ A b Nilsson EE, Skinner MK (říjen 2003). „Kostní morfogenetický protein-4 působí jako faktor přežití vaječníkových folikulů a podporuje vývoj prvotního folikulu.“ Biol. Reprod. 69 (4): 1265–72. doi:10.1095 / biolreprod.103.018671. PMID 12801979. S2CID 2141586.
- ^ Arteaga-Solis E, Gayraud B, Lee SY, Shum L, Sakai L, Ramirez F (červenec 2001). "Regulace vzorování končetin extracelulárními mikrofibrilami". J. Cell Biol. 154 (2): 275–81. doi:10.1083 / jcb.200105046. PMC 2150751. PMID 11470817.
- ^ A b Blázquez-Medela AM, Jumabay M, Boström KI (květen 2019). „Beyond the bone: Bone morphogenetic protein signaling in adipose tkáň“. Recenze obezity. 20 (5): 648–658. doi:10.1111 / obr.12822. PMC 6447448. PMID 30609449.
- ^ Miyazaki Y, Oshima K, Fogo A, Ichikawa I (březen 2003). „Důkaz, že kostní morfogenetický protein 4 má více biologických funkcí během vývoje ledvin a močových cest“. Kidney Int. 63 (3): 835–44. doi:10.1046 / j.1523-1755.2003.00834.x. PMID 12631064.
- ^ Hemmati-Brivanlou A, Thomsen GH (1995). „Ventrální mezodermální vzorování u embryí Xenopus: vzorce exprese a aktivity BMP-2 a BMP-4“. Dev. Genet. 17 (1): 78–89. doi:10.1002 / dvg.1020170109. PMID 7554498.
- ^ Selleck MA, García-Castro MI, Artinger KB, Bronner-Fraser M (prosinec 1998). „Účinky Shh a Noggin na tvorbu neurální lišty ukazují, že BMP je vyžadován v neurální trubici, ale ne ektoderm“. Rozvoj. 125 (24): 4919–30. PMID 9811576.
- ^ Lee TJ, Jang J, Kang S, Jin M, Shin H, Kim DW, Kim BS (leden 2013). „Posílení osteogenní a chondrogenní diferenciace lidských embryonálních kmenových buněk indukcí mezodermální linie pomocí léčby BMP-4 a FGF2“. Biochem. Biophys. Res. Commun. 430 (2): 793–7. doi:10.1016 / j.bbrc.2012.11.067. PMID 23206696.
- ^ Kurmann AA, Serra M, Hawkins F, Rankin SA, Mori M, Astapova I, Ullas S, Lin S, Bilodeau M, Rossant J, Jean JC, Ikonomou L, Deterding RR, Shannon JM, Zorn AM, Hollenberg AN, Kotton DN (Listopad 2015). "Regenerace funkce štítné žlázy transplantací diferencovaných pluripotentních kmenových buněk". Buňková kmenová buňka. 17 (5): 527–42. doi:10.1016 / j.stem.2015.09.004. PMC 4666682. PMID 26593959.
- ^ Watanabe Y, Le Douarin NM (červen 1996). "Role pro BMP-4 ve vývoji podkožní chrupavky". Mech. Dev. 57 (1): 69–78. doi:10.1016/0925-4773(96)00534-5. PMID 8817454. S2CID 16858412.
- ^ Abzhanov A, Protas M, Grant BR, Grant PR, Tabin CJ (září 2004). „Bmp4 a morfologická variace zobáků v Darwinových pěnkavách“. Věda. 305 (5689): 1462–5. Bibcode:2004Sci ... 305.1462A. doi:10.1126 / science.1098095. PMID 15353802. S2CID 17226774.
- ^ Aono A, Hazama M, Notoya K, Taketomi S, Yamasaki H, Tsukuda R, Sasaki S, Fujisawa Y (květen 1995). "Silná ektopická aktivita vyvolávající kostní morfogenetický protein-4/7 heterodimer". Biochem. Biophys. Res. Commun. 210 (3): 670–7. doi:10.1006 / bbrc.1995.1712. PMID 7763240.
- ^ A b Botchkarev VA, Botchkareva NV, Roth W, Nakamura M, Chen LH, Herzog W, Lindner G, McMahon JA, Peters C, Lauster R, McMahon AP, Paus R (červenec 1999). „Noggin je mesenchymálně odvozený stimulátor indukce vlasových folikulů“. Nat. Cell Biol. 1 (3): 158–64. doi:10.1038/11078. PMID 10559902. S2CID 8777441.
- ^ Metz A, Knöchel S, Büchler P, Köster M, Knöchel W (červen 1998). "Strukturální a funkční analýza promotoru BMP-4 v časných embryích Xenopus laevis". Mech. Dev. 74 (1–2): 29–39. doi:10.1016 / S0925-4773 (98) 00059-8. PMID 9651472. S2CID 14496024.
- ^ "Entrez Gene: BMP4 kostní morfogenetický protein 4".
- ^ A b C d Miyazono K, Kamiya Y, Morikawa M (leden 2010). „Receptory kostního morfogenetického proteinu a signální transdukce“. J. Biochem. 147 (1): 35–51. doi:10.1093 / jb / mvp148. PMID 19762341.
- ^ A b Cell Signaling Technology, Inc. „Proteinové kinázy aktivované mitogenem“. Citováno 17. listopadu 2012.
- ^ A b Derynck R, Zhang YE (říjen 2003). "Cesty závislé na Smad a nezávislé na Smad v signalizaci rodiny TGF-beta". Příroda. 425 (6958): 577–84. Bibcode:2003 Natur.425..577D. doi:10.1038 / nature02006. PMID 14534577. S2CID 4419607.
- ^ Kan L, Hu M, Gomes WA, Kessler JA (říjen 2004). „Transgenní myši nadměrně exprimující BMP4 vyvíjejí podobný fenotyp Fibrodysplasia Ossificans Progressiva (FOP)“. Dopoledne. J. Pathol. 165 (4): 1107–15. doi:10.1016 / S0002-9440 (10) 63372-X. PMC 1618644. PMID 15466378.
- ^ Dixon MJ, Marazita ML, Beaty TH, Murray JC (březen 2011). „Rozštěp rtu a patra: porozumění genetickým a environmentálním vlivům“. Nat. Genet. 12 (3): 167–78. doi:10.1038 / nrg2933. PMC 3086810. PMID 21331089.
- ^ Furuta Y, Hogan BL (prosinec 1998). „BMP4 je nezbytný pro indukci čočky v myším embryu“. Genes Dev. 12 (23): 3764–75. doi:10,1101 / gad.12.23.3764. PMC 317259. PMID 9851982.
- ^ Faber SC, Robinson ML, Makarenkova HP, Lang RA (srpen 2002). "Signalizace Bmp je vyžadována pro vývoj primárních optických buněk čočky". Rozvoj. 129 (15): 3727–37. PMID 12117821.
- ^ Cotsarelis G, Millar SE (červenec 2001). "Směrem k molekulárnímu porozumění vypadávání vlasů a jejich léčbě". Trends Mol Med. 7 (7): 293–301. doi:10.1016 / S1471-4914 (01) 02027-5. PMID 11425637.
- ^ A b Millar SE (únor 2002). "Molekulární mechanismy regulující vývoj vlasových folikulů". J. Invest. Dermatol. 118 (2): 216–25. doi:10.1046 / j.0022-202x.2001.01670.x. PMID 11841536.
- ^ Kulessa H, Turk G, Hogan BL (prosinec 2000). „Inhibice Bmp signalizace ovlivňuje růst a diferenciaci v anagenním vlasovém folikulu“. EMBO J.. 19 (24): 6664–74. doi:10.1093 / emboj / 19.24.6664. PMC 305899. PMID 11118201.
- ^ A b Huelsken J, Vogel R, Erdmann B, Cotsarelis G, Birchmeier W (květen 2001). „beta-katenin řídí morfogenezi vlasových folikulů a diferenciaci kmenových buněk v kůži“. Buňka. 105 (4): 533–45. doi:10.1016 / S0092-8674 (01) 00336-1. PMID 11371349. S2CID 16775006.
- ^ Feijen A, Goumans MJ, van den Eijnden-van Raaij AJ (prosinec 1994). „Exprese aktivinových podjednotek, receptorů aktivinu a follistatinu v postimplantačních myších embryích naznačuje specifické vývojové funkce pro různé aktiviny“. Rozvoj. 120 (12): 3621–37. PMID 7821227.
- ^ Botchkarev VA, Botchkareva NV, Nakamura M, Huber O, Funa K, Lauster R, Paus R, Gilchrest BA (říjen 2001). "Noggin je nutný pro indukci fáze růstu vlasových folikulů v postnatální kůži". FASEB J. 15 (12): 2205–14. doi:10.1096 / fj.01-0207com. PMID 11641247. S2CID 10236217.
Další čtení
- Wozney JM, Rosen V, Celeste AJ, Mitsock LM, Whitters MJ, Kriz RW, Hewick RM, Wang EA (1989). "Nové regulátory tvorby kostí: molekulární klony a aktivity". Věda. 242 (4885): 1528–34. doi:10.1126 / science.3201241. PMID 3201241.
- Rosenzweig BL, Imamura T, Okadome T, Cox GN, Yamashita H, ten Dijke P, Heldin CH, Miyazono K (1995). "Klonování a charakterizace lidského receptoru typu II pro kostní morfogenetické proteiny". Proc. Natl. Acad. Sci. USA. 92 (17): 7632–6. Bibcode:1995PNAS ... 92.7632R. doi:10.1073 / pnas.92.17.7632. PMC 41199. PMID 7644468.
- Nohno T, Ishikawa T, Saito T, Hosokawa K, Noji S, Wolsing DH, Rosenbaum JS (1995). „Identifikace lidského receptoru typu II pro kostní morfogenetický protein-4, který tvoří rozdílné heteromerní komplexy s kostními morfogenetickými proteiny typu I“. J. Biol. Chem. 270 (38): 22522–6. doi:10.1074 / jbc.270.38.22522. PMID 7673243.
- Yamaji N, Celeste AJ, Thies RS, Song JJ, Bernier SM, Goltzman D, Lyons KM, Nove J, Rosen V, Wozney JM (1995). „Savčí serin / threoninkinázový receptor se specificky váže na BMP-2 a BMP-4.“ Biochem. Biophys. Res. Commun. 205 (3): 1944–51. doi:10.1006 / bbrc.1994.2898. PMID 7811286.
- Harris SE, Harris MA, Mahy P, Wozney J, Feng JQ, Mundy GR (1994). "Exprese kostních morfogenetických proteinových nosičů RNA normálními krysími a lidskými buňkami prostaty a rakoviny prostaty". Prostata. 24 (4): 204–11. doi:10.1002 / pros.2990240406. PMID 8146069.
- van den Wijngaard A, van Kraay M, van Zoelen EJ, Olijve W, Boersma CJ (1996). „Genomická organizace genu morfogenetického proteinu-4 lidské kosti: molekulární základ pro více transkriptů“. Biochem. Biophys. Res. Commun. 219 (3): 789–94. doi:10.1006 / bbrc.1996.0312. hdl:2066/23948. PMID 8645259.
- Nishitoh H, Ichijo H, Kimura M, Matsumoto T, Makishima F, Yamaguchi A, Yamashita H, Enomoto S, Miyazono K (1996). „Identifikace receptorů serin / threoninkinázy typu I a typu II pro růstový / diferenciační faktor-5“. J. Biol. Chem. 271 (35): 21345–52. doi:10.1074 / jbc.271.35.21345. PMID 8702914.
- Bonaldo MF, Lennon G, Soares MB (1997). „Normalizace a odčítání: dva přístupy k usnadnění objevování genů“. Genome Res. 6 (9): 791–806. doi:10,1101 / gr. 6.9.791. PMID 8889548.
- Shore EM, Xu M, Shah PB, Janoff HB, Hahn GV, Deardorff MA, Sovinsky L, Spinner NB, Zasloff MA, Wozney JM, Kaplan FS (1998). „Gen lidské morfogenetické bílkoviny 4 (BMP-4): molekulární struktura a regulace transkripce“. Calcif. Tissue Int. 63 (3): 221–9. doi:10,1007 / s002239900518. PMID 9701626. S2CID 8339465.
- Tucker AS, Matthews KL, Sharpe PT (1998). "Transformace typu zubu vyvolaná inhibicí signalizace BMP". Věda. 282 (5391): 1136–8. Bibcode:1998Sci ... 282.1136T. doi:10.1126 / science.282.5391.1136. PMID 9804553.
- Van den Wijngaard A, Pijpers MA, Joosten PH, Roelofs JM, Van zoelen EJ, Olijve W (1999). "Funkční charakterizace dvou promotorů v genu morfogenetického proteinu-4 lidské kosti". J. Bone Miner. Res. 14 (8): 1432–41. doi:10.1359 / jbmr.1999.14.8.1432. PMID 10457277.
- Li W, LoTurco JJ (2000). „Noggin je negativní regulátor neuronové diferenciace ve vývoji neokortexu“. Dev. Neurosci. 22 (1–2): 68–73. doi:10.1159/000017428. PMID 10657699. S2CID 35547875.
- Raatikainen-Ahokas A, Hytönen M, Tenhunen A, Sainio K, Sariola H (2000). „BMP-4 ovlivňuje diferenciaci metanefrického mezenchymu a odhaluje časnou předozadní osu embryonální ledviny“. Dev. Dyn. 217 (2): 146–58. doi:10.1002 / (SICI) 1097-0177 (200002) 217: 2 <146 :: AID-DVDY2> 3.0.CO; 2-I. PMID 10706139.
- van den Wijngaard A, Mulder WR, Dijkema R, Boersma CJ, Mosselman S, van Zoelen EJ, Olijve W (2000). „Antiestrogeny specificky regulují aktivitu kostního morfogenetického proteinu-4 v lidských osteoblastických buňkách“. Mol. Endokrinol. 14 (5): 623–33. doi:10.1210 / mě. 14.5.623. PMID 10809227.
- Ying Y, Liu XM, Marble A, Lawson KA, Zhao GQ (2000). "Požadavek Bmp8b na generování prvotních zárodečných buněk u myši". Mol. Endokrinol. 14 (7): 1053–63. doi:10.1210 / oprava.14.7.0479. PMID 10894154.
- Nakade O, Takahashi K, Takuma T, Aoki T, Kaku T (2001). „Vliv extracelulárního vápníku na genovou expresi kostního morfogenetického proteinu-2 a -4 normálních lidských kostních buněk“. J. Bone Miner. Metab. 19 (1): 13–9. doi:10,1007 / s007740170055. PMID 11156467. S2CID 23873280.
- Hatta T, Konishi H, Katoh E, Natsume T, Ueno N, Kobayashi Y, Yamazaki T (2001). "Identifikace vazebného místa pro ligand receptoru BMP typu IA pro BMP-4". Biopolymery. 55 (5): 399–406. doi:10.1002 / 1097-0282 (2000) 55: 5 <399 :: AID-BIP1014> 3.0.CO; 2-9. PMID 11241215.
- Aoki H, Fujii M, Imamura T, Yagi K, Takehara K, Kato M, Miyazono K (2001). "Synergické účinky různých kostních morfogenetických proteinů typu I na indukci alkalické fosfatázy". J. Cell Sci. 114 (Pt 8): 1483–9. PMID 11282024.
- Kalinovsky A, Boukhtouche F, Blazeski R, Bornmann C, Suzuki N, Mason CA, Scheiffele P (2011). Polleux F (ed.). „Vývoj specificity Axon-Target u atocentů Ponto-Cerebellar“. PLOS Biology. 9 (2): e1001013. doi:10.1371 / journal.pbio.1001013. PMC 3035609. PMID 21346800.
- Cotsarelis G, Millar SE (červenec 2001). "Směrem k molekulárnímu porozumění vypadávání vlasů a jejich léčbě". Trends Mol Med. 7 (7): 293–301. doi:10.1016 / S1471-4914 (01) 02027-5. PMID 11425637.
- Feijen A, Goumans MJ, van den Eijnden-van Raaij AJ (prosinec 1994). "Expression of activin subunits, activin receptors and follistatin in postimplantation mouse embryos suggests specific developmental functions for different activins". Rozvoj. 120 (12): 3621–37. PMID 7821227.
- Graham A, Francis-West P, Brickell P, Lumsden A (prosinec 1994). „Signální molekula BMP4 zprostředkovává apoptózu v kosočtverečném nervovém hřebenu“. Příroda. 372 (6507): 684–6. Bibcode:1994Natur.372..684G. doi:10.1038 / 372684a0. PMID 7990961. S2CID 4361935.
- Huelsken J, Vogel R, Erdmann B, Cotsarelis G, Birchmeier W (May 2001). "beta-Catenin controls hair follicle morphogenesis and stem cell differentiation in the skin". Buňka. 105 (4): 533–45. doi:10.1016/S0092-8674(01)00336-1. PMID 11371349. S2CID 16775006.
- Kulessa H, Turk G, Hogan BL (December 2000). "Inhibition of Bmp signaling affects growth and differentiation in the anagen hair follicle". EMBO J.. 19 (24): 6664–74. doi:10.1093/emboj/19.24.6664. PMC 305899. PMID 11118201.
- Leong LM, Brickell PM (December 1996). "Bone morphogenic protein-4". Int. J. Biochem. Cell Biol. 28 (12): 1293–6. doi:10.1016/S1357-2725(96)00075-1. PMID 9022288.
- Liem KF, Tremml G, Roelink H, Jessell TM (September 1995). "Dorsal differentiation of neural plate cells induced by BMP-mediated signals from epidermal ectoderm". Buňka. 82 (6): 969–79. doi:10.1016/0092-8674(95)90276-7. PMID 7553857. S2CID 17106597.
- Millar SE (February 2002). "Molecular mechanisms regulating hair follicle development". J. Invest. Dermatol. 118 (2): 216–25. doi:10.1046/j.0022-202x.2001.01670.x. PMID 11841536.
- Pourquié O, Fan CM, Coltey M, Hirsinger E, Watanabe Y, Bréant C, Francis-West P, Brickell P, Tessier-Lavigne M, Le Douarin NM (February 1996). "Lateral and axial signals involved in avian somite patterning: a role for BMP4". Buňka. 84 (3): 461–71. doi:10.1016/S0092-8674(00)81291-X. PMID 8608600. S2CID 15824329.
- Wang EA, Israel DI, Kelly S, Luxenberg DP (1993). "Bone morphogenetic protein-2 causes commitment and differentiation in C3H10T1/2 and 3T3 cells". Growth Factors. 9 (1): 57–71. doi:10.3109/08977199308991582. PMID 8347351.
- Winnier G, Blessing M, Labosky PA, Hogan BL (September 1995). "Bone morphogenetic protein-4 is required for mesoderm formation and patterning in the mouse". Genes Dev. 9 (17): 2105–16. doi:10.1101/gad.9.17.2105. PMID 7657163.
externí odkazy
- BMPedia - the Bone Morphogenetic Protein Wiki[trvalý mrtvý odkaz ]
- BMP4 umístění lidského genu v UCSC Genome Browser.
- BMP4 podrobnosti o lidském genu v UCSC Genome Browser.






