Oocyt - Oocyte
| Oocyt | |
|---|---|
| Identifikátory | |
| Pletivo | D009865 |
| FMA | 18644 |
| Anatomická terminologie | |
An oocyt (Spojené království: /ˈoʊəsaɪt/, NÁS: /ˈoʊoʊ-/), oöcyte, vajíčkonebo jen zřídka ocyte[Citace je zapotřebí ]je žena gametocyty nebo zárodečná buňka zahrnutý do něčeho, zůčastnit se čeho reprodukce. Jinými slovy, je to nezralé vajíčko nebo vaječná buňka. Oocyt se produkuje ve vaječníku během ženská gametogeneze. Ženské zárodečné buňky produkují prvotní zárodečné buňky (PGC), které poté procházejí mitóza, formování oogonia. V době oogeneze se oogonie stávají primárními oocyty. Oocyt je forma genetického materiálu, který lze sbírat pro kryokonzervaci. Kryokonzervace živočišných genetických zdrojů byl uveden do činnosti jako prostředek k zachování tradičních hospodářských zvířat.
Formace
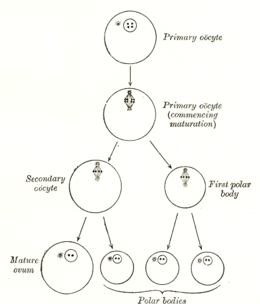
Tvorba oocytů se nazývá oocytogeneze, která je součástí oogeneze.[1] Oogeneze vede k tvorbě obou primární oocyty během fetálního období a sekundární oocytů po něm jako součást ovulace.
| Typ buňky | ploidie /chromozomy | chromatidy | Proces | Čas dokončení |
| Oogonium | diploidní / 46 (2N) | 2C | Oocytogeneze (mitóza ) | třetí trimestr |
| primární oocyt | diploidní / 46 (2N) | 4C | Ootidogeneze (redukční dělení buněk Já) (Folikulogeneze ) | Diktát ve fázi I po dobu až 50 let |
| sekundární oocyt | haploid / 23 (1N) | 2C | Ootidogeneze (redukční dělení buněk II) | Zastaven v metafázi II až do oplodnění |
| Ootid | haploid / 23 (1N) | 1C | Ootidogeneze (redukční dělení buněk II) | Minuty po oplodnění |
| Vajíčko | haploid / 23 (1N) | 1C |
Vlastnosti
Cytoplazma
Oocyty jsou bohaté na cytoplazma, který obsahuje žloutkové granule, které vyživují buňku v rané fázi vývoje.
Jádro
Během primárního oocytového stádia oogeneze se jádru říká zárodečný váček.[2]
Jediný normální lidský typ sekundárního oocytu má 23. (pohlaví) chromozom jako 23, X (určující pro ženy), zatímco spermie může mít 23, X (určující pro ženy) nebo 23, Y (určující pro muže).
Hnízdo
Prostor uvnitř vajíčka nebo nezralého vajíčka je umístěn buněčné hnízdo.[3]
Komplex kumulus-oocyt
Komplex cumulus-oocyt obsahuje vrstvy pevně zabalených buněk cumulus obklopujících oocyt ve Graafianově folikulu. Oocyt je zadržován v meióze II ve fázi metafáze II a je považován za sekundární oocyt. Před ovulací prochází komplex kupy strukturální změnou známou jako expanze kupy. Buňky granulózy se transformují z pevně zhutněné na expandovanou mukoidní matrici. Mnoho studií ukazuje, že expanze kupy je pro zrání oocytu rozhodující, protože komplex kupy je přímou komunikací oocytu s vyvíjejícím se folikulárním prostředím. Hraje také významnou roli při oplodnění, ačkoli mechanismy nejsou zcela známy a jsou druhově specifické.[4][5][6]
Mateřské příspěvky
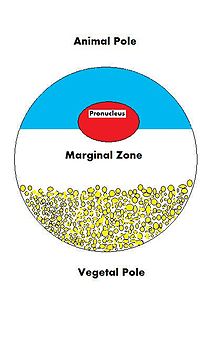
Protože osud oocytu má být oplodněn a nakonec vyroste v plně fungující organismus, musí být připraven regulovat více buněčných a vývojových procesů. Oocyt, velká a složitá buňka, musí být zásobován mnoha molekulami, které budou řídit růst embrya a řídit buněčné aktivity. Protože oocyt je produktem ženy gametogeneze, příspěvek matky k oocytu a následně k nově oplodněnému vajíčku je obrovský. Existuje mnoho typů molekul, které jsou mateřsky dodávány do oocytů, které budou řídit různé aktivity v rámci pěstování zygota.
Zabránění poškození DNA zárodečné linie
DNA buňky je citlivá na škodlivý účinek oxidačních volných radikálů produkovaných jako vedlejší produkty buněčného metabolismu. Poškození DNA vyskytující se v oocytech, pokud není opraveno, může být smrtelné a vést ke snížení plodnosti a ztrátě potenciálního potomka. Oocyty jsou podstatně větší než průměrné somatické buňky, a proto je pro jejich zásobování nezbytná značná metabolická aktivita. Pokud by tato metabolická aktivita byla prováděna vlastním metabolickým mechanismem oocytu, genom oocytu by byl vystaven generovaným reaktivním oxidačním vedlejším produktům. Zdá se tedy, že se vyvinul proces, aby se zabránilo této zranitelnosti DNA zárodečné linie. Bylo navrženo, aby se zabránilo poškození genomu DNA oocytů, metabolismus přispívající k syntéze většiny složek oocytů byl přesunut do jiných mateřských buněk, které poté tyto složky přenesly do oocytů.[7][8] Oocyty mnoha organismů jsou tedy chráněny před poškozením oxidační DNA, přičemž se ukládá velké množství látek, které vyživují zygotu v počátečním embryonálním růstu.
mRNA a proteiny
Během růstu oocytů se objevila řada mateřských transkribovaných mediálních RNA nebo mRNA, jsou dodávány mateřskými buňkami. Tyto mRNA mohou být uloženy v komplexech mRNP (zpráva ribonukleoprotein) a mohou být přeloženy ve specifických časových bodech, mohou být lokalizovány ve specifické oblasti cytoplazmy nebo mohou být homogenně dispergovány v cytoplazmě celého oocytu.[9] Mateřsky naloženo bílkoviny mohou být také lokalizovány nebo všudypřítomné v celé cytoplazmě. Přeložené produkty mRNA a naložených proteinů mají více funkcí; od regulace buněčného „udržování“, jako je progrese buněčného cyklu a buněčného metabolismu, až po regulaci vývojových procesů, jako je oplodnění, aktivace zygotické transkripce a tvorba os těla.[9] Níže uvádíme několik příkladů zděděných mRNA a proteinů nalezených v oocytech Africké drápy žába.
| název | Typ mateřské molekuly | Lokalizace | Funkce |
|---|---|---|---|
| VegT[10] | mRNA | Rostlinná polokoule | Transkripční faktor |
| Vg1[11] | mRNA | Rostlinná polokoule | Transkripční faktor |
| XXBP-1[12] | mRNA | Neznámý | Transkripční faktor |
| CREB[13] | Protein | Všudypřítomný | Transkripční faktor |
| FoxH1[14] | mRNA | Všudypřítomný | Transkripční faktor |
| p53[15] | Protein | Všudypřítomný | Transkripční faktor |
| Lef / Tcf[16] | mRNA | Všudypřítomný | Transkripční faktor |
| FGF2[17] | Protein | Jádro | Neznámý |
| FGF2, 4, 9 FGFR1[16] | mRNA | Neznámý | Signalizace FGF |
| Ektodermin[18] | Protein | Zvířecí polokoule | Ubikvitin ligáza |
| PACE4[19] | mRNA | Rostlinná polokoule | Proprotein konvertáza |
| Kokos[20] | Protein | Neznámý | Inhibitor BMP |
| Pokroucená gastrulace[16] | Protein | Neznámý | BMP / Chordin vazebný protein |
| fatvg[21] | mRNA | Rostlinná polokoule | Tvorba zárodečných buněk a kortikální rotace |

Mitochondrie
Oocyt přijímá mitochondrie z mateřských buněk, které budou dále řídit embryonální metabolismus a apoptotické události.[9] Rozdělení mitochondrií se provádí systémem mikrotubuly který lokalizuje mitochondrie v celém oocytu. V určitých organismech, jako jsou savci, jsou otcovské mitochondrie přivedené do oocytů spermatozoonem degradovány připojením ubikvitinovaných proteinů. Zničení otcovských mitochondrií zajišťuje striktně mateřskou dědičnost mitochondrií a mitochondriální DNA nebo mtDNA.[9]
Nucleolus
U savců jádro oocytu pochází pouze z mateřských buněk.[22] Nukleolus, struktura nacházející se v jádru, je místem, kde je rRNA transkribována a sestavována do ribozomů. Zatímco jádro je ve zralém oocytu husté a neaktivní, je nezbytné pro správný vývoj embrya.[22]
Ribozomy
Mateřské buňky také syntetizují a přispívají zásobou ribozomy které jsou nutné pro translaci proteinů před aktivací zygotického genomu. V savčích oocytech jsou ribozomy odvozené od matky a některé mRNA uloženy ve struktuře zvané cytoplazmatické mřížky. Bylo pozorováno, že tyto cytoplazmatické mřížky, síť fibril, bílkovin a RNA, rostou v hustotě, protože počet ribozomů klesá v rostoucím oocytu.[23]
Otcovské příspěvky
The spermatozoid který oplodňuje oocyt, přispěje svým pronucleus, druhá polovina zygotic genom. U některých druhů bude spermatozoon také přispívat a centriole, což pomůže vytvořit zygotiku centrosome požadované pro první divizi. U některých druhů, například u myší, se však celý centrosom získává mateřsky.[24] V současné době je vyšetřována možnost dalších cytoplazmatických příspěvků spermatu do embrya.
Během oplodnění poskytuje spermie oocytu tři základní části: (1) signalizační nebo aktivační faktor, který způsobuje aktivaci metabolicky spícího oocytu; (2) haploidní otcovský genom; (3) centrosom, který je odpovědný za udržování systému mikrotubulů. Viz anatomie spermie
Abnormality
- Nedisjunkce - selhání řádného oddělení homologu u meiózy I nebo sestry chromatid separace u meiózy II může vést k aneuploidie, ve kterém má oocyt nesprávný počet chromozomů, například 22, X nebo 24, X. To je příčina stavů jako Downův syndrom a Edwardsův syndrom u lidí. Pravděpodobnější je to u pokročilý mateřský věk.
- Některé oocyty mají více jádra, i když se předpokládá, že nikdy nedospějí.
Viz také
- Kortikální granule
- Kryokonzervace živočišných genetických zdrojů
- Folikulogeneze
- Inhibitor zrání oocytů
- Polární tělo
- Lámání symetrie a kortikální rotace
Reference
- ^ answer.com
- ^ Biologie - online
- ^ Grier HJ, Uribe MC, Parenti LR (duben 2007). „Germinální epitel, folikulogeneze a postovulační folikuly ve vaječnících pstruha duhového, Oncorhynchus mykiss (Walbaum, 1792) (Teleostei, protacanthopterygii, salmoniformes)“. J. Morphol. 268 (4): 293–310. doi:10.1002 / jmor.10518. PMID 17309079. S2CID 23482731.
- ^ Yokoo, M .; Sato, E. (2004). "Interakce komplexu kumulus-oocyt během zrání oocytů". International Review of Cytology. 235: 251–91. doi:10.1016 / S0074-7696 (04) 35006-0. ISBN 9780123646392. PMID 15219785.
- ^ Tanghe, S .; Van Soom, A .; Nauwynck, H .; Coryn, M .; De Kruif, A. (2002). "Minireview: Funkce cumulus oophorus během zrání, ovulace a oplodnění oocytů". Molekulární reprodukce a vývoj. 61 (3): 414–24. doi:10,1002 / mrd.10102. PMID 11835587. S2CID 5728551.
- ^ Huang, Zhongwei; Wells, Dagan (2010). „Vztah lidských oocytů a kupovité buňky: Nové poznatky z transkriptomu kupovité buňky“. MHR: Základní věda reprodukční medicíny. 16 (10): 715–725. doi:10,1093 / mol / gaq031. PMID 20435609.
- ^ Halliwell, Barry; Aruoma, Okezie I. (1993). „10“. DNA a volné radikály. ISBN 0132220350.
- ^ "4". ISBN 9789768056160. Chybějící nebo prázdný
| název =(Pomoc) - ^ A b C d Mtango, N.R .; Potireddy, S .; Latham, K.E. (2008). "Kvalita oocytů a mateřská kontrola vývoje". International Review of Cell and Molecular Biology. 268: 223–90. doi:10.1016 / S1937-6448 (08) 00807-1. PMID 18703408.
- ^ Zhang, J .; King, M. L. (1996). „RNA Xenopus VegT je během oogeneze lokalizována ve vegetativní kůře a kóduje nový transkripční faktor T-boxu, který se podílí na mezodermálním vzorování“. Development (Cambridge, Anglie). 122 (12): 4119–29. PMID 9012531.
- ^ Heasman, J .; Wessely, O .; Langland, R .; Craig, E. J .; Kessler, D. S. (2001). „Vegetální lokalizace mateřských mRNA je narušena vyčerpáním VegT“. Vývojová biologie. 240 (2): 377–86. doi:10.1006 / dbio.2001.0495. PMID 11784070.
- ^ Zhao, H .; Cao, Y .; Grunz, H. (2003). „Vazebný protein 1 Xenopus X-box, transkripční faktor leucinového zipu, je zapojen do signální dráhy BMP“. Vývojová biologie. 257 (2): 278–91. doi:10.1016 / s0012-1606 (03) 00069-1. PMID 12729558.
- ^ Sundaram, N .; Tao, Q .; Wylie, C .; Heasman, J. (2003). "Role mateřské CREB v časné embryogenezi Xenopus laevis". Vývojová biologie. 261 (2): 337–52. doi:10.1016 / s0012-1606 (03) 00303-8. PMID 14499645.
- ^ Kofron, M .; Puck, H .; Standley, H .; Wylie, C .; Old, R .; Whitman, M .; Heasman, J. (2004). „Nové role FoxH1 ve vzorcích raného embrya“. Development (Cambridge, Anglie). 131 (20): 5065–78. doi:10,1242 / dev.01396. PMID 15459100.
- ^ Takebayashi-Suzuki, K .; Funami, J .; Tokumori, D .; Saito, A .; Watabe, T .; Miyazono, K .; Kanda, A .; Suzuki, A. (2003). „Souhra mezi tumor supresorem p53 a TGF beta signalizací formuje osy embryonálního těla v Xenopus“. Development (Cambridge, Anglie). 130 (17): 3929–39. doi:10,1242 / dev.00615. PMID 12874116.
- ^ A b C Heasman, J. (2006). "Mateřské determinanty osudu embryonálních buněk". Semináře z buněčné a vývojové biologie. 17 (1): 93–8. doi:10.1016 / j.semcdb.2005.11.005. PMID 16426874.
- ^ Song, Jihwan; Slack, Jonathan M.W. (1994). "Prostorová a časová exprese mRNA a proteinu základního růstového faktoru fibroblastů (FGF-2) a proteinu v raném vývoji Xenopus". Mechanismy rozvoje. 48 (3): 141–151. doi:10.1016/0925-4773(94)90055-8. PMID 7893598. S2CID 20281053.
- ^ Dupont, S .; Zacchigna, L .; Cordenonsi, M .; Soligo, S .; Adorno, M .; Rugge, M .; Piccolo, S. (2005). „Specifikace zárodečné vrstvy a kontrola buněčného růstu pomocí Ectoderminu, ubikvitinové ligázy Smad4“. Buňka. 121 (1): 87–99. doi:10.1016 / j.cell.2005.01.033. PMID 15820681. S2CID 16628152.
- ^ Birsoy, B .; Berg, L .; Williams, P. H .; Smith, J. C .; Wylie, C. C .; Christian, J. L .; Heasman, J. (2005). „XPACE4 je lokalizovaná pro-proteinová konvertáza nezbytná pro indukci mezodermu a štěpení specifických proteinů TGFbeta ve vývoji Xenopus“. Development (Cambridge, Anglie). 132 (3): 591–602. doi:10,1242 / dev.01599. PMID 15634697.
- ^ Bell, E .; Muñoz-Sanjuán, I .; Altmann, C. R .; Vonica, A .; Brivanlou, A. H. (2003). "Specifikace osudu buněk a kompetence Coco, mateřského BMP, TGFbeta a WNT inhibitoru". Development (Cambridge, Anglie). 130 (7): 1381–9. doi:10,1242 / dev.00344. PMID 12588853.
- ^ Chan, A. P .; Kloc, M .; Larabell, C. A .; Legros, M .; Etkin, L. D. (2007). „Mateřsky lokalizovaný RNA fatvg je nutný pro kortikální rotaci a tvorbu zárodečných buněk“. Mechanismy rozvoje. 124 (5): 350–63. doi:10.1016 / j.mod.2007.02.001. PMC 2435194. PMID 17376659.
- ^ A b Ogushi, S .; Palmieri, C .; Fulka, H .; Saitou, M .; Miyano, T .; Fulka mladší, J. (2008). „Mateřské jádro je nezbytné pro časný embryonální vývoj u savců“. Věda. 319 (5863): 613–6. doi:10.1126 / science.1151276. PMID 18239124. S2CID 7799743.
- ^ Yurttas, P .; Vitale, A. M .; Fitzhenry, R. J .; Cohen-Gould, L .; Wu, W .; Gossen, J. A .; Coonrod, S.A. (2008). „Role pro PADI6 a cytoplazmatické mřížky v ribozomálním ukládání v oocytech a translační kontrola v časném myším embryu“. Development (Cambridge, Anglie). 135 (15): 2627–36. doi:10,1242 / dev.016329. PMC 2708103. PMID 18599511.
- ^ Sutovsky, P .; Schatten, G. (2000). "Otcovské příspěvky k savčímu zygotu: Oplodnění po fúzi spermatu a vajíčka". International Review of Cytology. 195: 1–65. doi:10.1016 / s0074-7696 (08) 62703-5. ISBN 9780123645999. PMID 10603574.
Zdroje
- William K. Purves, Gordon H. Orians, David Sadava, H. Craig Heller, Craig Heller (2003). Life: The Science of Biology (7. vydání), str. 823–824.
externí odkazy
| Předcházet Žádný | Fáze lidského vývoje Spermie + Oocyt | Uspěl Zygota |
