S-adenosyl methionin - S-Adenosyl methionine
 | |||
| Jména | |||
|---|---|---|---|
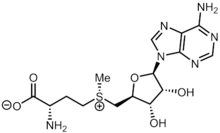
| Název IUPAC (S) -2-amino-4 - ((SS)-(((2S,3S,4R,5R) -5- (6-amino-9H-purin-9-yl) -3,4-dihydroxytetrahydrofuran-2-yl) methyl) (methyl) sulfonio) butanoát | |||
| Ostatní jména S-Adenosyl-L-methionin; Stejný; SAMe, AdoMet, ademethionin | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEMBL | |||
| ChemSpider | |||
| Informační karta ECHA | 100.045.391 | ||
| KEGG | |||
| Pletivo | S-adenosylmethionin | ||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C15H22N6Ó5S | |||
| Molární hmotnost | 398.44 g · mol−1 | ||
| Farmakologie | |||
| A16AA02 (SZO) | |||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
S-Adenosyl methionin (Stejný) je běžný kosubstrát zahrnutý do něčeho, zůčastnit se čeho methylová skupina transfery, transsulfurace a aminopropylace. Ačkoli tyto anabolický reakce probíhají v celém těle, většina SAM-e se produkuje a spotřebovává v játrech.[1] Je známo více než 40 přenosů methylu z SAM-e na různé substráty, jako je např nukleové kyseliny, bílkoviny, lipidy a sekundární metabolity. Je vyroben z adenosintrifosfát (ATP) a methionin podle methionin adenosyltransferáza. SAM-e byl poprvé objeven Giulio Cantoni v roce 1952.[1]
V bakteriích je SAM-e vázán SAM riboswitch, který reguluje geny zapojené do methionin nebo cystein biosyntéza. V eukaryotických buňkách slouží SAM-e jako regulátor různých procesů včetně DNA, tRNA a metylace rRNA; imunitní odpověď;[2] metabolismus aminokyselin; transsulfurace; a více. V rostlinách je SAM-e zásadní pro biosyntézu ethylen, důležitý rostlinný hormon a signální molekula.[3]
Chemicky je to sulfonium betain který slouží jako zdroj elektrofilní methylové skupiny nebo jako zdroj 5'-deoxyadenosylového radikálu.
Biochemie
Cyklus SAM-e
Reakce, které produkují, konzumují a regenerují SAM-e, se nazývají cyklus SAM-e. V prvním kroku tohoto cyklu závisí na SAM methylázy (EC 2.1.1), které používají SAM-e jako substrát S-adenosyl homocystein jako produkt.[4] S-Adenosyl homocystein je silným negativním regulátorem téměř všech methyláz závislých na SAM navzdory jejich biologické rozmanitosti. Toto je hydrolyzováno na homocystein a adenosin podle S-adenosylhomocystein hydroláza ES 3.3.1.1 a homocystein se recykluje zpět do methionin přenosem methylové skupiny z 5-methyltetrahydrofolát, jednou ze dvou tříd methionin syntázy (tj. kobalamin -závislý (ES 2.1.1.13 ) nebo nezávislé na kobalaminu (ES 2.1.1.14 )). Tento methionin lze poté převést zpět na SAM-e a dokončit cyklus.[5] V kroku omezujícím rychlost cyklu SAM MTHFR (methylenetetrahydrofolátreduktáza) nevratně redukuje 5,10-methylenetetrahydrofolát na 5-methyltetrahydrofolát.[6]
Radikální enzymy SAM-e
Velké množství enzymů obsahujících klastry železo-síra štěpí SAM-e reduktivně za vzniku a 5'-deoxyadenosyl 5'-radikál jako meziprodukt a jsou voláni radikální SAM enzymy.[7] Většina enzymů s touto schopností sdílí oblast sekvenční homologie, která zahrnuje motiv CxxxCxxC nebo blízkou variantu. Radikální meziprodukt umožňuje enzymům provádět širokou škálu neobvyklých chemických reakcí. Mezi příklady radikálových enzymů SAM patří Sporový fotoprodukt lyáza, aktivázy pyruvátformiát lyáza a anaerobní sulfatázy, lysin 2,3-aminomutáza a různé enzymy biosyntézy kofaktorů, modifikace peptidů, metaloprotein tvorba klastrů, tRNA modifikace, metabolismus lipidů atd. Některé radikální enzymy SAM-e používají jako donor methylu druhý SAM-e. Radikální enzymy SAM jsou mnohem hojnější v anaerobních bakteriích než v aerobních organismech. Lze je najít ve všech oblastech života a jsou do značné míry neprozkoumané. Nedávná bioinformatická studie dospěla k závěru, že tato rodina enzymů zahrnuje nejméně 114 000 sekvencí včetně 65 jedinečných reakcí.[8]
Polyaminová biosyntéza
Další významná role SAM-e je v polyamin biosyntéza. Zde je SAM-e dekarboxylován adenosylmethionin dekarboxyláza (EC 4.1.1.50 ) tvořit S-adenosylmethioninamin. Tato sloučenina pak daruje svoji n-propylaminovou skupinu při biosyntéze polyaminů, jako jsou spermidin a spermin z putrescine.[9]
SAM-e je vyžadován pro buněčný růst a opravu. Podílí se také na biosyntéze několika hormonů a neurotransmiterů, které ovlivňují náladu, jako např epinefrin. Methyltransferázy jsou také zodpovědné za přidání methylových skupin k 2 'hydroxylovým skupinám prvního a druhého nukleotidy vedle 5 'čepičky dovnitř messenger RNA.[10][11]
Terapeutické použití
Od roku 2012 byly důkazy neprůkazné, zda SAM může zmírnit bolest artróza; klinické studie, které byly provedeny, byly příliš malé na to, aby je bylo možné zobecnit.[12] Studie z roku 2016 dospěla k závěru, že pro velká depresivní porucha „Vzhledem k absenci vysoce kvalitních důkazů a neschopnosti vyvodit na základě těchto důkazů jednoznačné závěry by mělo být dále zkoumáno použití SAMe k léčbě deprese u dospělých.“[13]
Cyklus SAM-e je úzce spjat s játry od roku 1947, protože lidé s alkoholická cirhóza jater by akumulovalo velké množství methioninu v jejich krvi.[14] Zatímco několik důkazů z laboratorních testů na buňkách a zvířecí modely naznačují, že SAM může být užitečný k léčbě různých onemocnění jater Od roku 2012 nebyl SAM studován v žádných velkých randomizovaných placebem kontrolovaných klinických studiích, které by umožňovaly posoudit jeho účinnost a bezpečnost.[15][16]
Farmakokinetika
Perorální SAM dosahuje maximální plazmatické koncentrace tři až pět hodin po požití enterosolventní tablety (400–1000 mg). Poločas je asi 100 minut.[17]
Nepříznivé účinky
Gastrointestinální porucha, dyspepsie a úzkost může dojít při spotřebě SAM.[17] Dlouhodobé účinky nejsou známy. SAM je slabá DNA-alkylovat činidlo.[18]
Dalším hlášeným vedlejším účinkem SAM je nespavost; proto je doplněk často užíván ráno. Další zprávy o mírných vedlejších účincích zahrnují nechutenství, zácpu, nevolnost, sucho v ústech, pocení a úzkost / nervozitu, ale v placebem kontrolovaných studiích se tyto nežádoucí účinky vyskytují přibližně ve stejné incidenci ve skupinách s placebem.[nutná lékařská citace ]
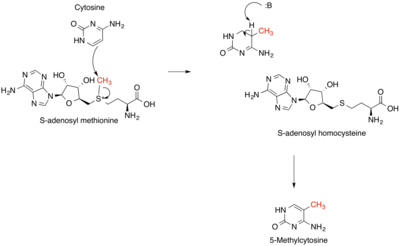
Nedávno bylo prokázáno, že SAM-e hraje roli v epigenetický nařízení. Methylace DNA je klíčovým regulátorem epigenetické modifikace během vývoje a diferenciace savčích buněk. V myších modelech byly nadměrné hladiny SAM-e zapleteny do chybných methylačních vzorů spojených s diabetickou neuropatií. SAM-e slouží jako donor methylu při methylaci cytosinu, což je klíčový epigenetický regulační proces.[19] Kvůli tomuto dopadu na epigenetickou regulaci byl SAM-e testován jako protinádorová léčba. Proliferace rakovinných buněk závisí na nízké úrovni methylace DNA. Bylo prokázáno, že přidání in vitro promíchává promotorové sekvence a snižuje produkci protoonkogenů.[20]
Nedostatky radikálních enzymů SAM-e byly spojeny s řadou nemocí včetně vrozené srdeční onemocnění, Amyotrofní laterální skleróza a zvýšená náchylnost k virům.[8]
Interakce a kontraindikace
Užívání SAM současně s některými léky může zvýšit riziko serotoninový syndrom, potenciálně nebezpečný stav způsobený příliš velkým množstvím serotoninu. Mezi tyto léky patří dextromethorfan (Robitussin), meperidin (Demerol), pentazocin (Talwin) a tramadol (Ultram). SAM může také interagovat s antidepresivy, čímž zvyšuje potenciál jejich vedlejších účinků a snižuje účinnost levodopa na Parkinsonovu chorobu.[nutná lékařská citace ]
Lidé, kteří mají bipolární porucha by neměl používat SAM, protože zvyšuje riziko manických epizod.[21]
Dostupnost v různých zemích
V Spojené státy a Kanada, SAM se prodává jako doplněk stravy pod marketingovým názvem SAM-e (také hláskováno SAME nebo SAMe; vyslovuje se „Sammy“ [22]; to bylo představeno v USA v roce 1999, po Zákon o doplňcích stravy o zdraví a školství byl schválen v roce 1994.[23]
To bylo představeno jako lék na předpis v Itálii v roce 1979, ve Španělsku v roce 1985 a v Německu v roce 1989;[23] od roku 2012 byl uveden na trh jako lék na předpis v Rusku, Indii, Číně, Itálii, Německu, Vietnamu a Mexiku.[16]
Viz také
- DNA methyltransferáza
- SAM-I riboswitch
- Riboswitch SAM-II
- Riboswitch SAM-III
- Riboswitch SAM-IV
- Riboswitch SAM-V
- Riboswitch SAM-VI
- Seznam hodnocených antidepresiv
Reference
- ^ A b Cantoni, GL (1952). „Povaha aktivního dárce methylu vznikla enzymaticky z L-Methionin a adenosinetrifosfát “. J Am Chem Soc. 74 (11): 2942–3. doi:10.1021 / ja01131a519.
- ^ Ding, Wei; Smulan, Lorissa J .; Hou, Nicole S .; Taubert, Stefan; Watts, Jennifer L .; Walker, Amy K. (06.10.2015). "S-Úrovně adenosylmethioninu řídí vrozenou imunitu prostřednictvím odlišných cest závislých na methylaci “. Buněčný metabolismus. 22 (4): 633–645. doi:10.1016 / j.cmet.2015.07.013. PMC 4598287. PMID 26321661.
- ^ Wang, X .; Oh, M. W .; Komatsu, S. (2016-06-01). "Charakterizace S-adenosylmethionin syntetázy v sóji pod tlakem povodní a sucha “. Biologia Plantarum. 60 (2): 269–278. doi:10.1007 / s10535-016-0586-6. ISSN 0006-3134. S2CID 15567646.
- ^ Finkelstein J, Martin J (2000). "Homocystein". Int J Biochem Cell Biol. 32 (4): 385–9. doi:10.1016 / S1357-2725 (99) 00138-7. PMID 10762063.
- ^ Födinger M, Hörl W, Sunder-Plassmann G (leden – únor 2000). "Molekulární biologie 5,10-methylenetetrahydrofolátreduktázy". J. Nephrol. 13 (1): 20–33. PMID 10720211.
- ^ Goyette, P .; Sumner, J. S .; Milos, R .; Duncan, A. M .; Rosenblatt, D. S .; Matthews, R. G .; Rozen, R. (01.06.1994). „Lidská methylenetetrahydrofolátreduktáza: izolace cDNA, mapování a identifikace mutací“. Genetika přírody. 7 (2): 195–200. doi:10.1038 / ng0694-195. ISSN 1061-4036. PMID 7920641. S2CID 23877329.
- ^ Booker, SJ; Grove, TL (2010). „Mechanická a funkční univerzálnost radikálních enzymů SAM“. F1000 biologické zprávy. 2: 52. doi:10.3410 / B2-52. PMC 2996862. PMID 21152342.
- ^ A b Landgraf, Bradley J .; McCarthy, Erin L .; Booker, Squire J. (2016-06-13). "Radikální S-Adenosylmethioninové enzymy v oblasti lidského zdraví a nemocí “. Roční přehled biochemie. 85: 485–514. doi:10,1146 / annurev-biochem-060713-035504. PMID 27145839.
- ^ Roje S (2006). "S-Adenosyl-L-methionin: nad rámec univerzálního dárce methylové skupiny “. Fytochemie. 67 (15): 1686–98. doi:10.1016 / j.phytochem.2006.04.019. PMID 16766004.
- ^ Loenen W (2006). "S-Adenosylmethionin: Jack všech obchodů a pán všeho? “. Biochem Soc Trans. 34 (Pt 2): 330–3. doi:10.1042 / BST20060330. PMID 16545107.
- ^ Chiang P, Gordon R, Tal J, Zeng G, doktor B, Pardhasaradhi K, McCann P (1996). "S-Adenosylmethionin a methylace ". FASEB J. 10 (4): 471–80. doi:10.1096 / fasebj.10.4.8647346. PMID 8647346.
- ^ Rutjes, AW; Nüesch, E; Reichenbach, S; Jüni, P (7. října 2009). "S-Adenosylmethionin pro osteoartrózu kolene nebo kyčle " (PDF). Cochrane Database of Systematic Reviews (4): CD007321. doi:10.1002 / 14651858.CD007321.pub2. PMC 7061276. PMID 19821403.
- ^ Galizia, I; Oldani, L; Macritchie, K; Amari, E; Dougall, D; Jones, TN; Lam, RW; Massei, GJ; Yatham, LN; Young, AH (10. října 2016). "S-Adenosyl methionin (SAMe) pro depresi u dospělých ". Cochrane Database of Systematic Reviews. 10: CD011286. doi:10.1002 / 14651858.CD011286.pub2. PMC 6457972. PMID 27727432.
- ^ Mato, Jose M (1997). "S-adenosylmethioninová syntéza: Molekulární mechanismy a klinické důsledky ". Farmakologie a terapeutika. 73 (3): 265–280. doi:10.1016 / s0163-7258 (96) 00197-0. hdl:10261/79246. PMID 9175157.
- ^ Anstee, QM; Den, CP (listopad 2012). "S-Adenosylmethioninová (SAMe) léčba onemocnění jater: přehled současných důkazů a klinické užitečnosti ". Journal of Hepatology. 57 (5): 1097–109. doi:10.1016 / j.jhep.2012.04.041. PMID 22659519.
- ^ A b Lu, SC; Mato, JM (říjen 2012). "S-Adenosylmethionin pro zdraví jater, úrazy a rakovinu ". Fyziologické recenze. 92 (4): 1515–42. doi:10.1152 / physrev.00047.2011. PMC 3698976. PMID 23073625.
- ^ A b Najm WI, Reinsch S, Hoehler F, Tobis JS, Harvey PW (únor 2004). "S-Adenosyl methionin (SAMe) versus celekoxib pro léčbu příznaků osteoartrózy: dvojitě zaslepená zkřížená studie. ISRCTN36233495 ". BMC Musculoskelet Disord. 5: 6. doi:10.1186/1471-2474-5-6. PMC 387830. PMID 15102339.
- ^ Rydberg B, Lindahl T (1982). „Neenzymatická methylace DNA dárcem intracelulární methylové skupiny S-adenosyl-L-methionin je potenciálně mutagenní reakce ". EMBO J.. 1 (2): 211–6. doi:10.1002 / j.1460-2075.1982.tb01149.x. PMC 553022. PMID 7188181.
- ^ Varela-Rey, Marta (2014). "S-Úrovně adenosylmethioninu regulují methylome DNA Schwannových buněk ". Neuron. 81 (5): 1024–1039. doi:10.1016 / j.neuron.2014.01.037. PMC 3960855. PMID 24607226.
- ^ Schmidt, Thomas; Leha, Andreas; Salinas-Riester, Gabriela (31. 12. 2016). "Léčba buněk rakoviny prostaty pomocí S-adenosylmethionin vede ke změnám v transkripčních profilech v celém genomu “. Gen. 595 (2): 161–167. doi:10.1016 / j.gene.2016.09.032. PMID 27688072.
- ^ "S-Adenosyl-L-Methionine (SAMe): In Depth ". NCCIH. 11. ledna 2017.
- ^ Woolston, Chris. „Co je SAM-e?“ 1. ledna 2019. Citováno dne 14. listopadu 2019.
- ^ A b Bottiglieri, T (listopad 2002). "S-Adenosyl-L-methionin (SAMe): od lavičky k lůžku - molekulární základ pleiotrofní molekuly ". American Journal of Clinical Nutrition. 76 (5): 1151S – 1157S. doi:10.1093 / ajcn / 76.5.1151S. PMID 12418493.
externí odkazy
- Číslo EINECS 249-946-8
- Shippy, R Andrew; Mendez, Douglas; Jones, Kristina; Cergnul, Irene; Karpiak, Stephen E (2004). "S-Adenosylmethionin (SAM-e) k léčbě deprese u lidí žijících s HIV / AIDS ". Psychiatrie BMC. 4: 38. doi:10.1186 / 1471-244X-4-38. PMC 535560. PMID 15538952.
