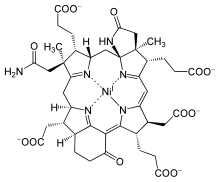
Kofaktor F430 - Cofactor F430
 | |
| Identifikátory | |
|---|---|
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Vlastnosti | |
| C 42H 51N 6NiO− 13 | |
| Molární hmotnost | 906.58014 |
| Vzhled | Žlutá pevná látka |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
F430 je kofaktor (někdy nazývaný koenzym) enzym methyl koenzym M reduktáza (MCR).[1][2]MCR katalyzuje reakci ES 2.8.4.1 který v posledním kroku uvolňuje metan methanogeneze:
- CH
3–S – CoM + HS – CoB → CH
4 + CoB – S – S – CoM
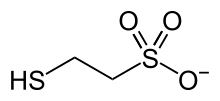 Struktura koenzymu M (HS-CoM) |  Struktura koenzymu B (HS-CoB) |
Nachází se pouze v methanogenní Archaea[3] a anaerobní methanotrofní Archea. Vyskytuje se v relativně vysokých koncentracích v archaeách, které se účastní reverzní methanogeneze: mohou obsahovat až 7% hmotnostních niklového proteinu.[4]
Struktura
The triviální jméno kofaktor F430 byl přidělen v roce 1978 na základě vlastností žlutého vzorku extrahovaného z Methanobacterium thermoautotrophicum, který měl a spektroskopické maximálně při 430 nm.[5] V roce 1982 byl identifikován jako kofaktor MCR[6] a úplná struktura byla odvozena Rentgenová krystalografie a NMR spektroskopie.[7] Koenzym F430 funkce a snížena porfyrin v makrocyklický prstencový systém zvaný corphin.[8] Kromě toho má ve srovnání se standardem dva další prsteny tetrapyrrol (kroužky A-D), které mají a y-laktam kruh E a obsahující keto karbocyklický kruh F. Je to jediný přírodní tetrapyrrol obsahující nikl, prvek zřídka nalezený v biologických systémech.[9]
Biosyntéza
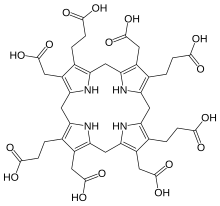 uroporphyrinogen III |  dihydrosirohydrochlorin |  sirohydrochlorin |
Biosyntéza vychází z uroporphyrinogen III, předek všech přírodních tetrapyrrolů, včetně chlorofylu, vitaminu B.12, phycobilins, siroheme, hem a heme d1. Je převeden na sirohydrochlorin přes dihydrosirohydrochlorin.[10] Vložení niklu do tohoto tetrapyrrolu je katalyzováno v reakci ES 4.99.1.11 stejně chelatáza, CbiX, který vloží kobalt do biosyntéza kobalaminu, přičemž se získá nikl (II) -sirohydrochlorin.[11]
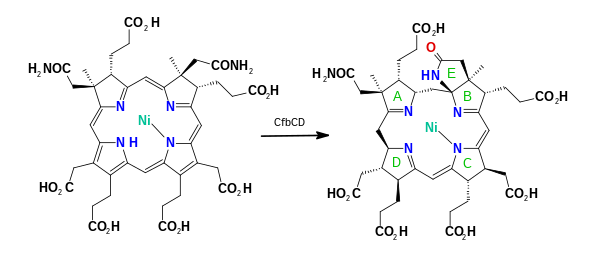
Závisí na ATP Ni-sirohydrochlorin a, c-diamid-syntetáza (CfbE) poté převede A a C acetátové postranní řetězce acetamid v reakcích ES 6.3.5.12 za vzniku nikl (II) -sirohydrochlorinu A,C-diamid. Pořadí obou amidací je náhodné.[11] Dvousložkový komplex Ni-sirohydrochlorin a, c-diamid reduktivní cykláza (CfbCD) provádí 6-elektronovou a 7-protonovou redukci kruhového systému v reakci ES 6.3.3.7 generování 15,173-seco-F430-173-kyselina (seco-F430) středně pokročilí. Redukce zahrnuje hydrolýzu ATP a elektrony jsou přenášeny prostřednictvím dvou center 4Fe-4S. V posledním kroku je karbocyklický kruh F obsahující keto tvořen enzymem závislým na ATP Koenzym F (430) syntetáza (CfbB) v reakci ES 6.4.1.9, generující koenzym F430.[11][12][13] Tento enzym je a MurF-podobná ligáza, jak je uvedeno v peptidoglykan biosyntéza.
Reference
- ^ Stephen W., Ragdale (2014). "Kapitola 6. Biochemistry of Methyl-Coenzyme M Reductase: The Nickel Metalloenzyme that Catalyzuje the Last Step in Synthesis and the First Step in Anaerobic Oxidation of the Greenhouse Gas Methane". V Peter M.H. Kroneck a Martha E. Sosa Torres (ed.). Kovem řízená biogeochemie plynných sloučenin v životním prostředí. Kovové ionty v biologických vědách. 14. Springer. 125–145. doi:10.1007/978-94-017-9269-1_6. ISBN 978-94-017-9268-4. PMID 25416393.
- ^ Hofer, Ursula (2016). „Mistři metanu“. Příroda Recenze Mikrobiologie. 14 (12): 727. doi:10.1038 / nrmicro.2016.170. PMID 27818502.
- ^ Thauer RK (1998). „Biochemistry of Methanogenesis: a Hold to Marjory Stephenson“. Mikrobiologie. 144 (9): 2377–2406. doi:10.1099/00221287-144-9-2377. PMID 9782487.
- ^ Krüger M, Meyerdierks A, Glöckner FO a kol. (Prosinec 2003). „Výrazný protein niklu v mikrobiálních podložkách, které anaerobně oxidují metan“. Příroda. 426 (6968): 878–81. Bibcode:2003 Natur.426..878K. doi:10.1038 / nature02207. PMID 14685246.
- ^ Gunsalus, R.P .; Wolfe, R.S. (1978). "Chromoforické faktory F342 a F430 z Methanobacterium thermoautotrophicum ". Mikrobiologické dopisy FEMS. 3 (4): 191–193. doi:10.1111 / j.1574-6968.1978.tb01916.x.
- ^ Ellefson, W. L .; Whitman, W. B .; Wolfe, R. S. (1982). „Faktor obsahující nikl F430: Chromofor methylreduktázy Methanobacterium“. Sborník Národní akademie věd. 79 (12): 3707–3710. Bibcode:1982PNAS ... 79,3707E. doi:10.1073 / pnas.79.12.3707. PMC 346495. PMID 6954513.
- ^ Färber G, Keller W, Kratky C, Jaun B, Pfaltz A, Spinner C, Kobelt A, Eschenmoser A (1991). „Koenzym F430 z Methanogenic Bacteria: Complete Assign of Configuration Based on the X-ray Analysis of 12,13-diepi-F430 Pentamethyl Ester and on NMR Spectroscopy ". Helvetica Chimica Acta. 74 (4): 697–716. doi:10.1002 / hlca.19910740404.
- ^ Eschenmoser, A. (1986). „Chemistry of Corphinoids“. Annals of the New York Academy of Sciences. 471 (1 mezinárodní): 108. Bibcode:1986NYASA.471..108E. doi:10.1111 / j.1749-6632.1986.tb48030.x.
- ^ Johnson, Michael K .; Scott, Robert A. (2. října 2017). Sestava aktivního místa metaloproteinů. ISBN 9781119159834.
- ^ Mucha, Helmut; Keller, Eberhard; Weber, Hans; Lingens, Franz; Trösch, Walter (07.10.1985). „Sirohydrochlorin, prekurzor biosyntézy faktoru F430 v Methanobacterium thermoautotrophicum“. FEBS Dopisy. 190 (1): 169–171. doi:10.1016/0014-5793(85)80451-8.
- ^ A b C Moore, Simon J .; Sowa, Sven T .; Schuchardt, Christopher; Deery, Evelyne; Lawrence, Andrew D .; Ramos, José Vazquez; Billig, Susan; Birkemeyer, Claudia; Chivers, Peter T .; Howard, Mark J .; Rigby, Stephen E. J .; Layer, Gunhild; Warren, Martin J. (2017). „Elucidace biosyntézy koenzymu methanového katalyzátoru F430“. Příroda. 543 (7643): 78–82. Bibcode:2017Natur.543 ... 78M. doi:10.1038 / nature21427. PMC 5337119. PMID 28225763.
- ^ Zheng, Kaiyuan; Ngo, Phong D .; Owens, Victoria L .; Yang, Xue-Peng; Mansoorabadi, Steven O. (2016). „Biosyntetická dráha koenzymu F430 v methanogenních a methanotrofních oblastech. Věda. 354 (6310): 339–342. Bibcode:2016Sci ... 354..339Z. doi:10.1126 / science.aag2947. PMID 27846569.
- ^ R. Caspi (01.01.2017). „Cesta: biosyntéza faktoru 430“. Databáze metabolických cest MetaCyc. Citováno 2020-04-27.
