Kyselina glutarová - Glutaric acid
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Kyselina pentandiová | |
| Ostatní jména Kyselina glutarová Kyselina propan-1,3-dikarboxylová Kyselina 1,3-propandikarboxylová Kyselina pentandiová kyselina n-pyrotartarová | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Informační karta ECHA | 100.003.471 |
| Číslo ES |
|
| KEGG | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C5H8Ó4 | |
| Molární hmotnost | 132,12 g / mol |
| Bod tání | 95 až 98 ° C (203 až 208 ° F; 368 až 371 K) |
| Bod varu | 200 ° C (392 ° F; 473 K) / 20 mmHg |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
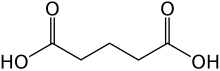
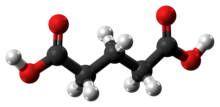
Kyselina glutarová je organická sloučenina s vzorec C3H6(COOH)2 . Ačkoli související „lineární“ dikarboxylové kyseliny adipický a jantarové kyseliny jsou při teplotě místnosti rozpustné ve vodě pouze na několik procent, rozpustnost kyseliny glutarové ve vodě je vyšší než 50% (hmotn./hmotn.).
Biochemie
Kyselina glutarová se přirozeně produkuje v těle během metabolismus některých aminokyseliny, počítaje v to lysin a tryptofan. Vady v této metabolické cestě může vést k poruše zvané glutarová acidurie, kde se hromadí toxické vedlejší produkty a mohou být závažné encefalopatie.
Výroba
Kyselinu glutarovou lze připravit otevřením kruhu butyrolakton s kyanid draselný za vzniku smíšeného karboxylátu draselnéhonitril který je hydrolyzován na dikyselinu.[1] Alternativně hydrolýza, následovaná oxidací dihydropyran dává kyselinu glutarovou. Může být také připraven z reakce 1,3-dibrompropan s sodík nebo kyanid draselný aby se získal dinitril, následovaný hydrolýzou.
Použití
- 1,5-pentandiol, běžný změkčovadlo a předchůdce polyestery vyrábí společnost hydrogenace kyseliny glutarové a jejích derivátů.[2]
- Samotná kyselina glutarová se používá při výrobě polymerů, jako je polyester polyoly, polyamidy. Lichý počet atomů uhlíku (tj. 5) je užitečný při snižování elasticity polymeru.[3]
- Kyselina uvitonová se získá působením amoniak na kyselině glutarové.
- Pyrogallol lze vyrobit z glutarového diesteru.[4]
Bezpečnost
Kyselina glutarová může způsobit podráždění kůže a očí.[5] Mezi akutní rizika patří skutečnost, že tato sloučenina může být škodlivá při požití, vdechování nebo absorpci kůží.[5]
Reference
- ^ G. Paris, L. Berlinguet, R. Gaudry, J. English, Jr. a J. E. Dayan (1963). „Kyselina glutarová a glutaramid“. Organické syntézy.CS1 maint: více jmen: seznam autorů (odkaz); Kolektivní objem, 4, str. 496
- ^ Peter Werle a Marcus Morawietz „Alkoholy, polyhydrické“ v Ullmann's Encyclopedia of Industrial Chemistry: 2002, Wiley-VCH: Weinheim. DOI 10.1002 / 14356007.a01_305
- ^ „Kyselina glutarová, kyselina pentandiová, 99%“. Chemkits.eu. Citováno 2020-09-29.
- ^ [1] „Metoda syntézy pyrogallolu“, vydaný 1976-02-17
- ^ A b Kyselina glutarová, cameochemicals.com
