Dusičnan lithný - Lithium nitrate
 | |
 | |
 | |
| Identifikátory | |
|---|---|
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.029.290 |
PubChem CID | |
| Číslo RTECS |
|
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| Linoleum3 | |
| Molární hmotnost | 68,946 g / mol |
| Vzhled | Bílá až světle žlutá pevná látka |
| Hustota | 2,38 g / cm3 |
| Bod tání | 255 ° C (491 ° F; 528 K) |
| Bod varu | 600 ° C (1112 ° F; 873 K) (rozkládá se) |
| 52,2 g / 100 ml (20 ° C) 90 g / 100 ml (28 ° C) 234 g / 100 ml (100 ° C) | |
| Rozpustnost | rozpustný v ethanol, methanolu, pyridin, amoniak, aceton |
| −62.0·10−6 cm3/ mol (+3 H2Ó) | |
Index lomu (nD) | 1.735[1] |
| Termochemie | |
Tepelná kapacita (C) | 64 J / mol K. |
Std molární entropie (S | 105 J / mol K. |
Std entalpie of formace (ΔFH⦵298) | -7,007 kJ / g nebo -482,3 kJ / mol |
Gibbsova volná energie (ΔFG˚) | -389,5 kJ / mol |
Std entalpie of spalování (ΔCH⦵298) | 25,5 kJ / mol |
| Nebezpečí | |
| Hlavní nebezpečí | Oxidační, dráždivý |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | Nehořlavé |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
LD50 (střední dávka ) | 1426 mg / kg (orálně, potkan) |
| Související sloučeniny | |
jiný kationty | Dusičnan sodný Dusičnan draselný Dusičnan rubidný Dusičnan cesný |
Související sloučeniny | Síran lithný Chlorid lithný |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
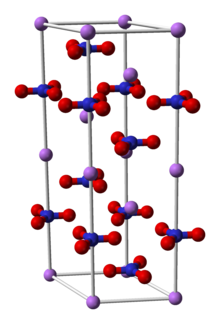
Dusičnan lithný je anorganická sloučenina se vzorcem LiNO3. To je lithium sůl z kyselina dusičná (an dusičnan alkalického kovu ). Sůl je rozmělněný absorbující vodu za vzniku hydratované formy, trihydrátu dusičnanu lithného. Jeho eutektika je zajímavá pro kapaliny pro přenos tepla.[2]
Vyrábí se ošetřením uhličitan lithný nebo hydroxid lithný s kyselina dusičná.
Použití
Tato křehká bezbarvá sůl je oxidující prostředek používaný při výrobě červeně zbarvených ohňostroj a světlice.
Tepelné skladování
The hydratovaný forma, trihydrát dusičnanu lithného, má extrémně vysokou hladinu specifické teplo fúze, 287 (± 7) J / g,[3] a proto jej lze použít pro skladování tepelné energie při jeho teplotě tavení 303,3 K.[4]
Dusičnan lithný byl navržen jako médium pro skladování tepla nashromážděného ze slunce pro vaření. A Fresnelova čočka by bylo použito k roztavení pevného dusičnanu lithného, který by pak fungoval jako „solární baterie“, což by umožnilo později distribuovat teplo konvekcí.[5]
Syntéza
Dusičnan lithný lze syntetizovat reakcí kyseliny dusičné a uhličitanu lithného.
- Li2CO3 + 2 HNO3 → 2 LiNO3 + H2O + CO2
Obecně při tvorbě LiNO3, a indikátor pH se používá k určení, kdy byla neutralizována veškerá kyselina. Tuto neutralizaci však lze rozpoznat také se ztrátou oxid uhličitý Výroba.[6] Aby se konečný produkt zbavil přebytečné vody, zahřeje se vzorek.
Toxicita
Dusičnan lithný může být při požití toxický pro tělo zaměřením na centrální nervový systém, tyroidy, ledviny a kardiovaskulární systém.[7] Pokud je dusičnan lithný vystaven pokožce, očím a sliznicím, může způsobit podráždění těchto oblastí.[8]
Další čtení
- Berchiesi, Gianfrancesco; Vitali, Giovanni; Amico, Antonio (1985). "Transportní vlastnosti binárních roztoků dusičnanu lithného a dusičnanu vápenatého v roztaveném acetamidu". Journal of Chemical & Engineering Data. 30 (2): 208–9. doi:10.1021 / je00040a023.
- Kelly, Michael T; Tuan, Christopher Y (2006). „Případová studie hodnotící použití dusičnanu lithného k zadržení alkalicko-křemičité reakce ve stávající betonové dlažbě“. Přistávací plocha letiště a dálnice. str. 625–35. doi:10.1061/40838(191)53. ISBN 978-0-7844-0838-4.
- Muniz-Miranda, Francesco; Pagliai, Marco; Cardini, Gianni; Righini, Roberto (2012). „Bifurkovaný vodíkový vazebný prostředek v trihydrátu dusičnanu lithného sondovaný ab Initio Molecular Dynamics“. The Journal of Physical Chemistry A. 116 (9): 2147–53. Bibcode:2012JPCA..116.2147M. doi:10.1021 / jp2120115. PMID 22309150.
- Ruiz, María L; Lick, Ileana D; Leguizamón Aparicio, María S; Ponzi, Marta I; Rodriguez-Castellón, Enrique; Ponzi, Esther N (2012). „ŽÁDNÝ vliv na katalytické spalování sazí: dusičnan lithný a katalyzátory zlata“. Výzkum průmyslové a inženýrské chemie. 51 (3): 1150–7. doi:10.1021 / ie201295s.
Reference
- ^ Pradyot Patnaik. Handbook of Anorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8.[stránka potřebná ]
- ^ Wietelmann, Ulrich a Bauer, Richard J. (2005) „Lithium and Lithium Compounds“ v Ullmann's Encyclopedia of Industrial Chemistry„Wiley-VCH: Weinheim. doi:10.1002 / 14356007.a15_393.
- ^ Shamberger, Patrick J; Reid, Timothy (2012). "Termofyzikální vlastnosti trihydrátu dusičnanu lithného od (253 do 353) K". Journal of Chemical & Engineering Data. 57 (5): 1404–11. doi:10.1021 / je3000469.
- ^ Kenisarin, Murat; Mahkamov, Khamid (2016). "Sůl hydratuje jako latentní teplo akumulující materiály: termofyzikální vlastnosti a náklady". Materiály pro solární energii a solární články. 145 (3): 255–86. doi:10.1016 / j.solmat.2015.10.029.
- ^ http://barbequelovers.com/grills/a-solar-grill-prototype-for-a-greener-tomorrow[úplná citace nutná ]
- ^ "Syntetická databáze: syntéza dusičnanu lithného". Síť amatérských věd. Citováno 18. června 2012.
- ^ "Arch s daty o bezpečnosti materiálu". Katalog Sigma-Aldrich. Citováno 12. dubna 2012.
- ^ "Chemický datový list". CAMEO Chemicals. Citováno 26. dubna 2012.

