Dusičnan berylnatý - Beryllium nitrate
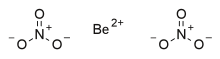 | |
| Jména | |
|---|---|
| Systematický název IUPAC Dusičnan berylnatý | |
| Ostatní jména Beryllium dinitrát | |
| Identifikátory | |
| |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.033.678 |
| Číslo ES |
|
PubChem CID | |
| UNII |
|
| UN číslo | 2464 |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| Buďte (NE3)2 | |
| Molární hmotnost | 133,02 1982 g / mol |
| Vzhled | bílá až žlutá pevná látka |
| Zápach | bez zápachu |
| Hustota | 1,56 g / cm3 |
| Bod tání | 60,5 ° C (140,9 ° F; 333,6 K) |
| Bod varu | 142 ° C (288 ° F; 415 K) (rozkládá se) |
| 166 g / 100 ml | |
| Termochemie | |
Std entalpie of formace (ΔFH⦵298) | -700,4 kJ / mol |
| Nebezpečí | |
| NIOSH (Limity expozice USA pro zdraví): | |
PEL (Dovolený) | PEL 0,002 mg / m3 C 0,005 mg / m3 (30 minut), s maximem maxima 0,025 mg / m3 (jako Be)[1] |
REL (Doporučeno) | Ca C 0,0005 mg / m3 (jako Be)[1] |
IDLH (Okamžité nebezpečí) | Ca [4 mg / m3 (jako Be)][1] |
| Související sloučeniny | |
jiný kationty | Dusičnan hořečnatý Dusičnan vápenatý Dusičnan strontnatý Dusičnan barnatý |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Dusičnan berylnatý, také známý jako beryllium dinitrát, je iontový berylium sůl z kyselina dusičná s chemický vzorec Buďte (NE3)2.[2] Každý vzorec jednotka se skládá z jednoho Be2+ kation a dva NE3− anionty.
Nebezpečí
Dusičnan berylnatý je toxická chemická látka,[2] jako všechny ostatní sloučeniny berýlia. V malých dávkách působí také dráždivě. Při hoření uvolňuje dráždivé nebo toxické výpary. Když však dojde k masivní krátkodobé expozici, akutní pneumonitida mohou nastoupit, ale příznaky se neprojeví po dobu 3 dnů.[2]
Příprava
Dusičnan berylnatý lze připravit reakcí hydroxid berylnatý v kyselina dusičná.[3]
- Být (OH)2 + 2 HNO3 → Buďte (NE3)2 + 2 H2Ó
Reference
- ^ A b C NIOSH Kapesní průvodce chemickými nebezpečími. "#0054". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ A b C „Dusičnan berylnatý (ICSC)“. IPCS INCHEM. Citováno 13. září 2010.
- ^ Walsh, Kenneth (2009). Chemie a zpracování berýlia. ASM International. s. 121–122. ISBN 978-0-87170-721-5. Citováno 3. ledna 2011.
Soli a kovalentní deriváty dusičnan ion
| Tento anorganické sloučenina –Vztahující se článek je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |
