Žloutenka typu B - Hepatitis B - Wikipedia
| Žloutenka typu B | |
|---|---|
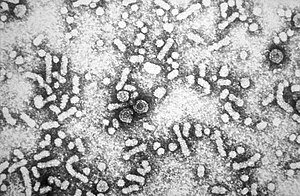 | |
| Elektronový mikrofotografie z virus hepatitidy B. | |
| Specialita | Infekční nemoc, gastroenterologie |
| Příznaky | Žádný, nažloutlá kůže, únava, tmavá moč, bolest břicha[1] |
| Komplikace | Cirhóza, rakovina jater[2] |
| Obvyklý nástup | Příznaky se mohou objevit až 6 měsíců[1] |
| Doba trvání | Krátkodobé nebo dlouhodobé[3] |
| Příčiny | Virus hepatitidy B. šíří někteří tělní tekutiny[1] |
| Rizikové faktory | Intravenózní užívání drog, pohlavní styk, dialýza, žijící s nakaženou osobou[1][4] |
| Diagnostická metoda | Krevní testy[1] |
| Prevence | Vakcína proti hepatitidě B.[1] |
| Léčba | Antivirová léčba (tenofovir, interferon ), transplantace jater[1] |
| Frekvence | > 391 milionů (2017)[5] |
| Úmrtí | 65 400 přímých (2015),> 750 000 (celkem)[1][6] |
Žloutenka typu B je infekční nemoc způsobené virus hepatitidy B. (HBV), který ovlivňuje játra;[1][7] je to typ virová hepatitida.[8] Může způsobit jak akutní, tak chronická infekce.[1] Mnoho lidí nemá během počáteční infekce žádné příznaky.[1] U akutní infekce se u některých může objevit rychlý nástup nemoci zvracením, nažloutlá kůže, únava, tmavá moč a bolest břicha.[1] Tyto příznaky často trvají několik týdnů a zřídka vede počáteční infekce k smrti.[1][9] Může trvat 30 až 180 dní, než příznaky začnou.[1] U těch, kteří se nakazí přibližně v době narození, se 90% vyvine chronicky žloutenka typu B zatímco méně než 10% infikovaných po dosažení věku pěti let ano.[4] Většina pacientů s chronickým onemocněním nemá žádné příznaky; nicméně, cirhóza a rakovina jater se může nakonec vyvinout.[2] Cirhóza nebo rakovina jater se vyskytují asi u 25% pacientů s chronickým onemocněním.[1]
Virus se přenáší vystavením infekčním látkám krev nebo tělní tekutiny.[1] Infekce v době narození nebo kontakt s krví jiných lidí během dětství je nejčastější metodou, kterou se hepatitida B získává v oblastech, kde je nemoc běžný.[1] V oblastech, kde je nemoc vzácná, intravenózní užívání drog a pohlavní styk jsou nejčastější způsoby infekce.[1] Mezi další rizikové faktory patří práce ve zdravotnictví, krevní transfuze, dialýza, žijící s infikovanou osobou, cestují do zemí, kde je vysoká míra infekce, a žijí v ústavu.[1][4] Tetování a akupunktura vedl v 80. letech k významnému počtu případů; to se však při zlepšené sterilizaci stalo méně obvyklým.[10] The žloutenka typu B viry nelze šířit držením za ruce, sdílením jídelního náčiní, líbáním, objímáním, kašláním, kýcháním nebo kojením.[4] Infekci lze diagnostikovat 30 až 60 dnů po expozici.[1] Diagnóza je obvykle potvrzena testováním krve na části viru a na protilátky proti viru.[1] Je to jeden z pěti hlavních hepatitida viry: A, B, C, D, a E.[11]
Infekci lze zabránit pomocí očkování od roku 1982.[1][12] Očkování doporučuje Světová zdravotnická organizace v první den života, pokud je to možné.[1] K plnému účinku jsou nutné další dvě nebo tři dávky později.[1] Tato vakcína funguje asi 95% času.[1] Asi 180 zemí poskytlo vakcínu v rámci národních programů od roku 2006.[13] Doporučuje se také, aby byla veškerá krev testována na hepatitidu B před transfuzí, a to kondomy být používán k prevenci infekce.[1] Během počáteční infekce je péče založena na symptomech, které člověk má.[1] U těch, u kterých se rozvine chronické onemocnění, antivirové léky jako tenofovir nebo interferon může být užitečné; tyto léky jsou však drahé.[1] Transplantace jater se někdy používá k cirhóze.[1]
Asi třetina světové populace byla nakažena v jednom okamžiku svého života.[1] Nejméně 391 milionů lidí nebo 5% světové populace mělo od roku 2017 chronickou infekci HBV.[5] Zatímco v tomto roce došlo k dalším 145 milionům případů akutní infekce HBV.[5] Více než 750 000 lidí každý rok zemře na hepatitidu B.[1] Asi 300 000 z nich je způsobeno rakovinou jater.[14] Toto onemocnění je nejčastější v regionech západního Pacifiku (6,2%) a Afriky (6,1%).[11] V Evropě jsou sazby 1,6% a v Americe 0,7%.[1] Původně byla známá jako „sérová hepatitida“.[15]
Příznaky a symptomy
Akutní infekce žloutenka typu B virus je spojován s akutním virem hepatitida, onemocnění, které začíná všeobecným zdravotním stavem, nechutenstvím, nevolností, zvracením, bolestmi těla, mírnou horečkou a tmavou močí a poté prochází vývojem žloutenka. Onemocnění trvá několik týdnů a poté se u většiny postižených lidí postupně zlepšuje. Několik lidí může mít závažnější formu onemocnění jater známou jako fulminantní selhání jater a v důsledku toho může zemřít. Infekce může být zcela bez příznaků a může být nerozpoznaná.[16]
Chronická infekce žloutenka typu B virus může být asymptomatický nebo může být spojen s chronickým zánětem jater (chronická hepatitida), který vede k cirhóza po dobu několika let. Tento typ infekce dramaticky zvyšuje výskyt hepatocelulární karcinom (HCC; rakovina jater). V celé Evropě způsobuje hepatitida B a C přibližně 50% hepatocelulárních karcinomů.[17][18] Chronickým dopravcům se doporučuje, aby se vyhýbali konzumaci alkohol protože to zvyšuje jejich riziko cirhóza a rakovina jater. Žloutenka typu B Virus byl spojen s vývojem membranózní glomerulonefritida (MGN).[19]
Příznaky mimo játra jsou přítomny u 1–10% lidí infikovaných HBV a zahrnují syndrom podobný sérové nemoci, akutní nekrotizující vaskulitida (polyarteritis nodosa ), membranózní glomerulonefritida a papulární akrodermatitida v dětství (Gianotti – Crostiho syndrom ).[20][21] Syndrom podobný sérové nemoci se vyskytuje na pozadí akutního stavu žloutenka typu B, často předcházející vzniku žloutenky.[22] Klinickými příznaky jsou horečka, vyrážka, a polyarteritida. Příznaky často ustupují krátce po nástupu žloutenky, ale mohou přetrvávat po celou dobu akutního stavu žloutenka typu B.[23] Přibližně 30–50% lidí s akutní nekrotizující vaskulitidou (polyarteritis nodosa) jsou nosiči HBV.[24] Související s HBV nefropatie byl popsán u dospělých, ale je častější u dětí.[25][26] Membranózní glomerulonefritida je nejčastější formou.[23] Jiné zprostředkované imunitou hematologické poruchy, jako jsou esenciální smíšené kryoglobulinémie a aplastická anémie byly popsány jako součást extrahepatálních projevů infekce HBV, ale jejich asociace není tak dobře definována; proto by pravděpodobně neměly být považovány za etiologicky spojené s HBV.[23]
Způsobit
Přenos
Přenos žloutenka typu B virus je výsledkem expozice infekční krvi nebo tělním tekutinám obsahujícím krev. Je 50 až 100krát infekčnější než virus lidské imunodeficience (HIV).[27] Možné formy přenosu zahrnují sexuální kontakt,[28] krevní transfuze a transfuze s jinými produkty lidské krve,[29] opětovné použití kontaminovaných jehel a stříkačky,[30] a vertikální přenos z matky na dítě (MTCT) během porodu. Bez zásahu má matka, která je pozitivní na HBsAg, 20% riziko přenosu infekce na své potomky v době narození. Toto riziko je až 90%, pokud je matka také pozitivní na HBeAg. HBV může být přenášen mezi členy rodiny v domácnostech, možná kontaktem nekontaktní pokožky nebo sliznice se sekrecemi nebo slinami obsahujícími HBV.[31] Nejméně 30% však bylo hlášeno žloutenka typu B mezi dospělými nelze spojovat s identifikovatelným rizikovým faktorem.[32] Zdá se, že kojení po správné imunoprofylaxi nepřispívá k přenosu HBV z matky na dítě (MTCT).[33] Virus může být detekován do 30 až 60 dnů po infekci a může přetrvávat a vyvinout se v chronickou hepatitidu B. Inkubační doba viru hepatitidy B je v průměru 75 dní, ale může se pohybovat od 30 do 180 dnů.[34]
Virologie
Struktura
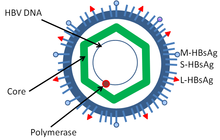
Žloutenka typu B virus (HBV) je členem rodina hepadnavirů.[35] Virová částice (virion ) se skládá z vnějšího lipid obálka a icosahedral nukleokapsid jádro složené z jádra protein. Tyto viriony mají průměr 30–42 nm. Nukleokapsid obklopuje virovou DNA a DNA polymerázu, která má reverzní transkriptáza aktivita.[36] Vnější obal obsahuje vložené proteiny, které se účastní virové vazby a vstupu do citlivých buněk. Virus je jedním z nejmenších obalených zvířecích virů. 42 nm viriony, které jsou schopné infikovat jaterní buňky známé jako hepatocyty, jsou označovány jako „Dane částice“.[37] Kromě dánských částic se v séru infikovaných jedinců nacházejí vláknitá a sférická těla bez jádra. Tyto částice nejsou infekční a jsou složeny z lipidů a bílkovin, které tvoří část povrchu virionu, který se nazývá povrchové antigeny (HBsAg ), a je produkován v přebytku během životního cyklu viru.[38]
Genom
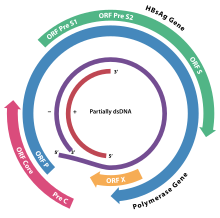
The genom HBV je vyroben z kruhu DNA, ale je to neobvyklé, protože DNA není úplně dvouvláknová. Jeden konec řetězce o celé délce je spojen s virem DNA polymeráza. Genom je 3020–3320 nukleotidy dlouhý (pro vlákno plné délky) a 1700–2800 nukleotidů dlouhý (pro vlákno krátké délky).[39] Negativní smysl (nekódující) je komplementární s virovým mRNA. Virová DNA se nachází v jádro brzy po infekci buňka. Částečně dvouvláknová DNA je plně dvojvláknová dokončena dokončením (+) sense řetězce a odstraněním protein molekula z (-) sense řetězce a krátké sekvence RNA z řetězce (+) smyslu. Nekódující báze se odstraní z konců řetězce (-) sense a konce se spojí. Existují čtyři známé geny kódované genomem, nazývané C, X, P a S. Jádrový protein je kódován genem C (HBcAg) a jeho začátek kodon předchází upstream in-frame AUG start kodon, ze kterého je produkován pre-core protein. HBeAg vyrábí společnost proteolytický zpracování pre-core proteinu. U některých vzácných kmenů viru známého jako Mutanti viru hepatitidy B prekurzorují mutanty, není přítomen HBeAg.[40]DNA polymeráza je kódován genem P. Gen S je gen, který kóduje povrch antigen (HBsAg). Gen HBsAg je jeden dlouhý otevřený čtecí rámec, ale obsahuje tři kodony „start“ (ATG) v rámci, které rozdělují gen na tři části, pre-S1, pre-S2 a S. Kvůli více startovacím kodonům polypeptidy tří různých velikostí, které se nazývají velké (pořadí od povrchu dovnitř: pre-S1, pre-S2 a S), střední (pre-S2, S) a malé (S)[41] jsou produkovány.[42] Na amino-terminálním konci preS1 části velkého (L) proteinu je myristylová skupina, která hraje důležitou roli při infekci.[43] Kromě toho mají N-konec proteinu L připojení k viru a vazebná místa pro kapsidu. Z tohoto důvodu jsou N konce poloviny molekul L proteinu umístěny mimo membránu a druhá polovina uvnitř membrány.[44]
Funkce proteinu kódovaného genem X není plně objasněna, ale je spojena s vývojem rakoviny jater. Stimuluje geny, které podporují růst buněk, a inaktivuje molekuly regulující růst.[45]
Patogeneze

Životní cyklus žloutenka typu B virus je složitý. Žloutenka typu B je jedním z mála známých pararetroviry: ne-retroviry které stále používají reverzní transkripce v procesu replikace. Virus získává vstup do buňky vazbou na NTCP[46] na povrchu a bytí endocytovaný. Protože se virus množí prostřednictvím RNA vytvořené hostitelským enzymem, musí být virová genomová DNA přenesena do buněčného jádra hostitelskými proteiny zvanými chaperony. Částečně dvouvláknová virová DNA je poté vytvořena plně dvouvláknovou pomocí virové polymerázy a transformována do kovalentně uzavřené kruhové DNA (cccDNA). Tato cccDNA slouží jako templát pro transkripci čtyř virů mRNA hostitelskou RNA polymerázou. Největší mRNA (která je delší než virový genom) se používá k vytváření nových kopií genomu ak tvorbě kapsid jádrový protein a virový DNA polymeráza. Tyto čtyři virové transkripty procházejí dalším zpracováním a dále vytvářejí potomstvo virionů, které se uvolňují z buňky nebo se vracejí do jádra a znovu se cyklují, aby se vytvořilo ještě více kopií.[42][47] Dlouhá mRNA je poté transportována zpět do cytoplazmy, kde protein virionu P (DNA polymeráza) syntetizuje DNA prostřednictvím své aktivity reverzní transkriptázy.
Sérotypy a genotypy
Virus je rozdělen do čtyř hlavních sérotypy (adr, adw, ayr, ayw) na základě antigenu epitopy prezentováno na obalových proteinech a do osmi hlavních genotypů (A – H). Genotypy mají odlišnou geografickou distribuci a používají se ke sledování vývoje a přenosu viru. Rozdíly mezi genotypy ovlivňují závažnost onemocnění, průběh a pravděpodobnost komplikací a reakci na léčbu a případně očkování.[48][49] Existují dva další genotypy I a J, ale od roku 2015 nejsou všeobecně přijímány.[50] Rozmanitost genotypů se ve světě neprojevuje stejně. Například genotypy A, D a E byly v Africe pozorovány převážně, zatímco genotypy B a C jsou v Asii pozorovány jako rozšířené.[51]
Genotypy se liší nejméně o 8% jejich sekvence a poprvé byly hlášeny v roce 1988, kdy bylo původně popsáno šest (A – F).[52] Od té doby byly popsány dva další typy (G a H).[53] Většina genotypů je nyní rozdělena na subgenotypy s odlišnými vlastnostmi.[54]
Mechanismy
Žloutenka typu B Virus primárně interferuje s funkcemi jater replikací hepatocyty. Funkční receptor je NTCP.[46] Existují důkazy, že receptor v úzce souvisí kachní virus hepatitidy B. je karboxypeptidáza D.[55][56] Viriony se vážou k hostitelské buňce přes doménu preS virového povrchového antigenu a jsou následně internalizovány endocytózou. Receptory specifické pro HBV-preS jsou exprimovány primárně na hepatocytech; virová DNA a proteiny však byly také detekovány v extrahepatálních místech, což naznačuje, že buněčné receptory pro HBV mohou také existovat na extrahepatálních buňkách.[57]
Během infekce HBV hostitel imunitní odpověď způsobuje jak hepatocelulární poškození, tak virovou clearance. I když vrozená imunitní odpověď nehraje v těchto procesech významnou roli, adaptivní imunitní odpověď, zejména specifická pro virus cytotoxické T lymfocyty (CTL), přispívá k většině poškození jater spojených s infekcí HBV. CTL eliminují infekci HBV zabíjením infikovaných buněk a produkcí antivirotik cytokiny, které se poté použijí k očištění HBV od životaschopných hepatocytů.[58] Ačkoli poškození jater je iniciováno a zprostředkováno CTL, antigen - nespecifické zánětlivé buňky může zhoršit CTL-indukovanou imunopatologii a krevní destičky aktivovaný v místě infekce může usnadnit akumulaci CTL v játrech.[59]
Diagnóza

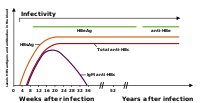
Volaly testy testy, pro detekci žloutenka typu B virová infekce zahrnuje sérum nebo krevní testy které detekují buď virové antigeny (proteiny produkované virem), nebo protilátky produkovaný hostitelem. Interpretace těchto testů je složitá.[60]
The žloutenka typu B povrchový antigen (HBsAg ) se nejčastěji používá k testování přítomnosti této infekce. Je to první detekovatelný virový antigen, který se objevil během infekce. Na počátku infekce však tento antigen nemusí být přítomen a může být nedetekovatelný později v průběhu infekce, protože je hostitelem vylučován. Infekční virion obsahuje vnitřní „jádrovou částici“ obklopující virový genom. Ikosahedrální jádrová částice je vyrobena ze 180 nebo 240 kopií jádrového proteinu, alternativně známého jako žloutenka typu B základní antigen, nebo HBcAg. Během tohoto „okna“, ve kterém hostitel zůstává infikován, ale úspěšně odstraňuje virus, IgM protilátky specifické pro žloutenka typu B základní antigen (anti-HBc IgM) může být jediným sérologickým důkazem choroby. Proto většina žloutenka typu B diagnostické panely obsahují HBsAg a celkovou anti-HBc (IgM i IgG).[61]
Krátce po objevení se HBsAg zavolal další antigen žloutenka typu B e antigen (HBeAg ) objeví se. Přítomnost HBeAg v hostitelském séru je tradičně spojena s mnohem vyšší rychlostí replikace viru a zvýšenou infekčností; varianty varianty žloutenka typu B Virus neprodukuje antigen „e“, takže toto pravidlo nemusí vždy platit.[62] Během přirozeného průběhu infekce může dojít k vyčištění HBeAg a vzniku protilátek proti antigenu „e“ (anti-HBe) vzniknou bezprostředně poté. Tato konverze je obvykle spojena s dramatickým poklesem virové replikace.

Pokud je hostitel schopen infekci odstranit, nakonec bude HBsAg nedetekovatelný a bude následován IgG protilátky proti žloutenka typu B povrchový antigen a základní antigen (anti-HBs a anti HBc IgG).[35] Čas mezi odstraněním HBsAg a výskytem anti-HBs se nazývá období okna. Osoba negativní na HBsAg, ale pozitivní na anti-HBs buď odstranila infekci, nebo byla očkována dříve.
Osoby, které zůstávají HBsAg pozitivní po dobu nejméně šesti měsíců, jsou považovány za žloutenka typu B dopravci.[63] Nositelé viru mohou mít chronickou hepatitidu B, což by se projevilo zvýšeným obsahem séra alaninaminotransferáza (ALT) a zánět jater, pokud jsou ve fázi imunitní clearance chronické infekce. Nositelé, kteří sérokonvertovali na negativní stav HBeAg, zejména ti, kteří získali infekci jako dospělí, mají velmi malé množení virů, a proto mohou být vystaveni malému riziku dlouhodobých komplikací nebo přenosu infekce na ostatní.[64] Je však možné, aby jednotlivci vstoupili do „imunitního úniku“ s HBeAg-negativní hepatitidou.

PCR byly vyvinuty testy k detekci a měření množství HBV DNA, nazývané virová zátěž v klinických vzorcích. Tyto testy se používají k hodnocení stavu infekce osoby ak monitorování léčby.[65] Jednotlivci s vysokou virové zátěže, charakteristicky mít broušené hepatocyty na biopsii.
Prevence
Vakcína
Vakcíny pro prevenci hepatitidy B se běžně doporučují pro kojence od roku 1991 ve Spojených státech.[66] První dávka se obvykle doporučuje do jednoho dne po narození.[67] Vakcína proti hepatitidě B byla první vakcínou schopnou předcházet rakovině, konkrétně rakovině jater.[68]
Většina vakcín se podává ve třech dávkách v průběhu měsíců. Ochranná reakce na vakcínu je definována jako koncentrace protilátek anti-HBs alespoň 10 mIU / ml v séru příjemce. Vakcína je účinnější u dětí a 95 procent očkovaných má ochranné hladiny protilátek. To klesá na přibližně 90% ve věku 40 let a na přibližně 75 procent u osob starších 60 let. Ochrana poskytovaná očkováním je dlouhotrvající i po poklesu hladiny protilátek pod 10 mIU / ml. U novorozenců matek pozitivních na HBsAg: samotná vakcína proti hepatitidě B, samotný imunoglobulin proti hepatitidě B nebo kombinace vakcíny plus imunoglobulin proti hepatitidě B, všechny zabraňují výskytu hepatitidy B.[69] Kromě toho je kombinace vakcíny plus imunoglobulinu proti hepatitidě B lepší než samotná vakcína.[69] Tato kombinace zabraňuje přenosu HBV v době narození v 86% až 99% případů.[70]
Tenofovir podávaný ve druhém nebo třetím trimestru může snížit riziko přenosu z matky na dítě o 77% v kombinaci s imunoglobulinem proti hepatitidě B a vakcínou proti hepatitidě B, zejména u těhotných žen s vysokými hladinami DNA viru hepatitidy B.[71] Neexistují však dostatečné důkazy o tom, že by podávání samotného imunoglobulinu proti hepatitidě B během těhotenství mohlo snížit přenosové rychlosti na novorozence.[72] Nebyla provedena randomizovaná kontrolní studie hodnotící účinky vakcíny proti hepatitidě B během těhotenství na prevenci infekce kojenců.[73]
Všichni, kteří mají riziko vystavení tělním tekutinám, jako je krev, by měli být očkováni, pokud již ne.[66] Doporučuje se testování k ověření účinné imunizace a další dávky vakcíny se podávají těm, kteří nejsou dostatečně imunizováni.[66]
V 10 až 22letých následných studiích nebyly mezi očkovanými osobami s normálním imunitním systémem žádné případy hepatitidy B. Byly zdokumentovány pouze vzácné chronické infekce.[74] Očkování se doporučuje zejména pro vysoce rizikové skupiny, včetně: zdravotnických pracovníků, osob s chronickým onemocněním selhání ledvin a muži, kteří mají sex s muži.[75][76][77]
Oba typy vakcín proti hepatitidě B, vakcína z plazmy (PDV) a rekombinantní vakcína (RV) mají podobnou účinnost při prevenci infekce jak u zdravotnických pracovníků, tak u skupin s chronickým selháním ledvin.[75][76] S jedním rozdílem zaznamenaným mezi skupinou zdravotnických pracovníků je, že RV intramuskulární cesta je významně účinnější ve srovnání s RV intradermální cestou podání.[75]
jiný
v technologie asistované reprodukce, mytí spermií u mužů s hepatitidou B není nutné zabránit přenosu, pokud partnerka nebyla účinně očkována.[78] U žen s hepatitidou B se riziko přenosu z matky na dítě s IVF neliší od rizika při spontánním početí.[78]
Osoby s vysokým rizikem infekce by měly být testovány, protože pro ty, kteří mají toto onemocnění, existuje účinná léčba.[79] Skupiny, pro které se screening doporučuje, zahrnují ty, kteří nebyli očkováni, a jednu z následujících: lidé z oblastí světa, kde se hepatitida B vyskytuje u více než 2%, lidé s HIV, uživatelé drog intravenózně, muži, kteří mají sex s muži, a ti, kteří žijí s někým s hepatitidou B.[79] Promítání během těhotenství se doporučuje ve Spojených státech.[80]
Léčba
Akutní žloutenka typu B infekce obvykle nevyžaduje léčbu a většina dospělých infekci vyléčí spontánně.[81][82] Včasnou antivirovou léčbu může vyžadovat méně než 1% lidí, jejichž infekce má velmi agresivní průběh (fulminantní hepatitida) nebo kteří jsou imunokompromitovaný. Na druhé straně může být nutné snížit riziko vzniku chronické infekce cirhóza a rakovina jater. Chronicky infikovaní jedinci s trvale zvýšeným obsahem séra alaninaminotransferáza, marker poškození jater, a hladiny HBV DNA jsou kandidáty na terapii.[83] Léčba trvá od šesti měsíců do roku, v závislosti na léčbě a genotypu.[84] Délka léčby, pokud se lék užívá ústy, je však variabilnější a obvykle delší než jeden rok.[85]
Ačkoli žádný z dostupných léků nedokáže infekci odstranit, může zastavit replikaci viru, čímž minimalizuje poškození jater. Jak 2018, existuje osm léků licencovaných pro léčbu žloutenka typu B infekce ve Spojených státech. Tyto zahrnují antivirový léky lamivudin, adefovir, tenofovir-disoproxil, tenofovir alafenamid, telbivudin, a entekavir a dva imunitní systém modulátory interferon alfa-2a a PEGylovaný interferon alfa-2a. V roce 2015 doporučila Světová zdravotnická organizace jako látky první linie tenofovir nebo entekavir.[86] Pacienti se současnou cirhózou nejvíce potřebují léčbu.[86]
Použití interferonu, které vyžaduje injekce denně nebo třikrát týdně, bylo nahrazeno dlouhodobým účinkem PEGylovaný interferon, který se injektuje pouze jednou týdně.[87] U některých jedinců je však mnohem větší pravděpodobnost, že odpoví, než u jiných, a to může být způsobeno tím, že genotyp infikujícího viru nebo dědičnosti dané osoby. Léčba snižuje virovou replikaci v játrech, čímž snižuje virová zátěž (množství virových částic měřené v krvi).[88] Odpověď na léčbu se u jednotlivých genotypů liší. Interferon Ošetření může vést k rychlosti sérokonverze e antigenu 37% u genotypu A, ale pouze 6% sérokonverze u typu D. Genotyp B má podobné rychlosti sérokonverze jako u typu A, zatímco sérokonverze typu C pouze u 15% případů. Trvalá ztráta e antigenu po léčbě je ~ 45% u typů A a B, ale pouze 25–30% u typů C a D.[89]
Prognóza

| žádná data <10 10–20 20–40 40–60 60–80 80–100 | 100–125 125–150 150–200 200–250 250–500 >500 |
Žloutenka typu B virová infekce může být buď akutní (samolimitující), nebo chronická (dlouhodobá). Osoby se samolimitující infekcí infekci samy vymizí během několika týdnů až měsíců.
U dětí je infekce méně pravděpodobná než u dospělých. Více než 95% lidí, kteří se nakazí jako dospělí nebo starší děti, dosáhne úplného uzdravení a vytvoří ochrannou imunitu proti viru. U mladších dětí to však klesne na 30% a infekci vyléčí pouze 5% novorozenců, kteří infekci získají od své matky při narození.[90] Tato populace má 40% celoživotní riziko úmrtí cirhóza nebo hepatocelulární karcinom.[87] Z infikovaných ve věku od jednoho do šesti let 70% infekci vyléčí.[91]
Hepatitida D (HDV) může nastat pouze při současném užívání žloutenka typu B infekce, protože HDV používá povrchový antigen HBV k vytvoření a kapsid.[92] Souběžná infekce s hepatitidou D zvyšuje riziko cirhózy jater a rakoviny jater.[93] Polyarteritis nodosa je častější u lidí s žloutenka typu B infekce.
Cirhóza
K určení stupně přítomné cirhózy je k dispozici řada různých testů. Přechodná elastografie (FibroScan) je test volby, ale je drahý.[86] Index poměru aspartátaminotransferázy k destičkám lze použít, když je problém s cenou.[86]
Reaktivace
Žloutenka typu B DNA viru zůstává v těle po infekci a u některých lidí, včetně těch, kteří nemají detekovatelný HBsAg, se onemocnění opakuje.[94][95] I když je reaktivace vzácná, nejčastěji se vyskytuje po užívání alkoholu nebo drog,[96] nebo u lidí se sníženou imunitou.[97] HBV prochází cykly replikace a nereplikace. Přibližně u 50% zjevných nosičů dochází k akutní reaktivaci. U mužů s výchozí hodnotou ALT 200 UL / L je třikrát vyšší pravděpodobnost reaktivace než u lidí s nižšími hladinami. I když k reaktivaci může dojít spontánně,[98] lidé, kteří podstoupí chemoterapie mít vyšší riziko.[99] Imunosupresivní léky upřednostňují zvýšenou replikaci HBV při inhibici cytotoxické T buňky funkce v játrech.[100] Riziko reaktivace se liší v závislosti na sérologickém profilu; pacienti s detekovatelným HBsAg v krvi jsou vystaveni největšímu riziku, ale pacienti s pouze protilátkami proti základnímu antigenu jsou také ohroženi. Přítomnost protilátek proti povrchovému antigenu, které jsou považovány za marker imunity, nevylučuje reaktivaci.[99] Léčba profylaktickými antivirotiky může zabránit závažné morbiditě spojené s reaktivací onemocnění HBV.[99]
Epidemiologie


Nejméně 391 milionů lidí nebo 5% světové populace mělo od roku 2017 chronickou infekci HBV.[5] Zatímco v tomto roce došlo k dalším 145 milionům případů akutní infekce HBV.[5] Regionální prevalence se pohybuje od přibližně 6% v Africe po 0,7% v Americe.[102]
Mezi způsoby infekce patří vertikální přenos (například porodem), horizontální přenos v raném věku (kousnutí, léze a hygienické návyky) a horizontální přenos v dospělosti (sexuální kontakt, intravenózní užívání drog).[103]
Primární metoda přenosu odráží prevalenci chronické infekce HBV v dané oblasti. V oblastech s nízkou prevalencí, jako jsou kontinentální Spojené státy a západní Evropa, je primární metodou zneužívání injekčních drog a nechráněný sex, i když mohou být důležité i další faktory.[104] V oblastech s mírnou prevalencí, které zahrnují východní Evropu, Rusko a Japonsko, kde jsou chronicky infikovány 2–7% populace, se nemoc šíří převážně mezi dětmi. V oblastech s vysokou prevalencí, jako je Čína a jihovýchodní Asie je nejčastější přenos během porodu, ačkoli v jiných oblastech s vysokou endemicitou, jako je Afrika, je přenos v dětství významným faktorem.[105] Prevalence chronické infekce HBV v oblastech s vysokou endemicitou je nejméně 8%, s prevalencí 10–15% v Africe / na Dálném východě.[106] Od roku 2010 má Čína 120 milionů infikovaných lidí, následuje Indie a Indonésie se 40 miliony, respektive 12 milionů. Podle Světová zdravotnická organizace (WHO), odhaduje se, že každý rok na tuto infekci zemře 600 000 lidí.[107]
Ve Spojených státech došlo v roce 2011 k přibližně 19 000 novým případům, což je téměř 90% pokles od roku 1990.[66]
Dějiny
Virus hepatitidy B infikoval člověka, protože přinejmenším Doba bronzová.[108][109] Důkazy byly získány od 4 500 let starých lidských ostatků.[109] Podle studie z roku 2018 je virová genomy získané sekvenování brokovnice se stal nejstarším, který se kdy získal ze vzorků obratlovců.[109] Bylo také zjištěno, že některé starověké hepatitidy virové kmeny stále infikují lidi, zatímco ostatní vyhynuli.[109] To vyvrátilo přesvědčení, že hepatitida B pocházela z Nového světa a rozšířila se do Evropy kolem 16. století.[109] Další studie pozůstatků a. Z roku 2018 mumifikovaný dítě nalezeno v bazilice v San Domenico Maggiore v Neapoli dospěl k závěru, že dítě, které žilo v 16. století, mělo formu HBV a že virus úzce souvisí s moderními variantami.[110] Genomické studie však potvrzují starší původ u lidí. Konkrétní subgenotyp hepatitidy B C4 je přítomen v australských domorodcích a nikde jinde v jihovýchodní Asii, což naznačuje starověký původ starý až 50 000 let.[111][112] Další studie potvrdily, že virus byl přítomen u lidí před 40 000 lety a šířil se společně s nimi.[113]
Nejstarší záznam o epidemii způsobené žloutenka typu B virus vytvořil Lurman v roce 1885.[114] Vypuknutí neštovice došlo v Brémy v roce 1883 a 1 289 zaměstnanců loděnice očkovaný s lymfy od ostatních lidí. Po několika týdnech a až o osm měsíců později onemocnělo 191 očkovaných pracovníků žloutenka a bylo jim diagnostikováno, že trpí sérovou hepatitidou. Ostatní zaměstnanci, kteří byli naočkováni různými dávkami lymfy, zůstali zdraví. Lurmanova práce, nyní považovaná za klasický příklad epidemiologické studie prokázala, že zdrojem ohniska byla kontaminovaná lymfa. Později bylo po zavedení, v roce 1909, hlášeno mnoho podobných ohnisek injekční jehly které byly použity, a co je důležitější, znovu použity pro podávání Salvarsan pro léčbu syfilis.
Největší epidemií hepatitidy B v historii byla infekce 330 000 amerických vojáků v letech 1941 až 1942, která způsobila u 50 000 žloutenku.[115] To bylo veřejnosti odhaleno až v roce 1987 a bylo to sledováno americkým úřadem pro veřejné zdraví ke kontaminované vakcíně proti žluté zimnici vyrobené z lidského séra chronického nosiče. Kontaminovaná vakcína proti žluté zimnici byla vyvinuta Eugenem Haagenem na výzkumném stipendiu Rockefellerovy nadace v New Yorku v roce 1937.[116] Hagen by se stal předním virologem v nacistickém Německu. Výzkum americké epidemie a modelu onemocnění hepatitidou B byl prováděn tajně, aby nedocházelo ke skandálům, a vyvinul se v tajný závod studené války se Sovětským svazem, který měl vyřešit problém kontaminace virem hepatitidy B vakcínou proti žluté zimnici. Počínaje rokem 1942, Dr. Jonas Salk a Dr. W. Paul Havens, Jr. provedli řadu neetických experimentů na vězních a psychiatrických zařízeních, kteří je záměrně vystavili hepatitidě, což jim umožnilo odlišit hepatitidu A od hepatitidy B.[117] Nacističtí lékaři včetně Hagen současně přinutili vězně z koncentračních táborů (včetně dětí) k jídlu vyškrábaného ze žaludku u lidí, kteří zežloutli z jaterního onemocnění, které zjistili, neměli hepatitidu A. Když byli vězni následně nemocní žloutenkou lékaři zjistili, že se jedná o nového infekčního agens.[118][119]
Virus byl veřejně objeven až v roce 1966 Baruch Blumberg, poté pracoval v Národní institut zdraví (NIH), objevil Antigen Austrálie (později známý jako žloutenka typu B povrchový antigen nebo HBsAg) v krvi domorodých Australanů.[120] Ačkoli byl virus podezřelý od výzkumu publikovaného Frederickem MacCallumem v roce 1947,[121] David Dane a další objevili virovou částici v roce 1970 elektronová mikroskopie.[122] V roce 1971 vydal FDA vůbec první příkaz k prověření přívodu krve do krevních bank.[123] Na začátku 80. let genom viru bylo sekvenováno.[124] Během Richarda NixonaVálka proti rakovině „(1971–1980) bylo poskytnuto obrovské množství finančních prostředků na neúspěšný program proti virům a rakovině a během této doby bylo vynaloženo značné úsilí na stanovení role hepatitidy B u rakoviny jater. Ačkoli se o hypotéze o viru a rakovině široce věří zdravotnického zařízení, nebylo nikdy prokázáno.[125]
V roce 1973 Dr. Wolfgang Szmusness Polský / židovský emigrant ze Sovětského svazu (s příběhem, který může být propagandou studené války) spolupracoval s Dr. Saulem Krugmanem z New York University na vývoji vakcíny. To nejprve otestoval Krugman na bezpečnosti u mentálně retardovaných dětí v nemocnici Willowbrook v Staten Island, což později ukázalo vyšetřování jako častý účastník pochybných lékařských studií. Dr. Szmuness spolupracovala s projektem Gay Men's Health Project, mizernou charitou ve čtvrti Meatpacking na Manhattanu, a bylo zjištěno, že bylo odhaleno až 50% homosexuálních mužů ve vysoce promiskuitních „gay ghettech“ z doby po Stonewallově éře na hepatitidu B.[126] Takoví „zrychlení“ homosexuálové vytvořili dokonalou testovací populaci pro důsledně navržený pokus o účinnost vakcíny a byla přijata politika veřejného zdraví s cílem usnadnit experiment s vakcínami zahrnující 10 000 homosexuálů (vytvoření prostředí, kde je pravděpodobný sexuální přenos mezi účastníky) , takové nevymáhání stávajících zdravotních kodexů v zařízeních, jako je newyorský klub Mineshaft, tolerování rozsáhlého užívání afrodiziakálních drog a zastavení policejních razií.[127] [128]Studie s vakcínami se opakovala také v gay komunitách v San Francisku, Los Angeles, Denveru, St. Louis a Chicagu.[129] Vakcína byla schválena v roce 1981 a studie drží rekord v nejrychlejší vakcíně, která bude vyvinuta od identifikace patogenu tradičními prostředky po schválení vakcíny založené na dvojitě zaslepené placebem kontrolované studii.[130]
Počáteční prodej vakcín byl velmi pomalý: Americká veteránská správa očekávala, že svým zaměstnancům rozdá 90 000 dávek, ale pouze 30 000 dávek bylo přijato zdravotnickými pracovníky, kteří jsou hlavní rizikovou skupinou pro expozici na pracovišti (jehly atd.).[131] The vaccine was produced from serum of homosexual chronic HBV carriers, and Dr. John Finkbeiner in January 1983 warned it "might be contaminated with a pathogen responsible for the acquired immune deficiency syndrome (AIDS) epidemic."[132] Others believed the vaccine could contribute to AIDS. In 1986, research began on a second generation of vaccines that do not use human serum, and the first vaccine was discontinued in 1990.[123]
Společnost a kultura
Světový den hepatitidy, observed 28 July, aims to raise global awareness of žloutenka typu B a hepatitida C. and encourage prevention, diagnosis, and treatment. It has been led by the World Hepatitis Alliance since 2007 and in May 2010, it received global endorsement from the Světová zdravotnická organizace.[133]
Viz také
Reference
- ^ A b C d E F G h i j k l m n Ó p q r s t u proti w X y z aa ab ac inzerát ae af "Hepatitis B Fact sheet N°204". kdo. v. Červenec 2014. Archivováno from the original on 9 November 2014. Citováno 4. listopadu 2014.
- ^ A b Chang MH (June 2007). "Hepatitis B virus infection". Semin Fetal Neonatal Med. 12 (3): 160–167. doi:10.1016/j.siny.2007.01.013. PMID 17336170.
- ^ GBD 2015 Incidence a prevalence nemocí a úrazů, spolupracovníci. (8. října 2016). „Globální, regionální a národní výskyt, prevalence a roky prožité se zdravotním postižením pro 310 nemocí a úrazů, 1990–2015: systematická analýza studie Global Burden of Disease Study 2015“. Lanceta. 388 (10053): 1545–1602. doi:10.1016 / S0140-6736 (16) 31678-6. PMC 5055577. PMID 27733282.
- ^ A b C d "Hepatitis B FAQs for the Public – Transmission". NÁS. Centra pro kontrolu a prevenci nemocí (CDC). Archivováno from the original on 11 December 2011. Citováno 29. listopadu 2011.
- ^ A b C d E GBD 2017 Disease and Injury Incidence and Prevalence, Collaborators. (10 November 2018). "Global, regional, and national incidence, prevalence, and years lived with disability for 354 diseases and injuries for 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017". Lanceta. 392 (10159): 1789–1858. doi:10.1016/S0140-6736(18)32279-7. PMC 6227754. PMID 30496104.
- ^ GBD 2015 Úmrtnost a příčiny smrti, spolupracovníci. (8. října 2016). „Globální, regionální a národní naděje dožití, úmrtnost ze všech příčin a specifická úmrtnost pro 249 příčin úmrtí, 1980–2015: systematická analýza studie Global Burden of Disease Study 2015“. Lanceta. 388 (10053): 1459–1544. doi:10.1016 / S0140-6736 (16) 31012-1. PMC 5388903. PMID 27733281.
- ^ Logan CM, Rice MK (1987). Logan's Medical and Scientific Abbreviations. J. B. Lippincott and Company. str.232. ISBN 0-397-54589-4.
- ^ "Hepatitis MedlinePlus". Americká národní lékařská knihovna. Citováno 19. června 2020.
- ^ Rubin R, Strayer DS (2008). Rubin's Pathology : clinicopathologic foundations of medicine (5. vydání). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. p. 638. ISBN 9780781795166.
- ^ Thomas HC (2013). Viral Hepatitis (4. vydání). Hoboken: Wiley. p. 83. ISBN 9781118637302.
- ^ A b Global hepatitis report 2017 (PDF). SZO. 2017. ISBN 978-92-4-156545-5.
- ^ Pungpapong S, Kim WR, Poterucha JJ (2007). "Natural History of Hepatitis B Virus Infection: an Update for Clinicians". Mayo Clinic Proceedings. 82 (8): 967–975. doi:10.4065/82.8.967. PMID 17673066.
- ^ Williams R (2006). "Global challenges in liver disease". Hepatologie. 44 (3): 521–526. doi:10.1002/hep.21347. PMID 16941687. S2CID 23924901.
- ^ GBD 2013 Mortality and Causes of Death, Collaborators (17 December 2014). „Globální, regionální a národní věková pohlaví specifická úmrtnost ze všech příčin a příčin specifická pro 240 příčin úmrtí, 1990–2013: systematická analýza studie Global Burden of Disease Study 2013“. Lanceta. 385 (9963): 117–71. doi:10.1016 / S0140-6736 (14) 61682-2. PMC 4340604. PMID 25530442.
- ^ Barker LF, Shulman NR, Murray R, Hirschman RJ, Ratner F, Diefenbach WC, Geller HM (1996). "Transmission of serum hepatitis. 1970". Journal of the American Medical Association. 276 (10): 841–844. doi:10.1001/jama.276.10.841. PMID 8769597.
- ^ Terrault N, Roche B, Samuel D (July 2005). "Management of the hepatitis B virus in the liver transplantation setting: a European and an American perspective". Transplantace jater. 11 (7): 716–32. doi:10.1002/lt.20492. PMID 15973718. S2CID 19746065.
- ^ El-Serag HB, Rudolph KL (June 2007). "Hepatocellular carcinoma: epidemiology and molecular carcinogenesis". Gastroenterologie. 132 (7): 2557–76. doi:10.1053/j.gastro.2007.04.061. PMID 17570226.
- ^ El-Serag HB (22 September 2011). "Hepatocellular carcinoma". New England Journal of Medicine. 365 (12): 1118–27. doi:10.1056/NEJMra1001683. PMID 21992124.
- ^ Gan SI, Devlin SM, Scott-Douglas NW, Burak KW (October 2005). "Lamivudine for the treatment of membranous glomerulopathy secondary to chronic hepatitis B infection". Canadian Journal of Gastroenterology. 19 (10): 625–9. doi:10.1155/2005/378587. PMID 16247526.
- ^ Dienstag JL (February 1981). "Hepatitis B as an immune complex disease". Semináře o onemocnění jater. 1 (1): 45–57. doi:10.1055/s-2008-1063929. PMID 6126007.
- ^ Trepo C, Guillevin L (May 2001). "Polyarteritis nodosa and extrahepatic manifestations of HBV infection: the case against autoimmune intervention in pathogenesis". Časopis autoimunity. 16 (3): 269–74. doi:10.1006/jaut.2000.0502. PMID 11334492.
- ^ Alpert E, Isselbacher KJ, Schur PH (July 1971). "The pathogenesis of arthritis associated with viral hepatitis. Complement-component studies". The New England Journal of Medicine. 285 (4): 185–9. doi:10.1056/NEJM197107222850401. PMID 4996611.
- ^ A b C Liang TJ (May 2009). "Hepatitis B: the virus and disease". Hepatologie. 49 (5 Suppl): S13–21. doi:10.1002/hep.22881. PMC 2809016. PMID 19399811.
- ^ Gocke DJ, Hsu K, Morgan C, Bombardieri S, Lockshin M, Christian CL (December 1970). "Association between polyarteritis and Australia antigen". Lanceta. 2 (7684): 1149–53. doi:10.1016/S0140-6736(70)90339-9. PMID 4098431.
- ^ Lai KN, Li PK, Lui SF, Au TC, Tam JS, Tong KL, Lai FM (May 1991). "Membranous nephropathy related to hepatitis B virus in adults". The New England Journal of Medicine. 324 (21): 1457–63. doi:10.1056/NEJM199105233242103. PMID 2023605.
- ^ Takekoshi Y, Tanaka M, Shida N, Satake Y, Saheki Y, Matsumoto S (November 1978). "Strong association between membranous nephropathy and hepatitis-B surface antigenaemia in Japanese children". Lanceta. 2 (8099): 1065–8. doi:10.1016/S0140-6736(78)91801-9. PMID 82085. S2CID 28633855.
- ^ "Hepatitis B FAQs for the Public". Centra pro kontrolu a prevenci nemocí. Archivováno z původního dne 20. srpna 2015. Citováno 24. srpna 2015.
- ^ Fairley CK, Read TR (February 2012). "Vaccination against sexually transmitted infections". Aktuální názor na infekční nemoci. 25 (1): 66–72. doi:10.1097/QCO.0b013e32834e9aeb. PMID 22143117. S2CID 13524636.
- ^ Buddeberg F, Schimmer BB, Spahn DR (September 2008). "Transfusion-transmissible infections and transfusion-related immunomodulation" (PDF). Osvědčené postupy a výzkum. Clinical Anaesthesiology. 22 (3): 503–17. doi:10.1016/j.bpa.2008.05.003. PMID 18831300.
- ^ Hughes RA (March 2000). "Drug injectors and the cleaning of needles and syringes". Evropský výzkum závislostí. 6 (1): 20–30. doi:10.1159/000019005. PMID 10729739. S2CID 45638523.
- ^ "Hepatitis B – the facts: IDEAS –Victorian Government Health Information, Australia". Stát Victoria. 28. července 2009. Archivováno z původního dne 18. září 2011. Citováno 19. září 2009.
- ^ Shapiro CN (May 1993). "Epidemiology of hepatitis B". Pediatr. Infikovat. Dis. J. 12 (5): 433–437. doi:10.1097/00006454-199305000-00036. PMID 8392167.
- ^ Shi Z, Yang Y, Wang H, Ma L, Schreiber A, Li X, Sun W, Zhao X, Yang X, Zhang L, Lu W, Teng J, An Y (2011). "Breastfeeding of Newborns by Mothers Carrying Hepatitis B Virus: A Meta-analysis and Systematic Review". Archives of Pediatrics and Adolescent Medicine. 165 (9): 837–846. doi:10.1001/archpediatrics.2011.72. PMID 21536948.
- ^ WHO | Žloutenka typu B Archivováno 9 November 2014 at the Wayback Machine
- ^ A b Zuckerman AJ (1996). „Viry hepatitidy“. In Baron S, et al. (eds.). Baronova lékařská mikrobiologie (4. vydání). University of Texas Medical Branch. ISBN 978-0-9631172-1-2. Archivováno from the original on 14 July 2009.
- ^ Locarnini S (2004). "Molecular Virology of Hepatitis B Virus". Semináře o onemocnění jater. 24: 3–10. CiteSeerX 10.1.1.618.7033. doi:10.1055/s-2004-828672. PMID 15192795.
- ^ Harrison T (2009). Desk Encyclopedia of General Virology. Boston: Academic Press. p.455. ISBN 978-0-12-375146-1.
- ^ Howard CR (1986). "The Biology of Hepadnaviruses". Journal of General Virology. 67 (7): 1215–1235. doi:10.1099/0022-1317-67-7-1215. PMID 3014045.
- ^ Kay A, Zoulim F (2007). "Hepatitis B virus genetic variability and evolution" (PDF). Virový výzkum. 127 (2): 164–176. doi:10.1016/j.virusres.2007.02.021. PMID 17383765.
- ^ Buti M, Rodriguez-Frias F, Jardi R, Esteban R (December 2005). "Hepatitis B virus genome variability and disease progression: the impact of pre-core mutants and HBV genotypes". Journal of Clinical Virology. 34 Suppl 1: S79–82. doi:10.1016/s1386-6532(05)80015-0. PMID 16461229.
- ^ Glebe D, Urban S (January 2007). "Viral and cellular determinants involved in hepadnaviral entry". World Journal of Gastroenterology. 13 (1): 22–38. doi:10.3748/wjg.v13.i1.22. PMC 4065874. PMID 17206752.
- ^ A b Beck J, Nassal M (January 2007). "Hepatitis B virus replication". World Journal of Gastroenterology. 13 (1): 48–64. doi:10.3748/wjg.v13.i1.48. PMC 4065876. PMID 17206754.
- ^ Watashi K, Wakita T (August 2015). "Hepatitis B Virus and Hepatitis D Virus Entry, Species Specificity, and Tissue Tropism". Perspektivy Cold Spring Harbor v medicíně. 5 (8): a021378. doi:10.1101/cshperspect.a021378. PMC 4526719. PMID 26238794.
- ^ Carter J (2013). Virology : principles and applications. Saunders, Venetia. Hoboken, N.J .: Wiley. ISBN 978-1-118-62979-6. OCLC 865013042.
- ^ Li W, Miao X, Qi Z, Zeng W, Liang J, Liang Z (2010). "Hepatitis B virus X protein upregulates HSP90alpha expression via activation of c-Myc in human hepatocarcinoma cell line, HepG2". Virol. J. 7: 45. doi:10.1186/1743-422X-7-45. PMC 2841080. PMID 20170530.
- ^ A b Yan H, Zhong G, Xu G, He W, Jing Z, Gao Z, Huang Y, Qi Y, Peng B, Wang H, Fu L, Song M, Chen P, Gao W, Ren B, Sun Y, Cai T, Feng X, Sui J, Li W (2012). "Sodium taurocholate cotransporting polypeptide is a functional receptor for human hepatitis B and D virus". eLife. 1: e00049. doi:10.7554/eLife.00049. PMC 3485615. PMID 23150796.
- ^ Bruss V (January 2007). "Hepatitis B virus morphogenesis". Svět J. Gastroenterol. 13 (1): 65–73. doi:10.3748/wjg.v13.i1.65. PMC 4065877. PMID 17206755.
- ^ Kramvis A, Kew M, François G (March 2005). "Hepatitis B virus genotypes". Vakcína. 23 (19): 2409–23. doi:10.1016/j.vaccine.2004.10.045. PMID 15752827.
- ^ Magnius LO, Norder H (1995). "Subtypes, genotypes and molecular epidemiology of the hepatitis B virus as reflected by sequence variability of the S-gene". Intervirologie. 38 (1–2): 24–34. doi:10.1159/000150411. PMID 8666521.
- ^ Araujo, NM (December 2015). "Hepatitis B virus intergenotypic recombinants worldwide: An overview". Infekce, genetika a evoluce. 36: 500–10. doi:10.1016/j.meegid.2015.08.024. PMID 26299884.
- ^ Mohsen RT, Al-azzawi RH, Ad'hiah AH (2019). "Hepatitis B virus genotypes among chronic hepatitis B patients from Baghdad, Iraq and their impact on liver function". Gene Reports. 17: 100548. doi:10.1016/j.genrep.2019.100548.
- ^ Norder H, Couroucé AM, Magnius LO (1994). "Complete genomes, phylogenic relatedness and structural proteins of six strains of the hepatitis B virus, four of which represent two new genotypes". Virologie. 198 (2): 489–503. doi:10.1006/viro.1994.1060. PMID 8291231.
- ^ Shibayama T, Masuda G, Ajisawa A, Hiruma K, Tsuda F, Nishizawa T, Takahashi M, Okamoto H (May 2005). "Characterization of seven genotypes (A to E, G and H) of hepatitis B virus recovered from Japanese patients infected with human immunodeficiency virus type 1". Journal of Medical Virology. 76 (1): 24–32. doi:10.1002/jmv.20319. PMID 15779062. S2CID 25288772.
- ^ Schaefer S (January 2007). "Hepatitis B virus taxonomy and hepatitis B virus genotypes". World Journal of Gastroenterology. 13 (1): 14–21. doi:10.3748/wjg.v13.i1.14. PMC 4065870. PMID 17206751.
- ^ Tong S, Li J, Wands JR (1999). "Carboxypeptidase D is an avian hepatitis B virus receptor". Journal of Virology. 73 (10): 8696–8702. doi:10.1128/JVI.73.10.8696-8702.1999. PMC 112890. PMID 10482623.
- ^ Glebe D, Urban S (January 2007). "Viral and cellular determinants involved in hepadnaviral entry". Svět J. Gastroenterol. 13 (1): 22–38. doi:10.3748/wjg.v13.i1.22. PMC 4065874. PMID 17206752.
- ^ Coffin CS, Mulrooney-Cousins PM, van Marle G, Roberts JP, Michalak TI, Terrault NA (April 2011). "Hepatitis B virus (HBV) quasispecies in hepatic and extrahepatic viral reservoirs in liver transplant recipients on prophylactic therapy". Játra Transpl. 17 (8): 955–62. doi:10.1002/lt.22312. PMID 21462295. S2CID 206211853.
- ^ Iannacone M, Sitia G, Ruggeri ZM, Guidotti LG (2007). "HBV pathogenesis in animal models: Recent advances on the role of platelets". Journal of Hepatology. 46 (4): 719–726. doi:10.1016/j.jhep.2007.01.007. PMC 1892635. PMID 17316876.
- ^ Iannacone M, Sitia G, Isogawa M, Marchese P, Castro MG, Lowenstein PR, Chisari FV, Ruggeri ZM, Guidotti LG (November 2005). "Platelets mediate cytotoxic T lymphocyte-induced liver damage". Nat. Med. 11 (11): 1167–9. doi:10.1038/nm1317. PMC 2908083. PMID 16258538.
- ^ Bonino F, Chiaberge E, Maran E, Piantino P (1987). "Serological markers of HBV infectivity". Ann. Ist. Super. Sanità. 24 (2): 217–23. PMID 3331068.
- ^ Karayiannis P, Thomas HC (2009). Mahy BW, van Regenmortel MH (eds.). Desk Encyclopedia of Human and Medical Virology. Boston: Academic Press. p.110. ISBN 978-0-12-375147-8.
- ^ Liaw YF, Brunetto MR, Hadziyannis S (2010). "The natural history of chronic HBV infection and geographical differences". Antivirová terapie. 15: 25–33. doi:10.3851/IMP1621. PMID 21041901.
- ^ Lok AS, McMahon BJ (February 2007). "Chronic hepatitis B". Hepatologie. 45 (2): 507–39. doi:10.1002/hep.21513. hdl:2027.42/55941. PMID 17256718. S2CID 8713169.
- ^ Chu CM, Liaw YF (November 2007). "Predictive factors for reactivation of hepatitis B following hepatitis B e antigen seroconversion in chronic hepatitis B". Gastroenterologie. 133 (5): 1458–65. doi:10.1053/j.gastro.2007.08.039. PMID 17935720.
- ^ Zoulim F (November 2006). "New nucleic acid diagnostic tests in viral hepatitis". Semin. Liver Dis. 26 (4): 309–317. doi:10.1055/s-2006-951602. PMID 17051445.
- ^ A b C d Schillie S, Murphy TV, Sawyer M, Ly K, Hughes E, Jiles R, et al. (Prosinec 2013). "CDC guidance for evaluating health-care personnel for hepatitis B virus protection and for administering postexposure management". MMWR. Recommendations and Reports. 62 (RR-10): 1–19. PMID 24352112. Archivováno from the original on 19 June 2017.
- ^ COMMITTEE ON INFECTIOUS DISEASES; COMMITTEE ON FETUS AND NEWBORN (September 2017). "Elimination of Perinatal Hepatitis B: Providing the First Vaccine Dose Within 24 Hours of Birth". Pediatrie. 140 (3): e20171870. doi:10.1542/peds.2017-1870. PMID 28847980.
- ^ Chan SL, Wong VW, Qin S, Chan HL (January 2016). "Infection and Cancer: The Case of Hepatitis B". Journal of Clinical Oncology. 34 (1): 83–90. doi:10.1200/JCO.2015.61.5724. PMID 26578611.
- ^ A b Lee C, Gong Y, Brok J, Boxall EH, Gluud C (April 2006). "Hepatitis B immunisation for newborn infants of hepatitis B surface antigen-positive mothers". Cochrane Database of Systematic Reviews (2): CD004790. doi:10.1002/14651858.CD004790.pub2. PMID 16625613.
- ^ Wong F, Pai R, Van Schalkwyk J, Yoshida EM (2014). "Hepatitis B in pregnancy: a concise review of neonatal vertical transmission and antiviral prophylaxis". Annals of Hepatology. 13 (2): 187–95. doi:10.1016/S1665-2681(19)30881-6. PMID 24552860.
- ^ Hyun MH, Lee YS, Kim JH, Je JH, Yoo YJ, Yeon JE, Byun KS (June 2017). "Systematic review with meta-analysis: the efficacy and safety of tenofovir to prevent mother-to-child transmission of hepatitis B virus". Alimentární farmakologie a terapeutika. 45 (12): 1493–1505. doi:10.1111/apt.14068. PMID 28436552. S2CID 23620357.
- ^ Eke AC, Eleje GU, Eke UA, Xia Y, Liu J (February 2017). "Hepatitis B immunoglobulin during pregnancy for prevention of mother-to-child transmission of hepatitis B virus". Cochrane Database of Systematic Reviews. 2: CD008545. doi:10.1002/14651858.CD008545.pub2. PMC 6464495. PMID 28188612.
- ^ Sangkomkamhang US, Lumbiganon P, Laopaiboon M (November 2014). "Hepatitis B vaccination during pregnancy for preventing infant infection". Cochrane Database of Systematic Reviews (11): CD007879. doi:10.1002/14651858.CD007879.pub3. PMC 7185858. PMID 25385500.
- ^ Shepard CW, Simard EP, Finelli L, Fiore AE, Bell BP (2006). "Hepatitis B virus infection: epidemiology and vaccination". Epidemiologické recenze. 28: 112–25. doi:10.1093/epirev/mxj009. PMID 16754644.
- ^ A b C Chen W, Gluud C (October 2005). "Vaccines for preventing hepatitis B in health-care workers". Cochrane Database of Systematic Reviews (4): CD000100. doi:10.1002/14651858.CD000100.pub3. PMID 16235273.
- ^ A b Schroth RJ, Hitchon CA, Uhanova J, Noreddin A, Taback SP, Moffatt ME, Zacharias JM (19 July 2004). "Hepatitis B vaccination for patients with chronic renal failure". Cochrane Database of Systematic Reviews (3): CD003775. doi:10.1002/14651858.CD003775.pub2. PMID 15266500.
- ^ "Men Who Have Sex with Men | Populations and Settings | Division of Viral Hepatitis | CDC". www.cdc.gov. 31. května 2015. Citováno 13. prosince 2017.
- ^ A b Lutgens SP, Nelissen EC, van Loo IH, Koek GH, Derhaag JG, Dunselman GA (22 July 2009). "To do or not to do: IVF and ICSI in chronic hepatitis B virus carriers". Lidská reprodukce. 24 (11): 2676–8. doi:10.1093/humrep/dep258. PMID 19625309.
- ^ A b LeFevre ML (July 2014). "Screening for hepatitis B virus infection in nonpregnant adolescents and adults: U.S. Preventive Services Task Force recommendation statement". Annals of Internal Medicine. 161 (1): 58–66. doi:10.7326/M14-1018. PMID 24863637.
- ^ Owens DK, Davidson KW, Krist AH, Barry MJ, Cabana M, Caughey AB, et al. (Červenec 2019). "Screening for Hepatitis B Virus Infection in Pregnant Women: US Preventive Services Task Force Reaffirmation Recommendation Statement". JAMA. 322 (4): 349–354. doi:10.1001/jama.2019.9365. PMID 31334800.
- ^ Hollinger FB, Lau DT (December 2006). "Hepatitis B: the pathway to recovery through treatment". Gastroenterologické kliniky Severní Ameriky. 35 (4): 895–931. doi:10.1016/j.gtc.2006.10.002. PMID 17129820.(registrace nutná)
- ^ HBV FAQs for Health Professionals | Division of Viral Hepatitis | CDC Archivováno 20 August 2017 at the Wayback Machine
- ^ Lai CL, Yuen MF (July 2007). "The natural history and treatment of chronic hepatitis B: a critical evaluation of standard treatment criteria and end points". Annals of Internal Medicine. 147 (1): 58–61. doi:10.7326/0003-4819-147-1-200707030-00010. PMID 17606962. S2CID 40746103.
- ^ Alberti A, Caporaso N (January 2011). "HBV therapy: guidelines and open issues". Onemocnění trávicího ústrojí a jater. 43 Suppl 1 (Suppl 1): S57-63. doi:10.1016/S1590-8658(10)60693-7. PMID 21195373.
- ^ Terrault NA, Bzowej NH, Chang KM, Hwang JP, Jonas MM, Murad MH (January 2016). „Pokyny AASLD pro léčbu chronické hepatitidy B“. Hepatologie. 63 (1): 261–83. doi:10.1002 / hep.28156. PMC 5987259. PMID 26566064.
- ^ A b C d GUIDELINES FOR THE PREVENTION, CARE AND TREATMENT OF PERSONS WITH CHRONIC HEPATITIS B INFECTION (PDF). Světová zdravotnická organizace. Březen 2015. ISBN 978924154905-9. Archivováno (PDF) from the original on 19 March 2015.
- ^ A b Dienstag JL (2008). "Hepatitis B Virus Infection". New England Journal of Medicine. 359 (14): 1486–1500. doi:10.1056/NEJMra0801644. PMID 18832247.
- ^ Pramoolsinsup C (February 2002). "Management of viral hepatitis B". Journal of Gastroenterology and Hepatology. 17 (Suppl): S125–45. doi:10.1046/j.1440-1746.17.s1.3.x. PMID 12000599. S2CID 26270129.(vyžadováno předplatné)
- ^ Cao GW (December 2009). "Clinical relevance and public health significance of hepatitis B virus genomic variations". World Journal of Gastroenterology. 15 (46): 5761–9. doi:10.3748/wjg.15.5761. PMC 2791267. PMID 19998495. Archivovány od originál dne 29. června 2011.
- ^ Bell SJ, Nguyen T (2009). "The management of hepatitis B". Aust Prescr. 32 (4): 99–104. doi:10.18773/austprescr.2009.048.
- ^ Kerkar N (2005). "Hepatitis B in children: complexities in management". Dětská transplantace. 9 (5): 685–691. doi:10.1111/j.1399-3046.2005.00393.x. PMID 16176431. S2CID 6437448.
- ^ Taylor JM (2006). "Hepatitis delta virus". Virologie. 344 (1): 71–76. doi:10.1016/j.virol.2005.09.033. PMID 16364738.
- ^ Oliveri F, Brunetto MR, Actis GC, Bonino F (November 1991). "Pathobiology of chronic hepatitis virus infection and hepatocellular carcinoma (HCC)". Ital J Gastroenterol. 23 (8): 498–502. PMID 1661197.
- ^ Peters MG (January 2019). "Hepatitis B Virus Infection: What Is Current and New". Topics in Antiviral Medicine. 26 (4): 112–116. PMC 6372357. PMID 30641484.
- ^ Vierling JM (November 2007). "The immunology of hepatitis B". Clin Liver Dis. 11 (4): 727–759, vii–759. doi:10.1016/j.cld.2007.08.001. PMID 17981227.
- ^ Villa E, Fattovich G, Mauro A, Pasino M (January 2011). "Natural history of chronic HBV infection: special emphasis on the prognostic implications of the inactive carrier state versus chronic hepatitis". Onemocnění trávicího ústrojí a jater. 43 (Suppl 1): S8–14. doi:10.1016/S1590-8658(10)60686-X. PMID 21195374.
- ^ Katz LH, Fraser A, Gafter-Gvili A, Leibovici L, Tur-Kaspa R (February 2008). "Lamivudine prevents reactivation of hepatitis B and reduces mortality in immunosuppressed patients: systematic review and meta-analysis". J. Viral Hepat. 15 (2): 89–102. doi:10.1111/j.1365-2893.2007.00902.x. PMID 18184191. S2CID 37659362.
- ^ Roche B, Samuel D (January 2011). "The difficulties of managing severe hepatitis B virus reactivation". Liver International. 31 (Suppl 1): 104–10. doi:10.1111/j.1478-3231.2010.02396.x. PMID 21205146. S2CID 19400774.
- ^ A b C Mastroianni CM, Lichtner M, Citton R, Del Borgo C, Rago A, Martini H, Cimino G, Vullo V (September 2011). "Current trends in management of hepatitis B virus reactivation in the biologic therapy era". World Journal of Gastroenterology. 17 (34): 3881–7. doi:10.3748/wjg.v17.i34.3881. PMC 3198017. PMID 22025876.
- ^ Bonacini, Maurizio, MD. "Hepatitis B Reactivation". University of Southern California Department of Surgery. Archivovány od originál dne 27. listopadu 2008. Citováno 24. ledna 2009.
- ^ "Hepatitis B incidence rate". Náš svět v datech. Citováno 5. března 2020.
- ^ "Žloutenka typu B". www.who.int. Citováno 20. dubna 2020.
- ^ Custer B, Sullivan SD, Hazlet TK, Iloeje U, Veenstra DL, Kowdley KV (November–December 2004). "Global epidemiology of hepatitis B virus". Journal of Clinical Gastroenterology. 38 (10 Suppl 3): S158–68. doi:10.1097/00004836-200411003-00008. PMID 15602165. S2CID 39206739.
- ^ Redd JT, Baumbach J, Kohn W, Nainan O, Khristova M, Williams I (May 2007). "Patient-to-patient transmission of hepatitis B virus associated with oral surgery". J. Infect. Dis. 195 (9): 1311–4. doi:10.1086/513435. PMID 17397000.
- ^ Alter MJ (2003). "Epidemiology and prevention of hepatitis B". Semináře o onemocnění jater. 23 (1): 39–46. doi:10.1055/s-2003-37583. PMID 12616449.
- ^ Komas NP, Vickos U, Hübschen JM, Béré A, Manirakiza A, Muller CP, Le Faou A (1 January 2013). "Cross-sectional study of hepatitis B virus infection in rural communities, Central African Republic". Infekční nemoci BMC. 13: 286. doi:10.1186/1471-2334-13-286. PMC 3694350. PMID 23800310.
- ^ "Healthcare stumbling in RI's Hepatitis fight". Jakarta Post. 13. ledna 2011. Archivovány od originál dne 4. března 2016.
- ^ Mühlemann B, Jones TC, Damgaard PB, Allentoft ME, Shevnina I, Logvin A, et al. (Květen 2018). "Ancient hepatitis B viruses from the Bronze Age to the Medieval period". Příroda. 557 (7705): 418–423. Bibcode:2018Natur.557..418M. doi:10.1038/s41586-018-0097-z. PMID 29743673. S2CID 13684815.
- ^ A b C d E Ben Guarino (9 May 2018). "New strains of hepatitis B virus discovered in ancient human remains". The Washington Post. Citováno 9. ledna 2018.
- ^ Patterson Ross Z, Klunk J, Fornaciari G, Giuffra V, Duchêne S, Duggan AT, et al. (Leden 2018). "The paradox of HBV evolution as revealed from a 16th century mummy". PLOS patogeny. 14 (1): e1006750. doi:10.1371/journal.ppat.1006750. PMC 5754119. PMID 29300782.
- ^ Davis, Jane (2013). "Molecular Epidemiology of Hepatitis B in the Indigenous People of Northern Australia". Gastroenterologie a hepatologie. 2013 July (7): 1234–41. doi:10.1111/jgh.12177. PMID 23432545. S2CID 5208526.
- ^ Gerlich, Wolfram (2013). "Medical Virology of Hepatitis B: how it began and where we are now". Virology Journal. 2013, 10: 239. doi:10.1186/1743-422X-10-239. PMC 3729363. PMID 23870415.
- ^ Paraskevis, Dimitrios (2013). "Dating the Origin and Dispersal of Hepatitis B Virus Infection in Humans and Primates". Hepatologie. 2013 (3): 908–16. doi:10.1002/hep.26079. PMID 22987324. S2CID 25933906.
- ^ Lurman A (1885). "Eine icterus epidemic". Berl Klin Woschenschr (v němčině). 22: 20–3.
- ^ "World War II Hepatitis Outbreak Was Biggest in History". Associated Press. Boston. 16 April 1987. Citováno 8. listopadu 2020.
- ^ Jacobsen, Annie (2014). Operation Paperclip: The Secret Intelligence Program that Brought Nazi Scientists to America. p. 6. ISBN 978-0-316-22104-7.
- ^ "Report: Yale professor intentionally gave patients hepatitis in 1940s study". CT příspěvek. 1. března 2011. Citováno 8. listopadu 2020.
- ^ Jakubik A, Ryn Z (1973). "Pseudomedical experiments in Nazi concentration camps". Przegl Lek. 30 (1): 64–72. PMID 4571138. Citováno 8. listopadu 2020.
- ^ "Nazi Medical Experiments". Encyklopedie holocaustu. United States Holocaust Memorial Museum. Citováno 8. listopadu 2020.
- ^ Alter HJ, Blumberg BS (March 1966). "Further studies on a "new" human isoprecipitin system (Australia antigen)". Krev. 27 (3): 297–309. doi:10.1182/blood.V27.3.297.297. PMID 5930797.
- ^ MacCallum FO (1947). "Homologous serum hepatitis". Lanceta. 2 (6480): 691–692. doi:10.1016/S0140-6736(47)90722-8.
- ^ Dane DS, Cameron CH, Briggs M (April 1970). "Virus-like particles in serum of patients with Australia-antigen-associated hepatitis". Lanceta. 1 (7649): 695–8. doi:10.1016/S0140-6736(70)90926-8. PMID 4190997.
- ^ A b "Hepatitis B Vaccine History". Hepatitis B Foundation. Citováno 8. listopadu 2020.
- ^ Galibert F, Mandart E, Fitoussi F, Tiollais P, Charnay P (October 1979). "Nucleotide sequence of the hepatitis B virus genome (subtype ayw) cloned in E. coli". Příroda. 281 (5733): 646–50. Bibcode:1979Natur.281..646G. doi:10.1038/281646a0. PMID 399327.
- ^ Duesberg, Peter (1996). Vynález viru AIDS. New York: Regenery. str. 114–116.
- ^ Dietzman D, Harnisch J, Ray G, Alexander R, Holmes K (1977). "Hepatitis B surfice antigen (HBsAG) and antibody to HBsAG. Prevalence in homosexual and heterosexual men". JAMA. 238 (24): 2625–6. doi:10.1001/jama.1977.03280250051022. PMID 579199.
- ^ Goodfield, June (1985). Quest for the Killers. Hill a Wang. p. 51–97.
- ^ Szmuness W, Stevens C, Harley E, et al. (1980). "Szmuness chooses healthy young homosexuals for his experiment". The New England Jounral of Medicine. 303 (15): 833–41. doi:10.1056/NEJM198010093031501. PMID 6997738.
- ^ Francis, Don (1982). "The prevention of hepatitis B with vaccine. Report of the Centers for Disease Control multi-center efficacy trial among homosexual men". Annals of Internal Medicine. 97 (3): 362–366. doi:10.7326/0003-4819-97-3-362. PMID 6810736.
- ^ Goodfield, June. Quest for the Killers. p. 94.
- ^ Rappoport, John (2004). AIDS, Inc. Namaste Publishing. p. 328. ISBN 0-9546590-1-5.
- ^ Martin, Noreen (2007). Surviving AIDS and Cancer: A Guide to Staying Healthy. iUniverse. p. 28. ISBN 9780595431526. Citováno 11. listopadu 2020.
- ^ "Viral hepatitis" (PDF). Světová zdravotnická organizace. Archivováno (PDF) from the original on 11 August 2011.
externí odkazy
| Klasifikace | |
|---|---|
| Externí zdroje |
- GUIDELINES FOR THE PREVENTION, CARE AND TREATMENT OF PERSONS WITH CHRONIC HEPATITIS B INFECTION (PDF). Světová zdravotnická organizace. Březen 2015. ISBN 978924154905-9.
- "Virus hepatitidy B.". Prohlížeč taxonomie NCBI. 10407.
